創傷弧菌的優化培養及快速檢測
鄧 曦,唐書澤,*,周鵬飛,李紅愛,吳希陽,馬 強
(1.暨南大學食品科學與工程系,廣東廣州510632;2.暨南大學微生物學系,廣東廣州 510632)
創傷弧菌(Vibrio vulnificus)普遍存在于溫帶溫暖水生環境中,屬兼性厭氧型微生物,在海洋、鹽湖和淡水中廣泛分布,為全球重要的海洋致病細菌,與霍亂弧菌、腸炎弧菌并稱為造成人類感染疾病的三大弧菌。該菌可通過進食生海鮮或皮膚傷口而感染,臨床上常造成嚴重的敗血癥及肢體壞死,病發過程相當迅速且死亡率高,并且嚴重的傷口感染,會引起胃腸道感染,70%的患者在入院48h內因多臟器功能不全而死亡,它被稱為“海洋中的無聲殺手”[1-2]。近年來,國內外關于創傷弧菌感染的報道逐漸增多,創傷弧菌造成的食品污染日益受到人們廣泛關注。我國水域廣闊,海產品豐富,準確快速檢測海產品中的可能污染的創傷弧菌對水產品安全具有重要意義。
目前,檢測創傷弧菌的方法主要有各種選擇性培養基、聚合酶鏈反應技術、酶聯免疫技術、自動酶聯熒光免疫檢測、核酸薄膜層析法、實時定量熒光PCR等方法[3-5],此外,PCR結合變性高效液相色譜技術也逐步得到發展[6]。生化特征目前仍是創傷弧菌鑒定分類的常用方法,然而該菌在不良環境中易進入非可培養狀態(VBNC)[7],導致鑒定結果呈假陰性,但一定條件下恢復培養后,該菌仍保持致病性。另外,該菌的生化特征不穩定,給其鑒定帶來很大困難和不確定性[8]。
創傷弧菌的準確檢測以菌種的有效培養為前提,優化創傷弧菌的培養條件,有利于對其快速、高效檢出。本實驗選用創傷弧菌標準菌株ATCC27562為實驗菌,通過對各種培養條件的探索,尋求創傷弧菌的最佳培養條件,并在此基礎上結合PCR技術進行了檢測。
1 材料與方法
1.1 材料與儀器
創傷弧菌標準菌株ATCC27562 廣東環凱微生物科技有限公司;胰蛋白胨大豆肉湯(TSB)、蛋白胨(APW)、多粘菌素B、2216E液體培養基、TCBS瓊脂培養基、mCPC瓊脂培養基、3%NaCl胰蛋白胨大豆瓊脂(TSA) 青島海博生物技術有限公司;細菌基因組DNA提取試劑盒 生工生物有限公司;1×Taq PCR MasterMix 天根生化科技(北京)有限公司;目的片段 針對創傷弧菌的特異基因thl設計引物,根據參考文獻[9],委托生工生物工程(上海)股份有限公司合成其序列如下,上游引物:Vvh-785F 5′-CCGCGG TACAGGTTGGCGCA-3′;下游引物:Vvh-1303R 5′-CGCCACCCACTTTCGGGCC-3′,目的片段大小為519bp。
酶標儀MK3(Thermo Labsystems) 美國賽默飛世爾;PHS-3C型精密pH計 上海雷磁分析儀器廠;梯度PCR儀 Eppendorf公司;數碼成像系統 KODAK公司;高速離心機 北京時代北利離心機有限公司。
1.2 實驗方法
1.2.1 培養基的篩選 APW,APW+多粘菌素B,TSB,2216E液體培養基各10mL,分裝于12支15mL離心管中(2組平行),滅菌后備用。向每只管中添加等量創傷弧菌菌液,37℃增菌培養16h,取菌液100μL,以1∶10梯度稀釋涂布于mCPC及TCBS平板上,培養24h后觀察。
1.2.2 菌體生長影響因素探究 通過1.2.1觀察平板菌落總數,確定出最佳增菌液。取培養于APW+多粘菌素B 16h的最佳增菌液200μL接種于10mL TSB培養基中,2組平行,使用酶標儀測定吸光度值。1.2.3 單因素實驗設計
1.2.3.1 不同鹽度對創傷弧菌生長影響 向增菌液中添加不同量的NaCl,使鹽濃度達到0.5%、1%、2%、3%、4%、5%、6%、7%、8%、9%、10%,用以優選適宜創傷弧菌生長的培養基鹽度范圍。取10μL菌液分別接種于液體培養基中,35℃下培養,分別于培養0、3、5、6、7、8、9、10h取樣,并使用酶標儀(595nm)測定菌液吸光度值,并繪制曲線圖。
1.2.3.2 不同pH對創傷弧菌生長影響 使用含0.5%NaCl的TSB液體培養基,將其pH分別調至4.0、5.0、6.0、7.0、7.5、8.0、8.5、9.0、10.0、11.0,取10μL菌液分別接種于液體培養基中,35℃下培養,其余操作同1.2.3.1。由此篩選出適宜創傷弧菌生長的pH范圍。
1.2.3.3 不同溫度對創傷弧菌生長影響 取200μL菌液分別接種于含0.5%NaCl的TSB液體培養基中,于25、30、35、40、45℃下培養,其余操作同1.2.3.1,從中測定創傷弧菌生長的適宜溫度。
1.2.4 響應面實驗設計 創傷弧菌的生長受諸多因素的影響,而且創傷弧菌的感染具有明顯的季節特征,在創傷弧菌的培養過程中,培養基含鹽量、pH以及培養溫度對創傷弧菌的生長均有較大影響[10-11]。本研究利用Design-Expert 8.05軟件中的Box-Behnken實驗設計原理,設計一組3因素3水平的共計17組的實驗。

表1 實驗的因素及水平編碼Table 1 Code of factors and levels
1.3 菌體的快速檢測
利用響應曲面法得出最優參數,采用優化培養基對創傷弧菌ATCC27562及五月市售海鮮(翡翠貽貝)進行培養,用試劑盒法提取細菌DNA,并采用PCR進行檢測。
PCR反應體系(50μL)為:PCR Master Mix 25μL,Primer F及Primer R(0.4μmol·L-1)各1μL,模板DNA 2μL,ddH2O 21μL。
PCR的反應程序為:94℃預變性5min,94℃變性30s,63.5℃退火30s,72℃延伸35s,循環25次,72℃再延伸5min。
用TAE緩沖液配制1%瓊脂糖凝膠,采用PCR擴增產物,進樣5μL,電壓80V,電泳40min,檢測和分析電泳結果。
2 結果與分析
2.1 單因素實驗結果及分析
2.1.1 鹽度對菌體生長的影響 Andrea等[12]研究發現高鹽度的環境可抑制創傷弧菌的生長,當鹽度為1.5%左右時,該菌生長良好,受到最少抑制。而由本實驗(如圖1)可以看出,鹽度在0.5%~5%時,創傷弧菌生長良好,尤其濃度在1%~4%時生長速率較快,而鹽度達到10%基本不生長,這是因為在鹽度較高的情況下,菌體滲透壓變化,引起細菌胞漿分離或脫水而死亡[13]。
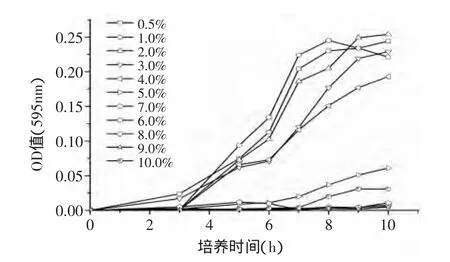
圖1 鹽度對創傷弧菌生長的影響Fig.1 Effect of salinity on growth of Vibrio vulnificus ATCC27562
2.1.2 pH對菌體生長的影響 培養基的pH必須控制在一定范圍內,以滿足細菌的生長繁殖或產生代謝產物,各類微生物生長繁殖或產生代謝產物的最適pH各不相同[14]。pH對創傷弧菌生長的影響結果見圖2,pH在5~9時,菌體均可生長,在pH過高或過低的條件下,菌體幾乎不能生長,其中pH 6~8時,菌體生長最佳。Bang等[15]通過研究發現創傷弧菌可以承受的最低酸度為pH3.5,并且只能在此環境中生存約50h,而在pH4.0~5.0的環境中可以存活,但幾乎不能生長,此與本實驗結果相符合。

圖2 pH對創傷弧菌生長的影響Fig.2 Effect of pH on growth of Vibrio vulnificus ATCC27562
2.1.3 溫度對菌體生長的影響 據文獻報道[16-17],創傷弧菌在20℃以上時才開始大量生長繁殖,且在35℃左右生長最快,據此設定單因素溫度區間為25~45℃。圖3表明,在30~40℃的條件下,菌體生長較快,其中,當溫度達到35℃左右時生長狀況最佳。因此選擇30~40℃為創傷弧菌的最適生長條件。

圖3 溫度值對創傷弧菌生長的影響Fig.3 Effect of temperature on growth of Vibrio vulnificus ATCC27562
2.2 響應曲面分析實驗設計方案及結果
2.2.1 響應曲面分析實驗 通過酶標儀在595nm下測定每個時間點時菌液的OD值為響應值(Y),響應曲面分析實驗設計及結果如表2所示。

表2 響應曲面分析實驗設計方案及結果Table 2 Experimental design and results of response surface methodology

表3 回歸模型的方差分析Table 3 Variance analysis of regression model
2.2.2 回歸模型的建立及方差分析 用Design-Expert 8.05軟件對實驗結果進行分析,結果見表3,該模型的F值為7.504337,p=0.0073<0.01,表明該模型具有意義;決定系數R2=0.9061表明該模型具有較高的可信度;該模型的失擬項在可接受范圍內,說明模型可用。根據數學模型對表2數據進行二次方多元回歸擬合可得到回歸方程為:Y=+0.48+0.044A-0.052B+0.059C+5.500E-003AB+0.10AC-0.020BC-0.081A2-0.037B2-0.092C2
2.2.3 響應曲面交互作用分析 根據上述回歸方程繪出等高線圖及響應曲面圖,以分析培養基含鹽量,pH,培養溫度3個因素對創傷弧菌生長的交互作用。曲線越陡,說明因素間的交互作用越強;圖形中曲面顏色越深的區域,說明結果越顯著[18]。結果表明,培養基含鹽量與培養溫度的交互作用顯著,其他兩組交互作用不顯著。圖4、圖5表明,培養溫度及pH不變的條件下,在0.5%~5%的范圍內,隨著鹽度的升高,弧菌生長速率先升高后降低。圖6表明,溫度一定時,隨著培養基pH的升高,在一定范圍內,弧菌的生長速率先升后降。圖5、圖6表明,在鹽度及pH不變的條件下,隨著溫度的升高,創傷弧菌的生長速率先增加后降低。
2.2.4 參數優化與驗證 在Design-Expert 8.05軟件中利用上述回歸方程對創傷弧菌生長條件進行優化,求解得各因素的理論最優條件為:含鹽量3.65%,pH6.75,培養溫度37.00℃,在該條件下培養液的OD595nm理論值為0.530056。為檢驗優化條件的可靠性,重復實驗3次,實際測得在該條件下595nm下的OD值為0.520,與理論預測值相比,預測準確率為98.1%,由此表明利用響應曲面法優化的培養條件是可行的。

圖4 培養基含鹽量與pH對創傷弧菌生長的影響Fig.4 Effect of salinity and pH on growth of Vibrio vulnificus ATCC27562

圖5 培養基含鹽量與培養溫度對創傷弧菌生長的影響Fig.5 Effect of salinity and temperature on growth of Vibrio vulnificus ATCC27562

圖6 培養基的pH與培養溫度對創傷弧菌生長的影響Fig.6 Effect of PH and temperature on growth of Vibrio vulnificus ATCC27562
2.3 PCR檢測結果
從圖7看來,采用優化培養基培養不同來源的創傷弧菌的菌株,通過PCR實驗可以準確檢測到不同來源的創傷弧菌的菌株。從30份樣品中篩出可能污染創傷弧菌的樣品有7份,將可疑樣品進行PCR檢測,結果呈陽性,如圖8所示。陳艷等[19]采用生化實驗及PCR法得出,東南沿海地區天然污染海產品試樣創傷弧菌的檢出率為19.8%;鄧志愛等[20]通過對海產品的檢測發現,廣東地區的創傷弧菌的檢出平均水平為9.06%,其中生食海產為42.86%,非生食海產為6.56%,而且檢出的污染水平有明顯季節差異。在本實驗中,創傷弧菌的檢出率高達23.3%(7/30),而且整個操作過程簡單易行,經濟節省,所需時間也較短。

圖7 不同來源創傷弧菌-瓊脂糖凝膠電泳圖Fig.7 Electrophoresis of Vibrio vulnificus注:1:Marker;2~13:不同菌落提取的DNA。

圖8 不同海產樣品的電泳圖Fig.8 Electrophoretograms of Vibrio vulnificus
3 結論
本實驗通過以培養基含鹽量、pH、溫度三個因素為條件,用酶標儀(595nm)測定一定時間點的菌液吸光度值,根據Design-Expert軟件的Box-Behnken中心組合響應面分析法優化出了最佳工藝參數為:含鹽量3.65%,pH6.75,溫度37.00℃,在該條件下菌液在595nm下的吸光度值的理論值0.530056,實際值為0.520,該模型的預測準確率為98.1%。該優化培養基結合PCR-瓊脂糖凝膠電泳的方法,能方便快捷地檢出產品中的創傷弧菌,且檢出率高達23.3%。該條件參數的培養基價廉易得,PCR技術的應用也非常廣泛。因此,該方法適合于創傷弧菌的優化培養及快速檢測,具有良好的實際應用價值。
[1]吳斌,盧中秋.創傷弧菌感染的致病機制研究現狀[J].中國急救醫學,2004,24(11):834-835.
[2]趙廣英,申科敏,勵建榮.水產品中多種致病性弧菌的分離鑒定[J].食品科技,2009,34(11):279-282.
[3]何閃閃,薛長湖,李兆杰,等.水產品中創傷弧菌的快速檢測與分離[J].中國食品學報,2005(3):86-89.
[4]石琰璟,王建廣.PCR-核酸薄膜層析法檢測創傷弧菌[J].青島科技大學學報:自然科學版2012,33(2):164-167.
[5]劉彤,鄭秋月,趙昕,等.變性高效液相色譜技術對創傷弧菌檢測的研究[J].中國微生態學雜志2011,23(5):470-472.
[6]Oliver JD,Hite F,McDougald D,et al.Entry into,and resuscitation from,the viable but nonculturable state by Vibrio vulnificus in an estuarine environment[J].Applied and Environment Microbi-ology,1995,61:2624-2630.
[7]鐘凱,田靜,李業鵬,等.食品中副溶血性弧菌PCR快速檢測方法的研究[J].中國食品衛生雜志,2004,16(4):317-320.
[8]Ji H,Chen Y,Guo YC,et al.Occurrence and characteristics of Vibrio vulnificus in retail marine shrimp in China[J].Food Control,2011,22:1935-1940.
[9]Staley C,Chase E,Harwood VJ.Detection and differentiation of Vibrio vulnificus and Vibrio Sinaloensis in water and oysters of a Gulf of Mexico estuary[J].Environmental Microbiology,2003,15(2):623-633.
[10]Ruppert J,Panzig B,Guertler L,et al.Two cases of severe sepsis due to Vibrio vulnificus wound infection acquired in the Baltic Sea[J].European Journal of Clinical Microbiology&Infectious Diseases,2004,23:912-915.
[11]Williams TC,Brett F,Oliver JD.A new culture-based method for the improved identifi cation of Vibrio vulnificus from environmentalsamples,reducing the need for molecular confirmation[J].Journal of Microbiological Methods,2013,93:277-283.
[12]Larsen AM,Rikard FS,Walton WC,et al.Effective reduction of Vibrio vulnificus in the Eastern oyster(Crassostrea virginica)using high salinity depuration[J].Food Microbiology,2013,34:118-122.
[13]文湘華,占新民,王建龍,等.含鹽沸水生物處理研究進展[J].環境科學,1999,20(3):104-106.
[14]江漢湖.食品微生物學[M].北京:中國農業出版社,2009.
[15]Bang W,Drake MA.Acid adaptation of Vibrio vulnificus and subsequent impact on stress tolerance[J].Food Microbiology,2005,22:301-309.
[16]Griffitt KJ,Grimes DJ.A novel agar formulation for isolation and direct enumeration of Vibrio vulnificus from oyster tissue[J].Journal of Microbiological Methods,2013,94:98-102.
[17]陳春梅,陳錦春.水產品中創傷弧菌的選擇性分離[J].檢驗檢疫科學,2007,17(6):37-39.
[18]Montgomery DC.Design and analysis of experiments[M].8Th Edition.New York:Wiley,2009.
[19]陳艷,梅玲玲,李秀桂,等.東南沿海地區零售海產品中創傷弧菌的檢測[J].中國食品衛生雜志,2009,21(4):344-347.
[20]鄧志愛,李佳旋,李孝權,等.廣州地區海產品和珠江水中致病性弧菌污染狀況監測[J].中國衛生檢驗雜志,2011,21(5):1237-1239.

