威靈仙不同提取部位對脂多糖誘導的RAW264.7細胞NO生成及iNOS和TNF-α表達的影響
劉光耀 王海燕 白彩虹 賀海波 鄧 為陳置豐 龔學謙 次旦多吉 顏為紅
(1.三峽大學 醫學院,湖北 宜昌 443002;2.三峽大學 中醫臨床醫學院/宜昌市中醫醫院,湖北 宜昌443001;3.天然產物研究與利用湖北省重點實驗室(三峽大學),湖北 宜昌 443002)
威靈仙系毛茛科鐵線蓮屬植物威靈仙(Clematis chinensis Osbeck)、棉團鐵線蓮(Clematis hexapetala Pall.)或東北鐵線蓮(Clematis manshurica Rupr.)的干燥根和根莖,別名靈仙、黑須公、鐵靈仙、鐵掃帚.威靈仙味辛、咸,性溫,為臨床廣泛使用的中藥.具有祛風除濕、通絡止痛之功,傳統多用于治療風濕性關節炎、類風濕關節炎、骨鯁咽喉、乳腺炎、癰瘡等[1-2].其化學成分主要有三萜及皂苷、黃酮、揮發油(有機酸、有機酸酯、苯丙素、倍半萜、酚類)、生物堿、香豆素、木脂素、甾體、烷烴及Zn、Ca、Fe、Ni、Mg等[3-4].隨著對其化學成分的日漸明晰,學者們發現,威靈仙除了有著突出的抗炎鎮痛作用外,在抗腫瘤、抗菌抑菌、抗利尿、抗瘧、降血糖、降血壓、利膽等方面的顯示了較好的療效[4-6],能顯著降低實驗小鼠血尿酸、血沉和C反應蛋白的水平[7],抑制T淋巴細胞的過度增殖、抑制細胞因子TNF-α、IL-1β和PEG2來發揮抗類風濕性關節炎作用[8].但威靈仙中各種部位間抗炎作用有否有差異及對巨噬細胞分泌炎癥因子的干預作用研究鮮有報道.基于此,本研究擬考查威靈仙不同提取部位(石油醚、乙酸乙酯、正丁醇和水萃取部位)對脂多糖(LPS)誘導的RAW264.7細胞NO生成及iNOS和TNF-α表達的影響,比較其作用的差異,明確威靈仙脂多糖誘導RAW264.7巨噬細胞炎癥反應的活性部位,為其抗炎鎮痛的臨床應用和進一步研究開發提供理論依據.
1 材 料
1.1 實驗藥物
威靈仙根和根莖購自宜昌市中醫醫院,經天然產物研究與利用湖北省重點實驗室(三峽大學)汪鋆植教授鑒定為威靈仙(Clematis chinensis Osbeck),植物標本現保存于天然產物研究與利用湖北省重點實驗室(標本編號:20120824).
1.2 細胞株
小鼠巨噬細胞株RAW264.7購自中國科學院上海細胞研究所.
1.3 儀器與試劑
電子分析天平,中國上海梅特勒-托利多有限公司;旋轉蒸發儀,中國無錫市星海王生化設備有限公司;Labconco低溫冷凍干燥儀,美國Labconco公司;UV-2000型紫外-可見分光光度計,尤尼柯儀器有限公司;LDZ5-2自動平衡離心機,北京醫用離心機廠;GENios酶標儀,瑞士Tecan公司;NU-4750E型CO2培養箱,Nu Aire公司;SW-4T-2F潔凈工作臺,上海博訊實業有限公司醫療設備廠;LS-B50L立式壓力蒸汽滅菌器,上海華線醫用核子儀器有限公司;EcoTM實時熒光定量PCR儀.RPMI1640細胞培養基、胰酶、二甲基亞砜(DMSO):Gibco公司;胎牛血清:杭州四季青生物材料有限公司;四甲基偶氮唑鹽(MTT)、LPS:美國Sigma公司;誘導型一氧化氮合酶(iNOS)、一氧化氮(NO)測試試劑盒:南京建成生物工程研究所;小鼠TNF-αELISA檢測試劑盒,北京達科為生物技術有限公司;iNOS、TNF-α以及GAPDH(上海生工生物工程有限公司合成,具體引物序列見表1);Trizol和DEPC(上海生工生物工程有限公司);Prime ScriptTM RT reagent Kit、Taq DNA 聚合酶(大連寶生物工程有限公司);其他試劑均為市售分析純.
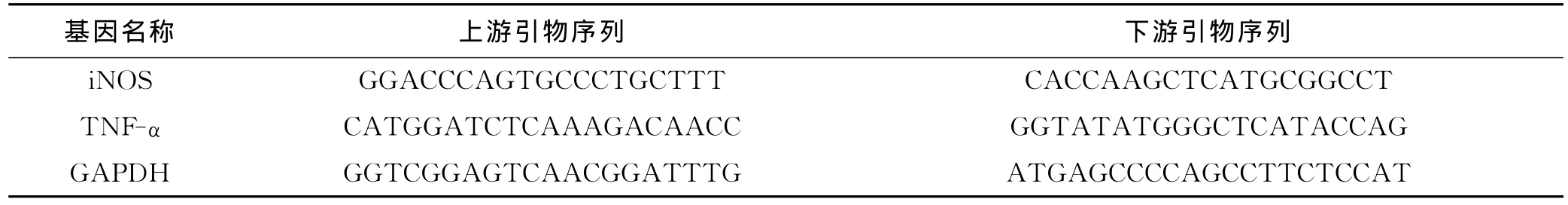
表1 實時定量PCR引物序列
2 方 法
2.1 威靈仙不同部位的制備
威靈仙根和根莖粉成粗粉,以95%乙醇為溶劑,在65℃條件下常壓回流提取,提取液過濾后用旋轉蒸發儀濃縮(溫度55℃),得深棕色浸膏,將浸膏在通風櫥中揮干至無醇味,加入蒸餾水混懸溶解,依次用石油醚、乙酸乙酯、水飽和的正丁醇萃取.在旋轉蒸發儀上濃縮并回收萃取液,回收后的溶劑繼續用于萃取.合并每一種萃取溶劑的萃取物,于通風櫥中揮干溶劑,在冷凍干燥儀上干燥.實驗時用DMSO溶解樣品配制成質量濃度為10mg/mL提取物藥液,再以細胞培養液稀釋成所需濃度,經過0.22μm孔徑濾膜過濾除菌后供實驗用,使用時用含10%血清的DMEM培養液稀釋成目標濃度.
2.2 RAW264.7細胞培養
RAW264.7細胞在37℃,5%CO2條件下,用含10%小牛血清、青霉素(1×105U/L)及鏈霉素(100 mg/L)的DMEM培養液傳代培養,實驗用細胞均處于對數生長期.
2.3 威靈仙不同提取部位對RAW264.7細胞的毒性作用
RAW264.7細胞按5×105/孔接種于96孔板中,貼壁4h后,加入不同質量濃度(0、25、50、100、200μg/mL)的威靈仙不同提取部位,每組設置3個復孔,孵育24h后,每次加入新配制的5mg/mL MTT液20μL,37℃避光孵育4h,終止培養.吸去上清液,每孔加入DMSO 150μL,置搖床上低速振蕩10min后,用酶標儀于490nm處測量各孔的吸光度值(OD490nm)根據公式:細胞抑制率=(1-藥物孔OD值/陰性對照孔OD值)×100%.
2.4 LPS對RAW264.7細胞的毒性作用
為了確定LPS刺激RAW264.7細胞分泌炎癥介質和促炎因子的作用濃度,需要確定LPS影響RAW264.7細胞安全濃度.取RAW264.7細胞按5×105/孔接種于96孔板中,貼壁4h后,加入不同質量濃度LPS(0.125、0.25、0.5、1、2μg/mL),空白對照組只加入培養基,每組設置3個復孔,作用24h,然后測定細胞活性,檢測方法同2.3.確定無細胞毒性的最大濃度,以下進行LPS刺激RAW264.7細胞分泌炎癥介質和促炎因子實驗時按照此濃度進行.
2.5 威靈仙不同提取部位對LPS刺激RAW264.7細胞釋放NO的影響
RAW264.7細胞按5×105個/mL接種于48孔板中,貼壁4h后,然后分別加入不同質量濃度(25、50、100μg/mL)的威靈仙不同提取部位孵育2h,再加入終質量濃度為1μg/mL的LPS刺激24h,正常對照孔或模型對照孔加入等體積的培養基),每組設置6個復孔.作用24h后,收集上清,采用Griess法[9]測定上清中NO含量,具體操作按試劑盒說明書進行.
2.6 威靈仙不同提取部位對LPS刺激RAW264.7細胞iNOS活性的影響
RAW264.7細胞按5×105個/mL接種于48孔板中,貼壁4h后,然后分別加入不同質量濃度(25、50、100μg/mL)的威靈仙不同提取部位孵育2h,再加入終質量濃度為1μg/mL的LPS刺激24h,正常對照孔或模型對照孔加入等體積的培養基),每組設置6個復孔.作用24h后,收集上清液,測定上清液中iNOS,具體操作按試劑盒說明書進行.
2.7 威靈仙不同提取部位對LPS刺激RAW264.7細胞分泌TNF-α的影響
RAW264.7細胞按5×105個/mL接種于6孔板,貼壁4h后,然后分別加入不同質量濃度(25、50、100μg/mL)的威靈仙不同提取部位孵育2h,再加入終質量濃度為1μg/mL的LPS刺激24h,正常對照孔或模型對照孔加入等體積的培養基),每組設置3個復孔.作用24h后,收集上清液,測定上清液中TNF-α含量,具體操作按各ELISA試劑盒說明書進行.
2.8 實時熒光定量PCR法檢測威靈仙不同提取部位對RAW264.7細胞iNOS和TNF-αmRNA表達量的影響
RAW264.7細胞按5×105個/mL接種于6孔板,貼壁4h后,然后分別加入不同質量濃度(25、50、100μg/mL)的威靈仙不同提取部位孵育2h,再加入終質量濃度為1μg/mL的LPS刺激24h,正常對照孔或模型對照孔加入等體積的培養基),每組設置3個復孔.作用24h后,移走培養液,用PBS輕輕洗滌一遍,加入1mL Trizol,室溫靜置5min,用移液槍吹打細胞,使其充分裂解.將Trizol轉移至1.5mL無RNase的EP管中,4℃,12000rpm離心5min,棄沉淀,將上清轉移至另一個1.5mL無RNase的EP管中,按照0.2mL氯仿/mL Trizol加入氯仿,振蕩混勻.室溫靜置15min.4℃,12000rpm 離心15min.吸取上層水相至另一個1.5mL無RNase的EP管中.按0.5mL異丙醇/mL Trizol加入異丙醇,混勻,室溫靜置10min.4℃,13000rpm離心10min,棄上清,RNA沉于管底.按1mL 75%乙醇/mL Trizol加入75%乙醇,溫和振蕩離心管,懸浮沉淀.4℃,13000 rpm離心15min,盡量棄上清.室溫晾干.用20μL E-lution buffer溶解RNA樣品.立即進行逆轉錄.逆轉錄完成后的樣品,立即進行熒光定量或放入-80℃保存備用.以GAPAH為內參照檢測iNOS和TNF-α基因的表達.每組樣本重復3次,以空白對照組RAW264.7細胞的檢測基因表達量為1,2-ΔΔCT法計算各組相對表達量,計算公式為:fold=2-ΔΔCT=2-(Δct實驗組-Δct空白對照組),ΔCT=CT待測樣品-CT內參.
2.9 統計學分析
3 結 果
3.1 威靈仙不同提取部位對RAW264.7細胞的毒性作用
利用MTT法測定不同濃度威靈仙不同提取部位對RAW264.7細胞的存活率,確定威靈仙不同提取部位是否對細胞有毒性作用.圖1結果顯示,威靈仙不同提取部位(25、50、100μg/mL)對 RAW264.7細胞的存活率沒有影響,但是威靈仙不同提取部位在200μg/mL時明顯降低RAW264.7細胞的存活率,同時顯微鏡下觀察細胞狀態與MTT實驗結果一致.表明威靈仙不同提取部位對RAW264.7細胞無明顯毒性,以下研究均在200μg/mL以下進行,即選擇威靈仙不同提取部位質量濃度為25、50、100μg/mL進一步觀察威靈仙不同提取部位的抗炎作用.

圖1 威靈仙不同提取部位對RAW264.7細胞的毒性影響
3.2 LPS對RAW264.7細胞的毒性影響
LPS處理細胞24h后,隨著LPS濃度的升高RAW264.7細胞存活率有所下降,當濃度達到2μg/mL時,可使RAW264.7細胞存活率顯著降低,與空白對照組比較具有顯著性差異(P<0.01).因此,本實驗選取的LPS刺激RAW264.7細胞的安全濃度為1.0μg/mL作用時間為24h,以此來進一步觀察威靈仙不同提取部位的抗炎作用及機制.
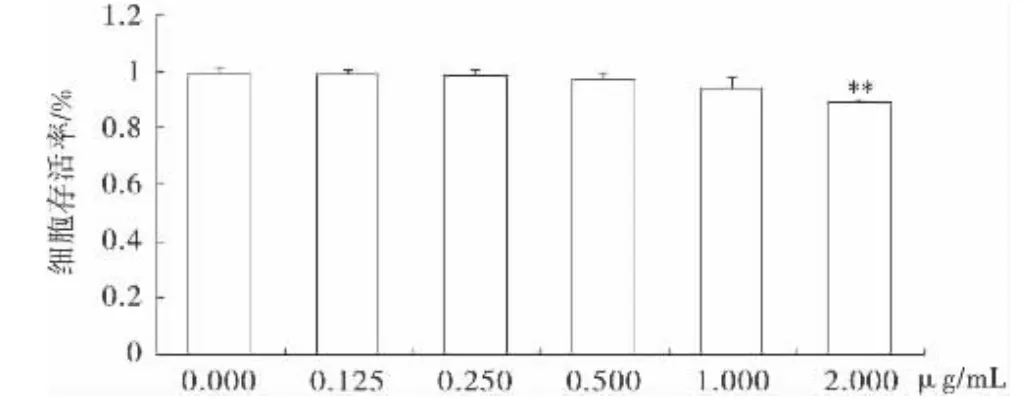
圖2 不同濃度LPS對RAW264.7細胞的毒性影響
3.3 威靈仙不同提取部位對LPS刺激RAW264.7細胞的NO釋放影響
如圖3所示,模型組RAW264.7細胞釋放NO顯著增加,與空白對照組比較具有顯著性差異(P<0.01);用威靈仙不同提取部位處理后,它們對激活狀態RAW264.7細胞NO釋放均具有不同程度的抑制作用,并呈良好的劑量依賴關系.實驗結果表明威靈仙不同提取部位均能夠抑制LPS誘導的RAW264.7細胞NO釋放,其作用強弱依次為威靈仙乙酸乙酯部位、石油醚部位、正丁醇部位和水部位.
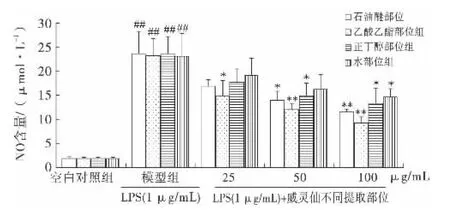
圖3 威靈仙不同提取部位對LPS刺激RAW264.7細胞釋放NO的影響
3.4 威靈仙不同提取部位對LPS刺激RAW264.7細胞iNOS的活性影響
圖4所示,模型組iNOS活性明顯增加,與空白對照組比較具有顯著性差異(P<0.01);用威靈仙不同提取部位處理后,它們對激活狀態RAW264.7細胞iNOS活性均具有不同程度的抑制作用,并呈良好的劑量依賴關系.實驗結果表明,威靈仙不同提取部位均能夠抑制LPS誘導的RAW264.7細胞iNOS表達,其作用強弱依次為威靈仙乙酸乙酯部位、石油醚部位、正丁醇部位和水部位.
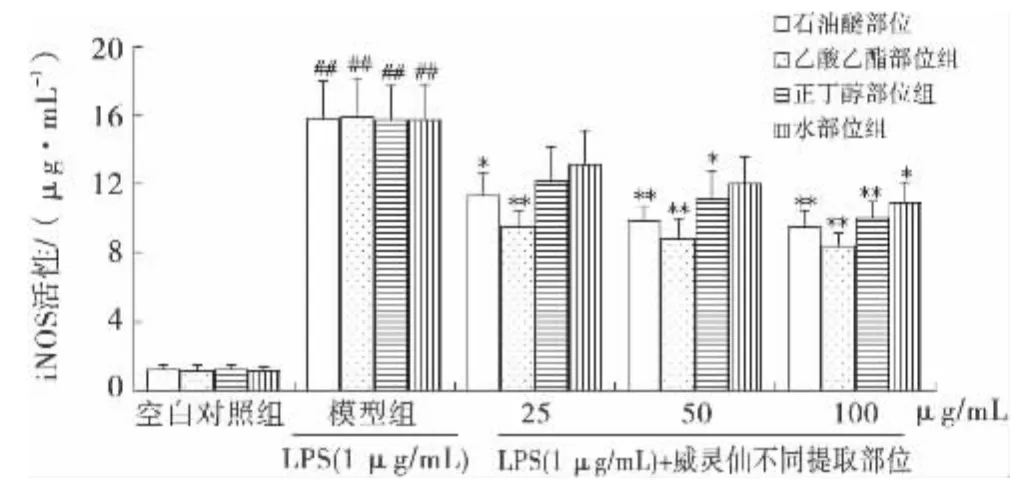
圖4 威靈仙不同提取部位對LPS刺激RAW264.7細胞iNOS的活性影響
3.5 威靈仙不同提取部位對LPS刺激RAW264.7細胞分泌TNF-α的影響
圖5所示,模型組TNF-α含量明顯增加,與空白對照組比較具有顯著性差異(P<0.01);用威靈仙不同提取部位處理后,它們對激活狀態RAW264.7細胞TNF-α含量均具有不同程度的抑制作用,并呈良好的劑量依賴關系.實驗結果表明威靈仙不同提取部位均能夠抑制LPS誘導的RAW264.7細胞TNF-α分泌,其作用強弱依次為威靈仙乙酸乙酯部位、石油醚部位、正丁醇部位和水部位.
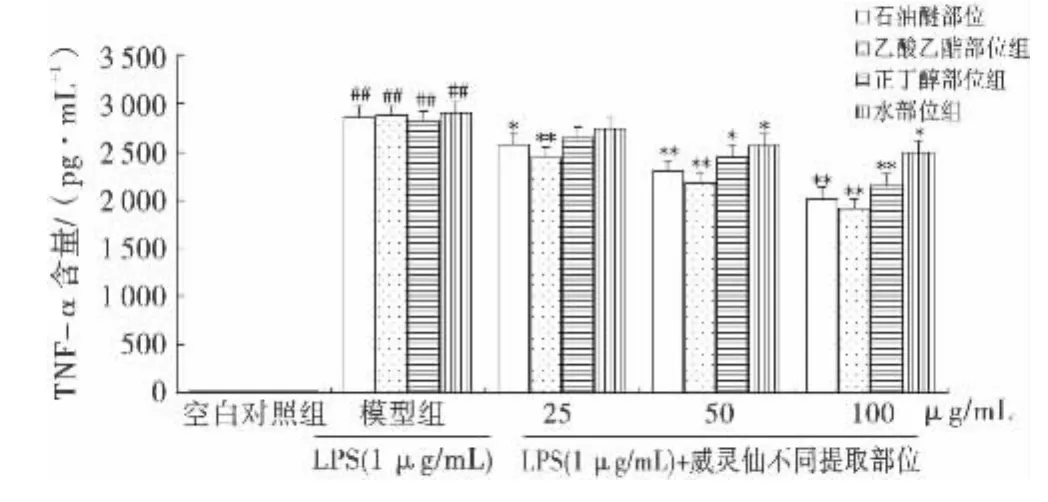
圖5 威靈仙不同提取部位對LPS刺激RAW264.7細胞分泌TNF-α的影響
3.6 威靈仙不同提取部位對LPS刺激RAW264.7細胞iNOS和TNF-αmRNA表達量的影響
圖6所示,模型組RAW264.7細胞iNOS和TNF-αmRNA表達量顯著升高,與空白對照組比較具有顯著性差異(P<0.01);用威靈仙不同提取部位處理后,它們均能降低iNOS和TNF-αmRNA表達量,其作用強弱依次為威靈仙乙酸乙酯部位、石油醚部位、正丁醇部位和水部位.
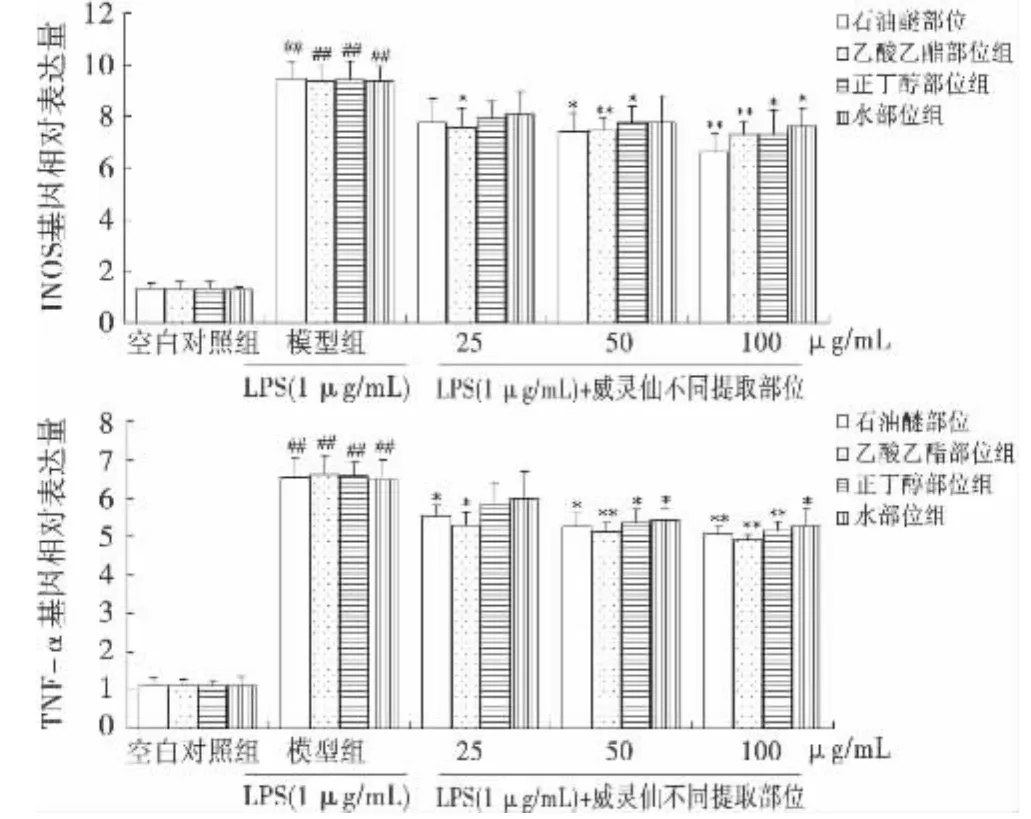
圖6 威靈仙不同提取部位對LPS刺激RAW264.7細胞iNOS和TNF-αmRNA表達量的影響
4 討 論
炎癥發生時,機體組織常常會分泌許多抗炎癥因子來保護組織免受損傷.在生理條件下,促炎因子(TNF-α、IL-1β、IL-6等)和抗炎因子(IL-4、IL-10等)的分泌在體內保持一種動態的平衡狀態.然而,當持續過量產生促炎癥因子會使得整個炎癥因子調節網絡的平衡被打破,進而誘發炎癥的級聯反應而導致不良的免疫反應和炎癥失調的疾病,如風濕性關節炎、類風濕關節炎等.中藥威靈仙為傳統的抗炎中藥,近年來研究發現其對促炎因子具有顯著的抑制作用[4],然而對其不同提取部位間作用的差異性卻鮮見報道.基于此,本研究LPS刺激RAW264.7細胞炎癥模型,比較其不同提取部位對LPS刺激的RAW264.7細胞分泌促炎因子的差異.實驗發現威靈仙威靈仙石油醚部位、乙酸乙酯部位、正丁醇部位和水部位均能不同程度抑制RAW264.7細胞分泌產生NO、iNOS、TNF-α,其作用強弱依次為乙酸乙酯部位、石油醚部位、正丁醇部位和水部位.
NO是具有廣泛生物活性的氣體分子,同時也是細胞間信息傳遞的重要調節因子,具有介導細胞免疫和炎癥反應的功能.NO是以左旋精氨酸為底物,在一氧化氮合酶(nitric oxide synthase,NOS)催化下合成的,它分為:結構型(constructive NOS,cNOS)和誘導型(inducible NOS,iNOS)兩種,其中iNOS主要存在于巨噬細胞內,生理條件下鈣/鈣調蛋白非依賴的NOS無活性表達,LPS僅刺激與炎癥有關的iNOS的表達,促使NO水平升高.研究發現機體內NO的過量生成與炎癥的發生密切相關[10-11],在炎癥區域,由于促炎因子的異常分泌,使得NO合成和釋放大量增加.大量生成的NO一方面可對細胞產生較強的細胞毒性,另一方面與氧自由基結合,生成毒性更強的ONOO-等物質,從而進一步加劇炎癥的損傷[12],因此抑制機體NO的異常合成和釋放是治療炎癥相關疾病的重要手段.實驗發現,RAW264.7細胞經LPS刺激后,其分泌iNOS水平明顯升高,NO釋放顯著增加,用威靈仙不同提取部位處理后,它們對激活狀態RAW264.7細胞iNOS活性和NO釋放均具有不同程度的抑制作用,并呈良好的劑量依賴關系.
LPS可刺激單核/巨噬細胞分泌多種促炎因子(如TNF-α、IL-6等)來誘導和加強局部炎癥反應,它們往往具有多種生物學活性,在炎癥的發生、發展以及炎癥的調控中發揮重要作用.在炎癥初期,炎癥區域的巨噬細胞分泌TNF-α,通過細胞因子級聯激活其它細胞因子(如IL-6、IL-1β等)加速炎癥部位的炎癥反應[13];在這個過程中,NF-κB扮演著極為重要的角色.炎癥初期,炎細胞分泌的 TNF-α、IL-6、IL-1β可誘導NF-κB核移位,加速促炎因子的轉錄,形成惡性循環[14].研究結果顯示LPS刺激RAW264.7巨噬細胞后,可見TNF-α分泌的大量增加;威靈仙不同提取部位均能明顯抑制LPS誘導RAW264.7巨噬細胞分泌TNF-α,并呈劑量依賴效應.
綜上所述,威靈仙具有潛在的抗炎藥理作用,其不同提取部位均能明顯抑制LPS誘導RAW264.7巨噬細胞分泌TNF-α、iNOS炎癥因子,并且同提取部位的抗炎作用效果不同,其作用強弱依次為威靈仙乙酸乙酯部位、石油醚部位、正丁醇部位和水部位.目前的研究初步證實,抑制炎癥因子的分泌和釋放可能是威靈仙發揮抗炎作用機制之一,但其具體的抗炎通路還有待進一步研究.
[1]國家藥典委員會.中華人民共和國國藥典:一部[M].北京:中國醫藥科技出版社,2010:234-235.
[2]Hsieh M S,Wang K T,Tseng S H,et al.Using 18FFDG MicroPET Imaging to Measure the Inhibitory Effects of Clematis Chinensis Osbeck on the Pro-inflammatory and Degradative Mediators Associated with Inflammatory Arthritis[J].J Ethnopharmacol,2011,136(3):511-517.
[3]Liu L F,Ma X L,Wang Y X,et al.Triterpenoid Saponins from the Roots of Clematis Chinensis Osbeck[J].J Asian Nat Prod Res,2009,11(5):389-396.
[4]趙燕強,楊立新,張憲民,等.威靈仙的成分、藥理活性和臨床應用的研究進展[J].中藥材,2008,31(3):465-470.
[5]Wu W,Xu X,Dai Y,et al.Therapeutic Effect of the Saponin Fraction from Clematis Chinensis Osbeck Roots on Osteoarthritis Induced by Monosodium Iodoacetate Through Protecting Articular Cartilage[J].Phytother Res,2010,24(4):538-546.
[6]柯頌遠.介入化療聯合威靈仙外治老年人頭頸部癌的臨床研究[J].中國老年學雜志,2003,23(4):256-257.
[7]徐先祥,夏倫祝,戴 敏,等.威靈仙總皂苷抗炎鎮痛作用研究[J].中藥藥理與臨床2005,21(4):34-35.
[8]李 特,李運曼,劉麗芳,等.威靈仙總皂苷抗類風濕性關節炎的作用機制[J].中國藥科大學學報,2009,40(2):157-160.
[9]Shin K M,Kim Y H,ParkW S,et al.Inhibition of Methanol Extract from the Fruits of Kochia Scoparia on Lipopolsaccharide Induced Nitric Oxide,Prostaglandin E2,and Tumor Necrosis Factor-a Production from Murine Macrophage RAW264.7Cells[J].Boil Pharm Bull,2004,27(4):538-543.
[10]胡亞娥,茅家慧,劉 霞,等.氧化苦參堿對脂多糖誘導的RAW264.7細胞一氧化氮及其誘導型合酶表達的影響[J].南通大學學報:醫學版,2011,31(3):166-169.
[11]李曉紅,齊 云,蔡潤蘭,等.蘆薈大黃素對LPS誘導的RAW264.7細胞NO生成及iNOS表達的影響[J].中國藥理學通報,2010,26(4):488-492.
[12]Lala P K,Chakraborty C.Role of Nitric Oxide in Carcinogenesis and Tumour Progression[J].Lancet Oncol,2001,2(3):149-156.
[13]Fleshner M,Johnson J D.Exogenous Extra-Cellular Heat Shock Protein 72:Releasing Signal(s)and Function[J].Int J Hyperthermia,2005,21(7):457-471.
[14]Xiao C,Li J,Dong X X,et al.Anti-Oxidative and TNF-αSuppressive Activities of Puerarin Derivative(4AC)in RAW264.7Cells and Collagen-Induced Arthritic rats[J].Eur J Pharmacol,2011,666(1-3):242-250.

