枸杞多糖對腦缺血再灌注損傷模型大鼠的保護作用
王昕,陳莉芬,譚昌洪,謝代鑫(1.重慶醫科大學附屬第二醫院,重慶 400010;.重慶市第六人民醫院,重慶 400060;.重慶市第三人民醫院,重慶 400014)
腦缺血再灌注損傷可造成神經元的壞死與凋亡,是腦梗死后遺癥產生的主要因素之一,而神經元凋亡會引發機體產生系列病理生理反應,因此減輕神經元凋亡對保護腦功能具有重要意義[1]。半胱氨酸蛋白酶(Caspase)家族與凋亡關系密切,Caspase-12前體位于細胞內質網中,是細胞凋亡的內質網相關性死亡途徑[2]。枸杞多糖(Lycium barbarum polysaccharides)是從寧夏特色植物枸杞(Lycium bararum)中分離出的主要多糖之一。現代藥理學研究證實,枸杞多糖有多種藥理學作用,如抗衰老、抗腫瘤、促免疫等[3-4],但對腦卒中保護還未見文獻報道。本研究擬通過大鼠腦缺血再灌注損傷模型,觀察枸杞多糖是否對其具有保護作用,為臨床腦缺血、腦卒中的治療提供理論依據。
1 材料
1.1 儀器
Mini-PROTEAN3型垂直板式電泳儀(美國Bio-Rad公司);電子天平(上海精科實業有限公司);HMIAS-2000型高清晰度彩色病理圖文分析系統(武漢同濟醫科大學)。
1.2 藥品與試劑
枸杞多糖(上海源葉生物科技有限公司,批號:91087,純度:>98%);兔抗Caspase-12抗體(美國Santa Cruz公司);辣根過氧化物(HRP)羊抗兔IgG(瑞典Amersham公司);逆轉錄-聚合酶鏈反應(RT-PCR)試劑盒(大連寶生物技術有限公司)。
1.3 動物
SPF級SD大鼠84只,♀♂兼半,體質量220~240 g,由重慶醫科大學實驗動物中心提供[實驗動物使用許可證號:SCXK(渝)2011-0002]。
2 方法
2.1 模型的復制
參照改良的Longa法[5],采用線栓法復制大鼠腦缺血再灌注損傷模型。ip 10%水合氯醛(350mg/kg)麻醉大鼠,將其仰臥固定,于頸部皮膚行常規縱行切口(約25.0mm),暴露并鈍性游離右側頸總動脈(CCA),結扎同側CCA近心端和頸外動脈(ECA)分叉部并反向拉直ECA,距CCA末端約5mm處剪口,用直徑0.26mm的魚線沿頸內動脈(ICA)方向插入,深度由分叉部算約計(18.5±0.5)mm,于ICA近心端結扎,全層縫合切口,阻斷2 h后,再灌注時抽出魚線10mm,術中室溫保持(22±2)℃。模型復制成功的判定標準:大鼠手術麻醉清醒后出現左側肢體癱瘓,無力,站立不穩,提尾時左側前爪抱爪。假手術對照僅線栓插入深度小于9mm,不閉塞大腦中動脈。
2.2 分組與給藥
84只SD大鼠隨機均分為7組,即正常對照(等容生理鹽水)組、假手術(等容生理鹽水)組、模型(等容生理鹽水)組、尼莫地平(0.5mg/kg)組與枸杞多糖高、中、低劑量(60.0、30.0、15.0mg/kg)組。于復制模型前2 d開始ig給藥,每天2次,連續3 d。
2.3 指標的測定
2.3.1 神經癥狀評分 >參考文獻評分標準[5],缺血2 h再灌注24h后觀察各組大鼠行為。0分:無任何神經功能缺失;1分:左前爪不能完全伸直;2分:向左側行走;3分:向左側轉圈成追尾狀;4分:不能自發行走,意識喪失。
2.3.2 腦組織含水量的測定 缺血2 h再灌注24h后各組隨機選取6只大鼠,麻醉后斷頭取腦,切開大鼠兩側大腦半球,左右各取兩側皮層區和基底節區兩個部位的腦組織0.2 g,用電子天平稱定其濕質量,在100℃烤箱中烘烤72h后再稱定其干質量。根據公式計算出腦組織含水量:腦組織含水量=(濕質量-干質量)/濕質量×100%。
2.3.3 RT-PCR法測定Caspase-12 mRNA的表達[6]Caspase-12引物序列為上游:5′-TCCTGGTCTTTATGTCCC-3′(GenBanknm-130422),下游:5′-CGATAGCCCAAGGAAGTG3′(GenBanknm-130422),片段長度:180 bp;內參β-actin引物序列為上游:5′-CACCCTGTGCTGCTCACCGAGGCC-3′,下游:5′-CCACACAGATGACTTGCGCTCAGG-3′,片段長度:690 bp。PCR體系:ddH2O 17.1 μl,cDNA 3 μl,10×buffer 2.5 μl,dNTPs(2.5mmol)2 μl,Taq-E(5 u/L)0.2 μl,Caspase-12、β-actin上下游引物各0.1μl。反應條件:94℃10min預變性,94℃40 s變性,51.5℃1min退火,72℃1min延伸,32個循環,72℃7min終止。
2.3.4 Western blot法測定Caspase-12蛋白的表達 大鼠迅速斷頭取腦,冰上分離缺血側頂葉大腦皮質約100mg,冰上研磨組織后加預冷的蛋白裂解液,繼續碾磨至液態,然后于4℃下,以離心半徑為8 cm、12000 r/min離心30min,留上清液,取40μl用BCA法進行蛋白定量測定,所剩上清液按4∶1(V/V)的比例加變性PAGE膠上樣緩沖液,100℃下水浴10min。取蛋白樣品(40μg)采用10%SDS-PAGE垂直電泳進行分離,然后轉至PVDF膜上進行免疫反應。5%脫脂奶粉37℃封閉2 h,然后依次加入兔抗Caspase-12抗體,37℃孵育2 h,4℃過夜;偶聯用HRP羊抗兔IgG室溫孵育2 h,LumiGLO(20×)發光劑中X-感光盒內曝光。以上反應均在塑料袋內進行,其間用PBS充分洗滌。將膠片進行掃描或拍照,采用病理圖文分析系統進行圖像分析,獲取各組蛋白條帶的平均光密度(OD),內參為GAPDH,目的蛋白與內參光密度比值即為目的蛋白的相對值。
2.4 統計學方法
3 結果
3.1 枸杞多糖對模型大鼠神經癥狀評分的影響
正常對照組與假手術組大鼠神經癥狀均正常;模型組大鼠神經癥狀評分增加,與假手術組比較差異有統計學意義(P<0.01),表明模型復制成功;與模型組比較,枸杞多糖高、中劑量組大鼠神經癥狀評分減少,差異有統計學意義(P<0.01或P<0.05),表明受損機體得到一定修復。枸杞多糖對模型大鼠神經癥狀評分的影響見表1。
表1 枸杞多糖對模型大鼠神經癥狀評分的影響()Tab 1 Effects of L.barbarum polysaccharide on neural symptoms score of model rats()
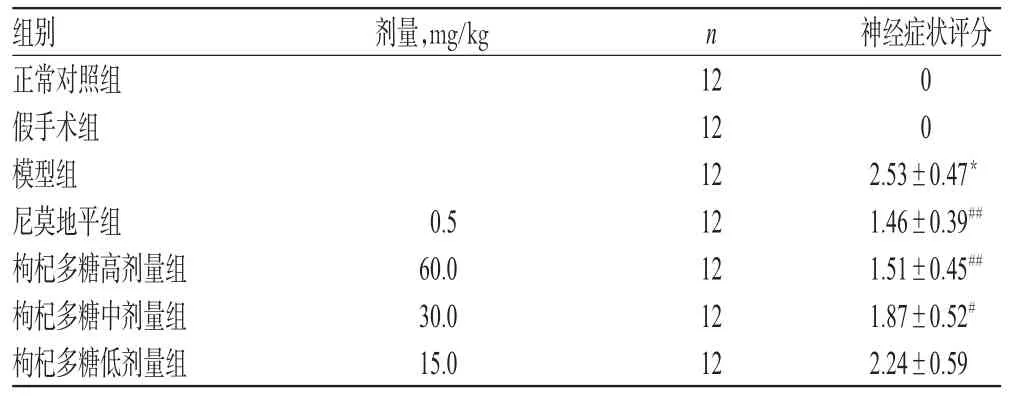
表1 枸杞多糖對模型大鼠神經癥狀評分的影響()Tab 1 Effects of L.barbarum polysaccharide on neural symptoms score of model rats()
與假手術組比較:*P<0.01;與模型組比較:#P<0.05,##P<0.01vs.sham-operation group:*P<0.01;vs.model group:#P<0.05,##P<0.01
組別正常對照組假手術組模型組尼莫地平組枸杞多糖高劑量組枸杞多糖中劑量組枸杞多糖低劑量組劑量,mg/kg n 神經癥狀評分0 02.53±0.47*1.46±0.39##1.51±0.45##1.87±0.52#2.24±0.590.560.030.015.012121212121212
3.2 枸杞多糖對模型大鼠腦組織含水量的影響
與假手術組比較,模型組大鼠腦含水量增加,差異有統計學意義(P<0.01);與模型組比較,枸杞多糖高、中劑量組大鼠腦含水量減少,差異有統計學意義(P<0.01或P<0.05)。枸杞多糖對模型大鼠腦組織含水量的影響見表2。
表2 枸杞多糖對模型大鼠腦組織含水量的影響()Tab 2 Effects of L.barbarum polysaccharide on water content of cerebral tissue in model rats()
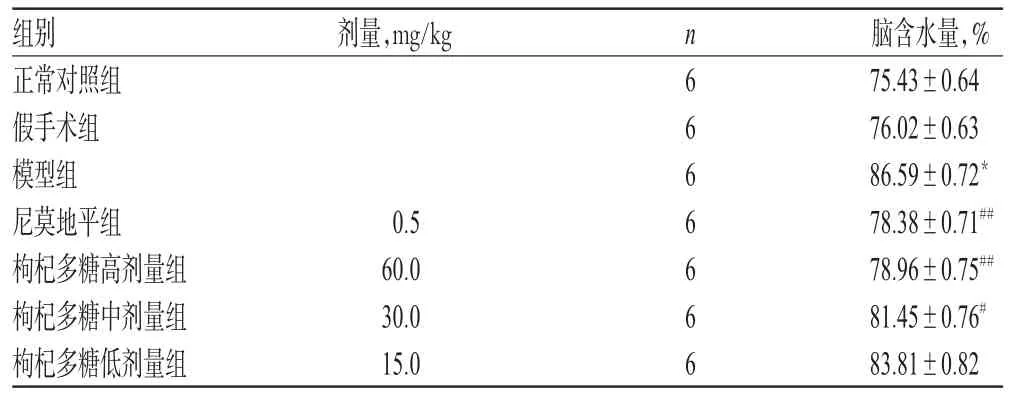
表2 枸杞多糖對模型大鼠腦組織含水量的影響()Tab 2 Effects of L.barbarum polysaccharide on water content of cerebral tissue in model rats()
與假手術組比較:*P<0.01;與模型組比較:#P<0.05,##P<0.01vs.sham-operation group:*P<0.01;vs.model group:#P<0.05,##P<0.01
組別正常對照組假手術組模型組尼莫地平組枸杞多糖高劑量組枸杞多糖中劑量組枸杞多糖低劑量組腦含水量,%75.43±0.6476.02±0.6386.59±0.72*78.38±0.71##78.96±0.75##81.45±0.76#83.81±0.82劑量,mg/kg 0.560.030.015.0 n 6 6 6 6 6 6 6
3.3 枸杞多糖對模型大鼠腦組織Caspase-12 mRNA表達的影響
由前述實驗可看出,枸杞多糖低劑量組未達到明顯變化,因此,以下實驗采用枸杞多糖高、中劑量組進行。與假手術組比較,模型組大鼠腦組織Caspase-12 mRNA表達增強,差異有統計學意義(P<0.01);與模型組比較,枸杞多糖高、中劑量組大鼠腦組織Caspase-12 mRNA表達減弱,差異有統計學意義(P<0.01)。Caspase-12 mRNA的表達見圖1。
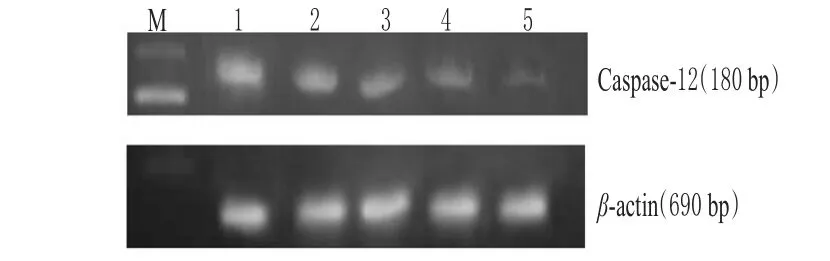
圖1 Caspase-12 mRNA的表達1.模型組;2枸杞多糖中劑量組;3.枸杞多糖高劑量組;4.尼莫地平組;5.假手術組;M.蛋白標記Fig 1 The expression of Caspase-12 mRNA1.model group;2.L.barbarum polysaccharide medium-dose group,3.L.barbarum polysaccharide high-dose group;4.nimodipine group;5.shamoperation group;M.Mark
3.4 枸杞多糖對模型大鼠腦組織Caspase-12蛋白表達的影響
與假手術組比較,模型組大鼠腦組織Caspase-12蛋白表達增強,差異有統計學意義(P<0.01);與模型組比較,枸杞多糖高、中劑量組大鼠腦組織Caspase-12蛋白表達減弱,差異有統計學意義(P<0.01)。Caspase-12蛋白的表達見圖2。
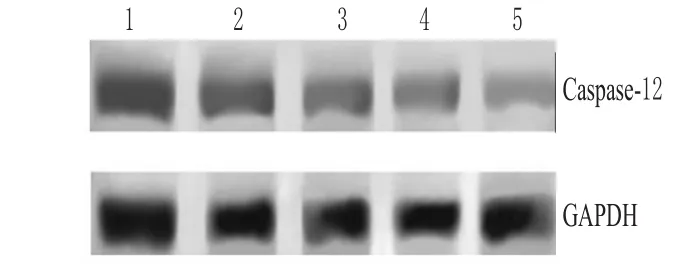
圖2 Caspase-12蛋白的表達1.模型組;2.枸杞多糖中劑量組;3.枸杞多糖高劑量組;4.尼莫地平組;5.假手術組Fig 2 The expression of Caspase-12 protein1.model group;2.L.barbarum polysaccharide medium-dose group,3.L.barbarum polysaccharide high-dose group;4.nimodipine group;5.sham-operation group
4 討論
腦缺血再灌注損傷是引起多種腦血管病的重要病理生理機制,故抗腦缺血再灌注損傷是治療腦梗死的有效措施。許多中藥對腦缺血再灌注損傷有保護作用,主要表現為抗氧化及病理損傷、減輕興奮性氨基酸的神經毒性、清除自由基、減輕鈣超載、影響血小板與血栓形成、影響基因表達與凋亡調控等諸方面[7-8]。本研究采用大鼠腦缺再灌注損傷模型探討枸杞多糖對腦缺血再灌注損傷的影響,結果表明,枸杞多糖可以明顯減少缺血再灌注損傷模型大鼠腦含水量,減輕腦水腫,說明其具有明顯的腦保護作用。
Mouw G等[9-10]發現,敲除Caspase-12基因的細胞雖然仍對其他各種凋亡誘導因素敏感,但對內質網應激誘導的凋亡卻產生耐受,說明Caspase-12在內質網應激誘發凋亡的通路中具有重要作用。本研究表明,枸杞多糖可以明顯減弱腦缺血再灌注損傷模型大鼠Caspase-12 mRNA與蛋白的表達,說明其可通過抑制Caspase-12酶的活性進而穩定內質網從而起到抑制神經細胞凋亡的作用。
本研究表明,高、中劑量枸杞多糖可使腦缺血再灌注損傷模型大鼠神經癥狀評分減少、腦含水量減少、Caspase-12 mRNA及蛋白表達減弱,說明枸杞多糖對腦缺血再灌注損傷模型大鼠有一定保護作用。
[1]Li Q,Huang XJ,He W,et al.Neuroprotective potential of fasudil mesylate in brain sschemia-reperfusion injury of rats[J].Cell Mol Neurobiol,2009,29(2):169.
[2]張建華,趙澤燕,張華.Caspase-12在胎鼠宮內缺血/再灌注后腦神經元凋亡中的作用[J].重慶醫學,2007,36(9):834.
[3]Gan L,Hua ZS,Liang YX,et al.Immunomodulation and antitumor activity by a polysaccharide-protein complex from Lycium barbarum[J].Int Immunopharmacol,2004,4(4):563.
[4]Yu MS,Ho YSh,Yuen WH,et al.Cytoprotective effects of Lycium barbarum against reducing stress on endoplasmic reticulum[J].Int J Mol Med,2006,17(6):1157.
[5]Longa EZ,Weinstein PR,Carlson S,et al.Reversible middle cerebral artery occlusion without craniectomy in rats[J].Stroke,1989,20(1):84.
[6]張鴻,宋利春,賈春紅,等.大鼠腦缺血/再灌注后神經元凋亡及Caspase-12 mRNA和蛋白表達的改變[J].中國藥理學通報,2008,24(8):1069.
[7]王寶亮,韓艷麗.中風皂貝化痰膠囊對大鼠腦缺血再灌注損傷后的神經保護作用及血管內皮生長因子表達的影響[J].中國實驗方劑學雜志,2011,17(3):138.
[8]楊德森,游秋云,田先翔,等.紅景天苷對老齡大鼠局灶性腦缺血再灌注損傷的保護作用[J].中國醫院藥學雜志,2011,31(9):738.
[9]Mouw G,Zechel JL,Gamboa J,et al.Activation of caspase-12,an endoplasmic reticulum resident caspase,after permanent focal ischemia in rat[J].Neuroreport,2003,14(2):183.
[10]Hu Q,Lee SY,O'Kusky JR,et al.Signalling through the type 1 insulin-like growth factor receptor(IGF1R)interacts with canonical Wnt signalling to promote neural proliferation in developing brain[J].ASN Neuro,2012,4(5):92.

