在低蛋白質飼料中補充必需氨基酸對大口黑鱸生長、體組成和免疫指標的影響
陳乃松 梁勤朗 肖溫溫 周恒永 馬秀麗 趙 明
?
在低蛋白質飼料中補充必需氨基酸對大口黑鱸生長、體組成和免疫指標的影響
陳乃松 梁勤朗 肖溫溫 周恒永 馬秀麗 趙 明
(上海海洋大學水產與生命學院, 上海 201306)
為了研究在低蛋白質飼料中補充晶體必需氨基酸對大口黑鱸生長、體組成和免疫指標的影響, 根據魚體的必需氨基酸組成模式設計了7種等能的試驗飼料。其中4種飼料(45CP、40CP、35CP和30CP)的粗蛋白質水平分別為45%、40%、35%和30%, 另3種飼料(40AA、35AA和30AA)是在低蛋白質飼料(40CP、35CP和30CP)的基礎上添加必需氨基酸, 使它們的必需氨基酸含量與45CP(對照組)相一致。用上述飼料對初始體重為(10.13 ± 0.01) g的大口黑鱸進行了89d的飼養試驗。飼養試驗在室內循環水養殖系統中進行, 每種飼料設3個重復, 每重復放養30尾魚。方差分析顯示: 試驗魚的生長性能、飼料效率、全魚和肌肉的粗蛋白質含量、成活率以及免疫指標均隨著飼料蛋白質含量的降低而顯著降低(<0.05)。添加必需氨基酸的35AA和30AA的飼料效率和蛋白質保留率分別顯著高于對應的未添加必需氨基酸的35CP和30CP組(<0.05), 但仍顯著低于45CP組(<0.05)。40AA的試驗魚血清溶菌酶活性和血清補體活性與45CP組差異不顯著(>0.05)。35AA和30AA組的頭腎白細胞呼吸爆發活性顯著高于35CP和30CP組(<0.05)。30AA組的全魚粗蛋白質含量以及肥滿度顯著高于30CP(<0.05)。各組試驗魚的水分和灰分均無顯著差異(>0.05)。回歸分析顯示: 在低蛋白質飼料中補充晶體必需氨基酸對大口黑鱸幼魚的生長、飼料效率和蛋白質保留率所產生的影響與其引起增加了的飼料蛋白質水平而不是飼料的必需氨基酸水平正相關。研究表明, 在低蛋白質飼料中補充的晶體必需氨基酸對大口黑鱸的生長、體組成和免疫指標產生的有益作用不及等量的以蛋白質為來源的必需氨基酸。
大口黑鱸; 飼料; 蛋白質; 必需氨基酸; 生長; 體組成; 免疫指標
蛋白質是動物生長、發育和健康等不可缺少的營養素。動物攝取蛋白質即是為了獲得氨基酸, 尤其是平衡的必需氨基酸[1]。研究表明, 魚類(特別是肉食性魚類)的飼料蛋白質最適需求量遠高于陸上動物[2]。這使得蛋白質時常是魚類飼料成本中花費最大的營養成分。同時, 當飼料中的蛋白質水平過高時, 還會因蛋白質的分解代謝引起過多的氮排放而產生水環境的污染。
在禽畜的低蛋白質飼料中, 補充晶體必需氨基酸能有效地改善飼料氨基酸平衡, 促進動物生長, 提高飼料效率和減少氮排放等[3]。然而, 在魚類的低蛋白質飼料中補充晶體必需氨基酸能否發揮同樣的效果則有不盡一致的研究報道[4, 5]。因而評價特定的養殖魚類對晶體必需氨基酸的利用效果, 對于了解其氨基酸代謝特點和開拓蛋白質飼料的來源具有理論和實踐意義。
大口黑鱸(), 俗名加州鱸, 具有生長快、抗病力強和產量高等特點, 是我國重要的淡水養殖魚類。但大口黑鱸專用人工配合飼料在我國尚未研發成功, 養殖生產中以冰鮮雜魚作飼料。大口黑鱸屬于典型的肉食性魚類, 理應其飼料蛋白質的需求量應當較高, 但已有的研究卻未得出一致的最適飼料蛋白質需求量的結論[6—10]。關于大口黑鱸對飼料中必需氨基酸的需求量的研究只見有賴氨酸[11]、蛋氨酸[12]和精氨酸[13]的最適需求量的報道。因此, 關于大口黑鱸飼料的蛋白質和必需氨基酸需求量的研究尚有待進一步地深入。
本研究通過養殖試驗評估不同飼料蛋白質水平以及在低蛋白質水平基礎上補充晶體必需氨基酸對大口黑鱸生長、體組成和免疫指標的影響, 著重探討在較低蛋白質飼料中添加晶體必需氨基酸的有效性, 進一步豐富大口黑鱸的蛋白質和必需氨基酸的營養學知識。
1 材料與方法
1.1 飼料配制
本試驗設計了7種等能的試驗飼料, 其配方與組成如表1。其中4種飼料(45CP、40CP、35CP和30CP)的粗蛋白質水平分別為45%、40%、35%和30%, 其必需氨基酸與非必需氨基酸含量比值均相同。另3種飼料(40AA、35AA和30AA)是在40CP、35CP和30CP的基礎上添加晶體必需氨基酸, 使它們的必需氨基酸含量與45CP相一致, 但這3種飼料的非必需氨基酸含量仍與原各自的基礎飼料相同。因此, 45CP被作為3種添加晶體必需氨基酸飼料的對照組。所有試驗飼料的必需氨基酸組成模擬與大口黑鱸全魚相似的必需氨基酸組成模式, 但其中賴氨酸(未發表數據)、蛋氨酸[12]含量參照本實驗室先前取得的大口黑鱸對它們的最適需求量的研究結果。試驗飼料的氨基酸組成分析值如表2。
所添加的晶體氨基酸事先經過如下的包膜處理:稱取待包膜晶體氨基酸質量的5%的醇溶玉米蛋白, 將其溶解于95%的乙醇中制成10%的玉米蛋白乙醇溶液, 向該溶液中加入待包膜的晶體氨基酸并混合均勻, 于50 ℃烘干后粉碎備用。
所有飼料原料都經過粉碎且過80目標準篩。各組分混合均勻后, 加35%水再一次混合均勻。按實驗魚生長過程中個體的變化, 用絞肉機制成直徑3—5 mm長條, 再切成長約5—10 mm顆粒, 于–20 ℃下保存備用。
1.2 養殖試驗
試驗用魚購自于一個商業性的大口黑鱸育苗場, 在室內循環水養殖系統中馴化4周, 以適應養殖環境。經馴化后, 實驗魚被饑餓24h, 選取體重相近的魚分組作養殖試驗。試驗魚按上述7種飼料處理, 每處理3重復, 被隨機分配于21個800 L的水槽中, 每水槽放養初始平均體重為(10.13±0.01) g的試驗魚30尾。本試驗采取表觀飽食投喂, 每天投飼兩次(8:00和16:00)。養殖水槽處于一個共同的循環水控制系統之中, 養殖用水經海綿層和珊瑚砂過濾, 紫外燈殺菌并且不間斷充氣。水溫控制在(28 ± 1)℃, 氨氮為(0.25 ± 0.05) mg/L, pH為7.2 ± 0.2。光周期為自然光照。養殖試驗共持續89d。
1.3 樣品采集
在養殖試驗開始前, 隨機選取40尾試驗魚作初始樣本, 以測定全魚體組成。在養殖試驗過程中按Lee[14]的方法收集糞便樣品。養殖試驗結束后, 饑餓24h, 以各養殖水槽為單元稱取體重, 并隨機抽取10尾魚, 其中5尾作全魚營養成分分析, 另外5尾在量取體重和體長后, 進行尾靜脈取血, 采集內臟和背部兩側肌肉。上述樣品均于–80℃超低溫冰箱中保存以待分析。剩余的魚繼續飼養用于免疫試驗的活體采樣。
1.4 化學分析
采用105℃常壓干燥法, 凱氏定氮法(Kjeltec- 2200, Foss Tecator, 瑞典)和550℃下灼燒法分別測定飼料和魚體的水分、粗蛋白質和灰分。采用索氏脂肪測定儀(Sox-416, Gerhardt, 德國)測定飼料的粗脂肪[15], 采用氯仿-甲醇法[16]測定魚體的粗脂肪。總能量用氧彈量熱儀(6200, Parr, 美國)測定。飼料中的氨基酸測定參照文獻[17]的方法, 用氨基酸自動分析儀(S-433D, Sykam, 德國)分析。飼料中色氨酸因酸解破壞而不能被分析, 其含量是根據NRC (2011)[18]提供的各飼料原料中所含色氨酸的理論值和晶體色氨酸的添加量計算而得。
1.5 免疫測定
血清溶菌酶活性采用比濁法測定[19]。經典途徑血清補體活性測定參照Zhou,[13]的方法, 采用抗綿羊紅細胞溶血素(浙江玉環生物制品廠)致敏綿羊紅細胞, 以其作為靶細胞進行補體經典途徑溶血分析。頭腎白細胞分離參照陳乃松[12]的方法。呼吸爆發活性測定參照Secombes[20]的方法。
1.6 計算公式
特定生長率(Specific growth rate,, %/d)= 100 × (ln終末體重–ln初始體重)/試驗天數;
攝食量(Feed intake,, g/尾) = 飼料攝入量/[(初始魚尾數+終末魚尾數)/2];
飼料效率(Feed efficiency,)= (終末體重–初始體重)/攝食量;
蛋白質保留率(Protein retention,, %)=100 ×體組織蛋白質增加量/蛋白質攝入量;
肥滿度(Condition factor,, g/cm3)=100 ×魚體重/魚體長3;
肝體比(Hepatosomatic index,, %)=100 ×肝臟重/魚體重;
臟體比(Viscerasomatic index,, %)=100 ×內臟重/魚體重;
成活率(Survival rate,, %)=100 ×終末魚尾數/初始魚尾數。
1.7 數據分析
相關數據采用平均值±標準誤表示, 采用SPSS 17.0統計軟件以飼料為單因素作方差分析(one-way ANOVA), 差異顯著時用Duncan’s法作多重比較。統計顯著水平設定為<0.05。
表1 試驗飼料配方及概略組成(%,風干基礎)

Tab.1 Formulation and approximate composition of experimental diets (%, on air-dry basis)
注:1)基礎蛋白質成分(風干基礎): 魚粉56.72%, 玉米蛋白粉7.46%, 谷朊粉11.94%, 豆粕16.42%, 噴干血球粉7.46%;2)預混料: 魷魚內臟粉1.00%, 酵母粉1.00%, 酵母提取物1.00%, 大豆磷脂粉1.00%, 多維a)0.80%, 多礦b)1.00%, 維生素C 0.05%, 三氧化二鉻0.50%, 氯化膽堿0.30%;3)包膜必需氨基酸: 蛋氨酸4.98%, 賴氨酸13.11%, 蘇氨酸7.28%, 纈氨酸12.90%, 異亮氨酸9.33%, 亮氨酸20.92%, 苯丙氨酸10.52%, 組氨酸6.18%, 精氨酸12.49%, 色氨酸2.28%;a)每千克飼料中添加: A 16000 IU, D38000 IU, K314.72 mg, B117.80 mg, B248.00 mg, B629.52 mg, Bl20.24 mg, E 160 mg, C 800 mg, 煙酸胺79.20 mg, 泛酸鈣73.60 mg, 葉酸6.40 mg, 生物素0.64 mg, 肌醇320 mg, 氯化膽堿1500 mg,-肉堿100 mg;b)每千克飼料中添加: 銅(CuSO4·5H2O) 2.00 mg, 鋅 (ZnSO4·5H2O) 34.44 mg, 錳(MnSO4·75H2O) 6.20 mg, 鐵 (FeSO4·7H2O) 21.09 mg, 碘(Ca(IO3)2)1.63 mg, 硒 (Na2SeO3) 0.18 mg, 鈷 (CoCl2·5H2O) 0.24 mg, 鎂(MgSO4·H2O) 52.70 mg
Note:1)Basal protein ingredients (air-dry basis): fish meal 56.72%, corn gluten meal 7.46%, wheat gluten meal 11.94%, soybean meal 16.42%, spray-dried blood meal 7.46%;2)Premix: squid viscera meal 1.00%, brewer’s yeast meal 1.00%, brewer’s yeast extract 1.00%, soybean phospholipid 1.00%, vitamin premixa)0.80%, mineral premixb)1.00%, ascorbic acid 0.05%, chromic oxide 0.50%, choline chloride 0.30%;3)Coated essential amino acids: methionine 4.98%, lysine 13.11%, threonine 7.28%, valine 12.90%, isolecine 9.33%, lecinine 20.92%, phenylalanine 10.52%, histidine 6.18%, arginine 12.49%, tryptophane 2.28%;a)Added to a kilogram of diet: vitamin A 16000 IU, vitamin D38000 IU, vitamin K314.72 mg, vitamin B117.80 mg, vitamin B248.00 mg, vitamin B629.52 mg, vitamin Bl20.24 mg, vitamin E 160 mg, ascorbic acid 800 mg, niacinamide 79.20 mg, calcium--pantothenate 73.60 mg, folic acid 6.40 mg, biotin 0.64 mg, inositol 320 mg, choline chloride 1500 mg,-carnitine 100 mg;b)Added to a kilogram of diet: Cu (CuSO4·5H2O) 2.00 mg, Zn (ZnSO4·5H2O) 34.44 mg, Mn (MnSO4·75H2O) 6.20 mg, Fe (FeSO4·7H2O) 21.09 mg, I (Ca(IO3)2)1.63 mg, Se (Na2SeO3) 0.18 mg, Co (CoCl2·5H2O) 0.24 mg, Mg (MgSO4·H2O) 52.70 mg
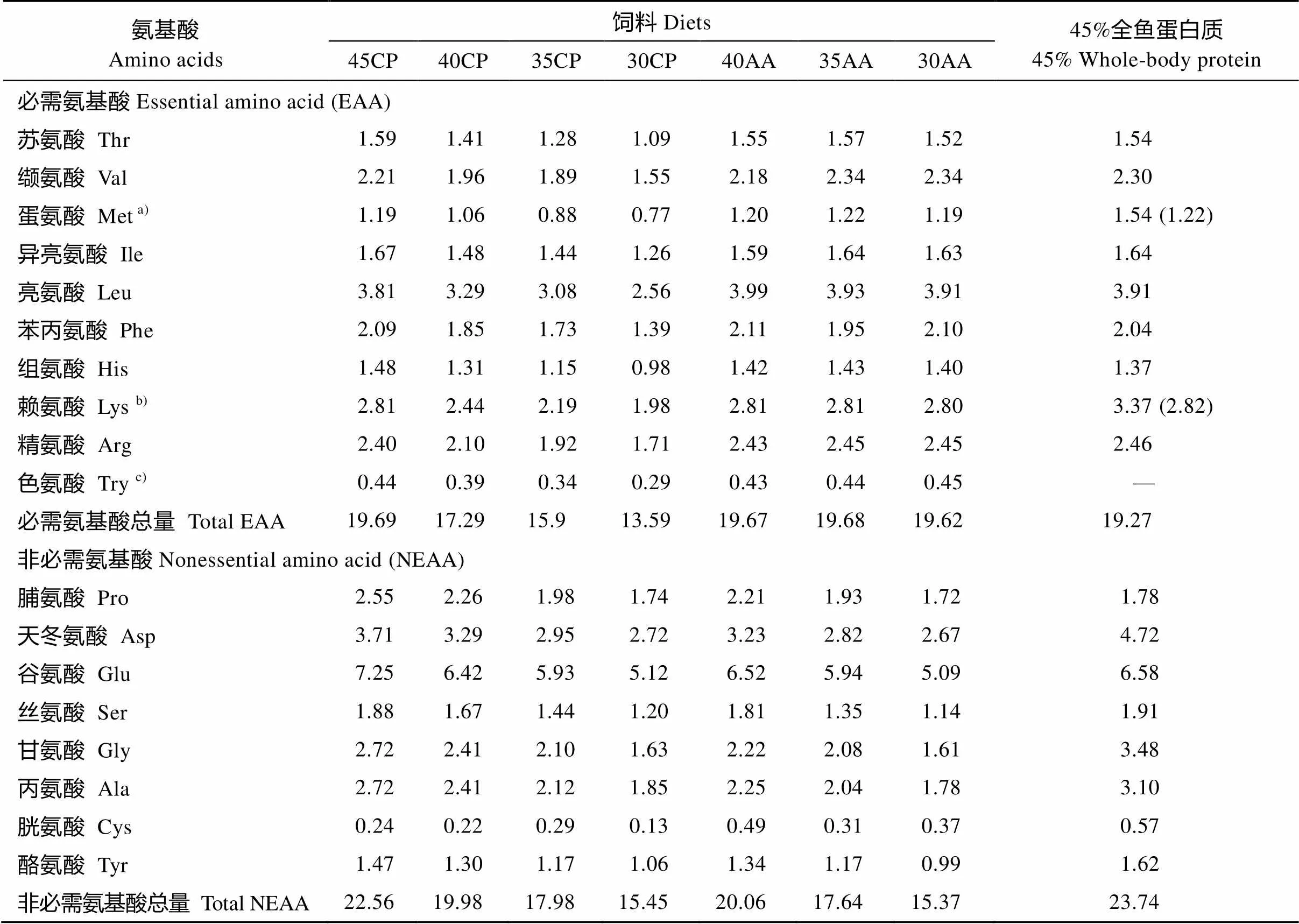
表2 試驗飼料的氨基酸組成分析(%, 風干基礎)
注:a)和b)分別為大口黑鱸飼料中蛋氨酸[12]和賴氨酸(待發表)需求量;c)色氨酸含量根據NRC(2011)[18]提供的各飼料原料中所含色氨酸含量和晶體色氨酸的添加量計算而得
Note:a)andb), the dietary methionine[12]and lysine (unpublished) requirements of largemouth bass.c), tryptophane concentrations are calculated according to the ingredient data from NRC (2011)[18]and the amounts of supplemented crystalline tryptophan
2 結果
2.1 試驗魚的生長、飼料利用率和成活率
表3顯示, 飼料的蛋白質水平和晶體必需氨基酸的補充對試驗魚的生長、飼料利用率和成活率均產生顯著影響(<0.05)。隨著飼料蛋白質水平的降低, 試驗魚的特定生長率、飼料效率、蛋白質保留率和成活率呈顯著下降趨勢(<0.05)。添加必需氨基酸的35AA和30AA組的飼料效率、蛋白質保留率和成活率分別顯著高于對應的未添加必需氨基酸的35CP組和30CP組(<0.05), 但40AA組與40CP組之間的生長、飼料效率和成活率無顯著性的差異(>0.05)。在生長方面, 僅有30AA組的特定生長率顯著高于30CP組(<0.05), 而40AA組和35AA組均與對應的40CP組和35CP組無顯著性差異(>0.05)。添加必需氨基酸的40AA、35AA和30AA組與對照組45CP相比, 除40AA組的特定生長率與對照組無顯著性差異外, 其他添加必需氨基酸的兩組的特定生長率、飼料效率和蛋白質保留率均顯著地低于45CP對照組(<0.05)。
回歸分析得出, 無論是沒有添加晶體必需氨基酸的45CP、40CP、35CP和30CP的飼料還是添加了晶體必需氨基酸的40AA、35AA和30AA飼料, 它們的蛋白質水平(CP和AA)與試驗魚的生長(1SGR和2SGR)、飼料效率(1FE和2FE)和蛋白質保留率(1PR和2PR)之間都存在著高度相關的線性關系。關系式分別為:1SGR= 0.0311CP+ 0.7196,2= 0.9892;2SGR= 0.0261AA+ 0.9360,2= 0.8354;1FE= 0.0431CP– 0.4365,2= 0.9955;2FE= 0.0351AA– 0.1984,2= 0.9764;1PR= 1.2057CP– 3.1931,2= 0.9814;2PR= 0.5743AA+ 22.231,2= 0.9748。然而, 就3種添加了晶體必需氨基酸的飼料而言, 它們的必需氨基酸水平卻與生長、飼料效率和蛋白質保留率不呈現出線性正相關。
2.2 試驗魚的體組成、體型、臟體比和肝體比
由表4可知, 試驗魚全魚和肌肉的粗蛋白質水平隨著飼料蛋白質含量減少而顯著降低(<0.05)。全魚的粗脂肪含量則呈遞增趨勢, 但肌肉中的粗脂肪含量未受顯著的影響(>0.05)。添加晶體必需氨基酸的飼料35AA和30AA與各自對應的35CP和30CP相比, 能顯著增加全魚的蛋白質含量, 但仍低于對照組45CP試驗魚的蛋白質含量(<0.05)。全魚和肌肉的水分和粗灰分未受飼料的影響(>0.05)。
試驗魚肥滿度、臟體比和肝體受到飼料蛋白質水平和添加晶體必需氨基酸的影響(表5)。飼料蛋白質水平降低, 試驗魚的肥滿也降低; 30AA組的肥滿度顯著高于30CP組(<0.05)。臟體比和肝體比受飼料蛋白質水平的影響呈現由下降到上升的趨勢, 但添加必需氨基酸并未使這兩個指標呈現顯著的不同(>0.05)。
2.3 試魚的免疫指標
如表6所示, 試驗魚的血清溶菌酶活性、補體活性和頭腎白細胞呼吸爆發活性隨飼料蛋白質水平降低而顯著下降(<0.05)。在飼料中添加必需氨基酸能不同程度地提高有關免疫指標。40AA組的血清溶菌酶活性和血清補體活性與45CP組相比, 均無顯著差異(>0.05), 但30AA組顯著低于45CP組(<0.05)。35AA和30AA的頭腎白細胞呼吸爆發活性均顯著高于相對應的35CP和30CP組, 但顯著低于45CP 對照組(<0.05)。
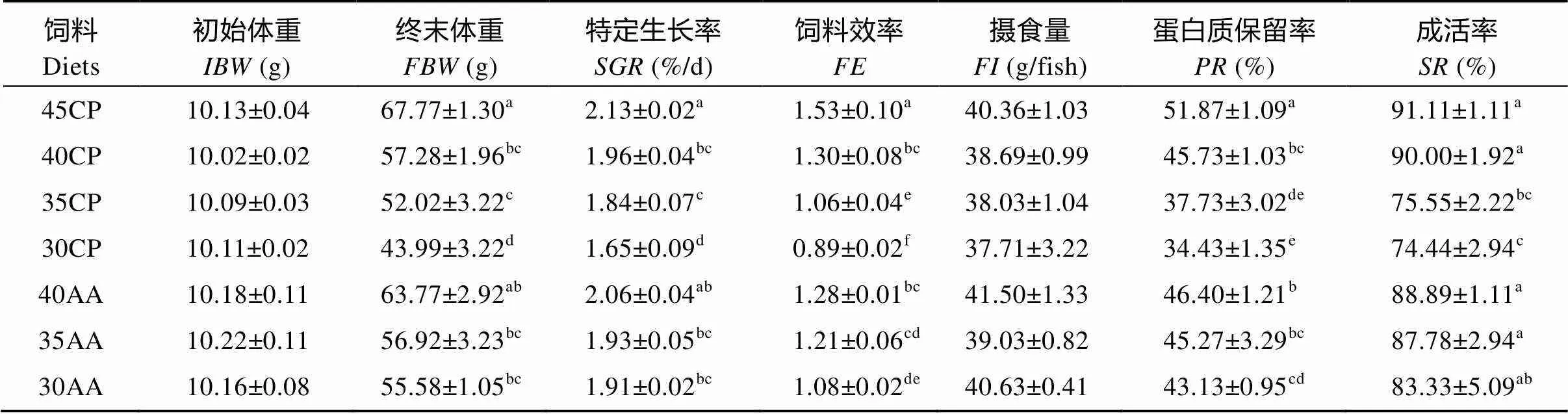
表3 飼料蛋白質水平和必需氨基酸的補充對大口黑鱸生長和飼料利用的影響(平均值±標準誤)
注: 同列數據無字母或具相同上標字母表示差異不顯著(>0.05)。下表同
Note: In the same column, values with no letter or the same superscript means no significant difference (>0.05). The same applies bellow
表4 飼料蛋白質水平和必需氨基酸的補充對大口黑鱸體組成的影響(平均值±標準誤)

Tab.4 Effects of dietary protein levels and EAA supplementation on composition of largemouth bass (mean ± SE)
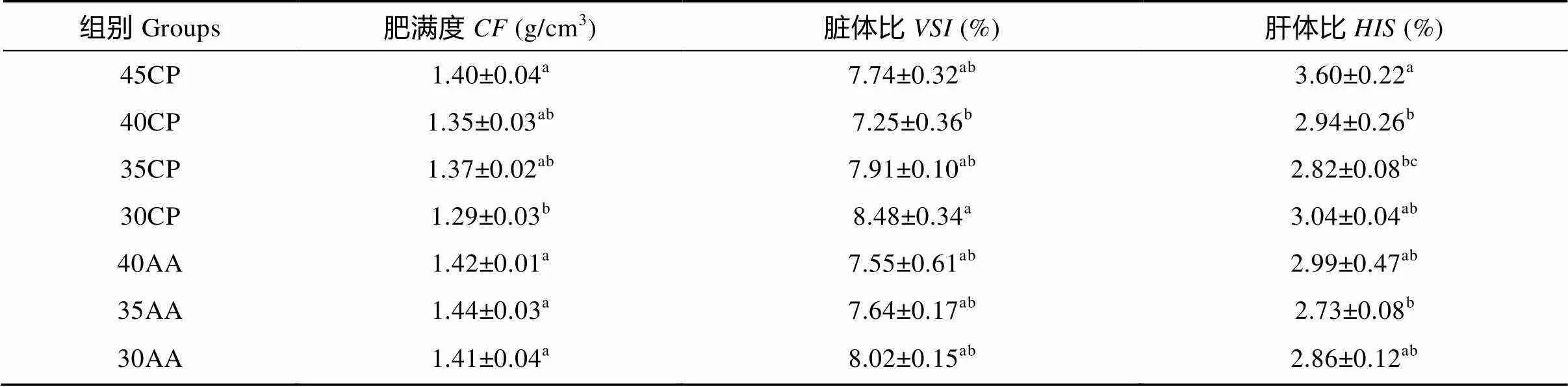
表5 飼料蛋白質水平和必需氨基酸的補充對大口黑鱸體型、肝體比、臟體比的影響(平均值±標準誤)
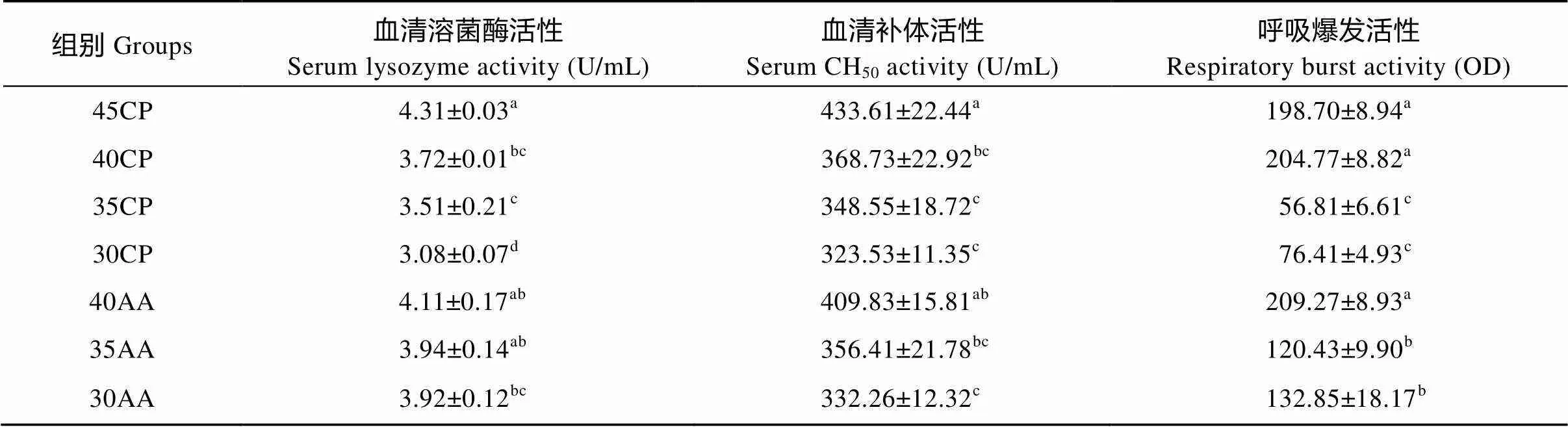
表6 飼料蛋白質水平和必需氨基酸的補充對大口黑鱸免疫指標的影響(平均值±標準誤)
3 討論
3.1 飼料的蛋白質水平對大口黑鱸生長、體組成和免疫指標的影響
本研究的45CP至30CP飼料的蛋白質水平呈梯度下降, 但這些飼料的氨基酸的組成模式相同。因此, 上述飼料引起的生長等指標的變化應歸因于飼料的蛋白質水平。隨著飼料蛋白質水平從45%降至30%, 試驗魚的生長、飼料利用率和免疫指標均顯著降低(表3和表6)。飼料的蛋白質水平對牙鲆()[21]和寶石鱸()[22]等魚類的生長也有類似的情形。如果以本研究的特定生長率、飼料效率和蛋白質保留率作判斷, 大口黑鱸飼料適宜的蛋白質需要量應在45%或以上。但就飼料效率和蛋白質保留率而言, 45CP和40CP飼料已取得了比其他研究更加優異的效果[11—13]。本研究在這一方面所取得的突破也將為大口黑鱸高效實用飼料的配制提供借鑒。

飼料的蛋白質水平對魚類的免疫力影響的研究報道尚不多見。Kiron,[29]對虹鱒()的研究顯示, 攝食35%蛋白質飼料的試驗魚的血清溶菌酶活性顯著高于攝食較低蛋白質飼料組, 但與高蛋白飼料組的差異不顯著。蔡春芳等[30]的試驗表明, 飼料蛋白質水平對異育銀鯽()免疫力有顯著影響, 飼料蛋白質水平在28%時免疫力最高, 過低或過高的飼料蛋白質水平都將導致試驗魚的免疫力下降。王吉橋等[31]在對黃顙魚()的研究也同樣發現, 與投喂蛋白質為30%和46%的飼料相比, 投喂蛋白質含量為38%的飼料時, 試驗魚的免疫指標最佳。在本試驗中, 攝取45CP與40CP的試驗魚的血清補體活性、頭腎呼吸暴發活性均無顯著差異, 但隨著飼料蛋白質含量進一步的降低, 試驗魚的這兩個免疫指標呈現出顯著降低的趨勢。這說明適宜的飼料蛋白質水平為大口黑鱸擁有良好的免疫力所必需, 但飼料蛋白質水平過高對其免疫指標則無明顯的促進作用。
3.2 飼料中添加晶體必需氨基酸對大口黑鱸生長、體組成和免疫指標的影響
本研究得出, 在較低蛋白質的飼料中添加晶體必需氨基酸能發揮改善生長和蛋白質保留率的作用。由35AA與35CP 以及30AA與30CP相比可知, 攝食添加必需氨基酸飼料的試驗魚的特定生長率和飼料效率分別提高了4.89%—15.76%和14.15%— 21.35%。40AA與對照組45CP相比卻發現, 攝食40AA的試驗魚的蛋白質保留率、特定生長率與攝食45CP的試驗魚相比差異不顯著, 但飼料效率仍有顯著的差異; 而35AA和30AA的試驗魚與45CP的試驗魚相比, 上述各項指標均有顯著差異。這一方面表明, 在低蛋白質飼料中, 以晶體氨基酸補足必需氨基酸能改善大口黑鱸的生長、飼料效率和蛋白質利用率; 另一方面又說明, 僅僅補足必需氨基酸的飼料難以全面提高至以魚粉為主要蛋白源并具有適宜水平的飼料所產生的總體效用。這與Gaylord,[32]在虹鱒()的試驗中得出的結論相似。該試驗通過向飼料中補充晶體賴氨酸、蛋氨酸和蘇氨酸, 虹鱒飼料的蛋白質水平由46%降至41.5%, 對虹鱒()的生長無影響。Cheng,[33]和Botaro,[34]的研究也指出, 補足晶體必需氨基酸能夠分別降低5%和3%的飼料蛋白質水平而不影響試驗魚的正常生長。但上述情況與Yamamot,[35]關于虹鱒()的研究結果有所不同。該研究通過向以魚粉為主要蛋白源的試驗飼料中添加晶體必需氨基酸至需求量的1.2倍, 飼料的粗蛋白質含量從45%降至30.6%, 不僅對試驗魚的生長沒有負面影響, 而且還提高蛋白質的利用率。
本研究得出, 添加晶體必需氨基酸的飼料, 能顯著增加全魚的蛋白質含量, 在一定程度上也能提高肥滿度, 降低肝體比和臟體比。這與在草魚()[36]和虹鱒()[35]的研究結果基本相一致, 表明在飼料的必需氨基酸缺乏時, 晶體必需氨基酸的補充有助于改善體組成。
本研究結果顯示, 40AA、35AA和30AA的試驗魚的免疫指標呈下降態勢, 但均高于各自對應的40CP、35CP和30CP的試驗魚, 唯40AA組的血清溶菌酶活性能達到45CP對照組的水平。這表明在低蛋白質飼料中添加晶體必需氨基酸可提高大口黑鱸機體的免疫指標。陳乃松等[11]關于大口黑鱸蛋氨酸需求量的研究表明, 飼料中的蛋氨酸缺乏時, 晶體蛋氨酸的補充也有利于試驗魚的非特異性免疫力的提高。在對幼建鯉(Jian)的研究中發現, 添加晶體色氨酸[37]、蘇氨酸[38]可促進魚類免疫器官的生長, 增強魚類非特異性免疫力。
3.3 影響大口黑鱸對飼料中晶體必需氨基酸利用效率的因素
在補充晶體必需氨基酸的飼料中, 盡管40AA、35AA和30AA中的必需氨基酸的組成模式與含量基本與45CP相一致(表2), 但除了40AA外, 試驗魚的生長性能、體組成和免疫指標均未達到45CP對照組的水平。這種現象的產生可能有兩方面的原因。一方面, 添加的晶體氨基酸可能未被充分地有效利用[39]。有研究表明, 在一些魚類中, 飼料中游離態的氨基酸與結合態的氨基酸存在著吸收不同步的現象。晶體氨基酸在腸道被吸收遠快于結合態氨基酸, 導致與結合態氨基酸的合成代謝不同步, 飼料中的部分氨基酸被氧化分解, 從而參與合成蛋白質的氨基酸減少。也有研究表明, 晶體氨基酸的包膜有助于延遲晶體氨基酸在腸道中的被吸收時間, 從而提高水產動物對飼料中兩種來源的氨基酸的利用率[40, 41]。本研究采用我們先前的方法[12, 13]對晶體氨基酸作了包膜處理, 這被證明對解決氨基酸的同步吸收是有效的。另一方面, 飼料中的非必需氨基酸的缺乏或不平衡也可能影響動物的蛋白質代謝。有學者提出, 非必需氨基酸在調節動物代謝和生理過程中具有多種獨特的功能, 從而影響試驗動物的健康和飼料轉化率。Krizova,[42]認為, 非必需氨基酸是豬體蛋白質分解產生的氨基酸重復利用的限制性因素, 或者是作為腸道微生物氨基酸合成過程中的前提物質。在魚類中, Gaye,[43]研究得出, 飼料中非必需氨基酸能顯著影響試驗魚的脂肪和蛋白質的積累以及能量的獲得。Tarik,[44]發現, 在大西洋鮭()處于維持狀態時非必需氨基酸對于魚體內蛋白質代謝起著很重要的作用。在本研究的40AA、35AA和30AA中盡管它們的必需氨基酸是等量的, 但非必需氨基酸是遞減的。基于上述非必需氨基酸的營養與生理功用的重要性, 可以推理: 在大口黑鱸的飼料中非必需氨基酸對于其生長、體組成和免疫指標也許有著重要的影響。這將值得進一步的研究與證實。
4 結論
以特定生長率、飼料效率和蛋白質保留率為評價指標, 大口黑鱸幼魚的飼料蛋白質水平在45%或以上較為適宜。在低蛋白質飼料中補充晶體必需氨基酸在不同程度上能提高大口黑鱸幼魚的生長、飼料利用效率和免疫指標, 但僅補充游離必需氨基酸的飼料依然不及以蛋白質配制的飼料的總體效能。
[1] Wilson R P. Animal Acids and Proteins [M]. New York: Academic Press. 2002, 143—148
[2] Kaushik S J, Seiliez I. Protein and amino acid nutrition and metabolism in fish: current knowledge and future needs [J]., 2010, 41(3): 322—332
[3] Verstegen M W A, Jongbloed A W. Crystalline Amino Acids and Nitrogen Emission [M]. Wallingford: CABI Publishing. 2003, 449—458
[4] Rodehutscord M, Becker A, Pack M,. Response of rainbow trout () to supplements of individual essential amino acids in a semipurified diet, including an estimate of the maintenance requirement for essential amino acids [J]., 1997, 127(6): 1166—1175
[5] Konrad D, Zhang Y F, Karolina K,. Effects of protein-, peptide- and free amino acid-based diets in fish nutrition [J]., 2010, 41(5): 668—683
[6] Anderson R J, Kienholz E, Flickinger S,. Protein requirements of smallmouth bass and largemouth bass [J]., 1981, 111(6): 1085
[7] Qian G Y. Effects of dietary protein, fibre and fat of the growth of largemouth bass () [J]., 1998, 7(3): 193—199[錢國英. 餌料中不同蛋白質, 纖維素, 脂肪水平對大口黑鱸生長的影響. 上海水產大學學報, 1998, 7(3): 193—199]
[8] Tidwell J H, Webster C D, Coyle S D,. Effects of dietary protein level on second year growth and water quality for largemouth bass () raised in ponds [J]., 1996, 145(1—4): 213—223
[9] Portz J E P, Cyrino R C, Martino. Growth and body composition of juvenile largemouth bassin response to dietary protein and energy levels [J]., 2001, 7(4): 247—254
[10] Chen N S, Xiao W W, Liang Q L,. Effects of lipid to protein ratios on growth performance, body composition and non-specific immunity of largemouth bass () [J]., 2012, 36(8): 1270—1280 [陳乃松, 肖溫溫, 梁勤朗, 等. 飼料中脂肪與蛋白質比對大口黑鱸生長、體組成和非特異性免疫的影響. 水產學報, 2012, 36(8): 1270—1280]
[11] Dairiki J K, Dias C T, Cyrino J. Lysine requirements of largemouth bass,: a comparison of methods of analysis of dose-response trials data [J]., 2007, 19(4): 1—27
[12] Chen N S, Ma J Z, Zhou H Y,. Assessment of dietary methionine requirement in largemouth bass,[J]., 2010, 34(8): 1245—1253 [陳乃松, 馬建忠, 周恒永, 等. 大口黑鱸對飼料中蛋氨酸需求量的評定. 水產學報, 2010, 34(8): 1245—1253]
[13] Zhou H, Chen N, Qiu X. Arginine requirement and effect of arginine intake on immunity in largemouth bass,[J]., 2012, 18(1): 107—116
[14] Lee S M. Apparent digetibility coeffidients of various feed ingredients for juvenile and grower rockfish () [J]., 2002, 207(1—2): 79—95
[15] AOAC. Official Methods of Analysis [M]. 16th edition. Arlington,V.A:Chemists:Association of Official Analytical Chemists.1995, 1234—1565
[16] Lee C, Trevino B, Chaiyawat M,. A simple and rapid solvent extraction method for determining total lipids in fish tissue [J]., 1996, 79(2): 487—492
[17] Liames C R, Fontaine J. Determination of amino acids in feeds: Collaborative study [J]., 1994, 77(6): 1362—1402
[18] NRC. Nutrient Requirements of Fish [M]. Washington, D C: National Academy Press. 2011, 337—339
[19] Sitj-Bobadilla A, Mingarro M, Pujalte M J,. Immunological and pathological status of gilthead sea bream (L) under different long-term feeding regimes [J]., 2003, 220(1—4): 707—724
[20] Secombes C J. Isolation of salmonid macrophages and analysis of their killing activity [J]. In: Stolen J S, Fletcher T C, Anderson D P, et al(Eds), TechniquesinFish Immunology(C). New Jersey: SOS Publications. 1990, 137—154
[21] Kim K W, Wang X J, Bai S C. Optimum dietary protein level for maximum growth of juvenile olive flounder(Temminck et Schlegel) [J]., 2002, (33): 673—679
[22] Shao Q J, Su X F. Effect of dietary protein levels on growth performance and body composition of jade perch () [J]., 2004, 28(4): 367—373 [邵慶均, 蘇小鳳. 飼料蛋白水平對寶石鱸生長和體組成影響研究. 水生生物學報, 2004, 28(4): 367—373]
[23] Tibbetts S M, Lall S P, Anderson D M. Dietary protein requirement of juvenile American eel () fed practical diets [J]., 2000, 186(1—2): 145—155
[24] Reis L M, Reutebuth E M. Protein to energy ratios in production diets and growth, feed conversion and body composition of channel catfish[J]., 1989, 77(1): 21—27
[25] Clark A E, Watanabe W O. Growth, feed conversion and protein utilization of Florida red tilapia fed isocaloric diets with different protein levels in seawater pools [J]., 1990, 88(1): 75—85
[26] Dabrowski K. Protein requirement of grass carp[J]., 1977, 12(1): 63—73
[27] Chen H Y, Tsai J C, Su M S,. Optimal dietary protein level for the growth of juvenile grouper,, fed semipurified diets [J]., 1994, 119(2—3): 265—271
[28] Shiau S Y, Lan C W. Optimal dietary protein level and protein to energy ratio for growth of grouper () [J]., 1996, 145(1—4): 259—266
[29] Kiron V. Protein nutrition and mechanisms in rainbow trout[J].:, 1995, 111(3): 351—359
[30] Cai C F, Wu K. The effects of protein nutrition on growth and immunological activity of allocgynogenetic silver crucian carp [J]., 2001, 25(6): 590—595 [蔡春芳, 吳康. 蛋白質營養對異育銀鯽生長和免疫力的影響. 水生生物學報, 2001, 25(6): 590—595]
[31] Wang J Q, Wang W H, Li W K,Effects of dietary protein and vitam in C levels on growth and immunity of juvenile[J]., 2005, 29(4): 512—518 [王吉橋, 王文輝, 李文寬, 等. 飼料蛋白質和維生素C含量對黃顙魚生長和免疫力的影響. 水產學報, 2005, 29(4): 512—518]
[32] Gaylord T G. Multiple amino acid supplementations to reduce dietary protein in plant-based rainbow trout ()feeds [J]., 2009, 287(1—2): 180—184
[33] Cheng Z J, Hardy R W. Plant protein ingredients with lysine supplementation reduce dietary protein level in rainbow trout () diets, and reduce ammonia nitrogen and soluble phosphorus excretion [J]., 2003, 218(1): 553—565
[34] Botaro D, Furuva W M. Dietary protein reduction based on ideal protein concept for Nile tilapia () cultured in net pens [J]., 2007, 36(3): 517—525
[35] Yamamto T, Sugita T. Essential amino acid supplementation to fish meal-based diets with low protein to energy ratios improves the protein utilization in juvenile rainbow trout[J]., 2005, 246(1—4): 379—391
[36] Ye Y T, Tan F F. Effects of microcapsule lysine and methionine supplementation on growth performance of grass crap () [J]., 2010, 22(3): 804—810. [葉元土, 譚芳芳. 補充微囊賴氨酸和蛋氨酸對草魚生長性能的影響. 動物營養學報, 2010, 22(3): 804—810]
[37] Tang L. The study of the effects of tryptophan on digestive and absorbtive capacity, disease resistant, and the TOR expression in organs and tissue in Jian carp (var. Jian) [D]. Thesis Master of Science. Sichuan Agricultural University, Ya’an. 2009 [唐凌. 色氨酸對幼建鯉消化吸收能力和疾病抗病能力及其組織器官中TOR表達影響研究. 碩士學位論文, 四川農業大學, 雅安. 2009]
[38] Feng L. Effect of threonine on digestive, absorb, immune function and TOR gene expression in organ and tissues of juvenile Jian carp [D]. Thesis Master of Science. Sichuan Agricultural University, Ya’an. 2009 [馮琳. 蘇氨酸對幼建鯉消化吸收能力和抗病力以及組織器官中蛋白質調控信號分子TOR表達的影響. 碩士學位論文, 四川農業大學, 雅安. 2009]
[39] Ambardekar A A, Reigh R C, Williams M B,. Absorption of amino acids from intact dietary proteins and purified amino acid supplements follows different time-courses in channel catfish () [J]., 2009, 291(3—4): 179—187
[40] Roelants I. Effective supplementation of arginine in the diets of juvenile marine shrimp,[J]., 1992, 108(1—2): 87—95
[41] Chen B A, Leng X J, Li X Q,Study on the effect of crystalline of coated amino acids for[J]., 2008, 32(5): 774—778 [陳丙愛, 冷向軍, 李小勤, 等. 晶體或包膜氨基酸對鯉魚的作用效果研究. 水生生物學報, 2008, 32(5): 774—778]
[42] Krizova K, Simecek K, Heger J,. Effect of nonessential amino acids on nitrogen retention in growing pigs fed on a protein-free diet supplemented with sulphur amino acids, threonine and tryptophan [J]., 2001, 85(9—10): 325—332
[43] Gaye S J, Focken U, Abel H J,. Influence of dietary non-essential amino acid profile on growth performance and amino acid metabolism of Nile tilapia,(L.) [J]., 2007, 146(1): 71—77
[44] Tarik A, Muriel M, Yvan L,. The effect of dispensable amino acids on nitrogen and amino acid losses in Atlantic salmon (L.) fry fed a protein-free diet [J]., 2009, 289(3—4): 327—333
Effects of Supplementing EAA to LowER protein diets on Growth, Body Composition and IMMUNOLOGICAL INDEX of Largemouth Bass ()
CHEN Nai-Song, LIANG Qin-Lang, XIAO Wen-Wen, ZHOU Heng-Yong, MA Xiu-Li and ZHAO Ming
(College of Fisheries and Life Science, Shanghai Ocean University, Shanghai 201306, China)
An 89-day growth trial was undertaken to evaluate effects of essential amino acid (EAA) supplementation to diets with lower protein levels on growth performance, body composition and immunological parameters in largemouth bass (). Seven isoenergetic diets were formulated according to the EAA profile of whole body of largemouth bass. Four diets of them contained crude protein concentrations of 45%, 40%, 35% and 30%, respectively (designated as 45CP, 40CP, 35CP and 30CP). The other three diets (designated as 40AA, 35AA and 30AA) were formulated by adding EAA to three lower protein diets of 40CP, 35CP and 30CP to make their EAA levels consistent with that of 45CP (used as a control). Triplicate groups of thirty juvenile largemouth bass with initial body weight of (10.13±0.01) g were reared in an indoor water-circulating system. It was showed by one-way ANOVA that growth performance, feed utilization, crude protein concentrations of whole body and muscle, immunological index and survival rate declined significantly among fish fed the diets with a reduction of dietary protein from 45% to 30% (<0.05). Feed efficiency and protein retention in fish fed 35AA and 30AA were significantly higher than those of 35CP- and 30CP-fed fish (<0.05), respectively. There were no significances in serum lysozyme activity and serum complement activity between 40AA-fed fish and 45CP-fed fish (>0.05). Respiratory burst activity of head kidney leukocytes with 35AA-fed fish and 30AA-fed fish was significantly higher (<0.05), compared to those of 35CP and 30CP, respectively. Crude protein concentrations of whole-body and condition factor of 30AA-fed fish were significantly higher than those 30CP-fed fish (<0.05). Among all the treatments, moisture and ash of whole body and muscle of tested fish showed no significant differences (>0.05). It was suggested by regression analysis that the effects of supplementing EAA to lower protein diets on,andin juvenile largemouth bass were positively related with increased levels of dietary protein rather than those of dietary EAA. This study indicates that crystalline EAA supplemented to lower protein diets for juvenile largemouth bass can cause improvement in growth performance, feed efficiency and immunological index but the improvement is inferior to what is caused by the same levels of EAA deriving from proteins.
Largemouth bass (); Diet; Essential amino acid; Protein; Growth; Body composition; Immunological index
2013-05-30;
2013-12-09
上海市科委高校能力建設項目(10320503100); 上海高校知識服務平臺(ZF1206)資助
陳乃松(1961—), 男, 江蘇濱海人; 教授; 主要從事水產動物營養與飼料學專業。E-mail: nschen@shou.edu.cn
S965.1
A
1000-3207(2014)02-0262-10
10.7541/2013.39

