鴨腸炎病毒囊膜糖蛋白gE基因序列分析及真核表達載體的構建
文晶亮,李啟紅,李俊平,劉 丹,李 嶺,楊承槐,李慧姣,夏業才
(中國獸醫藥品監察所,北京100081)
gE蛋白是皰疹病毒家族中較為重要的糖蛋白之一,由位于US區的US8基因編碼。據報道皰疹病毒gE基因是皰疹病毒從視網膜、嗅覺上皮細胞、三叉神經節侵入中樞神經組織所必須的毒力基因,對皰疹病毒在體內毒力表達、侵襲神經核沿著神經傳遞起著決定性的作用,另外還能促進病毒在細胞之間擴散[1-4]。 目前對人皰疹病毒、偽狂犬病毒、牛皰疹病毒等皰疹病毒糖蛋白gE基因及其編碼蛋白已有大量研究[5-7],而對鴨瘟病毒 gE基因及其編碼蛋白尚未有深入的報道。因此,本研究PCR擴增了DEV的gE基因完整開放閱讀框(gE)和去信號肽的gE基因(gE’),分別克隆至真核表達載體pCDNA3.1,轉染 vero細胞,并應用 RT-PCR 和間接免疫熒光檢測gE、gE’蛋白在vero細胞中的轉錄、表達,旨在探討gE蛋白在真核細胞中的表達,為gE蛋白的功能研究、鴨瘟抗體檢測奠定基礎,為深入了解鴨瘟病毒感染的發病機理提供科學數據。
1 材料與方法
1.1 材料
1.1.1 病毒與細胞 鴨腸炎病毒AV1221株,由中國獸醫藥品監察所菌種保藏中心提供;vero細胞,由本實驗室保存;E.coli DH5α感受態細胞,購于天根生化科技有限公司。
1.1.2 主要試劑 真核表達載體 pCDNA3.1,由本實驗室保存;pMD18-T載體、Ex Taq DNA聚合酶、dNTPs、EcoRⅠ、XhoⅠ、MarkerⅣ、T4 DNA 連接酶,均購自大連寶生物工程有限公司;Lipofectamine 2000,購自 Invitrogen 公司;OPTI-MEM?I培養液,購自gibco?公司;FITC標記的兔抗雞熒光二抗,購自美國sigma-aldrich公司;DMEM高糖細胞培養液、TBD標準胎牛血清購于賽墨飛世爾生物化學制品有限公司。
1.1.3 試劑盒 高純度質粒小提中量試劑盒、瓊脂糖凝膠DNA回收試劑盒購于天根生化科技有限公司。
1.1.4 血清 雞抗DEV陽性血清,由本實驗室制備;TBD標準胎牛血清,購于賽墨飛世爾生物化學制品有限公司。
1.2 方法
1.2.1 引物設計與合成 根據已發表的基因組序列,設計擴增鴨腸炎病毒AV1221株的gE基因完整ORF序列(gE)和去信號肽的gE基因(gE’)引物,由invitrogen公司合成。
針對gE的引物:
P1: 5’ -AAGAATTC ATGATGGTTACTTTTAT-3’,下劃線部分為酶切位點EcoR I;
P2:5’-AACTCGAGTCAGATGCGGAAACTAGA-3’,下劃線部分為酶切位點Xho I;
針對gE’的引物:
P11: 5’-AAGAATTCGACTATCATCAAGTGATT-3’,下劃線部分為酶切位點EcoR I;
P22: 5’-AACTCGAGTCAGATGCGGAAACTAGA-3’,下劃線部分為酶切位點Xho I;
1.2.2 DNA 模板提取 按參考文獻[8]進行。
1.2.3 gE基因的克隆 PCR反應體系:病毒DNA 2 μL,dNTPs 2 μL,上游引物 P11 μL,下游引物 P21 μL,10×Ex Taq buffer 2.5 μL,Ex Taq DNA 聚合酶0.125 μL,ddH2O 16.375 μL,總體積 25 μL。
反應條件:94℃預變性3 min,94℃變性40 s,46.2 ℃退火 40 s,72 ℃ 延伸 1 min 30 s,30 個循環后,72℃延伸10 min。反應結束后,取3 μL PCR產物進行0.8%瓊脂糖凝膠電泳鑒定。
1.2.4 去信號肽 gE 基因(gE’)序列的克隆 PCR
反應體系:病毒 DNA 2 μL,dNTPs 2 μL,上游引物P111 μL,下游引物 P221 μL,10 ×Ex Taq buffer 2.5 μL,Ex Taq DNA 聚 合 酶 0.125 μL, ddH2O 16.375 μL,總體積 25 μL。
反應條件:94℃預變性3 min,94℃變性40 s,47℃退火1 min,72℃延伸1 min 30 s,30個循環后,72℃延伸10 min。 反應結束后,取3 μL PCR產物進行0.8%瓊脂糖凝膠電泳鑒定。
1.2.5 gE基因測序及序列分析 PCR產物用膠回收試劑盒回收后,分別連接到pMD18-T載體,轉化DH5α,獲得重組質粒 pMD18T-gE、pMD18T- gE’。將酶切及PCR鑒定正確的重組質粒pMD18T-gE、pMD18T-gE’送Invitrogen公司測序,并用生物信息學軟件對測序正確的gE基因進行分析,預測gE基因編碼蛋白的功能。
1.2.6 真核表達載體的構建 gE基因測序正確后,用限制性內切酶EcoRⅠ和XhoⅠ分別雙酶切克隆質粒 pMD18-gE、pMD18-gE’和載體 pCDNA3.1。回收、純化雙酶切gE、gE’基因和pCDNA3.1線性質粒,并用T4 DNA連接酶使雙酶切gE、gE’基因分別與 pCDNA3.1線性質粒連接,轉化 E.coli DH5α 感受態細胞,挑取陽性克隆,提取質粒pCDNA3.1-gE、pCDNA3.1-gE’,進行酶切及 PCR 鑒定。
1.2.7 重組表達質粒轉染vero細胞 在轉染前20 h,消化vero細胞,轉入6孔細胞板,每孔6×105個細胞,待細胞鋪板密度在75%時進行轉染。
Lipofectamine 2000/DNA復合物的制備:分別將 0.8 μg pCDNA3.1- gE、pCDNA3.1- gE’質粒分別稀釋于不含血清和抗生素的opti-DMEM中,使混合液的終體積均為 50 μL,室溫孵育 5 min;2 μL Lipofectamine 2000分別稀釋于不含血清和抗生素的opti-DMEM中,使混合液的終體積均為50 μL,輕輕混勻,室溫孵育5 min;將50 μL Lipofectamine 2000稀釋液分別滴加到50 μL質粒稀釋液中,邊加邊混勻;室溫孵育20 min。
轉染 vero細胞:分別將 100 μL Lipofectamine 2000/DNA復合物加入到6孔板中,輕輕搖動使其均勻混合,置37℃培養4 h,棄去上清,加入10%胎牛血清的M199培養基,置37℃培養24 h后,用1%胎牛血清的M199培養基換液,置37℃培養24 h。
1.2.8 mRNA檢測 參照試劑盒操作說明,提取轉染后的細胞總RNA,將RNA反轉錄成cDNA,參照Invitrogen M-MLV反轉錄酶的說明書操作:模板RNA 5 μL,反轉錄引物 1 μL,dNTP(10 mmol/L)1 μL,DEPC 水補加至 12 μL,100℃ 水浴 5 min,馬上冰淬滅 1 min;短暫離心后加入 5×buffer 4 μL,DTT(0.1mol/L)2 μL,RNA 酶抑制劑 1 μL,輕輕混勻后 50℃水浴5 min;加入 M-MLV反轉錄酶1 μL,50 ℃水浴 50 min;70 ℃水浴15 min,冰淬滅;加入1 μL RNaseH,馬上進行PCR反應。PCR反應參照 1.2.3 和 1.2.4。
1.2.9 表達產物的檢測 應用間接免疫熒光法檢測表達蛋白,方法如下:取出6孔細胞板,用pH為7.2的PBST溶液漂洗細胞1次,加入0.5 mL預冷的甲醇溶液,固定15 min;棄去甲醇溶液,室溫放置2~5 min自然晾干;用PBST洗1次;加入100倍稀釋的雞抗DEV陽性血清,37℃孵育1 h,棄去DEV陽性血清,每孔用含0.05%吐溫-20的PBST洗3次后,用PBST液洗2次;加500倍稀釋的兔抗雞熒光抗體,37℃溫箱中避光孵育1 h,每孔用含0.05%吐溫-20的PBST洗3次后,用PBST洗2次,在熒光顯微鏡下觀察并照相。
2 結 果
2.1 gE基因的 PCR擴增 分別以 gE基因的P1/P2為引物、gE’基因的 P11/P22為引物,病毒 DNA為模板PCR擴增gE、gE’基因,擴增產物經0.8%瓊脂糖凝膠電泳分析,可見約1400 bp的DNA片段,與預期片段大小相符(圖1)。
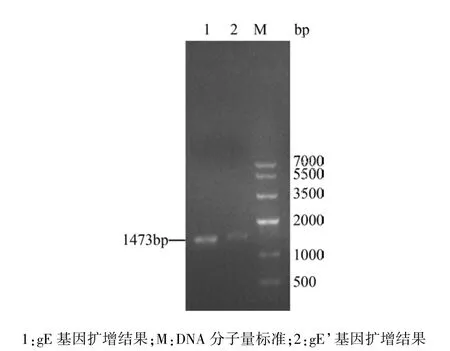
圖1 gE和gE’基因的PCR擴增結果
2.2 gE及gE’基因的克隆及酶切鑒定 回收純化后的gE、gE’PCR產物與pMD18-T連接,分別構建克隆質粒 pMD18T-gE、pMD18T-gE’,酶切、PCR 結果說明所克隆序列與目的片段大小相近(圖2、圖 3)。
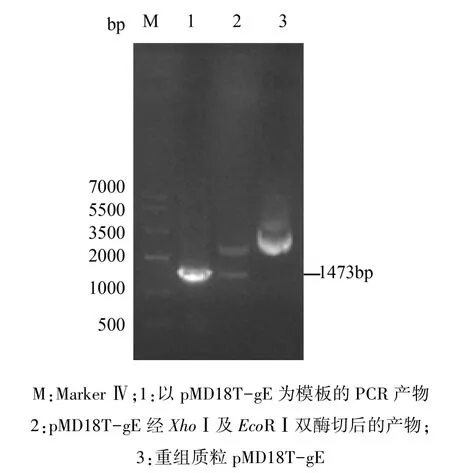
圖2 重組質粒pMD18T-gE酶切及PCR鑒定結果

圖3 重組質粒pMD18T-gE’酶切及PCR鑒定結果
2.3 gE基因序列分析及編碼蛋白的功能預測
2.3.1 同源性分析結果 用NCBI網站的在線程序BLASTN對鴨瘟AV1221株gE基因序列與國內分離強毒 CHv 株 (GenBank:EU071044.1)、 國 內 疫 苗 株(GenBank:EU082088.2)和德國分離強毒 2085 株(GenBank:JF999965.1)基因序列進行比對,結果表明:鴨瘟AV1221株gE基因序列與國內分離強毒CHv株、國內疫苗株同源性均為100%,與德國分離強毒2085株同源性為99%,143位堿基變異(T-C),導致第48位氨基酸由蘇氨酸(T)變成了異亮氨酸(I),此外,412位(G-A)和1351位(C-T)堿基同義突變。
2.3.2 信號肽預測結果 用CBS網站的在線程序SignalP4.1對gE氨基酸序列進行信號肽預測,結果顯示:gE蛋白序列中預測到的C值、S值或Y值都大于臨界值,推測gE蛋白第1~22位氨基酸為信號肽(圖4)。
2.3.3 跨膜區的預測結果 本研究利用 TMHMM 2.0預測鴨瘟AV1221株gE蛋白的跨膜區,其結果顯示:gE蛋白在397~419位氨基酸有一個跨膜區,1~396位氨基酸位于胞膜外(胞外區),420~490位氨基酸位于胞膜內(胞質區)(圖5)。
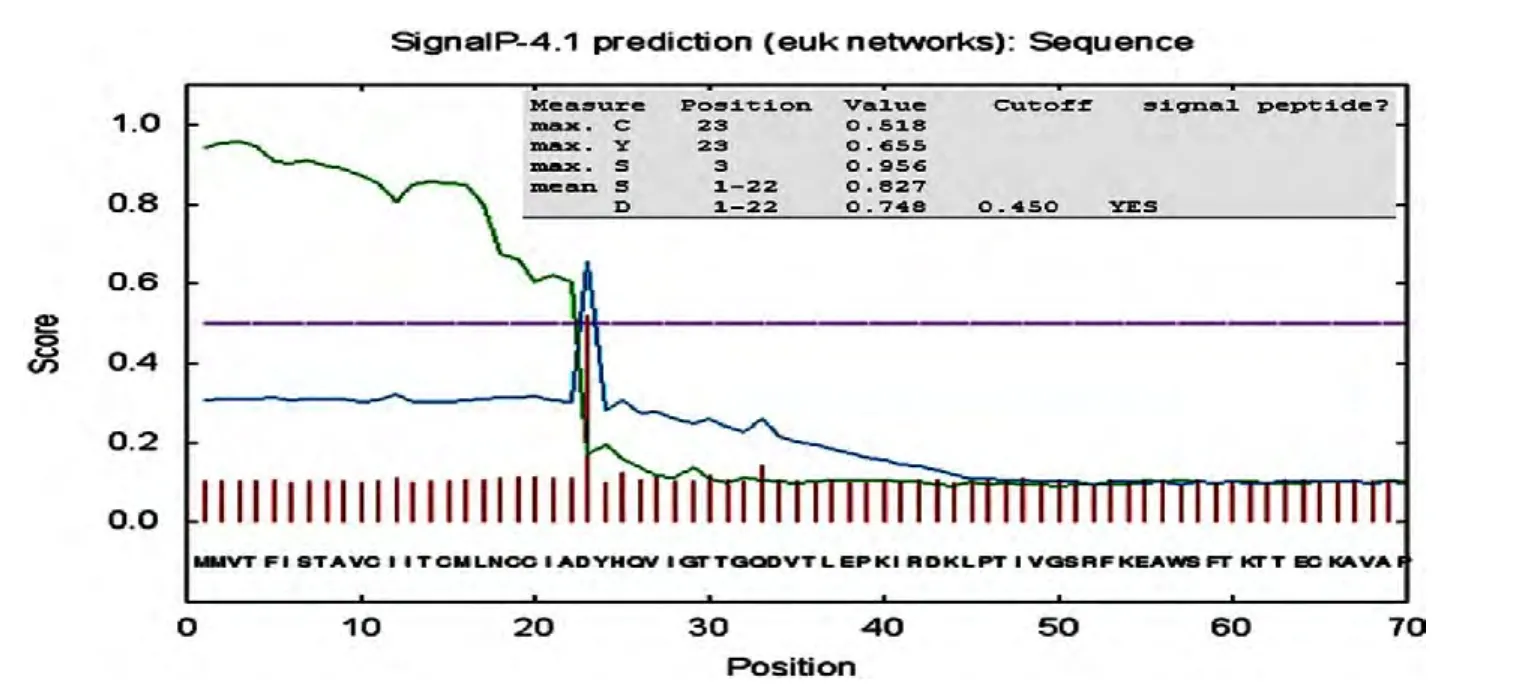
圖4 gE氨基酸序列推倒肽鏈信號肽預測結果
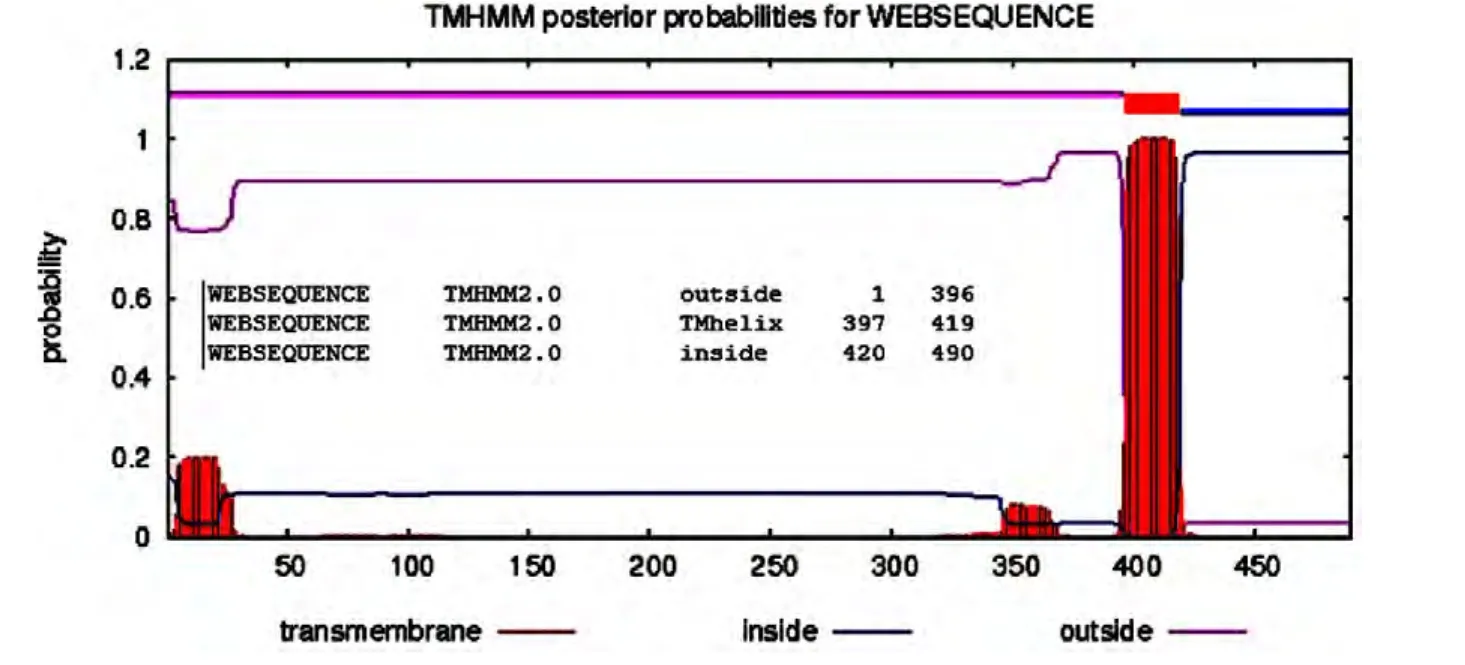
圖5 gE氨基酸序列推倒肽鏈跨膜區預測結果
2.4 真核表達質粒的構建及鑒定 重組質粒pCDNA3.1-gE、pCDNA3.1-gE’經 EcoRⅠ及 XhoⅠ雙酶切后分別得到約1400 bp和5400 bp的條帶,PCR鑒定結果也獲得了約1400 bp的條帶,說明成功構建了重組真核表達質粒 pCDNA3.1-gE、pCDNA3.1-gE’(圖 6)。

圖6 重組質粒 pcDNA3.1-gE、pcDNA3.1-gE’酶切及PCR鑒定結果
2.5 PCR 鑒定轉染結果 提取 pCDNA3.1-gE、pCDNA3.1-gE’轉染后的 vero 細胞總 RNA,并以提取的細胞總RNA為模板,分別以gE基因的P1/P2、gE’基因的 P11/P22為引物進行 RT-PCR 擴增,得到了相應大小DNA片段(圖7),而以提取的空載體pCDNA3.1轉染的 vero細胞總 RNA為模板RT-PCR擴增后則未見相應條帶,從轉錄水平上說明gE和gE’基因均在vero細胞獲得表達。

圖7 pCDNA3.1-gE、pCDNA3.1-gE’和 pCDNA3.1轉染vero細胞RT-PCR結果
2.6 表達產物的免疫熒光鑒定 轉染48h后,經用熒光顯微鏡觀察,只有重組質粒pCDNA3.1-gE’轉染的 vero細胞可見綠色熒光(圖 8 A),而pCDNA3.1-gE、pCDNA3.1 轉染的 vero 細胞中未見明顯熒光(圖8B,C),結果表明gE’基因在vero細胞中獲得了正確表達,具有免疫原性,能與抗體結合。

圖8 真核表達載體轉染vero細胞后間接免疫熒光檢測結果
3 討論與小結
本研究結果表明,鴨腸炎病毒AV1221株 gE基因完整的開放閱讀框長為1473 bp,共編碼490個氨基酸,其中第1~22位氨基酸為信號肽序列。其基因序列與國內分離強毒CHv株[9]、國內疫苗株[10]和德國分離強毒 2085 株[11]均具有較高同源性,說明鴨腸炎病毒AV1221株gE比較保守。而軟件TMHMM 2.0預測表明gE蛋白是典型的囊膜糖蛋白,包括較長的胞外區(396個氨基酸)、跨膜區(23個氨基酸)和胞質區(71個氨基酸),這與常華[12]結果一致。
皰疹病毒gE蛋白表達載體的構建及表達是其功能研究的重要方面,Zhu等[13]將VZV gE構建在真核表達質粒pSVK3上,轉染COS-7細胞,用間接免疫熒光方法檢測到VZV gE蛋白在COS-7細胞中表達并定位于COS-7細胞的高爾基體。常華[12]利用間接免疫熒光方法檢測到DEV gE蛋白可在感染鴨胚成纖維細胞的胞漿中表達。在本研究中,含信號肽的表達載體pCDNA3.1-gE在vero細胞內完成了轉錄過程,但卻未能在vero細胞內檢測到熒光,與上述研究結果并不一致,推測可能與所用毒株、宿主細胞不同以及存在信號肽有關。因此又構建了去信號肽的真核表達載體pCDNA3.1-gE’,轉染vero細胞后完成了轉錄過程,并進行了表達,證實gE自身所具有的信號肽序列可以有效誘導gE蛋白分泌到細胞外,與軟件TMHMM 2.0預測結果一致。實驗表明,在真核表達體系中,信號肽的有無對gE蛋白的表達具有顯著的影響。
本研究通過酶切和PCR方法證實,成功構建了真核表達質粒 pCDNA3.1-gE 和 pCDNA3.1-gE’,并在轉錄水平和蛋白水平上檢測了pCDNA3.1-gE、pCDNA3.1-gE’在 vero細胞中的表達,下一步將通過G418抗生素篩選穩定表達gE的vero細胞系,為gE蛋白的體外表達、功能研究、鴨瘟抗體檢測試劑盒的開發奠定了基礎。
[1]Mettenleiter T C.Pathogenesis of neurotropic herpesviruses: role of viral glycoproteins in neuroinvasion and transneuronal spread[J].Virus Res, 2003, 92(2): 197-206.
[2]Brideau A D, Enquist L W, Tirabassi R S.The role of virion membrane protein endoeytosis in the herpesvirus life cycle[J].J ClinVirol, 2000, 17(2): 69-82.
[3]Tirabassi R S, Enquist L W.Role of envelope protein gE endo eytosis in the pseudorabies virus life cycle[J].J Virol, 1998, 72(6): 4571-4579.
[4]Ao J Q,Wang J W,Chen X H,et al.Expression of pseudorabies virus gE epitopes in Pichia pastoris and its utilization in an indirect PRV gE-ELISA[J].J Virol Methods, 2003, 114(2):145-150.
[5]Snyder A, Poleieova K, Johnson D C.Herpes simplex virus gE/gI and US9 proteins promote transport of both capsids and virion glycoproteins in neuronal axons [J].J Virol, 2008, 82(21): 10613-10624.
[6]Wang F, Tang W, McGraw H M, et al.Herpes simplex virus type 1 glycoprotein e is required for axonal localization of capsid,tegument, and membrane glycoproteins[J].J Virol, 2005, 79(21): 13362-13372.
[7]Tomishima M J, Enquist L W.A conserved alpha-herpesvirus protein necessary for axonal localization of viral membrane proteins[J].J Cell Biol, 2001, 154(4):741-752.
[8]楊承槐,李俊平,李啟紅,等.含LacZ表達盒的鴨瘟病毒TK基因缺失轉移載體的構建[J].中國獸藥雜志,2013,47(1):7-9.
[9]Wu Y,Cheng A,Wang M,et al.Complete genomic sequence of Chinese virulent duck enteritis virus[ J].J Virol, 2012, 86(10): 5965.
[10]Li Y, Huang B, Ma X, et al.Molecular characterization of the genome of duck enteritis virus[J].Virology, 2009, 391(2):151-161.
[11]Wang J, Hoper D, Beer M, et al.Complete genome sequence of virulent duck enteritis virus(DEV)strain 2085 and comparison with genome sequences of virulent and attenuated DEV strains[J].Virus Res, 2011, 160(1/2): 316-325.
[12]常 華.鴨瘟病毒gE基因功能初步研究[D].雅安:四川農業大學,2011.
[13]Zhu Z, Hao Y, Gershon M D,et al.Targeting of glycoprotein Ⅰ(gE)of varicella-zoster virus to the trans-goligi network by an AYRV sequence and an acidic amino-rich patch in the cytosolic domain of the molecule[J].J Virol, 1996, 70(10):6563-6575.

