γ-干擾素釋放試驗對結核病患者臨床診斷性能評價研究
秦建成,徐軍,戴亮,趙靜,王衛東,李想,張嵐,毛遠麗
γ-干擾素釋放試驗對結核病患者臨床診斷性能評價研究
秦建成,徐軍,戴亮,趙靜,王衛東,李想,張嵐,毛遠麗
目的評價采用A.TB試劑[酶聯免疫吸附試驗(enzyme-linked immunosorbentassay,ELISA)]進行結核桿菌特異性γ-干擾素釋放試驗(interferon-gamma release assays,IGRAs)對結核病的臨床診斷性能及應用價值。方法108例研究對象中,臨床明確診斷結核病60例(結核組),非結核病對照者48例(非結核對照組)。同時采用A.TB試劑(ELISA法)和T-SPOT. TB試劑[酶聯免疫斑點試驗(enzyme-linked immunosorbentspot,ELISPOT)]進行IGRAs。結果A.TB試劑(ELISA法)檢測的靈敏度為86.67%,特異度為85.42%,受試者工作特征曲線(receiver-operating characteristic curve,ROC曲線)下面積為0.822,95%可信區間(confidence interval,CI)為0.733~0.912。T-SPOT.TB試劑(ELSPOT法)檢測靈敏度為91.67%,特異度為87.50%,ROC曲線下面積為0.884,95%CI為0.806~0.962。ROC曲線下面積差異無統計學意義(χ2=0.081,P=0.776)。2種檢測方法一致率為87.04%(94/108),Kappa值為0.738。結論A.TB試劑和T-SPOT.TB試劑檢測的整體診斷性能相似,且A.TB試劑檢測在操作和檢測結果判讀方面明顯優于T-SPOT.TB試劑。
干擾素γ釋放試驗;結核分枝桿菌;預測;免疫印跡法;指示劑和試劑
結核病不僅是嚴重危害公眾健康的全球性公共衛生問題,更是社會經濟和居民健康水平等社會宏觀因素的一種外在表現[1-2]。我國是全球第二大結核病高負擔國家,結核病發病人數始終位居法定報告甲、乙類傳染病前列[3]。因此結核病的防控十分重要,但傳統的方法難以滿足臨床檢測的需求。近年來結核分枝桿菌基因組學的研究成果——γ-干擾素釋放試驗(interferon-gamma release assays,IGRAs)在結核病診斷中的應用與研究越來越受到國內外專家學者的重視[4]。其中,T-SPOT. TB試劑[酶聯免疫斑點試驗(enzyme-linked immunosorbent spot,ELISPOT)]作為IGRAs的試劑于2001年獲得美國食品藥品監督管理局批準應用于臨床,美國疾病預防控制中心推薦T-SPOT.TB試劑(ELISPOT法)檢測為替代結核菌素試驗更有效的方法,并為其制訂了使用指南[5-6]。我國臨床實驗室及科研機構近幾年也進行了基于IGRAs原理的結核檢測產品研制與應用。本研究對基于同一IGRAs原理的國產A.TB試劑[酶聯免疫吸附試驗(enzyme-linked im-munosorbent assay,ELISA)]進行臨床診斷性能評估,并與T-SPOT.TB試劑(ELISPOT法)對結核病患者的臨床診斷性能進行比較。
1 對象與方法
1.1 對象共納入108例研究對象。臨床明確診斷結核病60例(結核組),其中菌陽肺結核21例,菌陰肺結核39例;男36例,女24例,年齡(43.1±5.4)歲。入選標準:菌陽肺結核為痰抗酸桿菌涂片連續2次(+),或1次(++),或1次結核分枝桿菌(Mycobacterium tuberculosis,Mtb)培養陽性;菌陰肺結核為痰抗酸桿菌涂片3次陰性以及Mtb培養1次陰性,有典型的肺結核臨床癥狀和X線胸片表現,抗結核治療有效,臨床可排除其他非結核性肺部疾病。排除標準:急性病毒感染、妊娠和長期大量應用免疫抑制劑者。非結核病對照者48例(非結核對照組),其中男27例,女21例,年齡(42.6±12.4)歲。非結核對照組均經病理或臨床檢查確診,既往無結核病史和接觸史,結核菌素試驗均為陰性,為Mtb感染低暴露風險的慢性乙型肝炎患者。本研究經醫院倫理委員會批準,受試者均簽署知情同意書。
1.2 試劑和儀器
1.2.1 試劑A.TB試劑盒系海口維瑅璦生物研究院產品;T-SPOT.TB試劑盒系英國Oxford Immunotec公司產品;AIM-V培養液和PRMI 1640培養液系美國Gibcobrl公司產品;淋巴細胞分離液系CEDARLANE公司產品。
1.2.2 儀器儀器包括美國伯樂Bio-rad酶標儀、Sanyo CO2培養箱(CO2Incubator)、Thermo MSC-1.2 1PE AC超凈工作臺、contess細胞計數儀和C.T.L. S6UV酶聯斑點計數儀。
1.3 檢測方法
1.3.1 A.TB試劑(ELISA法)檢測采集3ml外周血標本置于肝素鋰抗凝試管中,立即混勻,16 h內將新鮮全血分別加入到含有陰性刺激劑(N)、陽性刺激劑(P)和特異性抗原刺激劑(T)的3支試管中,每管1ml,混勻,37℃孵育22~24 h后收集血漿,ELISA法檢測血漿中干擾素γ的含量,孵育后血漿可于2~8℃保存,2周內檢測,或-20℃以下長期保存。結果判讀:參照A.TB試劑盒說明書,當N<500 IU/L時,(T-N)/(P-N)≥0.6;或N≥500 IU/L時,(T-N)/(P-N)≥0.85,均判定為陽性,否則為陰性。
1.3.2 T-SPOT.TB試劑(ELISPOT法)檢測采集6 ml外周血,4 h內進行單個核細胞(peripheral blood mononuclear cells,PBMCs)分離;將細胞多次洗滌后計數,并將標本濃度調整至250萬/m l。按TSPOT.TB試劑盒說明書將細胞懸液加入專用微孔板。37℃5%CO2孵育箱中孵育16~20 h,磷酸鹽緩沖液洗板,加抗體,于2~8℃冰箱孵育1 h,洗板,顯色7min,蒸餾水沖洗后觀察結果。用酶聯斑點計數儀觀察并計數每個孔中的斑點。結果判讀:陰性斑點數為0~5個,抗原A和抗原B檢測孔計數-陰性孔計數≥6判定為陽性;如果陰性對照孔斑點數≥6,檢測孔斑點數≥2倍陰性孔斑點數判定為陽性。
1.4 統計學處理應用SPSS 16.0軟件進行統計分析。計算2種方法的靈敏度和特異度。A.TB與T-SPOT.TB試劑檢測診斷效能采用一致性檢驗。分別繪制2種試劑檢測的受試者工作特征曲線(receiver-operating characteristic curve,ROC曲線),比較曲線下面積。檢驗水準α=0.05。
2 結果
2.1 診斷試驗結果A.TB試劑(ELISA法)檢測靈敏度為86.67%,特異度為85.42%;T-SPOT.TB試劑(ELISPOT法)檢測靈敏度為91.67%,特異度為87.50%。見表1~2。
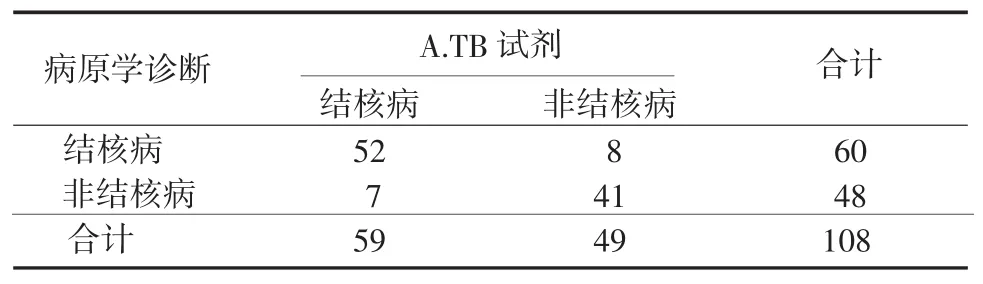
表1 A.TB試劑(ELISA法)診斷試驗結果(例)Table 1 Diagnostic results of ELISA-based IGRAs w ith A.TB kit(cases)
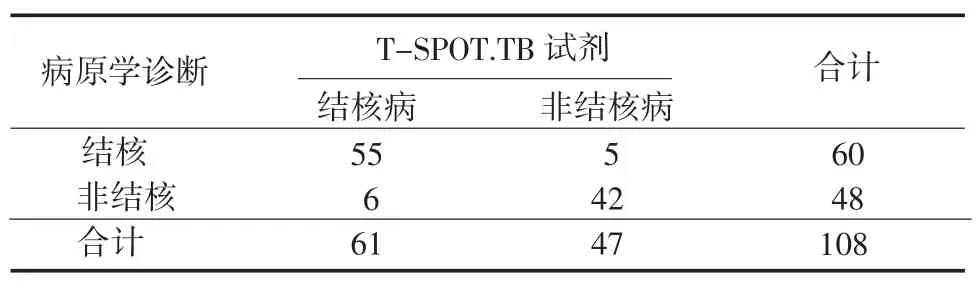
表2 T-SPOT.TB試劑(ELISPOT法)診斷試驗結果(例)Table 2 Diagnostic results of ELISPOT-based IGRAs w ith T-SPOT.TB kit(cases)
2.2 一致性檢驗結果比較A.TB試劑(ELISA法)和T-SPOT.TB試劑(ELISPOT法)檢測的診斷結果,檢測均為陽性的53例,均為陰性的41例,一致率為87.04%(94/108),Kappa=0.738,提示2種試劑檢測具有較高的一致性。見表3。
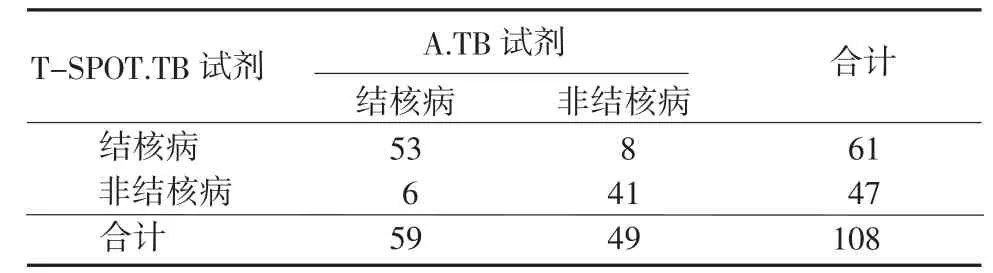
表3 A.TB試劑(ELISA法)和T-SPOT.TB試劑(ELISPOT法)檢測的一致性檢驗(例)Table 3 Consistency between ELISA-based IGRAs w ith A.TB kit and ELISPOT-based IGRAs w ith T-SPOT.TB kit(cases)
2.3 ROC曲線分析以病原學檢測為金標準,做A.TB試劑(ELISA法)和T-SPOT.TB試劑(ELISPOT法)診斷108例患者的ROC曲線。用雙正態參數法計算曲線下面積。A.TB試劑(ELISA法)檢測的ROC曲線下面積為0.822,95%可信區間(confidence interval,CI)為0.733~0.912;T-SPOT.TB試劑(ELISPOT法)檢測的ROC曲線下面積為0.884,95%CI為0.806~0.962(圖1)。2個ROC曲線下面積差異無統計學意義(χ2=0.081,P=0.776)。取曲線斜率45度切點位置為診斷閾值,A.TB試劑(ELISA法)的診斷閾值為0.6(比值),對應的靈敏度為86.67%,特異度為85.42%;T-SPOT.TB試劑(ELISPOT法)得診斷閥為6(斑點數),對應的靈敏度為91.67%,特異度為87.50%。

圖1 A.TB試劑(ELISA法)和T-SPOT.TB試劑(ELISPOT法)診斷結核病的ROC曲線Figure 1 ROC curves of ELISA-based IGRAsw ith A.TB kit and ELISPOT-based IGRAsw ith T-SPOT.TB kit
3 討論
IGRAs是近年來發展起來的用于檢測Mtb感染的新方法,國外資料報道其檢測潛伏性Mtb感染的靈敏度達70%~80%,特異度達88%~97%[6]。我國Mtb感染率高,流行病學背景不同于歐美國家,IGRAs主要應用于結核病的診斷和鑒別。Mtb感染與結核病也有著較大差別,IGRAs并不能明確區分活動性結核病和潛伏性Mtb感染。本研究旨在探討A.TB試劑(ELISA法)對結核病患者的臨床診斷性能及應用價值。
根據IGRAs原理發展來的檢測方法有基于全血培養的ELISA法,如QuantiFERON-TB、Gold In-Tube、QFT-GIT等檢測方法和基于PBMCs培養的ELISPOT法,如T-SPOT.TB檢測方法。目前已有大量國內外研究表明,IGRAs的2種方法(ELISA法和ELISPOT法)的診斷性能相似[7-9],這與本研究結果相符。
雖然A.TB試劑(ELISA法)檢測與T-SPOT.TB試劑(ELISPOT法)檢測都是基于IGRAs原理的結核檢測方法,但它們在檢測技術、試驗操作以及在臨床檢驗科室使用的便捷性等方面有著顯著區別。A.TB試劑(ELISA法)檢測是通過ELISA法檢測全血中的干擾素γ水平,而T-SPOT.TB試劑(ELISPOT法)是通過ELISPOT法檢測PBMCs中釋放干擾素γ的效應T細胞數量。在樣本采集和處理過程中,A.TB試劑(ELISA法)檢測要求采集3ml肝素抗凝靜脈全血,室溫保存,可16 h內使用,從樣品處理到檢測只需要全血分裝和37℃培養2步,操作簡單,不需要專業培訓。檢測過程使用ELISA法,通過制作標準曲線來計算患者特異性T細胞因特異性抗原刺激后干擾素γ分泌的水平。通過標準曲線計算出N、P和T 3個培養管中干擾素γ的含量,以此來判斷結果。因為全血培養檢測模擬人體內自然的免疫反應過程,不改變T細胞的數目和存在環境,結果更真實。T-SPOT.TB試劑(ELISPOT法)檢測要求采集6ml肝素抗凝靜脈全血,室溫保存,僅4 h內使用。處理過程需要PBMCs分離、多次洗滌、T細胞稀釋計數、二氧化碳培養等步驟。操作要求高,需要專門細胞間進行細胞操作。對操作人員的操作要求高,需要進行專門的培訓。該檢測以計算陽性細胞數目來判斷檢測結果,細胞計數可使用顯微鏡和放大鏡進行人工計數,工作量大,受主觀因素影響多;使用酶聯斑點圖像分析儀,其計數準確,但價格昂貴。T-SPOT.TB試劑(ELISPOT法)檢測在試驗操作、試驗條件、人員技術以及儀器設備等方面均要求較高,在臨床檢驗科室使用的便捷性等方面受到限制,不太適合社區等的小型醫院使用。實際操作中T-SPOT.TB試劑(ELISPOT法)檢測結果判讀常見斑點模糊不易計數,陰、陽性對照孔斑點容易污染,甚至出現不確定結果等現象。而A.TB試劑(ELISA法)檢測結果判讀為綜合考慮全血細胞的本底對照、特異性細胞免疫反應、非特異性細胞免疫反應等因素的影響,避免了不確定結果的出現。
雖然A.TB試劑(ELISA法)檢測和T-SPOT.TB試劑(ELISPOT法)檢測是目前檢測結核病的較為準確、先進的2種方法,但它們在試驗技術與臨床應用等方面還存在一些問題,如試驗結果的影響因素不是十分明確,試驗條件有待進一步優化,在結核病伴嚴重免疫系統疾病中的研究不足等。相信通過不斷的探索、研究與改進,定會使A.TB試劑(ELISA法)檢測在結核病檢測中發揮其更大的作用。
[1]王宇.全國第五次結核病流行病學抽樣調查資料匯編[M].北京:軍事醫學科學出版社,2011.
[2]L?nn r oth K,C o r bett E,Golub J,et al.Sy s tematic s c r eening fo r active tube r culo s i s:r ationale,definition s and key con s ide r ation s[J]. I nt J Tube r c L ung Di s,2013,17(3):289-298.
[3]王永怡,王姝,盧福昱,等.2013年感染性疾病熱點回顧[J].傳染病信息,2014,27(1):1-7.
[4]B eh r MA,Wil s on MA,Gill W P,et al.C ompa r ative genomic s of BC G vaccine s bywhole-genome DNAmic r oa rr ay[J].Science,1999, 284(5419):1520-1523.
[5]Mazu r ek GH,J e r eb J,L obue P,et al.Guideline s fo r u s ing the Q uantiFE R O N-T B Gold te s t fo r detecting Mycobacterium tuberculosis infection,U nited State s[J].MMW R R ecomm R ep,2005,54 (RR-15):49-55.
[6]L alvani A.Diagno s ing tube r culo s i s infection in the 21s t centu r y:new tool s to tacklean old enemy[J].C he s t,2007,131(6):1898-1906.
[7]Diel R,L oddenkempe r R,Nienhau s A.Evidence-ba s ed compa r i s on of comme r cial inte r fe r on-gamma r elea s e a ss ay s fo r detecting active T B:ameta analy s i s[J].C he s t,2010,137(4):952-968.
[8]鄭建洲,王亞楠,俞小衛.兩種γ-干擾素釋放試驗診斷結核病的性能比較[J].臨床檢驗雜志,2013,31(7):556-557.
[9]C onnell TG,R itz N,P a x ton GA,etal.A th r ee-way compa r i s on of tube r culin s kin te s ting,Q uantiFE R O N-T B gold and T-S P O T.T B in child r en[J].PL O S O ne,2008,3(7):e2624.
(2014-08-12收稿2014-09-11修回)
(責任編委王永怡本文編輯王姝)
Evaluation of clinical diagnostic performance of interferon-gamma release assays for tuberculosis
QIN Jian-cheng,XU Jun,DAILiang,ZHAO Jing,WANGWei-dong,LIXiang,ZHANG Lan,MAO Yuan-li*
Clinical Laboratory Center,302 Hospital of PLA,Beijing 100039,China
*Corresponding author,E-mail:maoyuanlee@163.com
Objective To evaluate the diagnostic performance and application value of enzyme-linked immunosorbent assay (ELISA)-based interferon-gamma release assays(IGRAs)with A.TB kit for patientswith tuberculosis.M ethods Of 108 patients enrolled in the study,60 were definitely diagnosed with tuberculosis(tuberculosis group),and 48 were controls(non-tuberculosis group). ELISA-based IGRAs with A.TB kit and enzyme-linked immunosorbent spot(ELISPOT)-based IGRAswith T-SPOT.TB kitwere carried out simultaneously.Results The sensitivity and specificity of ELISA-based IGRAs with A.TB kit were 86.67%and 85.42%, and the area under a receiver-operating characteristic(ROC)curve was 0.822[95%confidence interval(CI),0.733-0.912].The sensitivity and specificity of ELISPOT-based IGRAs with T-SPOT.TB kitwere 91.67%and 87.50%,and the area under ROC curve was0.884(95%CI,0.806-0.962).The difference in the area under ROC curvewas notsignificantbetween the two assays(χ2=0.081,P= 0.776).The consistency of the two assays was 87.04%(94/108)with the Kappa value of 0.738.Conclusions ELISA-based IGRAs with A.TB kit and ELISPOT-based IGRAs with T-SPOT.TB kit have a similar overall diagnostic performance,but ELISA-based IGRAswith A.TB kit is superior to ELISPOT-based IGRAswith T-SPOT.TB kit in the operation and interpretation of the test results.
interferon-gamma release tests;Mycobacterium tuberculosis;forecasting;immunoblotting;indicators and reagents
R392.114;R378.911
A
1007-8134(2014)05-0302-04
國家“十二五”科技重大專項(2013ZX09J13106-06A)
100039北京,解放軍第三○二醫院臨床檢驗醫學中心(秦建成、徐軍、戴亮、趙靜、王衛東、李想、張嵐、毛遠麗)
毛遠麗,E-mail:maoyuanlee@163.com

