功能性蛋黃肽的制備及體外活性研究
何 晨,王彥超,常耀光,薛長湖
(中國海洋大學食品科學與工程學院,山東青島 266003)
作為禽蛋的生產大國,我國的雞蛋生產總量連續多年位居世界第一。2012年我國禽蛋產量達到2861萬t,占世界總產量的40%以上。盡管如此,我國市場上的蛋加工制品種類卻非常貧乏,絕大多數以帶殼鮮蛋的形式出售。僅有的幾種蛋加工產品也多是粗加工品(如蛋黃粉)。蛋黃富含多種營養物質,例如蛋白質、脂肪、鐵、鈣、磷、鋅和其他維生素等。
隨著生活水平提高,人們對于從自然生物中提取具有生物活性分子,應用于人類健康和食品貯藏的需求越來越強烈[1]。研究顯示,在所有的生物活性分子中,生物活性肽具有很大的潛力。天然蛋白中的肽往往沒有生物活性,只有在經過蛋白酶水解后才具有了多種生物活性[2]。在眾多的生物活性肽中,磷酸肽因其具有非常鮮明的結構和活性,而成為一類具有很高研究價值的生物大分子物質,高磷酸肽的主要功能基團是磷酸肽絲氨酸殘基。而磷酸酞絲氨酸殘基可以與鈣離子有效結合,阻止不溶性的鈣磷酸鹽形成,從而提高生物價效[3]。
雖然目前國內外對于從蛋黃中分離高磷蛋白及制備磷酸肽的研究已較多,但其制備方法得率相對較低,難以引入工業化的規模生產,例如徐彩娜等人采用雙酶分步水解法的最高得率也僅為11.49%[4]。本文試圖通過優化蛋黃粉的脫脂過程和酶解過程,獲得一種優質蛋黃磷酸肽的制備工藝。同時以商業化產品酪蛋白磷酸肽(CPP)為對照,對本實驗所得產物多肽的功能性質和體外活性進行探究。
1 材料與方法
1.1 材料與儀器
蛋黃粉 購自威海大豐實業有限公司;酪蛋白磷酸肽(CPP) 購自北京奧博星生物技術有限責任公司;DPPH、Ferrozine試劑 購自 Sigma-Aldrich;Alcalase 2.4L 購自諾維信生物有限公司;95%乙醇、正己烷、氯仿、甲醇、濃硫酸、鉬酸鈉、硫酸聯銨、硫酸銅、硫酸鉀、氯化亞鐵、氯化鈣等 均為國產分析純。
SG-4050C型數顯電子恒溫水浴鍋 上海碩光電子科技有限公司;101型電熱鼓風干燥箱 東莞市立佳精密儀器有限公司;BSAZ23S-CW型電子天平Sartorius;TDL-5-A型高速離心機 上海安亭科學儀器廠;3c starter通用型pH計 奧豪斯儀器上海有限公司;HJ-2型磁力攪拌器 常州國華電器有限公司。
1.2 實驗方法
1.2.1 蛋黃肽產品酶解工藝研究
1.2.1.1 工藝過程 蛋黃粉→脫脂→烘干→酶解→滅酶(100℃,10min)→離心取上清(5000r/min,10min)→噴霧干燥
1.2.1.2 脫脂 本文采用乙醇—正己烷脫脂:將蛋黃粉與95%乙醇按照(1/10,w/v)混合,室溫下攪拌提取30min,加入5倍體積的正己烷,室溫下攪拌提取6h,靜置 2h,抽濾,取濾渣,50℃烘干備用[5]。
1.2.1.2 酶解 粗蛋白按照(1/10,w/v)加蒸餾水,用一定濃度的氫氧化鈉調節pH至7,加入Alcalase 2.4L酶(E/S=4%),50℃恒溫水浴鍋中酶解5h。采用水解度(DH)值,即水解度,考察酶解過程中的蛋白質的水解程度隨時間的變化情況。DH值的測定方法采用pH-Stat法[6]。測定方法如下:酶解的過程中,通過補加NaOH溶液,保持反應體系的pH恒定為7。在特定的條件下,水解反應的最終結果只與DH值有關,而在一定條件下,DH值與補加的NaOH體積成正比,水解度的計算公式如式1所示。
本研究以酪蛋白酸鈉為乳化劑,通過pH循環法制備丁香酚微乳,再通過海藻酸鈉對丁香酚微乳進行修飾。考察兩種微乳的粒徑分布、包封率、pH、離子、儲藏穩定性及釋放特性。結果表明,海藻酸鈉修飾能提高丁香酚微乳平均粒徑,具有相當丁香酚的包封率;海藻酸鈉修飾能夠顯著提高丁香酚微乳的pH穩定性,且具有良好的離子和儲藏穩定性;在環境pH為7.0條件下,海藻酸鈉修飾微乳的釋放速率稍高于丁香酚微乳。
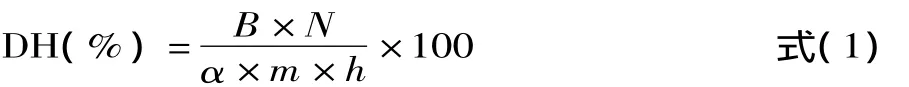
式中:B為消耗NaOH體積;N為NaOH的摩爾濃度;α為平均解離度,0.44;m為被水解蛋白質量;h為每克蛋白質底物具有的肽鍵毫摩爾數,6.850。
1.2.1.3 二次酶解 為了使粗蛋白酶解的更完全,本研究采用兩次酶解的方法。第一次酶解的酶渣烘干后重復第一次酶解的過程。將兩次酶解產物進行混合,計算整個酶解過程的酶解得率。
1.2.2 蛋黃肽的基本性質測定
1.2.2.1 基本成分測定 灰分:按照國標GB/T 5009.4-2010 中的方法測定[7];蛋白質:采用國標GB/T5009.5-2010 中的凱氏定氮法[8];磷元素:采用鉬藍比色法[9]。
1.2.2.2 蛋黃肽在不同pH下的溶解度 分別稱取粗蛋白和蛋黃肽,配成濃度為1%的懸浮液或溶液,用10%鹽酸和4%氫氧化鈉分別調pH至2~10,室溫下振搖10min,使其溶解。2000r/min離心5min取上清。用Folin-酚法[10]測定可溶性蛋白,計算溶解度,公式如式2:

1.2.2.3 蛋黃肽的熱穩定性 分別稱取粗蛋白,蛋黃肽和CPP,配成濃度為1%的懸浮液或溶液,于100℃水浴鍋中加熱30min,測定加熱前后420nm波長下的吸光度值。以吸光度值的變化作為衡量溶液熱穩定性的指標。
1.2.3 蛋黃肽的體外活性實驗
1.2.3.2 DPPH自由基清除實驗 參考文獻[12],分別稱取一定量的粗蛋白,蛋黃肽和CPP,配制成濃度為1.0mg/mL的溶液。取該溶液200μL,加入甲醇600μL,0.15mmol/L 的 DPPH 溶液200μL,混勻2min,室溫條件下避光靜置,測定不同時間517nm波長處的吸光度值,同時做空白對照實驗,實驗過程同上。代入清除率計算式3,計算清除率:

1.2.3.3 金屬鐵離子螯合能力實驗 參考文獻[12],分別稱取一定量的粗蛋白,蛋黃肽和CPP,配制成濃度為1.0、2.0mg/mL的溶液。取該溶液200μL,加入2mmol/L 氯化亞鐵溶液10μL,超純水600μL,5mmol/L Ferrozine溶液 20μL,搖勻 2min,室溫下靜置 10min,測定562nm波長處的吸光度值。同時做空白對照和EDTA陽性對照實驗,實驗過程同上。
2 結果與分析
2.1 酶解工藝研究
由圖1可以看出,兩次酶解的酶解曲線形狀基本相同。在2h內水解率增長迅速,隨后3h內繼續增長但速率明顯減緩。對比兩次酶解過程水解度的變化情況,說明第二次酶解過程中水解度依舊較高,尤其是在反應初始的1h內,甚至超過第一次酶解過程的水解度。通過測定酶解后上清液中的固形物含量得出,第二次水解上清液的固形物含量為3.5%,與第一次水解上清液的3.9%幾乎相同,說明二次酶水解對提高產物的得率具有重要的貢獻。因此,從減低成本和充分利用資源的角度,本實驗優化得蛋黃肽的制備工藝為:二次酶水解,水解時間3h。脫脂率為61.4%,酶解得率為41.0%。
2.2 蛋黃肽的基本性質測定
2.2.1 樣品的灰分與蛋白質含量 由表1可以看出,與粗蛋白相比,蛋黃肽的灰分含量有小幅增加,這是因為在酶解過程中為了使pH保持在最佳酶活范圍內,需要不斷添加堿造成的。雖然目前我國對以蛋黃為原料的多肽產品還沒有標準出臺,但是依據成分類似的大豆肽粉 GB/T22492-2008[13]中的規定,灰分在8%以內,符合標準。蛋黃肽的蛋白含量為86.20%,依照大豆肽粉 GB/T22492-2008[14]中的規定,粗蛋白含量在85%以上,屬于二級質量標準。2.2.2 樣品的磷含量 由表2得出,盡管2.1表明第二次酶解與第一次酶解的水解度相差無幾,但是所得的蛋黃肽的磷含量卻有大幅的降低,大量的磷被留在了酶渣中。磷含量減少而氮含量未明顯降低意味著N/P(摩爾比)比值升高。有研究表明[15],N/P(摩爾比)越低,阻止磷酸鈣沉淀效果越好。因此,本實驗對兩次水解所得產物的體外活性進行了測定。
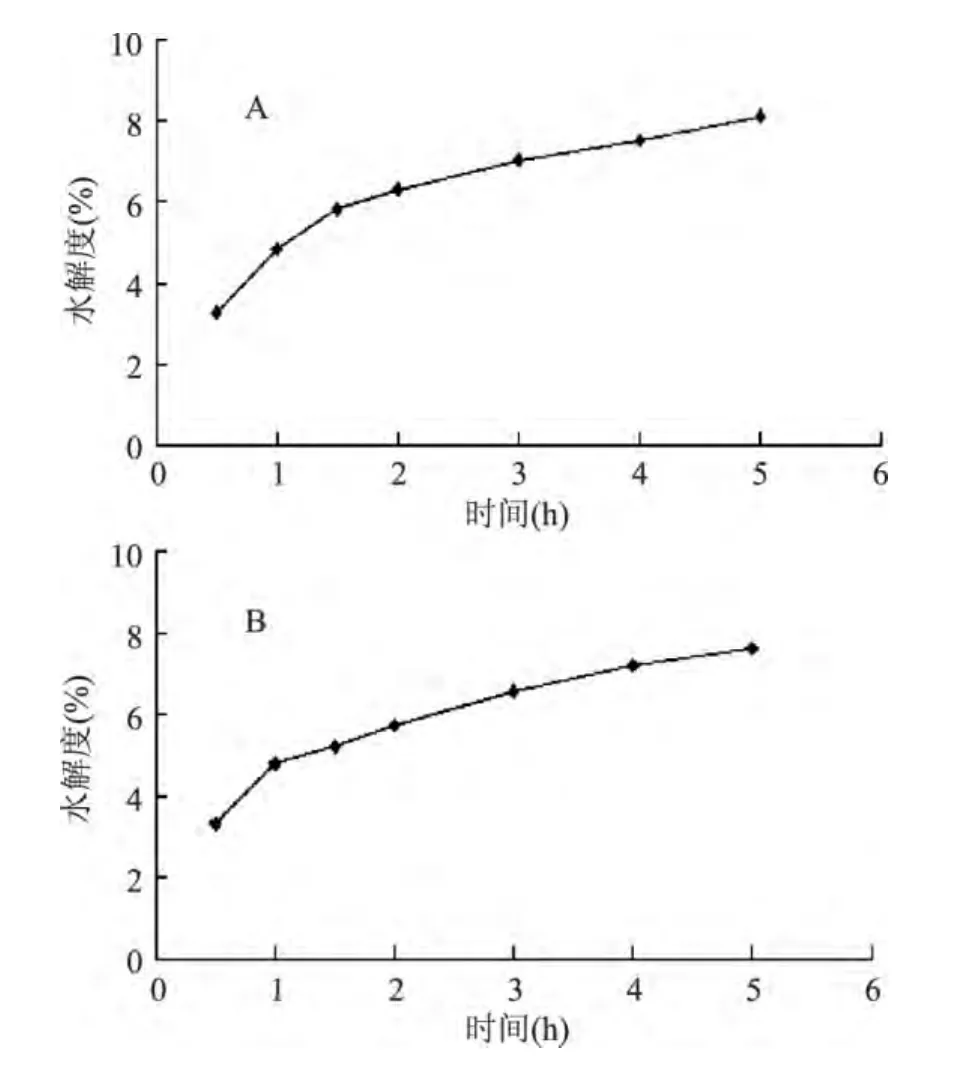
圖1 酶解過程中水解度的變化曲線Fig.1 Changes of hydrolysis degree with a function of reaction time

表1 樣品的蛋白質和灰分含量測定結果Table 1 Determination of protein and ash content in the samples

表2 樣品的磷含量測定結果Table 2 Determination of phosphorus content in the samples
2.2.3 溶解度 能否在寬的pH范圍內都有較好的溶解能力是產品的重要性質。由圖2可以看出,酶解后粗蛋白的溶解度有了較大程度的提高。對于粗蛋白,溶液pH在2~10范圍內,其溶解度分別處于5%~40%。對于蛋黃肽,溶液pH在2~10范圍內,其溶解度均高于40%。溶解度的增大歸因于,蛋白經過水解后親水性的離子化氨基和羥基的暴露。相比較而言,酶解的蛋黃肽的溶解度隨pH的變化更為明顯。pH=4時,溶解度最低(50%),此pH環境接近蛋黃肽的等電點。隨著pH的升高,其溶解度最高可達到90%以上,推測在較低pH時小肽之間容易聚合或生成小聚合物[14]。
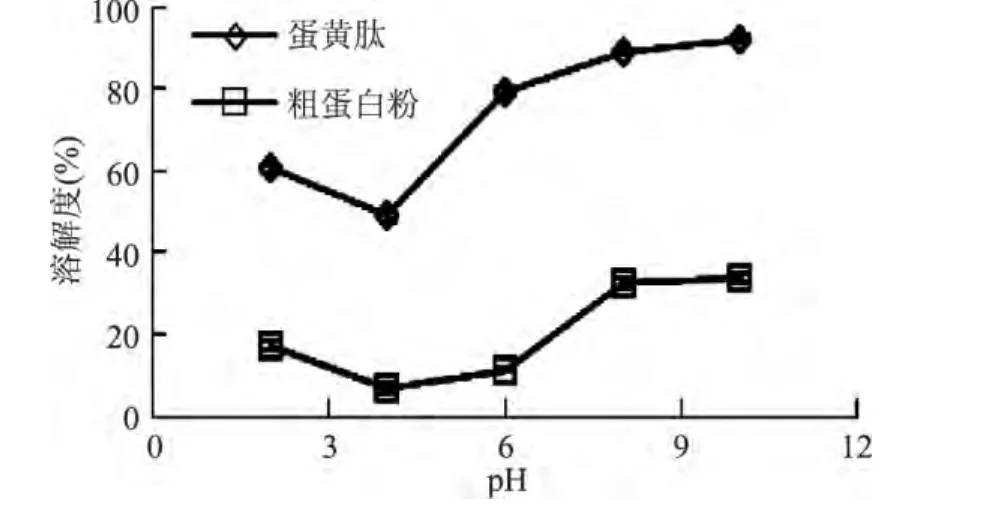
圖2 pH對溶解度的影響Fig.2 Changes of solubility with a function of pH
2.2.4 熱穩定性 產品是否具有較好的熱穩定性,關系到該產品在生產、加工、運輸、貯藏過程中的多項技術指標。由圖3得出,在25℃和100℃條件下,酶解后的蛋黃肽產品較粗蛋白的熱穩定性均顯著增加(p<0.05)。100℃條件下,CPP與蛋黃肽產品的熱穩定性差異不顯著。所以在該產品的加工過程中,可以進行有效的滅菌處理,而不必擔心產品性質的變化。
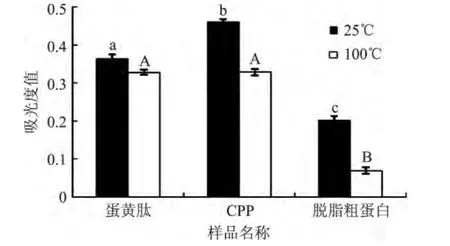
圖3 不同產品的穩定性測定結果Fig.3 Thermal stability determination of different samples
2.3 產品功能體外研究實驗
2.3.1 阻止磷酸鈣沉淀的定性實驗 由圖4得出,空白組和添加粗蛋白組,NaOH滴定量在15min之內迅速上升到8mL,歸因于Ca2+與 PO3+4形成Ca3(PO4)2沉淀,說明粗蛋白不能阻止磷酸鈣沉淀的發生。而添加CPP組和添加蛋黃肽組,NaOH滴定量的突變時間變成了10~30min。說明添加CPP和蛋黃肽可以有效延遲Ca3(PO4)2沉淀的發生。Ca3(PO4)2沉淀生成的時間越遲,說明該樣品的持鈣能力越強。當添加蛋黃肽的濃度達到0.2g/L時,Ca3(PO4)2最終沉淀量僅為空白樣品的1/3。
2.3.2 抗氧化性研究 由圖5得出,蛋黃肽的DPPH自由基清除率顯著高于粗蛋白和CPP的DPPH自由基清除率。隨著反應時間的延長,蛋黃肽和CPP的DPPH自由基清除率均不斷增加。CPP的最高清除率僅為7%,不足蛋黃肽清除率的一半,而粗蛋白幾乎沒有DPPH自由基清除能力。
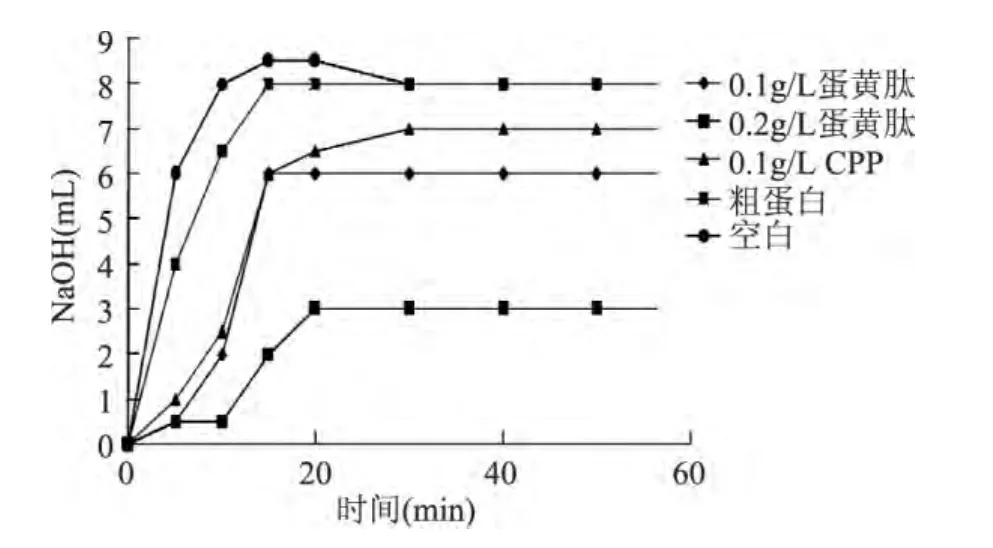
圖4 不同樣品阻止磷酸鈣沉淀效果測定結果Fig.4 Determination of calcium phosphate precipitation with the addition of different samples
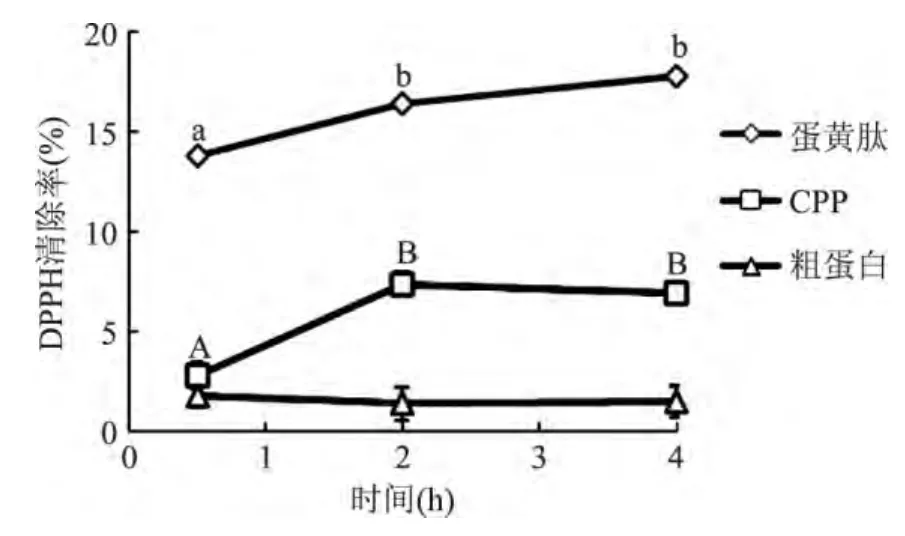
圖5 樣品的DPPH清除率測定結果Fig.5 Determination of DPPH-scavenging abilities of different samples
與Fe2+的螯合能力是一種有效的評價物質抗氧化活性的方法[16]。Fe2+由于具有很強的吸電子能力,能夠誘導自由基反應的產生和傳播。Ferrozine試劑能與Fe2+反應產生紅色的復合物,因此可以通過測定反應液的吸光度值來計算其 Fe2+螯合能力[17]。結果如圖6,粗蛋白幾乎沒有亞鐵離子螯合能力,而CPP和蛋黃肽產品都有明顯的亞鐵離子螯合能力。無論是在1mg/mL還是2mg/mL濃度下,蛋黃肽產品都較CPP在亞鐵離子螯合能力方面有顯著提高。
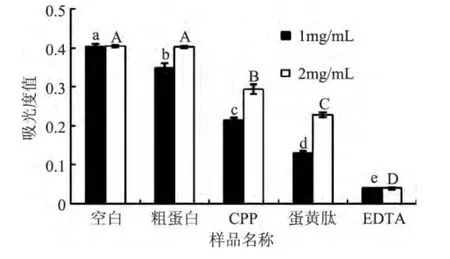
圖6 樣品的亞鐵離子螯合能力測定結果Fig.6 Determination of Fe2+-chelating abilities of different samples
上述實驗結果表明,本實驗所得蛋黃肽產品具有良好的體外抗氧化性,具有開發抗氧化產品的潛在價值。
3 結論
本實驗采用Alcalase 2.4L兩次酶解經乙醇-正己烷脫脂后的粗蛋白可以獲得高品質蛋黃肽產品:得率為41%;蛋白含量大于85%,灰分低于8%;在較寬的pH范圍內有較好的溶解性;熱穩定性良好,可以進行有效的熱滅菌處理。體外活性實驗表明,蛋黃肽產品可以有效延緩和抑制磷酸鈣沉淀的發生,具有較好的DPPH自由基清除能力和亞鐵離子螯合能力,抗氧化性良好。本實驗的工藝簡單,可以高效制備高品質蛋黃肽,對蛋黃粉的有效利用和其加工制品的開發應用具有重要的應用價值。
[1]McCann KB,Shiell BJ,Michalski WP,et al.Isolation and characterization of antibacterial peptides derived from the f(164-207)region of bovine αs2- casein[J].International Dairy Journal,2005,15:113-143.
[2]Korhonen H,Pihlanto A.Bioactive peptides:production and functionality[J].International Dairy Journal,2006,16:549-560.
[3]徐彩娜,殷涌光,王二雷,等.卵黃高磷蛋白及其磷酸肽的研究進展[J].食品工業科技,2010,31(9):428-451.
[4]徐彩娜,林松毅,劉靜波,等.雙酶分步水解制備卵黃高磷蛋白磷酸肽的實驗研究[J].食品科技,2008,11:6-10.
[5]張維農,劉大川,胡小泓.正己烷-含水乙醇混合溶劑制取大豆濃縮蛋白工藝的研究[J].中國油脂,2002,04:42-44.
[6]Nissen JA.Enzymic Hydrolysis of Food Proteins[M].Elsevier Applied Science Publishers,1986:132-152.
[7]GB/T 5009.4-2010 食品中灰分的測定[S].
[8]GB/T5009.5-2010食品中蛋白質的測定[S].
[9]馬文,趙亮,謝復新,等.鉬藍法測定玉米漿中磷含量[J].安徽大學學報,1996,01:31-33.
[10]蔡武城,袁厚積.生物物質常用化學分析法[M].北京:科學出版社,1982,93.
[11]劉小麗.卵黃高磷蛋白及其磷酸肽的制備和研究[D].西安:西北大學,2003.
[12]Mina MY,Ahmad A,JamshidKhan C.A novel antioxidant and antimicrobial peptide from hen egg white lysozyme hydrolyzates[J].Journal of Functional Food,2012(4):278-286.
[13]GB/T 22492-2008 大豆肽粉[S].
[14]陳歷俊.大豆活性肽的研制與應用[D].哈爾濱:東北農業大學,1998.
[15]LiY,TomeD,DesjeuxJF.Indirecteffectofcasein phosphopeptides on calcium absorption in rat ileumin vitro[J].Reproduction,Nutrition,Development,1989,29:227-233.
[16]Hsu CL,Chen WL,Weng YM,et al.Chemical composition,physical properties,and antioxidant activities of yam flours as affected by different drying methods[J].Food Chemistry,2003,83:85-92.
[17]Ishikawa S,Yano Y,Arihara K,et al.Egg yolk phosvitin inhibits hydroxyl radical formation from the Fenton reaction[J].Bioscience, Biotechnology, and Biochemistry, 2004, 68:1324-1331.

