N-甲基-N,N-雙十二烷基殼聚糖鹽酸鹽的合成及自組裝囊泡性能
洪鍵淞,辛梅華,李明春,方江海
(華僑大學材料科學與工程學院,環境友好功能材料教育部工程中心,福建 廈門 361021)
囊泡既有親水性又有疏水性,結構上自我封閉,具有保護藥物生物活性、有效地控制藥物釋放、提高穩定性和療效、延長半衰期及降低藥物毒副作用等諸多優點,作為新型藥物載體被廣泛研究,并用于動物體內外藥物實驗。
囊泡作為藥物載體有兩大特點[1]:一是具有包載多種類型藥物的能力,囊泡的空腔可包載較大量的水溶性藥物,夾在兩層親水基團中間的疏水微相也可包裹一些疏水性藥物,囊泡的不同形態也使其包載藥物分子的范圍更加廣泛;二是賦予藥物更好的生物相容性和靶向性,囊泡具有雙層膜結構,與生物膜有良好的相容性和細胞透過性。
囊泡制備方法很多,有乙醇注射法、薄膜分散法及逆相蒸發法等[2-5]。但除了乙醇注射法外,其他的制備方法往往大量使用有機溶劑,可能會使藥物變性,且會造成環境污染及藥物有機溶劑殘留。乙醇注射法因制備簡單、成本低、條件溫和以及不會導致藥物降解或氧化等優點而備受關注。Yang等[5]設計了自動乙醇注射法制囊泡及自動檢測粒徑的裝置,獲得一系列不同配方的磷脂載藥囊泡,對囊泡配方進行優選。Justo等[6]研究了溫度和放大生產對乙醇注射法制囊泡的影響,結果表明,在較高溫度下制得的囊泡粒徑分布更窄,能夠得到更為均勻的體系,放大實驗表明結果可重復。殼聚糖具有無毒、可生物降解和良好的生物相容性等優點。但采用乙醇注射法制備殼聚糖載藥囊泡未見報道,一個重要的原因是乙醇注射法制囊泡要求囊材溶于乙醇而不溶于水。本文作者課題組[7]合成的高取代N,N-雙長鏈烷基殼聚糖(NLCS)具有良好的有機溶劑溶解性,在NLCS的氨基進一步引入甲基得到N-甲基-N,N-雙十二烷基殼聚糖鹽酸鹽(TMC),能溶于甲醇、乙醇和乙醚等,為進一步應用提供了方便。本文采用乙醇注射法制備TMC囊泡,并分別以維生素B12和酮洛芬作為親/疏水性模型藥物,研究不同pH值制備介質中制得的載藥TMC囊泡的載藥性能。
1 實驗部分
1.1 主要儀器和試劑
Nexusu 470 型傅里葉變換紅外光譜儀(Nicolet);Vario MICRO 元素分析儀(Elementar);THZ-82型恒溫振蕩器(江蘇常州國華儀器廠);TU-1810紫外可見分光光度計(北京普析通用儀器有限公司);FD-1B-50冷凍干燥機(北京博醫康實驗儀器有限公司);ZEN3600納米激光粒度及 Zeta電位分析儀(Malvern);超速冷凍離心機(Kendro SORVALL)。
1.2 N-甲基-N,N雙十二烷基殼聚糖鹽酸鹽的制備
參照本實驗室的方法合成 N,N-雙十二烷基殼聚糖(NLCS)[7],見圖1。然后將1g NLCS溶解于100 mL四氫呋喃中,加入過量碘甲烷,50 ℃下回流攪拌反應72 h。旋轉蒸發儀除去溶劑和過量的碘甲烷,真空干燥得N-甲基-N,N-雙十二烷基殼聚糖碘酸鹽(TMIC)。將TMIC溶解于少量乙醇中,分別用 NaCl溶液和去離子水透析,冷凍干燥至恒重得N-甲基-N,N-雙十二烷基殼聚糖鹽酸鹽(TMC)。制得的產物能溶于乙醇等有機溶劑。采用元素分析法,由C/N 摩爾比計算產物的季胺化取代度為0.75,高的季胺化度提高了產物的親水能力。
1.3 TMC載藥囊泡的制備
參照文獻[6]的操作制備載親/疏水性藥物囊泡。
(1)載親水性藥物囊泡的制備 將 50 mg N-甲基-N,N-雙十二烷基殼聚糖鹽酸鹽溶解于1 mL乙醇中。在450 r/min攪拌下以100 μL/min的速度緩慢滴加到50 ℃的含維生素B12的水溶液或pH值為 4.0和pH值為 1.2的鹽酸溶液中。滴加完后繼續攪拌90 min,以揮發盡乙醇,即得載藥囊泡。將囊泡溶液調為中性。超速冷凍離心除去未包封的藥物得載維生素B12囊泡。
(2)載疏水性藥物囊泡的制備 將 50 mg N-甲基-N,N-雙十二烷基殼聚糖鹽酸鹽和8 mg酮洛芬溶解于1 mL乙醇中,在450 r/min攪拌下以100 μL/min的速度緩慢滴加到50 ℃的水溶液或pH值為4.0和pH值為1.2的鹽酸溶液中。按照(1)操作得載酮洛芬囊泡。
1.4 載藥囊泡的體外釋放
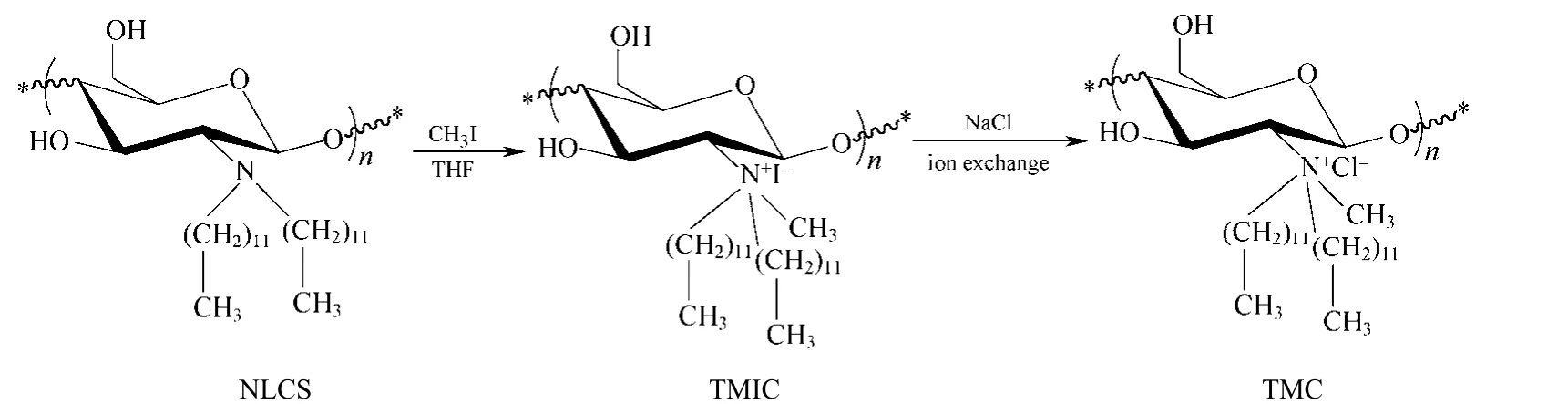
圖1 N-甲基-N,N-雙十二烷基殼聚糖鹽酸鹽的制備
取一定量載藥囊泡于透析袋中,在模擬腸液或模擬胃液中釋放。間隔一定時間取出5 mL透析液,再補充5 mL相應的新鮮介質。取出的溶液在361 nm(維生素B12)或260 nm(酮洛芬)下測定吸光度。根據相應的線性回歸方程計算釋放量繪制釋放曲線。
1.5 載藥囊泡的包封率和載藥量
根據標準曲線回歸方程計算釋放平衡時藥物的總釋放量M1(g)。然后將透析袋中的囊泡倒出,加入其5倍體積的無水乙醇將囊泡破壞后,分光光度計測定未釋放藥物的質量 M2(g)。總投藥量為 M(g),囊泡質量為M3(g)。載藥囊泡的包封率和載藥量計算如式(1)、式(2)。
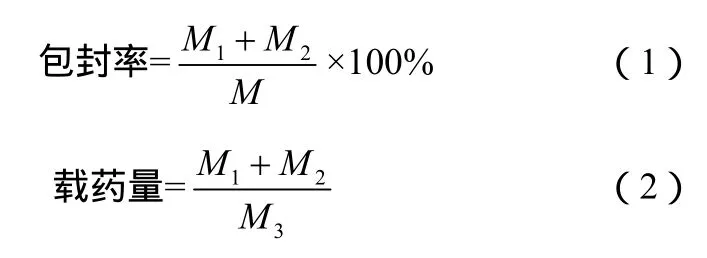
2 結果與討論
2.1 N-甲基-N,N-雙十二烷基殼聚糖鹽酸鹽的FT-IR分析
采用 KBr壓片法,測得CS、NLCS和TMC的FT-IR如圖2所示。CS上1520~1640 cm?l的混合譜帶是氨基的變形振動吸收峰,而 NLCS和 TMC上這個峰消失,表明其氨基已經發生了反應。與CS相比,NLCS 和 TMC 在 2850 cm?l和 2920 cm?l左右的 C—H 伸縮振動峰增強,說明其在殼聚糖上引入了甲基和亞甲基。并且NLCS和TMC在1470 cm?l和720 cm?1附近出現了新峰,其中1470 cm?1是亞甲基的C—H變形振動,720 cm?1是(CH2)n(n≥4)基團的骨架吸收峰,說明兩種產物都引入了長鏈烷基。對比NLCS與TMC的紅外譜圖,兩者亞甲基與甲基峰面積的比值不同,NLCS在2850 cm?1亞甲基峰面積與1380 cm?1甲基峰面積的比值為0.576,而TMC為0.220。亞甲基與甲基峰面積比值的降低說明NLCS已季銨化。
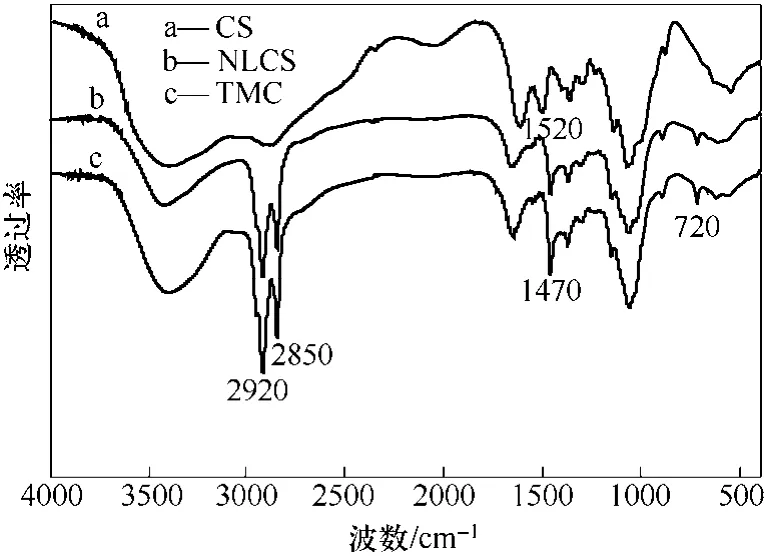
圖2 原料及產物的FTIR譜圖
2.2 囊泡的粒徑分布及Zeta電位
囊泡的粒徑大小及其分布影響藥物在體內的滯留時間,測定粒徑及其分布可以預測制劑的體內行為,為優化制備工藝及其配方提供依據。乙醇注射法制得的囊泡粒徑可通過調整制備參數來改變,如囊材組成及濃度、注射速度、囊材/溶液比例、溫度及攪拌速度等[5-6]。調節制備水相pH值成本低、操作簡便、可操作性強。本文主要研究pH值對TMC囊泡的影響。
取囊泡混懸液,25 ℃下用激光粒度儀測定在不同介質中制得的載不同藥物囊泡的粒徑、分布以及Zeta電位,結果見表1。可見,制得的囊泡粒徑范圍在50~100 nm,多分散系數為0.17~0.26。Justo等[6]研究表明,制備介質pH值對乙醇注射法制得的磷脂囊泡粒徑影響不大。而表1顯示,降低制備水相pH值可使TMC囊泡粒徑大大降低,這可能是因為制備介質pH值的變化對N-甲基-N,N-雙十二烷基殼聚糖鹽酸鹽的自組裝行為產生了影響,本文將在2.4節引入Langmuir膜技術進一步討論。囊泡的粒徑大小除了影響藥物在體內的滯留時間外,還會影響囊泡的釋藥行為,這將在后面囊泡的釋放性能中進一步討論。
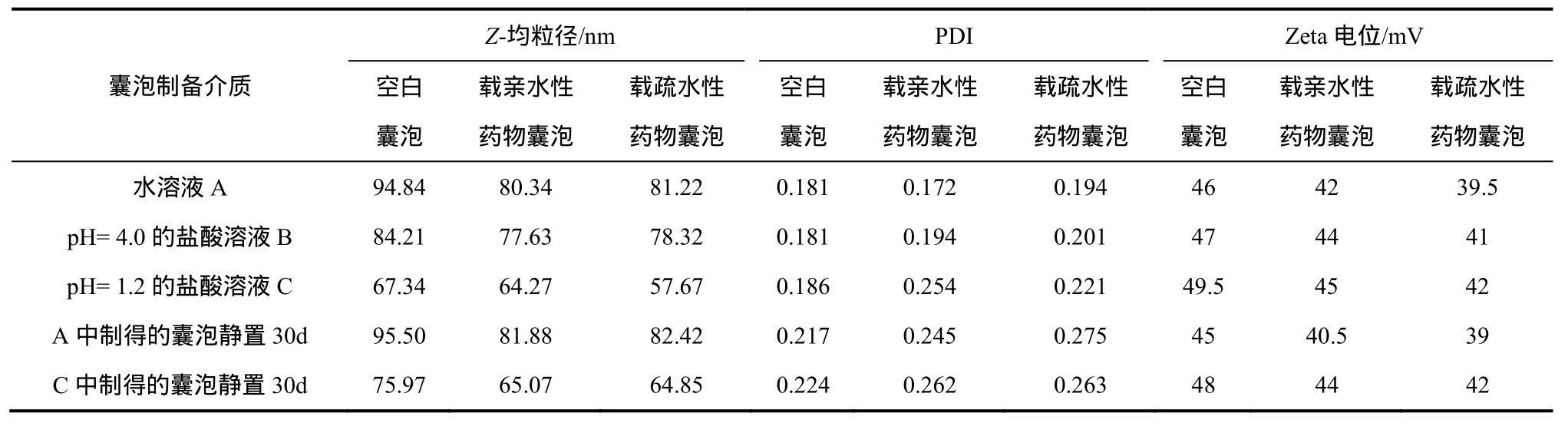
表1 囊泡的粒徑大小、分布以及Zeta電位
將在不同介質中制得的囊泡靜置30天,均未出現沉淀或分層現象。制備介質為水溶液的囊泡靜置前后粒徑幾乎不變,而制備介質為pH值為1.2鹽酸溶液的囊泡靜置后粒徑略有增大(約8 nm)。這可能是因為制備介質為pH值為1.2的囊泡制備完成后將pH值調至中性,結果囊泡在靜置過程中略微溶脹。不同囊泡靜置后PDI只是略微增大,說明不同制備介質下制備的囊泡在 30天內均保持較好的穩定性。
Zeta電位一定程度上可反映微粒分散體的穩定性,通常認為Zeta電位絕對值大于30 mV時微粒分散體能穩定存在,即微粒之間需要克服較高能壘才能聚集在一起[8]。表1顯示,各種囊泡的Zeta電位均大于35 mV,說明囊泡能夠穩定存在。載疏水性藥物囊泡的Zeta電位降低較多,可能因為囊泡表面吸附著一些藥物或疏水性藥物部分鑲嵌到囊泡表面,降低了囊泡的表面電荷[9]。制備介質pH值降低,囊泡的Zeta電位也略為增大,這可能因為囊泡粒徑的降低,增大了囊泡表面的電荷密度[9]。靜置30天后,囊泡的Zeta電位只是略為降低,進一步說明囊泡能穩定存在。
2.3 囊泡的體外釋放性能
2.3.1 載親水性藥物囊泡的釋放曲線
按照實驗部分 1.4節的操作進行載維生素 B12囊泡的釋放試驗。取出的溶液在UV361 nm下測定吸光值,根據維生素 B12的線性回歸方程(模擬腸液:A=0.05829C?0.00036,R2=0.9995。模擬胃液:A=0.05692C+0.0032,R2=0.9985。線性范圍均為0~53.6 μg/mL)計算釋放量,繪制不同介質制備載親水性藥物囊泡在不同釋放介質下的藥物釋放曲線如圖3,符合緩控釋制劑0~2 h內藥物累計釋放率需低于30%的要求[10]。由圖3可見,在不同pH值的釋放介質中,制備介質的pH值越低,囊泡藥物釋放速率和平衡釋藥率越低。一般地,囊泡的粒徑較小其藥物釋放率和平衡釋放率較高[9]。而本文制備介質pH值降低后,TMC囊泡粒徑減小(表1),藥物釋放率和平衡釋放率反而下降,這可能是因為介質pH值降低增加了N-甲基-N,N-雙十二烷基殼聚糖鹽酸鹽的親水性,使囊泡自組裝更易形成,囊泡變得更為致密,這將在2.4節中引入Langmuir膜技術進一步討論。
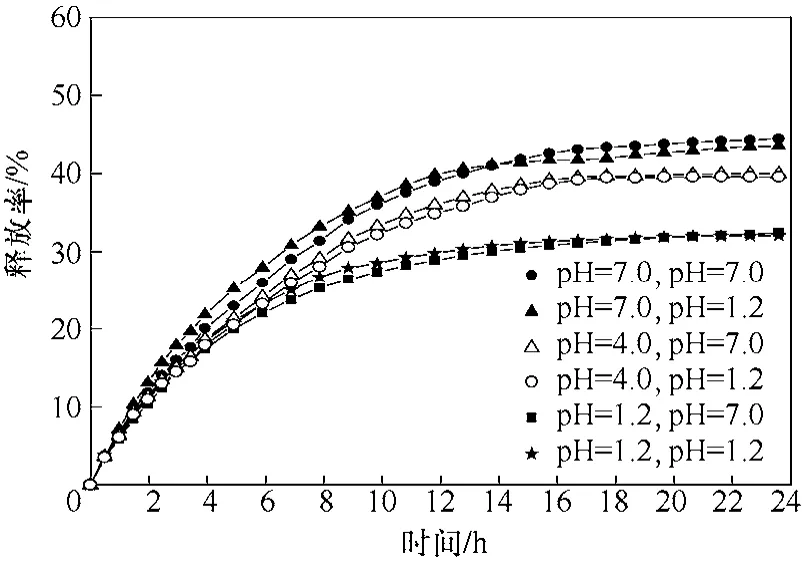
圖3 不同介質制備載親水藥物囊泡在不同介質的釋放曲線
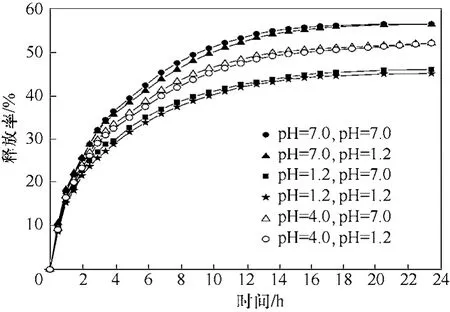
圖4 不同介質制備載疏水藥物囊泡在不同介質的釋放曲線
由圖3還可以看出,同一介質制備的載親水性藥物囊泡在不同釋放介質的釋放速率和平衡釋放率相差不大,說明釋放介質的pH值變化對載維生素B12的TMC囊泡釋藥行為影響較小。這與阿奇霉素囊泡在不同pH值下的釋放行為沒有明顯變化的結果一致[11]。
2.3.2 載疏水性藥物囊泡的釋放曲線
按照實驗部分1.4節的操作進行載酮洛芬囊泡的釋放試驗。取出的溶液在UV260 nm下測定吸光值,根據酮洛芬的線性回歸方程(模擬腸液:A=0.0681C?0.007,R2=0.9999。模擬胃液:A=0.0611C+0.0101,R2=0.9998。線性范圍均為0~30 μg/mL)計算釋放量,繪制不同介質制備的載疏水性藥物囊泡在不同釋放介質的藥物釋放曲線如圖 4,同樣符合緩控釋制劑的釋藥要求。由圖4可見,與載親水性藥物囊泡的釋放曲線規律相似,在不同pH值的釋放介質下,制備介質的pH值越低,囊泡藥物釋放速率和平衡釋藥率越低。同一介質制得的載疏水性藥物囊泡的釋放行為相差不大。
比較圖4和圖3可以發現,同一介質下制得的載疏水性藥物囊泡的釋放速率和平衡釋藥率比載親水性藥物囊泡的高,并且載疏水藥物囊泡的突釋更加明顯。而不同介質制得的載疏水性藥物囊泡藥物釋放行為變化程度比載親水性藥物囊泡藥物釋放行為變化低。這可能是因為疏水性藥物主要包含在囊材的疏水微相中,能夠更好地擴散出來[12]。
2.4 不同亞相pH值下TMC的Langmuir膜行為
囊材的 Langmuir膜行為與囊泡的藥物釋放行為有很大的聯系[3]。改變亞相的pH值測得TMC的Langmuir膜π-A等溫線如圖5所示。由圖5中可以看出,隨著亞相 pH值的降低,TMC的 Langmuir膜π-A等溫線逐漸向左移,極限分子表面積逐漸降低,說明單分子膜排列得更為緊密;崩潰壓略有升高,說明Langmuir膜穩定性上升。TMC的Langmuir膜行為表明,在較低的pH值下,TMC具有更好的成膜性,亦即在較低pH值下,TMC能夠更好地自組裝,這與2.2節和2.3.1節的分析一致。
2.5 包封率和載藥量測定
按照實驗部分1.5節操作,測定在不同介質中制得的載親/疏水藥物 TMC囊泡的載藥量和包封率,結果見表2。
從表2可見,由于乙醇注射法制備載親水性藥物囊泡是將藥物分散在水相,所以制得的囊泡包封率和載藥量比較低,可考慮將含藥物的水相重復使用。并且載親水性藥物囊泡的載藥量比載疏水性藥物低,這可能是因為在形成囊泡時,親水性藥物傾向于擴散到體積更大的液相中,而疏水性藥物則傾向于包埋到囊泡的疏水層中[13]。采用乙醇注射法制備 TMC載疏水性藥物囊泡的載藥量高于逆相蒸發法制備 N,N-雙十二烷基殼聚糖囊泡的載藥量 0.14 mg/mg[7],并且高于微乳化法制備羧甲基殼聚糖十八烷基季銨鹽囊泡的載藥量0.20 mg/mg[8]。
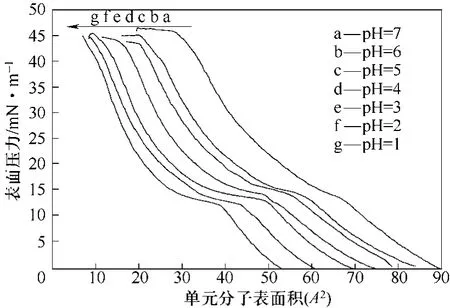
圖5 不同亞相pH值下TMC的Langmuir膜π-A等溫線
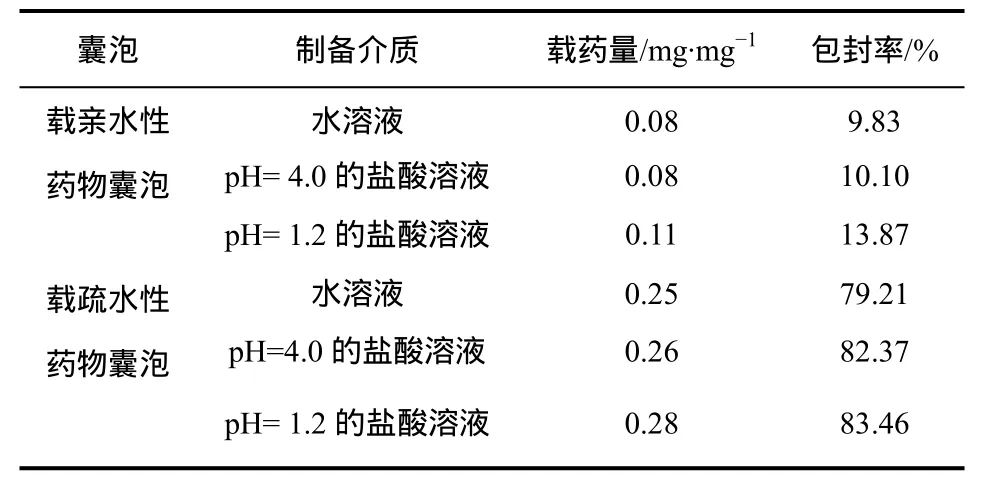
表2 不同介質制備囊泡的載藥量和包封率
由表2還可以看出,制備介質的pH值降低,所制得的載親/疏水性藥物囊泡的包封率和載藥量均有所提高。這可能是因為在酸性條件下制得的囊泡較為致密,制備過程藥物泄漏較少;并且因為囊泡體積較小(表 1),總表面積較大,藥物包封量增加[9]。
3 結 論
以殼聚糖為原料制備 N-甲基-N,N-雙十二烷基殼聚糖鹽酸鹽(TMC),烷基鏈取代度達 1.58,季銨化取代度為0.75,季銨化增加了產物親水性。產物可溶于乙醇、甲醇、氯仿和四氫呋喃等有機溶劑中,為進一步制備自組裝囊泡提供方便。采用乙醇注射法制備TMC囊泡,研究不同pH值介質中制得的載親/疏水TMC囊泡的載藥及釋放性能。結果表明,制得的TMC自組裝囊泡為納米級,靜置30天后仍保持穩定。Langmuir膜行為研究表明在較低pH值下TMC更易自組裝,但制備介質pH值不同對囊泡的粒徑、藥物釋放行為影響較大,而釋藥環境pH值對囊泡的藥物釋放行為影響較小,為N-甲基-N,N-雙十二烷基殼聚糖鹽酸鹽自組裝載藥囊泡的應用提供依據。
[1]Tian B,Tao X G,Ren T Y,et al. Polypeptide-based vesicles:Formation,properties and application for drug delivery[J]. Journal of Materials Chemistry,2012,22:17404-17414.
[2]鄧英杰. 脂質體技術[M]. 北京:人民衛生出版社,2007.
[3]Li M C,Su S,Xin M H,et al. Relationship between N,N-dialkyl chitosan monolayer and corresponding vesicle[J]. Journal of Colloid and Interface Science,2007,311:285-288.
[4]Gianolio E,Porto S,Napolitano R,et al. Relaxometric investigations and MRI evaluation of a liposome-loaded pH-responsive gadolinium(iii) complex[J]. Inorg. Chem.,2012,51:7210-7217.
[5]Yang K,Delaney J T,Schubert U S. et al. Fast high-throughput screening of temoporfin-loaded liposomal formulations prepared by ethanol injection method[J]. Journal of Liposome Research,2012,22(1):31-41.
[6]Justo O R,Moraes ? M. Analysis of process parameters on the characteristics of liposomes prepared by ethanol injection with a view to process scale-up:Effect of temperature and batch volume[J].Chemical Engineering Research and Design,2011,89:785-792.
[7]Li M C,Xin M H,Su S. Novel biomaterial study Ι:N,N-dilong chain alkyl chitosan (NCS) for self-assembled nanovesicle and NCS/PLLA blend for tissue engineering scaffold[J]. Proceedings of the International Conference on BioMedical Engineering and Informatics,2008,1:748-750.
[8]Chatterjee S,Salaun F,Campagne C,et al. Preparation of microcapsules with multi-layers structure stabilized by chitosan and sodium dodecyl sulfate[J]. Carbohydrate Polymers,2012,90:967-975.
[9]Laouini A,Jaafar-Maalej C,Gandoura S,C et al. Spironolactoneloaded liposomes produced using a membrane contactor method:An improvement of the ethanol injection technique[J]. Progr. Colloid.Polym. Sci.,2012,139:23-28.
[10]國家藥典委員會. 中華人民共和國藥典[M]. 北京:化學工業出版社,2010.
[11]鐘萌,譚群友,馮悅. 阿奇霉素囊泡體外釋放行為的初步研究[J].中國抗生素雜志,2012,37(6):476-480.
[12]Liang X F,Hu J Y,Chen F H. Characterization of chitosan polymeric ethosomes capable of encapsulating hydrophobic and hydrophilic drugs prepared by a microemulsion method[J]. Acta Phys. Chim. Sin,2012,28(4):897-902.
[13]Yin Y T,Misni M,Kah H L. Effect of ph on physicochemical properties and encapsulation efficiency of PEGylated linolenic acid vesicles[J]. E-Journal of Chemistry,2012,9(2):729-738.

