不同煎煮方法對麻杏石甘湯中成分變化研究
饒 毅,張五萍,魏惠珍,高 萌,金浩鑫,王躍生
(1.中藥固體制劑制造技術國家工程研究中心,江西南昌 330006;2.江西省人民醫院,江西南昌 330006;3.江西中醫藥大學,江西南昌 330006;4.中國中醫科學院中藥研究所,北京 100700)
麻杏石甘湯源自漢代張仲景的《傷寒論》,由麻黃、杏仁、石膏、炙甘草四味藥組成。煎煮方法為:“上四味,以水七升,煮麻黃,減二升,去上沫,納諸藥,煮取二升,去滓。”即麻黃先煎。石膏為礦物質藥,質重、堅硬、難以煎出藥味的藥物應先煎[1],《中國藥典》中亦規定石膏的用法為先煎[2]。《中國藥典》2010年版中記載小兒清熱口服液采用麻黃石膏先煎。目前對麻杏石甘湯先煎的合理性及必要性存在較大爭議[3-7],因此對目前存在的3種煎煮方法 (麻黃先煎、石膏先煎、麻黃石膏先煎)的合理性進行研究。麻黃堿、偽麻黃堿、甘草苷、甘草酸、苦杏仁苷、鈣及金屬元素為麻杏石甘湯主要藥效成分[9-10]。本實驗通過固定湯劑煎煮時間,以合煎為參照,湯劑中除Ca外的金屬元素含有量較低,Mg、Zn、Mn、V含有量最高,研究通過測定各藥效成分及這幾種金屬元素的量,從化學成分的角度考察確定最優的煎煮方法,為麻杏石甘湯臨床用煎煮方式提供參考依據。
1 儀器與材料
1.1 儀器 Waters2695-2996高效液相色譜儀(PDA檢測器);Agilent 1100高效液相色譜儀(DAD檢測器);Optima-5300DV型等離子體發射光譜儀 (美國PerkinElmer公司);Millipore-Q純水器 (美國MILLIPORE公司);KDM型調溫電熱套(山東鄄城華魯電熱儀器有限公司)。
1.2 材料 鹽酸麻黃堿、鹽酸偽麻黃堿、苦杏仁苷、甘草苷、甘草酸均由中國藥品生物制品檢定所提供,供含量測定用。生麻黃、生石膏、炙甘草飲片購于北京市雙橋燕京飲片廠,苦杏仁購于江中(武寧)中藥飲片有限公司,經江西中醫學院付曉梅教授鑒定。
Ca(鈣)、Mg(鎂)、Zn(鋅)、Mn(錳)、V(釩)標準液,國家標準物質研究中心提供,100 μg/mL,臨用時用1%HNO3(體積分數)配制成應用液。
甲醇、乙腈為色譜純,高氯酸、硝酸為優級純,氨水、乙醚、磷酸為分析純,水為超純水。
2 方法與結果
2.1 湯劑的煎煮方法
2.1.1 麻黃先煎 稱取麻黃24 g,加水1344 mL,開始煎煮,待沸騰后,調整煎煮火候至文火煎煮30 min后,再加入苦杏仁24 g、甘草24 g、石膏96 g,文火繼續煎煮40 min,紗布濾過,即得。
2.1.2 石膏先煎 稱取石膏96 g,加水1344 mL,開始煎煮,待沸騰后,調整煎煮火候至文火煎煮30 min后,再加入麻黃24 g、苦杏仁24 g、甘草24 g,文火繼續煎煮40 min,紗布濾過,即得。
2.1.3 麻黃石膏先煎 稱取麻黃24 g、石膏96 g,加水1344 mL,開始煎煮,待沸騰后,調整煎煮火候至文火煎煮30 min后,再加入苦杏仁24 g,甘草24 g,文火繼續煎煮40 min,紗布濾過,即得。
2.1.4 合煎 稱取麻黃24 g、苦杏仁24 g、甘草24 g、石膏96 g,加水1344 mL,開始煎煮,待沸騰后,調整煎煮火候至文火煎煮40 min,紗布濾過,即得。
2.2 麻杏石甘湯中麻黃堿、偽麻黃堿測定
2.2.1 供試品溶液的制備 精密量取麻杏石甘湯10 mL至50 mL量瓶中,加甲醇35 mL,超聲30 min,放冷后,用甲醇定容至刻度,以0.45 μm微孔濾膜濾過,即得。
2.2.2 對照品溶液的配制 精密稱取麻黃堿、鹽酸偽麻黃堿對照品適量,加甲醇分別制成每1 mL含0.051 mg麻黃堿、0.0454 mg偽麻黃堿的溶液。
2.2.3 方法學考察 對麻黃堿、偽麻黃堿進行了方法學指標考察,結果麻黃堿回歸方程為y=25330x-1586,r=0.9998,偽麻黃堿回歸方程為y=16525x-532.18,r=0.9999;線性范圍分別為0.0510 ~2.040 μg、0.0454 ~1.8160 μg;精密度試驗兩者的RSD分別為0.57%、1.08%;重復性試驗RSD分別為1.94%、1.24%;穩定性試驗RSD分別為0.76%、0.74%;平均回收率分別為99.60%、99.03%,RSD分別為1.27%、1.96%。
2.2.4 樣品測定 流動相為乙腈-0.1%磷酸(5∶95),檢測波長207 nm,柱溫為室溫;體積流量1 mL/min;進樣體積10 μL。色譜圖見圖1。

圖1 麻杏石甘湯中麻黃堿、偽麻黃堿測定色譜圖Fig.1 Chromatograms of ephedrine and pseudoephedrine
2.3 麻杏石甘湯中苦杏仁苷測定
2.3.1 供試品的制備 精密量取煎煮液5 mL,加氨水5 mL,渦旋混合1 min,超速離心 (12000 r/min,3 min)后取上清液以乙醚洗滌2次 (每次10 mL),棄去醚層,將水層置氮氣流下吹干,殘渣加甲醇1 mL溶解,超速離心后取上清液,即得。
2.3.2 對照品的配制 精密稱取苦杏仁苷對照品適量,用甲醇配制為每1 mL含0.0431 mg苦杏仁苷的溶液。
2.3.3 方法學考察 對苦杏仁苷進行了方法學指標考察,結果苦杏仁苷回歸方程為y=28837x-1305,r=0.9999,線性范圍分別為0.0431~1.724 μg;精密度試驗RSD為1.06%;重復性試驗RSD為1.37%;穩定性試驗RSD為0.83%;平均回收率為98.75%,RSD為2.97%。
2.3.4 樣品測定 流動相為甲醇-水 (20∶80),檢測波長207nm;柱溫為室溫;體積流量1 mL/min;進樣體積10 μL。色譜圖見圖2。
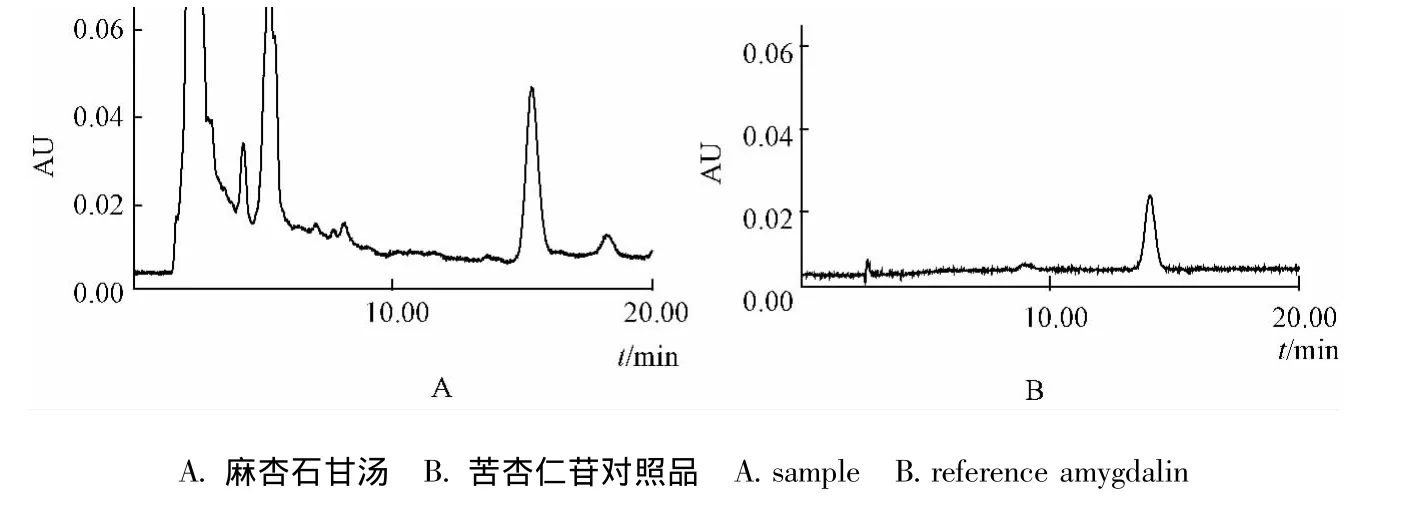
圖2 麻杏石甘湯中苦杏仁苷測定色譜圖Fig.2 Chromatograms of amygdalin
2.4 麻杏石甘湯中甘草苷、甘草酸測定
2.4.1 供試品的制備 同麻黃堿、偽麻黃堿供試品的制備。
2.4.2 對照品的配制 稱取甘草苷、甘草酸對照品適量,加70%乙醇制成每1 mL含0.02032 mg甘草苷、0.08445 mg甘草酸對照品溶液 (甘草酸對照品質量濃度=甘草酸銨對照品質量濃度/1.0207)。
2.4.3 方法學考察 對甘草苷、甘草酸進行了方法學指標考察,結果甘草苷回歸方程為y=44043x+11448,r=0.9998,甘草酸為 y=137754x+466.33,r=0.9998,線性范圍分別為0.0203 ~0.8128 μg、0.0845~3.37804 μg;精密度試驗 RSD分別為1.29%、2.01%;重復性試驗RSD分別為2.54%、2.89%;穩定性試驗RSD分別為1.09%、0.74%;平均回收率分別為99.29%、100.75%,RSD分別為2.54%、2.86%。
2.4.4 樣品測定 流動相為乙腈-0.1%磷酸,進行梯度洗脫 [0 min,乙腈-0.1%磷酸 (18∶82);10 min,乙腈-0.1%磷酸 (18∶82);40 min,乙腈-0.1%磷酸 (40∶60);60 min,乙腈-0.1%磷酸(40∶60)];檢測波長237 nm;柱溫為室溫;體積流量1 mL/min;進樣體積10 μL。色譜圖如圖3。
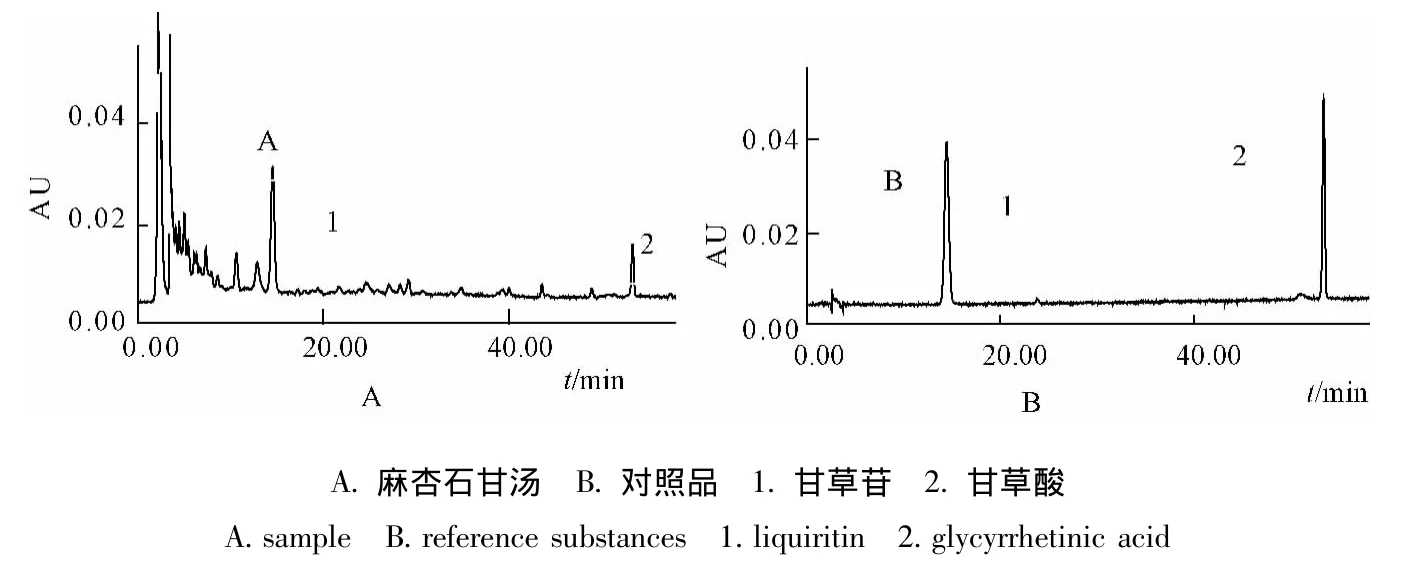
圖3 麻杏石甘湯中甘草苷、甘草酸測定色譜圖Fig.3 Chromatograms of liquiritin and glycyrrhetinic acid
2.5 麻杏石甘湯中金屬元素測定
2.5.1 供試品的制備 精密量取麻杏石甘湯水煎液5 mL,加入硝酸-高氯酸 (4∶1)混合酸10 mL,電熱套加熱蒸發至無白煙,液體應澄清,冷卻后用2%硝酸定容至25 mL。平行制備空白溶液,待測(所使用的玻璃儀器均在10%硝酸浸泡過夜,并用超純水清洗)。
2.5.2 樣品測定 采用ICP-AES,Ca分析波長為317.933 nm;Mg為279.077 nm;Zn為213.857 nm;Mn為257.610 nm;V為290.880 nm。對標準溶液進行測試,化學工作站自動繪制校正曲線,確認后進行樣品測定。將測定值代入標準曲線中進行計算,求得待測液濃度。
2.5.3 方法學考察 對各元素進行了方法學指標考察,將Ca、Mg元素的標準貯備液配制成一系列混合標準溶液,質量濃度分別為0、0.1、1、10、20、50、100 mg/L;Zn、Mn、V元素的標準貯備液配制成一系列混合標準溶液,質量濃度分別0、0.1、1、5、10 mg/L。在選定的儀器操作下對標準工作液進行測定,工作站自動繪制工作曲線,得到各元素回歸方程Ca y=12936x+3139.4,r=0.9999;Mg y=1784.7x+1417.4,r=0.9995;Zn y=3439.2x+566.29,r=0.9993;Mn y=160223x+15561,r=0.9994;V y=17409x+1762.7,r=0.9994;精密度試驗RSD分別為0.78%、1.82%、0.94%、0.95%、0.95%;重復性試驗RSD分別為1.72%、1.07%、2.73%、3.93%、2.06%;平均回收率分別為94.50%、95.63%、95.83%、94.44%、98.18%,RSD分別為 1.98%、1.02%、3.88%、4.56%、2.94%。
2.6 統計分析 應用SPSS 13.0統計軟件對實驗數據進行統計學處理。采用單因素方差分析(One-way ANOVA)對各組數據與合煎進行組組間分析比較,數據以均數 ±標準差 ()表示。
2.7 樣品測定結果 見表1~2。
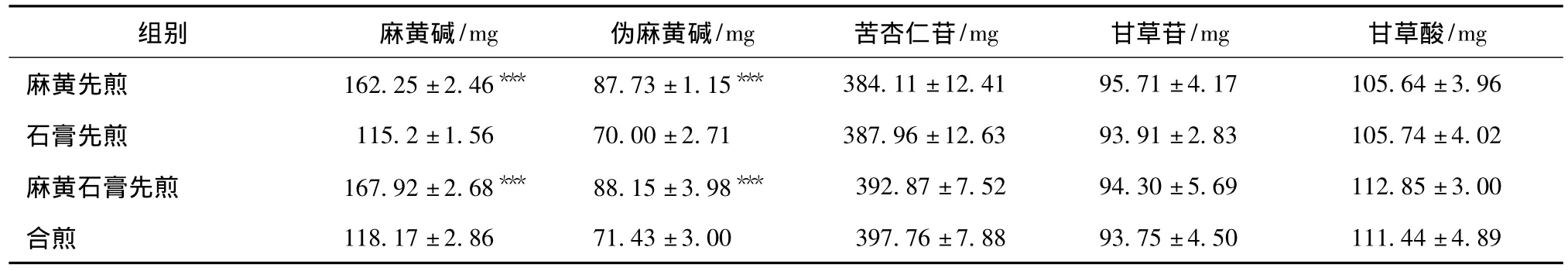
表1 不同煎煮方式中各藥效成分的量 (n=3)Tab.1 Active components amount of different herbs decocted first(n=3)
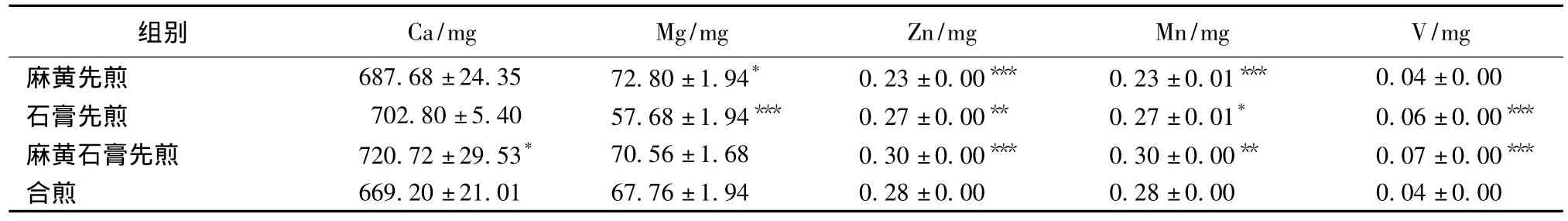
表2 不同煎煮方式中5種元素的量 (n=3)Tab.2 Five trace elements’content of different herbs decoted first(n=3)
3 討論
3.1 麻黃的藥效成分之一偽麻黃堿難溶于水[11],先煎有利于偽麻黃堿的溶出[6]。通過對4種煎煮方法的比較得到:麻黃先煎與麻黃石膏先煎,都有利于麻黃堿、偽麻黃堿成分的溶出。前3種煎煮方法與合煎相比,對甘草苷、甘草酸、苦杏仁苷的溶出量影響不大。
3.2 ICP-AES[12]具有多元素同時測定、速度快及線性范圍寬等優點,是中藥金屬元素通常使用的檢測方法。從表2可見,麻黃石膏先煎中金屬元素量最高,表示麻黃石膏先煎最有利于金屬元素的溶出,可能由于麻黃石膏先煎有利于麻黃堿與Zn2+、Mn2+等金屬離子形成了金屬絡合物,從而增加了5種元素的溶出量[13]。
3.3 本實驗結果表明麻黃石膏先煎有利于麻黃堿、偽麻黃堿的及金屬元素的溶出。由于各元素來源廣泛,含有量較低,造成研究較為困難,特別是體內研究本體干擾大。整體而言,目前對各元素在中藥中發揮的作用研究偏少,造成各元素發揮的具體作用機制尚不明確。本實驗從化學成分量的角度分析了麻黃石膏先煎的合理性,為研究麻杏石甘湯中無機元素與療效之間的內在聯系提供參考,為麻杏石甘湯臨床使用提供參考依據。
[1]徐偉輝,龔高柏.《傷寒雜病論》中麻黃與石膏配伍規律探討[J].國醫論壇,2001,16(2):2-3.
[2]國家藥典委員會.中華人民共和國藥典:2010年版一部[S].北京:中國醫藥科技出版社,2010:87-88.
[3]劉春海,羅杰英.麻黃湯麻黃先煎的試驗研究[J].中醫藥學報,2002,30(6):16-17.
[4]劉 旭.小議張仲景麻黃葛根先煎之理[J].國醫論壇,2007,22(4):44-45.
[5]張 寧,閆美琳,金東明.《傷寒論》方中藥物先煎的機理探討[J].吉林中醫藥,2008,28(1):52.
[6]陸維承.麻黃用法再榷[J].中藥材,1999,22(2):106-108.
[7]吳施國,葉冰生.生石膏是否需要先煎[J].光明中醫,2010,25(7):1290.
[8]陳 娜,梁 仁.麻杏石甘湯的現代藥理研究及臨床應用[J].廣東藥學院學報,2004,20(5):545-546.
[9]劉元芬,李 祥,高錦飚,等.石膏炮制前后微量元素分析[J].現代中藥研究與實踐,2007,21(3):35-37.
[10]萬益群,柳英霞,郭 嵐,等.電感耦合等離子體原子發射光譜法測定當歸補血湯中多種微量元素[J].光譜學與光譜分析,2007,27(1):160-163.
[11]肖崇厚.中藥化學[M].上海:上海科學技術出版社,1988:97.
[12]萬益群,肖麗鳳,柳英霞,等.ICP-AES法測定柚子不同部位中多種微量元素[J].光譜學與光譜分析,2008,28(9):2177-2180.
[13]李易非.β2-腎上腺素受體色譜篩選麻杏石甘湯的活性成分[D].西安:西北大學,2012.

