從煉鎳廢渣中綜合回收有價金屬
肖景波,夏嬌彬,陳居玲
(南陽東方應用化工研究所,河南 南陽 473000)
煉鎳工業有大量廢渣產生。據估算,每生產1t金屬鎳,廢渣產出量在55t左右。由于沒有合適的處理方法,形成了嚴重的環境負擔[1]。煉鎳廢渣含有硅、鎂、鐵、鈣、鎳等有價元素,可能的利用途徑大致有以下幾點:用于煉鐵及制備微晶玻璃;替代鐵粉用作水泥的生產原料;用于回收硅鈣合金。但由于鎳渣組成變化較大,其工業上的應用受到一定限制。為了找到一條切實可行、易于實現工業化的途徑,研究了以濕法冶金工藝綜合回收鎳渣中的有價元素 。
1 試驗部分
1.1 試驗原料
煉鎳廢渣由江西航冠集團提供,其主要成分為:MgO 31.51%,SiO252.28%,∑Fe 10%,CaO 0.67%,Ni 0.21%。
硫酸,雙氧水,氨水,氫氧化鈉,草酸,均為分析純;鐵粉,工業品;助劑FN、SN、LN,復合助劑JC,均為試驗室配制。
1.2 試驗儀器與設備
BS423S型電子天平,025-2F型電動攪拌機,HH-4型數顯恒溫水浴鍋,SHB-ⅢA型循環水式多用真空泵,HG101型電熱恒溫鼓風干燥箱,XKMF-2000A型馬弗爐。
1.3 分析方法
煉鎳廢渣成分分析采用HG/T 357—2006;試驗過程中,鐵、鎂、鎳、硅、鈣等元素成分分析采用 HG/T 3575—2006;水玻璃分析采用 GB/T 4209—2008 ;白炭黑分析采用 HG/T 3061—2009;高純氧化鐵分析采用 HG/T2574—2009;鎳精礦分析采用YS/T 340—2005。
1.4 試驗方法與流程
稱取一定量鎳渣粉末置于燒杯中,加水攪拌均勻;加入助劑FN和硫酸,在加熱和攪拌條件下進行酸解反應;反應結束后抽濾,得酸浸液和酸浸殘渣。將酸浸殘渣用水洗滌,再與水混合并加入計量的氫氧化鈉,反應后過濾得水玻璃[2]。采用濃酸法在特殊工藝條件下處理水玻璃,制得高分散性白炭黑產品[3]。向酸浸液中加入氧化劑,使其中的二價鐵轉化為三價鐵,然后在有底液存在條件下,將氧化后的酸浸液與pH控制劑一起加入到底液中,經反應生成鐵沉淀物。鐵沉淀物分離、精制、脫水后與硫酸作用生成硫酸鐵溶液。硫酸鐵溶液精制[4]后,加入氧化劑,采用氧化沉淀法制得高純鐵沉淀物,高純鐵沉淀物經分離、漂洗、脫水、煅燒制得高純氧化鐵產品[5]。
向沉鐵后溶液中加入硫化物,使其中的鎳轉化為硫化鎳沉淀,再經過濾、洗滌、干燥制得鎳精礦。向提鎳后溶液中加入助劑LN,進一步去除溶液中的各種金屬及非金屬雜質。過濾后的溶液中加入氨水,采用共沉淀法強化精制過程,過濾后得精制硫酸鎂溶液[6]。硫酸鎂溶液與氨水反應,經陳化、分離、漂洗、脫水、干燥制得氫氧化鎂產品[7-8]。
從煉鎳廢渣中綜合回收有價金屬的工藝流程如圖1所示。
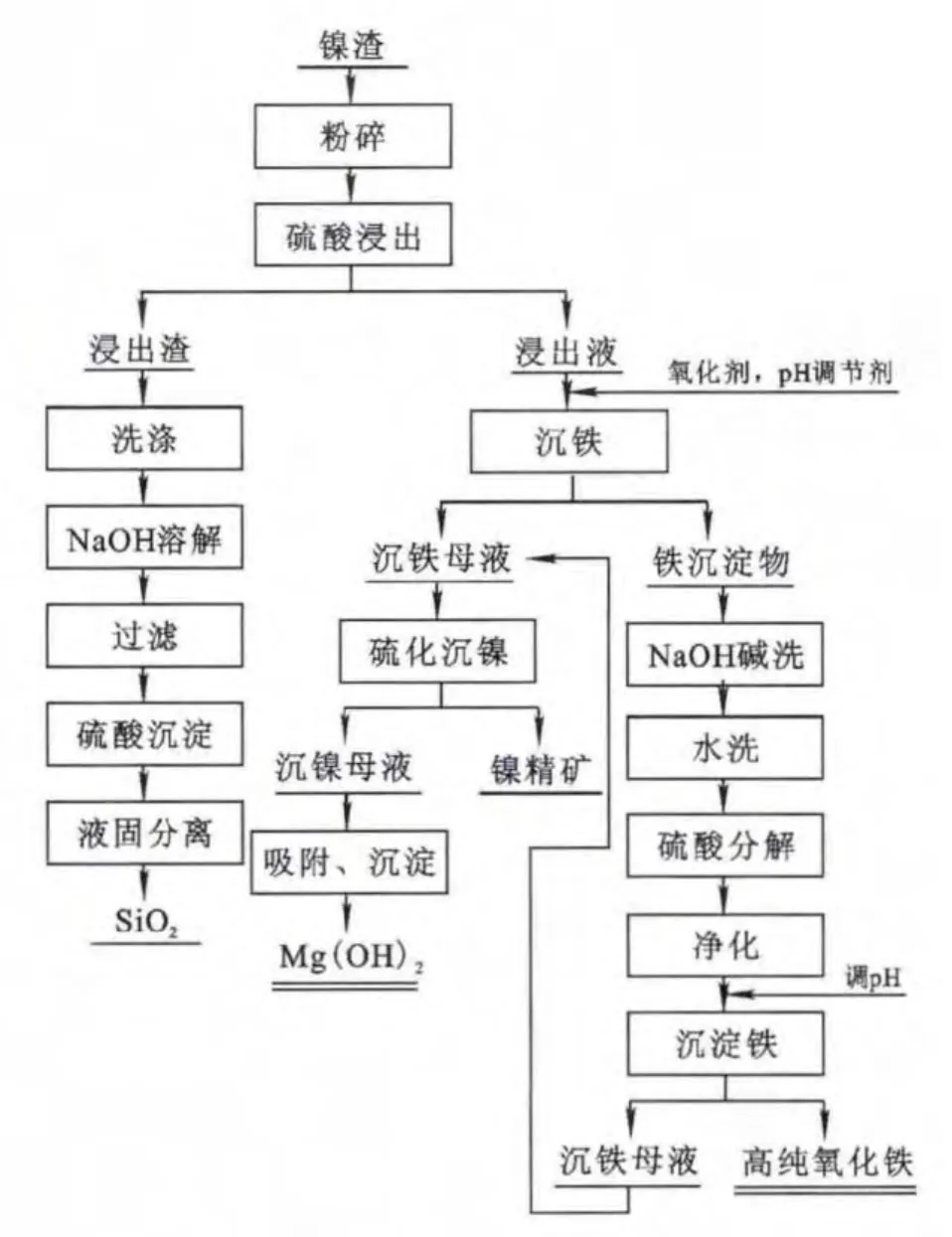
圖1 鎳渣綜合利用工藝流程簡圖
2 試驗結果與討論
2.1 鎳渣的酸解
2.1.1 鎳渣細度對分解率的影響
鎳渣粉碎至一定細度會增大表面積,提高化學反應活性,有利于分解。鎳渣細度對酸解過程分解率的影響試驗結果如圖2所示。
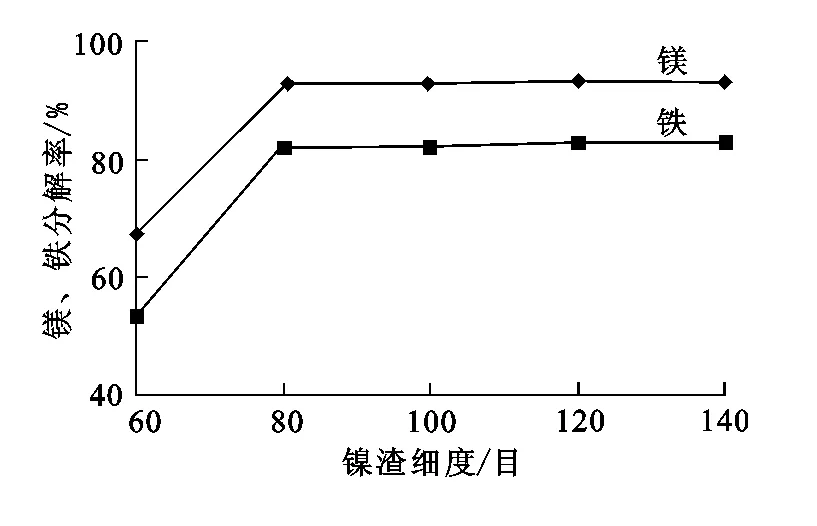
圖2 鎳渣細度對鎂、鐵分解率的影響
由圖2看出:鎳渣分解率隨鎳渣細度增大而升高;細度為80目時鎂分解率為92.8%,鐵分解率為82.6%;80目以后鎂、鐵分解率均變化不大。因此,確定鎳渣細度以不小于80目為宜。
2.1.2 酸解溫度對分解率的影響
控制鎳渣細度為80目,反應溫度對鎂、鐵分解率的影響試驗結果如圖3所示。可以看出:鎳渣分解率隨溫度升高而升高,當溫度達到90℃后,再升高溫度分解率升高不明顯。因此,確定酸解反應溫度為90~95℃,此溫度下,鎂、鐵分解率分別在93.5%和83%以上。
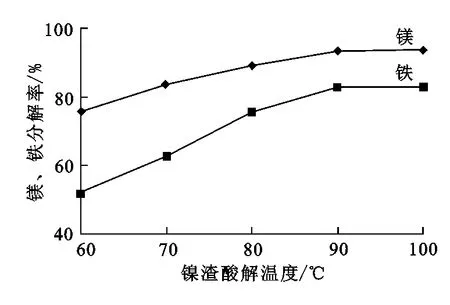
圖3 鎳渣酸解溫度對鎂、鐵分解率的影響
2.1.3 pH對分解率的影響
增大酸的用量有利于提高分解率,但酸性過強不僅會造成酸耗增大,而會對設備造成腐蝕。在固定鎳渣細度為80目、酸解反應溫度為90~95℃條件下,反應終點pH對鎳渣中鎂、鐵分解率的影響試驗結果如圖4所示。
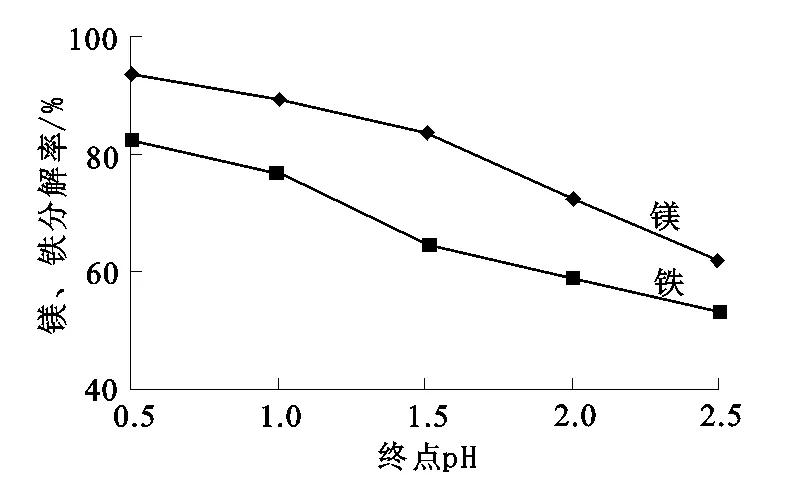
圖4 酸解終點pH對鎂、鐵分解率的影響
由圖4看出,鎳渣分解率隨反應終點pH升高而降低,反應終點的pH為0.5時,鎂、鐵分解率分別為93.2%和82.1%,加大酸量,鎂、鐵分解率降低。因此,確定酸解反應終點pH以0.5為宜。
2.1.4 反應時間對分解率的影響
在鎳渣細度為80目,酸解反應溫度為90~95℃、酸解終點pH為0.5條件下,反應時間對鎳渣中鎂、鐵元素分解率的影響試驗結果如圖5所示。

圖5 酸解反應時間對鎂、鐵分解率的影響
由圖5看出:鎳渣分解率隨反應時間延長而升高;反應210min后,鎂、鐵分解率分別達93.5%和82.5%;再繼續反應,分解率變化不大。因此,反應時間以加完計量硫酸并達到溫度條件后保溫210min為宜。
2.1.5 酸解助劑的選擇及加入量對分解率的影響
用自行復配的FN、SN和LN 3種助劑,在前述優化工藝條件下,以鎳渣粉質量2%的比例添加,考察3種助劑對鎳渣中鎂、鐵分解率的影響,試驗結果如圖5所示。
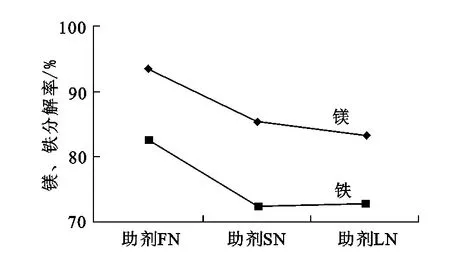
圖6 酸解助劑對鎂、鐵分解率的影響
由圖6看出:反應助劑不同對鎳渣分解率的影響也不同,3種助劑中,以助劑FN的效果最好。
助劑FN用量對鎳渣分解率的影響試驗結果如圖7所示。
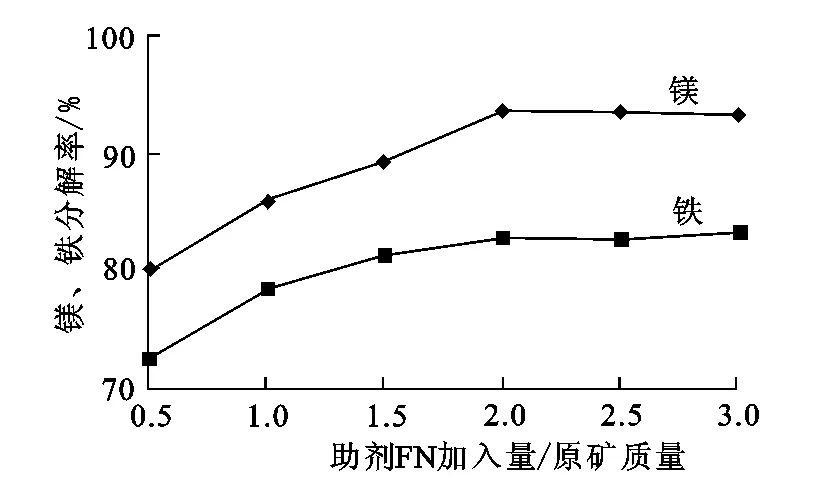
圖7 酸解助劑FN加入量對鎂、鐵分解率的影響
由圖7看出:鎳渣分解率隨助劑FN用量加大而升高,當加入量為鎳渣質量的2%時,鎳渣分解率達到最大。因此,確定助劑FN的加入量為鎳渣質量的2%。
2.2 有價元素的提取及化工產品的制備
2.2.1 高分散性白炭黑的制備
酸解渣的主要成分為二氧化硅,其干基二氧化硅質量分數高達97%,而且呈多孔結構,具有較大的比表面積和較高的化學活性。漂洗后的酸解渣與水混合,加入一定量氫氧化鈉,在加熱條件下反應一定時間后過濾,制得水玻璃。
試驗條件:配料固液質量體積比1∶4,氫氧化鈉用量依目標產品水玻璃的摩數隨機調整,堿解反應溫度70℃,堿解反應時間為添加完一定量氫氧化鈉并溫度達標后30min。結果表明,以酸解渣與氫氧化鈉反應,SiO2分解率為95.2%,可制得摩數為3~3.2,波美度為18~20Be’的水玻璃產品。
以水玻璃、水和硫酸配制反應底液,然后在控制體系pH穩定前提下向裝有反應底液的沉淀反應器中投加水玻璃和硫酸,加完計量的水玻璃后繼續加注硫酸改變體系pH。當體系pH達到設定值時停止加酸,此時反應體系內生成了白炭黑沉淀,經陳化、分離、漂洗、脫水、干燥制得具有良好性能的白炭黑產品。優化的工藝條件為:水玻璃與加入的水體積比為3∶7;一步反應,反應底液酸化終點pH為9;二步反應控制pH為7;三步反應,即最后階段反應終點pH為5;反應溫度80℃;表面活性劑加入量為二氧化硅總質量的2%;加濃硫酸;沉淀反應結束后陳化60min。在此條件下,SiO2收率為90%;所制得的白炭黑主含量達96%,吸油值為3~3.5mL/g,比表面積為250~340m2/g。
2.2.2 高純氧化鐵的制備
2.2.2.1 從鎳渣酸浸液中沉淀鐵
試驗采用氧化沉淀法沉淀分離鐵。
首先向酸浸液中加入氧化劑,使其中的二價鐵轉化為三價鐵;向反應器中加入適量清水作為底液(后續試驗以沉鐵后酸解液為底液),在加熱和攪拌條件下向底液中加入經氧化的酸解液和pH調節劑。反應之后過濾,得除鐵后溶液和鐵沉淀物。除鐵后溶液用于制備鎳精礦和氫氧化鎂,鐵沉淀物經凈化處理、酸解、分離、凈化、氧化、沉淀、分離、漂洗、煅燒后,制得高純氧化鐵產品。
反應底液用量為氧化后酸解液體積的20%~30%,酸解液與pH控制劑的加入方式為并流滴加,反應溫度75℃,反應終點pH為3.5,反應時間以加完計量酸解液后保溫反應30min,酸解液與pH控制劑的加入速度為將計量酸解液與pH調節劑在30min內加完。在此條件下,酸解液中鐵沉淀率達到99.6%,沉鐵過程中鎂的夾帶損失率為0.18%,鎳的夾帶損失率為3.76%。
2.2.2.2 高純氧化鐵的制備
鐵沉淀物中含有一定量的鋁、鎂、鎳等雜質。制備高純氧化鐵時,先對鐵沉淀物進行漂洗,然后與水混合,打制成漿,再加入反應助劑,使其中的鋁轉化為可溶性鋁鹽,再經分離、洗滌制得精制鐵沉淀物。精制鐵沉淀物用酸溶解制得硫酸鐵溶液,去除鎂、鎳等雜質后得到純凈的硫酸鐵溶液。加入氧化劑使溶液中少量的二價鐵轉化為三價鐵。最后以純水為底液,以并流方式加入純凈硫酸鐵溶液和pH調節劑,使溶液中的鐵轉化為高純鐵沉淀物,再經分離、漂洗、脫水、干燥、煅燒制得高純氧化鐵。
試驗確定的最佳條件:含鐵沉淀物漂洗終點pH為6.5,堿洗時氫氧化鈉加入量為理論量,堿洗溫度為75℃,鐵沉淀物酸解時固液質量體積比為1∶14,反應時間30min,反應終點pH為1.5。
溶液凈化條件:鈣、鎂的去除,反應溫度80℃,反應時間30min,助劑加入量為理論量的3倍;重金屬的去除,反應溫度75℃,反應時間30 min,助劑加入量為理論量的10倍。
高純鐵沉淀物的制備條件:反應底液為純水,電導率小于5s/m,底液用量為硫酸鐵溶液的20%;pH控制劑為1+9氨水;沉鐵過程反應溫度75℃;沉鐵反應終點pH為3.5。優化條件下,所得產物為α-Fe2O3,純度在99.65%~99.82%之間。
2.2.3 鎳精礦的制備
將沉鐵后液送入沉鎳反應器,在一定溫度條件下加入硫化物溶液,將其中的鎳轉化成硫化鎳沉淀,經過濾、洗滌、干燥得主要成分為硫化鎳的鎳精礦。試驗確定的工藝條件:加入硫化物時溶液pH為3.5~5.5,硫化物加入量為理論量的6倍,硫化物加入時料液溫度為50℃,反應溫度為75℃,反應時間30min。在此條件下,鎳沉淀率為98%,鎳沉淀物中Ni質量分數為28.97%,Fe質量分數為0.28%。
2.2.4 氫氧化鎂的制備
沉鎳母液中還殘留有一定量的金屬或重金屬雜質,加入氧化劑,在加熱和攪拌條件下加入堿性吸附劑,將殘余的金屬雜質進一步沉淀,溶液得到進一步凈化。之后加入氨水進一步沉淀凈化,過濾之后得純凈的硫酸鎂溶液。最佳工藝條件:堿性吸附凈化劑用量:以溶液pH穩定在7為準,吸附劑加入后反應溫度為85℃,吸附反應時間30 min;加料溫度40℃;反應溫度50℃;共沉淀劑加入量以被處理液出現渾濁為準;共沉淀反應時間30min。此工藝條件下,所得氫氧化鎂純度達到99.6%,產品粒徑在2.5μm以下。
3 結論
采用濕法冶金工藝處理鎳渣,可以回收高分散性白炭黑、高純氫氧化鎂、高純氧化鐵,具有顯著的經濟效益和社會效益。
試驗確定了鎳渣處理優化工藝條件及工藝流程。在優化條件下,鎳渣中鎂、鐵分解率分別達到93.5%和83.1%;酸解殘渣中二氧化硅堿溶分解率為95.2%,所制備的白炭黑主含量達到96%,吸油值為3~3.5mL/g,比表面積為250~340 m2/g,具備高分散性產物特點;所制備的高純氧化鐵為α-Fe2O3,純度達到99.82%;所得鎳沉淀物中Ni質量分數達到28.97%;所制備的氫氧化鎂粒徑在2.5μm以下,純度達99.6%。
[1]王成彥,尹飛,陳永強等.國內外紅土鎳礦處理技術及進展[J].中國有色金屬學報,2008,18(6):1-8.
[2]陳虹,于少明,單承湘.由蛇紋石酸浸渣制取白炭黑工藝研究[J].化工礦物與加工,2010(4):20-24;
[3]趙杰,錢海燕.高分散性白炭黑的生產工藝和性能[J].化工新型材料,2010,38(2):98-100.
[4]王漢棟,王學欽,張永宏,等.鈦白粉副產物硫酸亞鐵的精致工藝:中國,CN1104999A[P].1995-07-12.
[5]吳展,陳志友,侯瓊美,等.從粗硫酸鎳溶液中凈化分離鐵砷試驗研究[J].濕法冶金,2013,32(2):122-124.
[6]聞振乾,劉忠臣,劉會武,等.沉淀法分離鎳、鋅研究進展[J].濕法冶金,2013,32(5):281-283.
[7]陳向鋒,黃西平,魏炳舉,等.一種生產環保型氫氧化鎂的新工藝:海水、鹵水-輕燒白云石沉淀法[J].鹽業與化工,2008(1):43-45.
[8]胡慶福.鎂化合物生產與應用[M].北京:化學工業出版社,2004:318-319.

