抗CD20單抗治療難治性重癥系統性紅斑狼瘡臨床觀察*
南方醫科大學珠江醫院血液科(廣州510282) 易 亮 孫 璨 林 遐 羅漳福 陳土珍 吳秉毅
系統性紅斑狼瘡(Systemic lupus erythematosus,SLE)是一種臨床表現為多系統損害的慢性自身免疫病。糖皮質激素和細胞毒類藥物為主的非特異性免疫抑制治療是目前主要的常規治療;但有部分患者采用糖皮質激素和細胞毒類藥物治療無效,成為難治性或病情進一步演化成重癥SLE。如何治療這部分患者目前仍是難題,尚處探索和研究階段。近年來研究表明:B淋巴細胞過度活化產生致病性高效價自身抗體(如抗核抗體等),是SLE發病機制的關鍵環節[1]。近年國外報道:用特異性抗體清除B淋巴細胞可以減少自身抗體的產生,部分SLE患者用去B細胞治療獲得了一定效果,國內也有文獻報道[2,3]。我們用抗CD20單克治療難治性重癥SLE6例,取得了較好效果,現分析報告如下。
資料與方法
1 臨床資料 難治性重癥SLE 6例為近3年來在珠江醫院或南海醫院腎臟風濕免疫科住院的患者,其中女5例,男1例,年齡14~56歲,平均31.8歲。病程:2~80月,平均32個月。隨診:8~20月,平均3個 月。臨床表現為:關節疼痛5例,發熱3例,面部紅斑2例,眼瞼及全身浮腫2例,皮疹或皮膚紫瘀2例,器質性腦病2例,出現精神癥狀2例。神經精神狼瘡2例,狼瘡性腎炎(LN)2例,合并血小板減少性紫癜1例。診斷均符合1997年美國風濕病學會SLE分類標準,并且均為難治性或重癥SLE。
2 治療方法 在使用激素的基礎上應用抗CD20單抗,具體用法:抗CD20單抗 (RTX)500mg,溶于生理鹽水500ml中,靜脈滴注。用藥之前半小時口服苯海拉明25mg、肌肉注射非那根25mg并靜脈推注地塞米松5mg,滴注RTX過程中需進行心電監護。兩周1次,共使用2~4次。與此同時據病情逐漸減少糖皮質激素用量。
3 療效判定 分別在RTX使用前和使用后的1、3、6個月對患者臨床癥狀和體征的變化、實驗室指標及狼瘡活動度進行跟蹤隨訪;實驗室指標包括有血常規、肝腎功能、血脂、補體、血沉、C反應蛋白、尿常規及24小時尿蛋白定量檢測等,并用多參數流式細胞術檢測外周血淋巴細胞中CD19+或CD20+B淋巴細胞的計數。臨床完全緩解(CR)定義為:BILAG所有系統均≤C級,臨床部分緩解(PR)定義為:BILAG治療前后比較至少有1個系統等級下降1級,其他系統無病情進展且分級≤B級。臨床無緩解(NR)定義:不滿足上述完全緩解或部分緩解標準,死亡或退出病例歸為臨床無緩解。
4 統計學處理 患者接受RTX治療前后的疾病活動度和實驗室指標作自身對照,采用SPSS17.0統計軟件進行配對t檢驗,以P<0.05為有顯著性差異,P<0.01為有極顯著性差異。
結 果
1 患者臨床資料、RTX治療方法及緩解情況 5例伴有關節疼痛的患者治療后約2周疼痛癥狀均明顯緩解;2例伴精神癥狀的患者RTX治療后10d左右,癥狀逐漸改善;1例存在雷諾現象患者癥狀基本緩解,表現為出現次數減少及程度減輕;2例面部紅斑患者治療后1個月紅斑逐漸消褪;2例LN患者的浮腫減輕;1例伴有紫癜的患者紫癜消失,且不伴有其他部位出血征象。6例患者在給藥后第1個月病情明顯改善,部分患者3~6個月階段病情可進一步改善,隨訪超過1年的3例患者病情均持續緩解。
2 RTX治療前后血清學變化 見附表。1例SLE合并血小板減少性紫癜患者治療前血小板計數為2×109/L,RTX治療1個月后血小板計數上升至135×109/L,其余5例患者外周血象在治療前后變化不大。6例患者在RTX治療前后其轉氨酶、腎功能等指標均無明顯異常。所有患者治療前ANA抗體均為陽性,治療6個月后有3例患者ANA抗體轉為陰性。6例患者的補體C3、C4、SLEDAI評分、BILAG評分明顯改善,激素用量減少(P<0.05)。
3 外周血B淋巴細胞變化 6例患者中有3例進行了外周血淋巴細胞的檢測。用流式細胞術測定治療前CD19+B細胞計數分別為0.24×109個/L,0.685×109個/L,0.562×109個/L,RTX治療后2周分別降為0.013 ×109個/L,0.025 ×109個/L,0.018×109個/L,均較應用前明顯下降。我們觀察到B淋巴細胞數量下降與癥狀改善有一定關系。另外3例患者因經濟原因未同意接受B淋巴細胞的檢測。
4 尿蛋白及血清白蛋白改變 見附圖。2例LN患者24h尿蛋白定量均有明顯下降(P<0.05)、血清白蛋白均上升明顯(P<0.05),治療前后變化明顯,而且,這兩例患者完全脫離激素和免疫抑制劑。
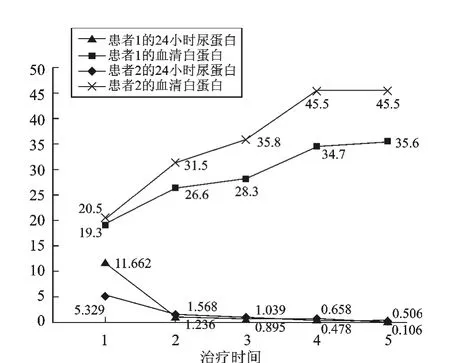
附圖 2例LN患者的尿蛋白及血清白蛋白變化 橫軸:1:治療前;2:治療1個月后;3:治療3個月后;4:治療6個月后;5:治療近2年后
5 安全性及并發癥 6例患者在治療過程中耐受性良好,其中有1例在隨訪過程中發生帶狀皰疹(治愈),其余5例均未出現發熱、寒戰、乏力、頭痛、皮疹、喉頭水腫、低血壓、感覺異常、惡心、嘔吐等常見不良反應,亦未出現心力衰竭、骨髓抑制、肝功能衰竭等嚴重不良反應。
6 隨訪 6例患者應用RTX治療后隨訪中位時間為13個月(7~20個月),目前癥狀控制良好。隨訪到6個月時,激素(以潑尼松量計算)平均用量也得以大幅減少(由治療前的266mg/d減少至4.2mg/d)。
附表 RTX治療前后免疫學指標及疾病活動度變化(±s)

附表 RTX治療前后免疫學指標及疾病活動度變化(±s)
注:*與治療前相比,P<0.05
43±11.61 C3 0.49±0.14 0.87±0.24* 0.89±0.10* 0.90±0.08*C4 0.12±0.08 0.26±0.07* 0.31±0.07* 0.34±0.08*BILAG 17.8±2.48 7.83±2.48* 5.5±2.07* 3.50±2.59*SLEDAI 17.8±6.31 10±3.35* 6.3±1.37* 4.17±1.60個月后ESR 61.83±14.19 58.17±18.84 37.17±14.91*治療前 1個 月后 3個月后 6*
討 論
近年來研究表明:B細胞在SLE發病中能起重要作用,SLE患者的B細胞顯著增多,功能異常活躍,生存期明顯延長,持續地產生大量自身抗體,促進SLE的發生、發展。因此B細胞是SLE合適的治療靶點。通過清除B細胞治療可能達到從源頭上治療SLE的目的。
CD20是B細胞向成熟淋巴細胞分化過程中表達的表面抗原。RTX是一種嵌合型抗CD20單克隆抗體,它與體內CD20+細胞有很高的親和力,能選擇性靶向性殺傷B淋巴細胞。
近年來,對傳統治療方法如糖皮質激素、免疫抑制劑、大劑量丙種球蛋白等無效或反復復發的難治性自身免疫性疾病患者,國內外已有用RTX成功治療這類病例的報道[4~7]。目前,國內外也有用RTX治療難治性SLE的報道,結果提示:CD20單抗對部分難治性重癥SLE有效[8],可以降低SLE活動度,改善SLE患者臨床癥狀。
本研究中入組的6例SLE患者,SLEDAI都大于15分,表現為多器官和多系統受累,分別有神經系統、腎臟以及血液系統被累及。入組前均經大劑量激素治療,同時使用環磷酰胺或環孢素A、硫唑嘌呤等免疫抑制劑治療。2例表現為嚴重的腎病綜合征,2例伴有明顯的神經精神癥狀,1例伴嚴重血小板減少,病情危重。該6例患者經抗CD20單抗治療后第1個月病情明顯改善,部分患者3~6個月階段病情進一步改善,隨訪超過1年的3例患者均病情持續緩解。
6例患者中3例進行了外周血B淋巴細胞的檢測。結果發現:經RTX治療后這3例患者雖然未達到B細胞清除的標準,但其B細胞的數量均較應用前明顯下降。我們觀察到這3例患者臨床癥狀緩解情況與B細胞下降程度有一定關系,該3例患者治療1月后測定抗核抗體,表現為滴度開始降低,至6個月復查抗核抗體已經轉陰,說明RTX治療后去除了部分B細胞,使自身抗體的分泌減少,有利于病情緩解。
隨訪6個月,根據BILAG評估,在本研究的病例中,總有效率為100%,顯示了較好的總體療效。與國外的研究結果比較,國外報道[9~11]的緩解率為70%~100%,而本研究的緩解率為100%,其緩解率較高,分析其原因可能是我們的病例數較少,另外,可能是這些患者前期或同時使用了激素和其他免疫抑制劑的原因。6例病例在應用RTX治療過程中,無嚴重不良事件發生,且明顯減少了激素的療程和用量。因此,大大的減少了發生感染的機會以及激素導致的其他不良反應的發生。但在臨床上要嚴格掌握RTX的適應證,做好應急預案,積極采取措施預防過敏等不良反應的發生,還可以進一步探討擴展治療疾病的范圍。
本研究結果提示:RTX治療難治性SLE,可以緩解患者臨床癥狀、降低自身抗體滴度、減少蛋白尿、升高補體等。其機制可能是通過清除異常克隆B淋巴細胞而起作用的。
RTX對難治性SLE也具有良好的耐受性和安全性。這就為難治性SLE提供了一個低毒而高效的全新的治療途徑。但如何聯合用藥,怎樣降低醫療成本,對不同臨床表現的SLE患者選用哪些藥物聯合,藥物劑量是多少,每次藥物間隔時間多長才能達到最好療效,聯合用藥對患者的近期療效、遠期預后的影響及不同聯合用藥方案的不良反應,都需要臨床不斷探索和總結;由于本研究的病例數較少,目前得出的結論,還需要大樣本和長時間的研究來進一步驗證。
[1] 戴莉萍,葉志中,尹志華,等.B淋巴細胞刺激因子相關生物制劑治療系統紅斑狼瘡的研究進展[J].國外醫學內科學分冊,2006,(12):512-515.
[2] 樊貞瑜,蔡宇波,顧越英,等.利妥昔單抗治療難治性重癥系統性紅斑狼瘡的臨床初步觀察[J].中國藥物與臨床,2009,9(8):675-678.
[3] 王金鎧,宋曉寧,張金巧,等.利妥昔單抗治療難治性自身免疫性疾病[J].臨床薈萃,2010,25(3):241-243.
[4] Gorman C,Leandro M,Isenberg D.B cell depletion in autoimmune disease[J].Arthritis Res Ther,2003,15(Suppl 4):17-21.
[5] Vallerskog T,Heimburge M ,Gunnarsson I,etal.Differential effects on BAFF and APRIL levels in rituximabtreated patients with systemic lupus erythematosus and rheumatoid arthritis[J].Arthritis Res Ther,2006,8(6):167.
[6] Edwards JC,Cambridge G.B-cell targeting in rheumatoid arthritis and other autoimmune diseases.[J].Nat Rev Immunol,2006,6(5):394-403.
[7] Reynolds JA,Toescu V,Yee CS.Effects of rituximab on resistant SLE disease including lung involvement[J].Lupus,2009,18(1 ):67-73.
[8] 中華醫學會風濕病學分會.系統性紅斑狼瘡的診斷和治療指南[J].中華風濕病學雜志,2010,14(5):342-346.
[9] Looney RJ,Anolik JH,Campbell D,etal.B cell depletion as a novel treatment for systemic lupus erythematosus:aphase I/II dose-escalation trial of rituximab[J].Arthritis Rheum,2004,50(8):2580-2589.
[10] Sfikakis PP,Boletis JN,Lionaki S,etal.Remission of proliferative lupus nephritis following B cell depletion therapy is preceded by down-regulation of the T cell costimulatory molecule CD40ligand:an open-label trial[J].Arthritis Rheum,2005,52(2):501-513.
[11] Vigna-Perez M,Hernandez-Castro B,Paredes-Saharopulos O,etal.Clinical and immunological effects of Rituximab in patients with lupus nephritis refractory to convetional therapy:apilot study[J].Arthritis Research &Therapy,2006,8(3):83-85.

