理論空燃比天然氣汽車尾氣中H2O和O2對CH4與NO反應的影響
尚鴻燕 胡 偉 王 云 任成軍 龔茂初 陳耀強,,*(四川大學化學工程學院,成都60065; 四川省中自尾氣凈化有限公司,成都67;四川大學化學學院,教育部綠色化學與技術重點實驗室,成都60064)
理論空燃比天然氣汽車尾氣中H2O和O2對CH4與NO反應的影響
尚鴻燕1胡 偉1王 云2任成軍3龔茂初3陳耀強1,3,*
(1四川大學化學工程學院,成都610065;2四川省中自尾氣凈化有限公司,成都611731;3四川大學化學學院,教育部綠色化學與技術重點實驗室,成都610064)
共沉淀法制備CeZrYLa+LaAl復合氧化物載體,等體積浸漬法制備了Pt催化劑,用于研究理論空燃比天然氣汽車(NGVs)尾氣凈化反應中CH4與NO的反應規律.并考察了10%(體積分數,φ)H2O和計量比O2對CO2存在時的CH4+NO反應的影響.結果表明:對于不同條件下的NO+CH4反應,主要生成N2和CO2,高溫區有CO生成.低溫區無O2時可以生成N2O,有O2時可以生成NO2;添加10%(φ)的H2O后,CH4轉化活性降低,NO轉化活性基本不變,這是由于H2O減弱了CH4與CO2的重整反應,但是對CH4與NO的反應基本沒有影響;添加計量比的O2后,CH4轉化活性提高,而NO轉化活性降低,這是由于O2和NO之間存在競爭吸附,CH4被O2氧化為主要反應,從而減弱了NO的轉化;同時添加計量比的O2和10%(φ)H2O,CH4與CO2的重整反應受到抑制, CH4與NO的反應、甲烷蒸汽重整反應和甲烷被O2氧化反應同時發生,CH4和NO的轉化活性均提高.
Pt;CeZrYLa+LaAl;尾氣組分;CH4對NO的還原;天然氣汽車尾氣凈化
1 引言
天然氣的主要成分是CH4,CH4是H/C比值最高的碳氫化合物(HC),因此CH4相比其他HC燃料在燃燒過程中有更少的CO2生成量,1-3并且天然氣還具有使用范圍廣、價格低廉及污染排放少等優點,這使得天然氣汽車(NGVs)在全世界范圍內廣泛使用.NGVs通常有理論空燃比和稀燃兩種工作方式,理論空燃比燃燒方式為燃料與計量空氣混合;稀燃方式為空氣過量.對于理論空燃比NGVs,其主要污染排放物為CH4、NOx和CO.其中,CH4是一種具有強溫室效應的氣體,由于CH4是最為穩定的HC化合物之一,其轉化和活化困難,表現在CH4的自身氧化反應比一般HC化合物反應難度大;同時CH4和NO的反應也比其他HC與NO的反應困難得多,這導致NO的轉化難度大,而NO對人類及環境帶來嚴重的危害.為了滿足日益嚴格的汽車尾氣排放標準,裝備具有同時轉化CH4、CO和NO的尾氣處理催化劑必不可少.
理論空燃比NGVs催化劑主要借鑒汽油車的三效催化劑(TWC),一般采用CeO2改性的Al2O3為載體,Pt、Pd或Rh等貴金屬為活性組分.1,4,5在本課題組過去的研究中,所制備CeO2-ZrO2-Al2O3、CeO2-ZrO2-MxOy(M=Y,La)/Al2O3及CeO2-ZrO2-Y2O3-La2O3+ La2O3-Al2O3等材料在汽油車及NGVs尾氣凈化催化劑中體現了優異的性能.6-8而且研究發現,在稀燃和理論空燃比條件下,Pd對CH4完全氧化的活性高于Rh或者Pt;9在富燃還原性條件下,Pt的活性略高于Pd.10
理論空燃比NGVs尾氣凈化催化劑上進行的主要反應有CH4氧化,CO氧化和NO還原(包括CH4對NO的還原和CO對NO的還原).由于CH4和NO的反應比其他HC與NO的反應困難得多而備受關注.11-14Burch和Ramli15報道了Pt、Pd和Rh催化劑上CH4對NO的還原反應,發現NO和CH4的反應與氣體組成和溫度有關,不同催化劑的反應活性與催化劑可被CH4還原的程度相關,這是由于NO轉化生成N2主要發生在還原表面活性位上,這些活性位可能是金屬單質原子,如Pt,也可能是氧空缺,如Pd和Rh,并且在Pt和Pd催化劑上可以生成N2O.對于Pt/ Al2O3和Pt/SiO2催化劑上的NO與CH4反應,NO的還原與NO的分壓相關,而與CH4關系不大,對于NO/O2/CH4反應,NO轉化率隨O2含量增加先升高后降低,表明O2存在時的NO還原存在一個最佳的表面氧物種和碳氫化合物的覆蓋量.16Ohtsuka等17研究了水蒸氣和SO2存在條件下的CH4與NO反應,所制備的Pt-Pd催化劑具有優異的耐久性.實際上理論空燃比NGVs尾氣中除了CH4、CO和NO外,還存在化學計量比的氧氣,10%(體積分數,φ)的水蒸氣和12%(φ)的CO2氣體等,并且這些組分對尾氣轉化反應具有重要的影響作用.由于CH4和NO的反應是理論空比尾氣凈化的主要反應,尾氣中O2和H2O對該反應的影響作用關系到催化劑的性能.研究O2和H2O對CO2存在條件下的CH4+NO反應的影響,對尾氣凈化反應過程的分析和操作條件的控制將會有指導意義.
本文以共沉淀法制備結合儲氧材料和耐高溫氧化鋁材料兩者優點的70%(質量分數,w) Ce45Zr45Y5La5+30%(w)La3Al97納米復合材料為載體,在該材料上負載Pt活性組分制備了Pt催化劑,用于研究理論空燃比NGVs尾氣中O2和H2O對大量CO2存在條件下的CH4與NO反應活性的影響.
2 實驗部分
2.1 載體的制備
按配比稱取Ce(NO3)3·6H2O(化學純,四川樂山五通橋東風化工廠),ZrO(NO3)2·6H2O(化學純,江蘇宜興新興鋯業公司),Y(NO3)3·6H2O(化學純,山東淄博市吉利浮選廠),La(NO3)3·6H2O(化學純,成都科龍化學試劑廠)配成濃度為10%(w)的混合鹽溶液,使用NH3·H2O(分析純,成都露橙化工試劑廠)作沉淀劑進行滴定,得到沉淀物;同樣按配比稱取La(NO3)3·6H2O(化學純,成都科龍化學試劑廠)和Al(NO3)3·9H2O(化學純,山東淄博市吉利浮選廠)配成濃度為10%的混合鹽溶液,使用NH3·H2O(分析純,成都露橙化工試劑廠)作沉淀劑進行滴定,得到沉淀物.并將兩沉淀物通過劇烈攪拌混合.將所得沉淀混合物進行陳化、過濾、洗滌和干燥后,在800°C焙燒3 h,即制得CeO2-ZrO2-Y2O3-La2O3+La2O3-Al2O3樣品,記為CeZrYLa+LaAl.其中CeZrYLa占70% (w),LaAl含量為30%(w).在CeZrYLa中CeO2和ZrO2含量均為45%(w),Y2O3和La2O3含量均為5% (w);在LaAl中,La2O3和Al2O3含量分別為3%(w)和97%(w).
2.2 催化劑的制備
采用等體積浸漬法,在上述制備的載體上,浸漬Pt(NO3)2(分析純,成都光明光電信息股份公司)溶液.然后在120°C干燥,550°C焙燒3 h,得到Pt/ CeZrYLa+LaAl催化劑粉末,貴金屬含量為1.2% (w);所得催化劑粉末加去離子水混合球磨制漿,涂覆在堇青石蜂窩基體(體積2.5 cm3,高2.7 cm)上,涂覆量180 g·L-1,涂層中貴金屬Pt含量2.14 g·L-1.經120°C干燥后,550°C焙燒3 h,即得整體式催化劑,記為Pt.
2.3 催化活性評價
活性測試在自組裝的一套專用多路固定床連續流動微型反應器中進行,各路氣體分別用質量流量計控制流速,在進入反應器之前混合均勻.氣體的體積空速均為34000 h-1.評價所用反應氣CH4、NO、H2O、CO2的體積分數分別為0.087%、0.074%、10%、12%,O2含量可調(調節理論空燃比條件),并以N2為平衡氣.反應前后的CH4使用上海科創色譜儀器有限公司生產的GC9800型氣相色譜儀進行檢測,NO與CO用佛分環保儀器檢測設備制造有限公司FGA-4100型汽車排氣分析儀進行檢測.
3 結果與討論
3.1 CO2存在時各反應條件下CH4與NO的轉化活性
圖1給出了O2與H2O對Pt催化劑上不同反應活性的影響結果.從圖中可以看出,(i)對于CH4+NO+ CO2反應,Pt催化劑的CH4轉化T50(起燃溫度:污染物轉化50%時溫度)和T90(完全轉化溫度:污染物轉化90%時溫度)分別為445和490°C,NO轉化T50和T90分別為286和297°C;(ii)添加10%(φ)H2O后, CH4活性明顯下降,NO轉化活性基本不變.說明H2O減弱了CH4與CO2的重整反應,而對CH4和NO的反應基本沒有影響;(iii)添加計量比的O2后,CH4轉化活性明顯提高,NO轉化活性遠低于無O2(CH4+ NO+CO2和CH4+NO+H2O+CO2)條件,說明O2的出現會存在甲烷被O2氧化反應與甲烷被NO氧化反應的競爭,甲烷被O2氧化反應優先進行,減弱了甲烷與NO的反應使得NO轉化活性低于無O2條件,這與文獻18報道一致;(iv)同時添加計量比O2和10%(φ) H2O后,460°C以下CH4轉化率提高,這是由于O2和H2O同時存在時,Pt催化劑上放熱的甲烷被O2氧化反應和強吸熱的甲烷水蒸氣重整反應同時發生,反應體系本身實現了自供熱,在較低的反應溫度下達到較高的甲烷轉化率.19同時NO轉化活性得到明顯提高,這是由于Pt催化劑上甲烷蒸汽重整反應產生H2,促進催化劑三效性能,從而對NO轉化有利.5接下來我們針對圖1的實驗結果對各反應條件下的CH4與NO反應進行詳細地分析.
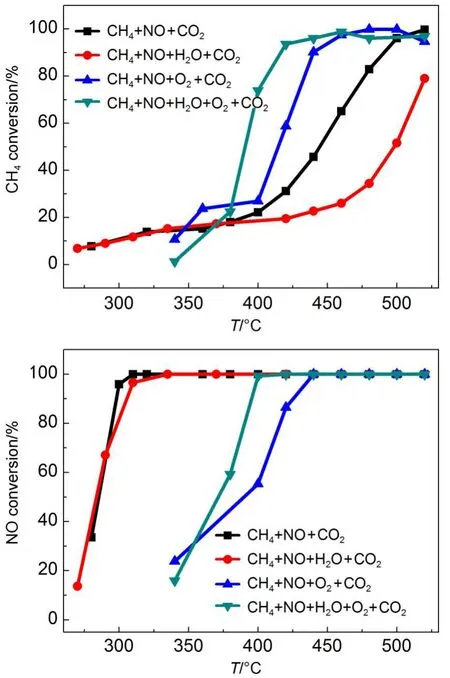
圖1 O2與H2O對Pt催化劑上不同反應活性的影響Fig.1 Effects of O2and H2O on the activities of Pt-based catalyst for different reactions
3.2 無氧無水時CH4+NO+CO2的反應
從圖1可以看出,Pt催化劑對于CH4和NO分別在490和297°C達到完全轉化,此條件下污染物轉化過程中可能發生的反應有:20,21
CH4與NO以1:3反應
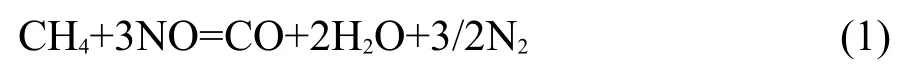
CH4與NO以1:4反應

CH4與NO以1:8反應
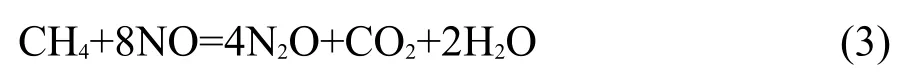
CH4與CO2重整反應

體系中多余的CO2與H2反應

由CH4和NO的化學反應式(1)-(3)的化學計量比可以發現,同一溫度下NO的轉化率與CH4轉化率之比值R應處于:3≤R≤8.反應(4)會造成R<3.
表1給出了不同溫度條件下各反應的NO/CH4轉化率比值及尾氣中CO含量,其中,COa是活性測試反應器出口處檢測到的CO含量,COb是假設高溫區所有轉化的NO和CH4均按著方程(1)進行反應能夠生成的CO含量.從表中可以看出:對于CH4+ NO+CO2反應,在體系溫度處于520-440°C時,R<3,這說明有反應(4)發生使得R<3,尾氣中CO生成量大于0.11%高達0.23%,如此高的CO生成量遠大于體系中全部的CH4(0.087%(φ))與NO(0.074%(φ))以反應(1)生成的CO含量,也大于全部的CH4以反應(4)生成的CO量,說明高溫區還存在逆水汽變換反應(5).此時NO的轉化主要依靠CH4與NO的反應(但是不能確定以(1)-(3)哪種途徑反應);在體系溫度T≤420°C時,3<R<8,尾氣中CO生成量遠小于高溫區,說明隨著溫度降低反應(4)和(5)減少.溫度越低R越接近8,說明低溫時反應(3)逐漸增多,生成了N2O.為了驗證低溫區生成了N2O,我們對該反應前后的NOx(NO、N2O和NO2)使用ANTARIS IGS在線分析儀進行檢測,結果顯示整個溫度范圍內只生成極少量的NO2,溫度較低時逐漸生成了N2O,并且隨著溫度降低N2O選擇性提高.這與文獻15報道的CH4與NO反應中N2O主要在400°C以下生成一致.
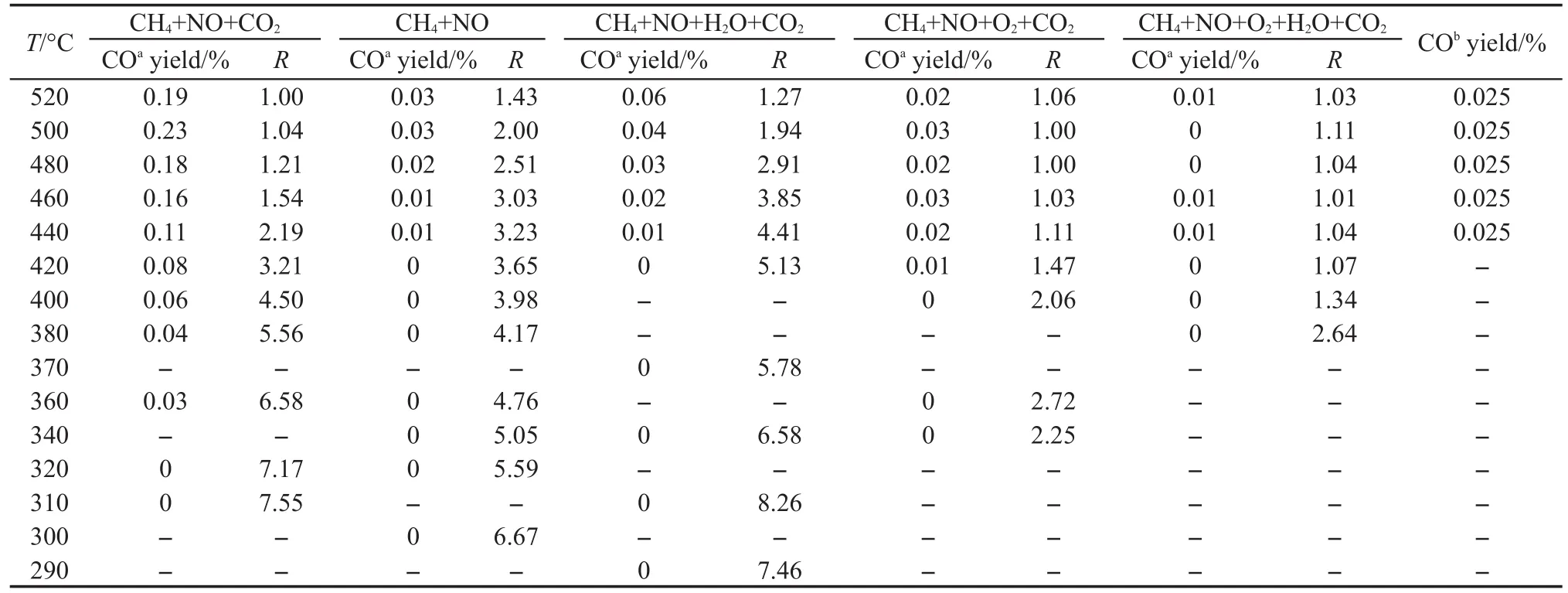
表1 不同溫度條件下各反應的NO/CH4轉化率比值及尾氣中CO含量Table 1 Ratios of NO to CH4consumed and the CO yields for all reactions at different temperatures
為了確定不同溫度段CH4與NO以何種途徑反應,我們測試了Pt催化劑上沒有CO2存在時的CH4+ NO反應,并與CO2存在時的CH4+NO反應進行對比,結果示于圖2.無CO2存在時CH4+NO反應的NO/CH4轉化率比值R和尾氣中CO含量結果列于表1.圖2中,沒有CO2存在時的CH4+NO反應,CH4轉化活性低于有CO2存在時的活性,NO活性基本不變.這是由于沒有反應(4)的發生造成的.從表1可以看出,CH4+NO反應在520-500°C之間時,R<3, COa>COb,說明CH4除了發生反應(1)以外還可能發生了少量的CH4與載體儲氧材料的反應或者CH4在催化劑上的裂解,使得R<3;480°C時,R<3,COa<COb,除了反應(1)還可能發生了CH4在催化劑上的裂解反應使得R<3;460-400°C之間,3<R<4,COa遠小于COb,說明主要發生反應(2),只存在少量的反應(1);400-300°C之間,4<R<8,體系中沒有CO生成,說明主要發生反應(2)和(3),而且隨著溫度降低,R接近8,說明低溫主要發生反應(3),生成了N2O.ANTARIS IGS在線分析儀測試結果也證明低溫生成了N2O,并且隨溫度降低N2O選擇性提高.N2O的產生是由于該條件下CH4轉化率極低,催化劑表面存在NOads和Nads物種,N2O可以通過簡單的Nads+ NOads反應途徑生成的.16
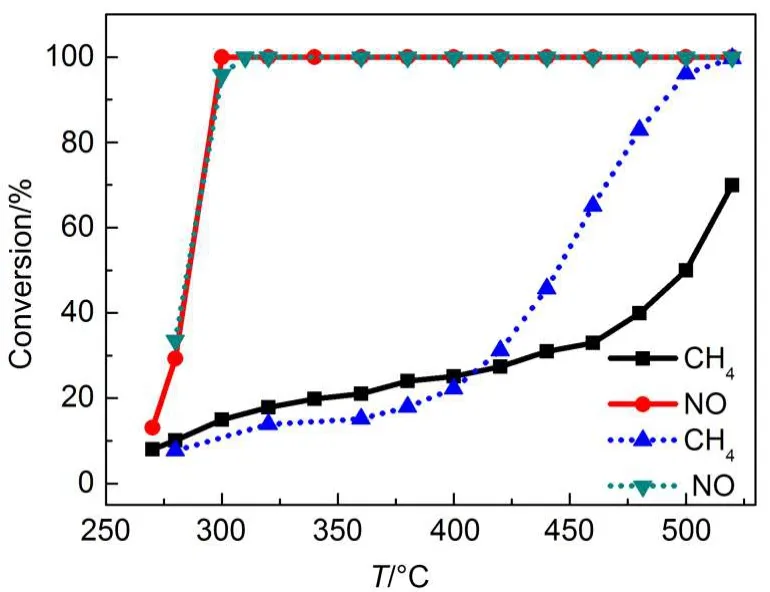
圖2 CO2對Pt催化劑上CH4+NO反應活性的影響Fig.2 Effect of CO2on the activity of Pt-based catalyst for CH4+NO reaction
3.3 10%(φ)H2O對CH4+NO+CO2反應的影響
從圖1可以看出,添加H2O后,Pt催化劑上CH4在520°C達到最大轉化率79%,NO在304°C完全轉化,相比無H2O條件,CH4轉化率在360°C以上出現明顯下降,而NO轉化率不變,說明水蒸氣對CH4與NO的反應影響不大,但是減弱或者抑制了CH4與CO2的重整反應(4)和逆水汽變換反應(5),從而降低了CH4轉化率.此條件下污染物轉化過程中在上述五個反應基礎上還可能發生蒸汽重整反應:
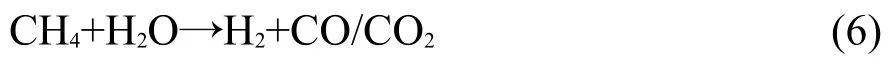
不同溫度條件下CH4+NO+H2O+CO2反應的NO/CH4轉化率比值及尾氣中的CO含量列于表1.從表中可以看出:尾氣中COa遠低于上述CH4+NO+ CO2反應的CO生成量,說明添加H2O減弱或抑制了反應(4)和(5).在520-480°C之間:R<3,COa>COb,可見除了發生反應(1)之外,還發生了CH4與CO2的重整反應(4)和/或者CH4與H2O的重整反應(6)生成了CO.此時不能確定反應(4)和(6)哪個反應為主,根據文獻22報道CH4與CO2的重整反應遠慢于CH4與H2O的重整反應,表明此時可能主要發生反應(6); 460°C時,3<R<4,COa<COb,說明同時發生反應(1)和(2),并以(2)為主;420-290°C之間,4<R≤8.26,尾氣中沒有CO生成,說明發生反應(2)和(3),隨著溫度降低,R增大,更多的反應以途徑(3)進行,生成了N2O.ANTARIS IGS在線分析儀測試結果也證明低溫生成了N2O,并且隨溫度降低N2O選擇性提高.
3.4 計量比的O2對CH4+NO+CO2反應的影響
從圖1可以看出有氧條件下Pt催化劑對于CH4和NO分別在439和425°C達到完全轉化.此條件下污染物轉化過程中還可能發生以下反應:

相比無O2條件,NO轉化活性明顯降低,說明O2出現后體系中存在甲烷被O2氧化和甲烷被NO氧化的競爭,甲烷被O2氧化優先發生,18使得CH4轉化活性迅速提高,NO轉化活性低于無O2條件.
不同溫度條件下CH4+NO+O2+CO2反應的NO/ CH4轉化率比值及尾氣中的CO含量列于表1.從表中可以看出:O2的添加使得尾氣中COa生成量相比CH4+NO+H2O+CO2條件進一步降低.在整個溫度范圍內,R值都小于3,說明除了CH4與NO的反應外,在整個溫度范圍內CH4主要發生了氧化反應(7)使得R<3.在520-440°C之間,COa與COb基本一致,不能確定是反應(1)還是反應(4)生成的;420°C時, COa<COb,說明反應(1)或(4)減弱,CH4和NO以途徑(2)反應增多;400-340°C之間,尾氣中沒有CO生成,R值比高溫區增大,但是仍然小于3,有反應(2)的發生.但是不能根據R值判斷有沒有反應(3)和(8)的發生.使用ANTARIS IGS在線分析儀檢測反應前后的NOx(NO、N2O和NO2),結果發現,整個溫度范圍內有極少量的N2O生成,在低溫時逐漸檢測到NO2,隨著溫度降低NO2選擇性提高.說明低溫時CH4轉化率降低,沒有足夠的CH4將NO還原,從而發生了反應(8)生成了NO2.
3.5 10%(φ)H2O和計量比的O2同時存在對CH4+ NO+CO2反應的影響
此時反應體系存在CH4、NO、H2O、O2和CO2,污染物轉化過程中上述的8個反應都可能發生.從圖1也可以看出H2O和O2同時存在時Pt催化劑對于CH4和NO分別在416和395°C達到完全轉化,CH4的轉化活性優于上述各條件.這可能由于O2和H2O同時存在時,Pt催化劑上放熱的甲烷氧化反應和強吸熱的甲烷水蒸氣重整反應同時發生,反應體系本身實現了自供熱,在較低的反應溫度下達到較高的甲烷轉化率.19對于NO的轉化活性,雖低于無O2條件(CH4+NO+CO2和CH4+NO+H2O+CO2),但是高于CH4+NO+O2+CO2條件的NO活性,這可能是由于蒸汽重整反應產生H2,H2作為還原劑提高了NO的轉化,從而提高催化劑的三效性能.5不同溫度條件下CH4+NO+H2O+O2+CO2反應的NO/CH4轉化率比值及尾氣中的CO含量列于表1.從表1可以看出,只有少部分溫度下檢測到0.01%的CO,大部分溫度下沒有檢測到CO,說明O2和H2O同時存在抑制了反應(4)和(5).我們知道只發生CH4與NO的反應時3≤R≤8,然而在O2和H2O同時存在條件下R值在整個溫度范圍內均小于3且大部分在1左右.說明此條件下主要反應為氧化反應(7)和蒸汽重整反應(6)(蒸汽重整反應中產生的CO也可以進一步發生氧化或通過水汽變換反應除去).NO的轉化主要依靠CH4與NO以1:4反應(2)進行,可能有CH4與NO以1:3反應生成CO,但CO進一步會發生氧化反應或通過水汽變換反應除去.ANTARIS IGS在線分析儀檢測結果顯示,低溫區有NO2生成,證明低溫CH4轉化率較低時,NO可被O2氧化生成NO2.
為了進一步證明H2O和O2同時存在條件下有蒸汽重整反應(6)的發生,對H2O和O2同時存在時不同溫度下的CH4相應轉化率下所需氧原子含量(記為A)、NO相應轉化率下提供的氧原子含量(記為B)及原始氣提供的氧原子含量(記為C),進行了計算并列于表2.
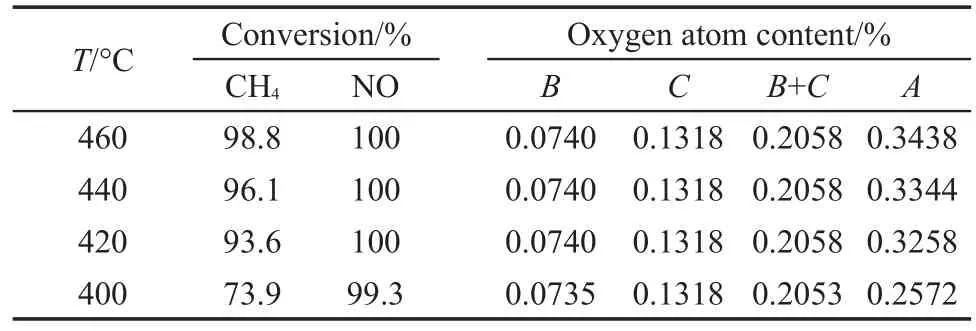
表2 不同溫度下各氧含量結果Table 2 Oxygen atom contents at different temperatures
原始反應氣組成為0.087%(φ)CH4+0.074%(φ) NO,從CH4氧化反應方程CH4+2O2=CO2+2H2O可以看出,1 mol CH4需要4 mol氧原子,而1 mol NO提供1 mol氧原子.從表2結果可以看出,各溫度條件下對應NO轉化率所提供的氧與原始氣所提供的氧原子含量之和均小于相應CH4轉化率下所需要的氧原子含量,說明有H2O參與反應,提供了氧原子,從而證明H2O和O2同時存在條件下,有蒸汽重整反應的發生.
4 結論
各條件下的CH4與NO反應高溫時存在以CH4: NO摩爾比1:3反應生成CO和N2;中溫區以摩爾比1:4反應生成N2和CO2;低溫區,無氧時有N2O生成,有氧時NO被氧化生成NO2.
有CO2存在條件下的CH4+NO反應,大量CH4發生CO2與CH4的重整反應;添加10%(φ)H2O,減弱CO2與CH4的重整反應;添加計量比O2,主要發生CH4被O2氧化反應,降低了NO轉化率,CO2與CH4的重整反應受到抑制;同時添加計量比O2和10%(φ) H2O,CH4被O2氧化、蒸汽重整、CH4與NO反應同時發生,Pt催化劑上CH4與NO轉化活性均提高.
(1) Bounechada,D.;Groppi,G.;Forzatti,P.;Kallinen,K.; Kinnunen,T.Appl.Catal.B:Environ.2012,119,91.
(2) Xia,W.S.;Chang,G.;Hou,Y.H.;Weng,W.Z.;Wan,H.L. Acta Phys.-Chim.Sin.2011,27,1567.[夏文生,常 剛,侯玉慧,翁維正,萬惠霖.物理化學學報,2011,27,1567.]doi: 10.3866/PKU.WHXB20110627
(3) Li,C.L.;Chen,W.;Yuan,J.;Shangguan,W.F.Acta Phys.-Chim.Sin.2012,28,450.[李曹龍,陳 威,袁 堅,上官文峰.物理化學學報,2012,28,450.]doi:10.3866/PKU. WHXB201112141
(4) Klingstedt,F.;Neyestanaki,A.K.;Byggningsbacka,R.; Lindfors,L.E.;Lundén,M.;Petersson,M.;Tengstr?m,P.; Ollonqvist,T.;V?yrynen,J.Appl.Catal.A:Gen.2001,209, 301.doi:10.1016/S0926-860X(00)00768-7
(5) Salaün,M.;Kouakou,A.;Da Costa,S.;Da Costa,P.Appl. Catal.B:Environ.2009,88,386.doi:10.1016/j. apcatb.2008.10.026
(6) Lan,L.;Chen,S.H.;Zhao,M.;Gong,M.C.;Chen,Y.Q. J.Mol.Catal.A:Chem.2014,394,10.doi:10.1016/j. molcata.2014.06.032
(7) Yuan,S.H.;Wang,Y.J.;Shi,Z.H.;Zhao,M.;Gong,M.C.; Liu,Z.C.;Chen,Q.Z.;Chen,Y.Q.Chin.J.Catal.2007,28, 401.[袁書華,王永軍,史忠華,趙 明,龔茂初,劉忠長,陳啟章,陳耀強.催化學報,2007,28,401.]doi:10.1016/S1872-2067 (07)60036-9
(8) Guo,J.X.;Shi,Z.H.;Wu,D.D.;Yin,H.Q.;Gong,M.C.; Chen,Y.Q.Appl.Surf.Sci.2013,273,527.doi:10.1016/j. apsusc.2013.02.074
(9) Oh,S.H.;Mitchell,P.J.;Siewert,R.M.J.Catal.1991,132, 287.doi:10.1016/0021-9517(91)90149-X
(10) Burch,R.;Loader,P.K.Appl.Catal.B:Environ.1994,5,149. doi:10.1016/0926-3373(94)00037-9
(11) Descorme,C.;Gélin,P.;Lécuyer,C.;Primet,M.J.Catal.1998, 177,352.doi:10.1006/jcat.1998.2112
(12) Marques,R.;Kabouss,K.E.;Da Costa,P.;Da Costa,S.; Delacroix,F.;Djéga-Mariadassou,G.Catal.Today 2007,119,166.doi:10.1016/j.cattod.2006.08.019
(13) Ozkan,U.S.;Kumthekar,M.W.;Karakas,G.Catal.Today 1998,40,3.doi:10.1016/S0920-5861(97)00112-0
(14) Li,B.;Wang,H.;Ding,F.C.;Li,C.Q.;Song,Y.J.;Ke,M.; Ren,C.T.Acta Phys.-Chim.Sin.2013,29,1289.[李 濱,王 虹,丁福臣,李翠清,宋永吉,柯 明,任翠濤.物理化學學報,2013,29,1289.]doi:10.3866/PKU.WHXB201304162
(15) Burch,R.;Ramli,A.Appl.Catal.B:Environ.1998,15,49.doi: 10.1016/S0926-3373(97)00036-2
(16) Burch,R.;Ramli,A.Appl.Catal.B:Environ.1998,15,63.doi: 10.1016/S0926-3373(97)00037-4
(17) Ohtsuka,H.;Tabata,T.;Hirano,T.Appl.Catal.B:Environ. 2000,28,L73.
(18) Fang,H.;Cai,L.;Liu,P.;Zhao,M.;Zhang,L.J.;Gong,M.C.; Chen,Y.Q.Acta Phys.-Chim.Sin.2006,22,1004.[房 華,蔡 黎,劉 萍,趙 明,張麗娟,龔茂初,陳耀強.物理化學學報,2006,22,1004.]doi:10.3866/PKU.WHXB20060819
(19) Cai,X.L.Catalyst forAutothermal Reforming of Methane to Produce Hydrogen.Ph.D.Dissertation,South China University of Technology,Guangzhou,2007.[蔡秀蘭.甲烷、氧氣和水蒸氣自熱重整制氫催化劑的研究[D].廣州:華南理工大學, 2007.]
(20) Subramanian,S.;Kudla,R.J.;Chattha,M.S.Ind.Eng.Chem. Res.1992,31,2460.doi:10.1021/ie00011a009
(21) Gao,J.;Hou,Z.Y.;Lou,H.;Zheng,X.M.Fuel Cells: Technologies for Fuel Processing,1st ed.;Elsevier Science: Amsterdam,2011;pp 191-221.
(22) Grenoble,D.C.;Estadt,M.M.;Ollis,D.F.J.Catal.1981,67, 90.doi:10.1016/0021-9517(81)90263-3
Effects of H2O and O2on the Reaction of NO Reduction by CH4under Stoichiometric Natural Gas Vehicles
SHANG Hong-Yan1HU Wei1WANG Yun2REN Cheng-Jun3GONG Mao-Chu3CHEN Yao-Qiang1,3,*
(1College of Chemical Engineering,Sichuan University,Chengdu 610065,P.R.China;2Sichuan Zhongzi Exhaust Gas Cleaning Co.,Ltd.,Chengdu 611731,P.R.China;3Key Laboratory of Green Chemistry&Technology, Ministry of Education,College of Chemistry,Sichuan University,Chengdu 610064,P.R.China)
Composite support CeZrYLa+LaAl was prepared by co-precipitation,and platinum catalyst supported on the composite support was prepared by impregnation.The behavior of the Pt catalyst for the reaction of NO reduction by CH4from the exhausts of natural gas vehicles(NGVs)was studied under stoichiometric conditions.Additionally,the effects of 10%(volume fraction,φ)H2O and stoichiometric O2on the reaction in the presence of CO2were also investigated.Results show that N2and CO2were the main products for the different reactions,CO was detected under high temperature,and NOxwas detected under low temperature(in the presence of O2,the NOxwas NO2,whereas the NOxwas N2O when no O2was present).In the presence of 10%(φ)H2O,the conversion of CH4noticeably decreased and NO conversion remained unchanged,possibly because the presence of H2O weakens the reforming reaction of CH4with CO2,but does not affect the activity of NO reduction by CH4.In the presence of stoichiometric O2,there was an obvious increase of CH4conversion and a decrease of NO conversion.These could be explained by the competition between NO and O2,where the oxidation of methane by O2is the main reaction,limiting the reaction of NOreduction by CH4.Moreover,in the presence of 10%(φ)H2O and stoichiometric O2,CO2reforming of CH4was negligible.Numerous reactions were detected simultaneously,such as the oxidation of CH4by NO,steam reforming of CH4,and the reduction of NO by CH4,thus improving the conversions of CH4and NO.?Editorial office ofActa Physico-Chimica Sinica
Pt;CeZrYLa+LaAl;Gas composition;Reduction of NO by CH4; Natural gas vehicle exhaust purification
O643
10.3866/PKU.WHXB201502051www.whxb.pku.edu.cn
Received:November 2,2014;Revised:February 4,2015;Published on Web:February 5,2015.
?Corresponding author.Email:nic7501@scu.edu.cn;Tel:+86-28-85418451.
The project was supported by the National Natural Science Foundation of China(21173153),Project from Sichuan Provincial Environment Office,
China(2011HB002),and Science and Technology Support Project of Science and Technology Department of Sichuan Province,China(2012FZ0008).
國家自然科學基金(21173153),四川省環境保護廳項目(2011HB002)及四川省科技廳科技支撐項目(2012FZ0008)資助

