早產兒腦損傷與宮內感染引起細胞因子網絡反應的臨床研究
莫坤梅,黎遠團,謝建紅,陳雨彬,梁伯泉,陳忠其,鄧 玲(佛岡縣人民醫院.兒科; .檢驗科; .病理科; .產科,廣東 佛岡 511600)
早產兒腦損傷與宮內感染引起細胞因子網絡反應的臨床研究
莫坤梅a,黎遠團a,謝建紅a,陳雨彬a,梁伯泉b,陳忠其c,鄧 玲d(佛岡縣人民醫院a.兒科; b.檢驗科; c.病理科; d.產科,廣東 佛岡 511600)
目的 研究宮內感染與早產兒腦損傷的因果關系,從細胞因子網絡反應角度探討宮內感染早產兒腦損傷機制,為防治早產兒腦損傷提供新途徑。方法 將100例早產兒根據頭顱超聲及CT檢查結果分為早產腦損傷組(31例)和早產無腦損傷組(69例)。通過對2組胎膜、胎盤的病理檢測(主要以檢測絨毛膜羊膜炎為主),判斷是否有宮內感染導致的早產兒腦損傷。采用酶聯免疫吸附試驗(ELISA)檢測2組血清中細胞因子[IL-1β、IL-6、IL-10及腫瘤壞死因子(TNF-α)]的水平。結果 100例患兒中發生宮內感染40例,60例為非宮內感染,宮內感染患病率為40.0%。宮內感染患兒腦損傷的患病率為47.5%(19/40),非宮內感染患兒腦損傷的患病率為20.0%(12/60)。宮內感染患兒腦損傷患病率顯著高于非宮內感染患兒(χ2=8.485,P<0.05)。早產腦損傷組IL-1β、IL-6、IL-10及TNF-α分別為(6.33±2.17)(8.20±4.10)(1.46±0.25)及(5.35±2.00)μg·L-1;早產無腦損傷組IL-1β、IL-6、IL-10及TNF-α分別為(1.44±1.01)(1.58±2.33)(1.65±0.30)及(3.57±1.33)μg·L-1。早產腦損傷組IL-1β、IL-6、TNF-α顯著高于早產無腦損傷組,IL-10低于早產無腦損傷組(均P<0.05)。結論 早產兒腦損傷與宮內感染關系密切,細胞因子網絡反應可能介導該損傷過程。
早產兒; 腦損傷; 宮內感染; 細胞因子
隨著當代醫學的飛速發展,早產兒的存活率越來越高,但早產兒腦損傷及其損傷后遺癥,在嚴重影響患兒生活質量的同時,給社會及家庭也帶來巨大負擔。早產兒腦損傷已逐漸成為早產兒死亡的重要原因,是導致早產兒發生嚴重神經系統后遺癥的主要危險因素[1]。出生體質量<1 500 g的早產兒5.0%~15.0%長大后遺留有嚴重的神經系統缺陷,其中約10.0%發生腦性癱瘓(CP),25.0%~50.0%表現為輕度神經發育障礙;腦損傷所致后遺癥不僅累及運動系統,而且累及認知和行為,從而引起學習障礙[2]。有研究[3]表明,早產兒腦損傷除其自身腦部病理基礎外,宮內感染后引起炎性細胞因子網絡反應是導致早產兒腦損傷的主要原因。本研究主要是為了明確宮內感染與早產兒腦損傷的因果關系,從細胞因子網絡反應角度探討宮內感染早產兒腦損傷機制,為防治早產兒腦損傷提供新的途徑。
1 對象與方法
1.1 研究對象
選擇2011年6月至2013年6月在佛岡縣人民
醫院產科分娩的早產兒100例,男50例,女50例,均為單胎,出生體質量為2.0~3.1 kg。分娩孕周為28~36+6周,其中28~30周14例,31~33周65例,34~36+6周21例。自然分娩80例,臀位助產分娩2例,剖腹產18例。Apgar評分:8分35例,9分50例,10分15例。均排除:1)孕婦產前有妊娠合并癥(子癇前期、妊娠期糖尿病、妊娠合并心臟病及胎盤早剝等);2)新生兒出生<12 h,有遺傳代謝性疾病、神經系統畸形及其他系統嚴重畸形;3)圍生期早產兒有窒息缺氧史。
早產兒出生3~7 d由專人經前、后囟進行頭顱超聲檢查(探頭頻率為7.5~10.0 MHz),以后每隔l周復查1次,直至出院;對頭顱B超正常、但疑有顱內病變者行頭顱CT檢查。根據頭顱超聲及CT檢測結果將100例患兒分為早產腦損傷組(31例)和早產無腦損傷組(69例)。
2組日齡、性別、出生體質量、Apgar評分等比較差異均無統計學意義(均P>0.05),見表1。
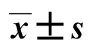
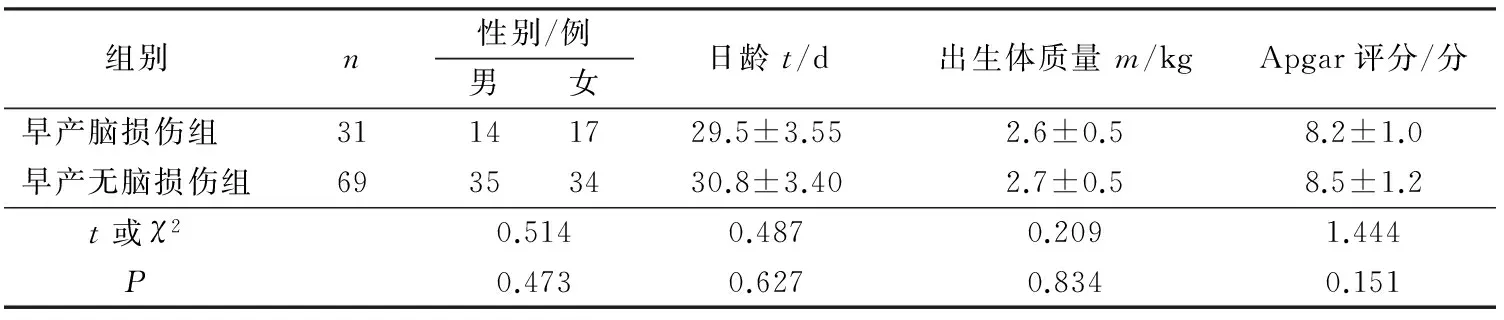
組別n性別/例男女日齡t/d出生體質量m/kgApgar評分/分早產腦損傷組 31141729.5±3.552.6±0.58.2±1.0早產無腦損傷組69353430.8±3.402.7±0.58.5±1.2t或χ20.5140.4870.2091.444P0.4730.6270.8340.151
1.2 方法
通過對產婦胎膜、胎盤的病理檢測,判斷是否存在宮內感染;行早產兒頭顱超聲及CT檢測,確定是否有腦損傷;通過酶聯免疫吸附試驗檢測細胞因子IL-1β、IL-6、IL-10及腫瘤壞死因子(TNF-α)等。
1.2.1 胎膜、胎盤的病理檢測及診斷標準
產婦分娩后,及時進行胎膜、胎盤病理檢測(主要以檢測絨毛膜羊膜炎為主),判斷是否有宮內感染。絨毛膜羊膜炎診斷標準[4]:在絨毛膜及羊膜組織中,顯微鏡下可見中性粒細胞浸潤5~10個/HP為輕度,11~30個為中度,>30個為重度。臨床診斷標準:如胎盤病理檢測為絨毛膜羊膜炎,產婦發熱,體溫≥37.5 ℃,心率>100次·min-1,胎心率>160次·min-1,羊水臭味,子宮壓痛,末梢血WBC>15×109L-1,可診斷為宮內感染[5]。
1.2.2 頭顱超聲檢查
患兒在出生3~7 d后進行頭顱超聲檢查,后每隔1周進行復查,超聲檢測正常但懷疑有病變者行CT檢查。頭顱超聲檢查早產兒腦損傷:1)生發基質-腦室內出血,腦室周圍出血及梗死;2)腦室周圍白質軟化(PVL);3)其他部位的損傷,如蛛網膜下腔、小腦的出血、基底核及橋腦的變性或壞死等[6]。
1.2.3 臍帶血細胞因子檢測
新生兒娩出后未斷臍帶前,臍靜脈穿刺抽取臍血6 mL,靜置5 min后,以3 000 r·min-1的速度離心5 min, 收取上層血清液,低溫(—70 ℃)保存,待檢。采用酶聯免疫吸附試驗(ELISA)檢測血清中細胞因子IL-1β、IL-6、IL-10及TNF-α水平。ELISA試劑盒購自博谷生物科技有限公司,嚴格按試劑盒說明書進行操作。
1.3 統計學方法
2 結果
2.1 胎膜、胎盤的病理檢測
100例患兒中有40例患兒被診斷為宮內感染,60例患兒為非宮內感染。宮內感染患病率為40.0%。
2.2 2組患兒宮內感染發生率的比較
40例宮內感染患兒腦損傷的患病率為47.5%(19/40),60例非宮內感染患兒為20.0%(12/60)。宮內感染患兒腦損傷患病率顯著高于非宮內感染患兒(χ2=8.485,P<0.05)。早產腦損傷組宮內感染發生率明顯高于早產無腦損傷組(P<0.05)。見表2。
表2 2組宮內感染發生率的比較

組別n宮內感染非宮內感染例%例%早產腦損傷組311961.3*1238.7早產無腦損傷組692130.44869.6
*P<0.05與早產無腦損傷組比較。
2.3 2組細胞因子及TNF-α水平的比較
早產腦損傷組IL-1β、IL-6、TNF-α顯著高于早產無腦損傷組,IL-10低于早產無腦損傷組,差異均有統計學意義(均P<0.05)。見表3。
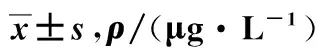
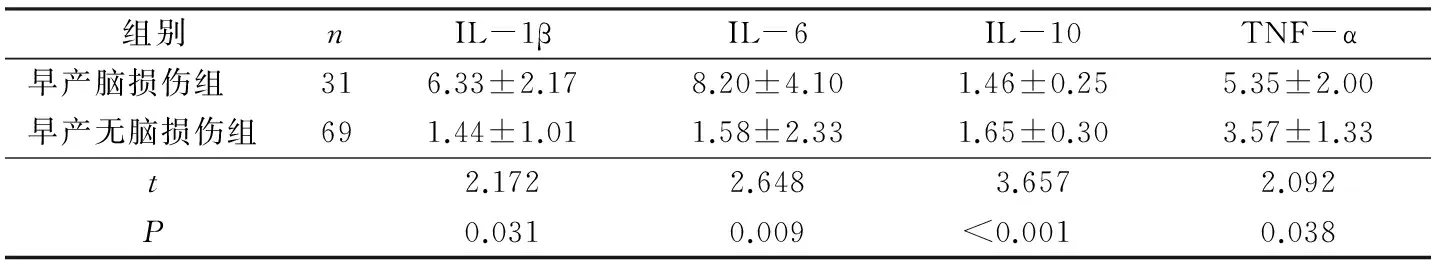
組別nIL-1βIL-6IL-10TNF-α早產腦損傷組316.33±2.178.20±4.101.46±0.255.35±2.00早產無腦損傷組691.44±1.011.58±2.331.65±0.303.57±1.33t2.1722.6483.6572.092P0.0310.009<0.0010.038
3 討論
隨著圍產醫學水平的提高,早產兒出生率也逐年提高,但如何提高早產兒的成活率及生存質量是當前關注的問題。新生兒重癥監護病房(NICU)出現后,保暖箱、機械通氣以及其他醫療技術的引進,使早產兒病死率顯著降低。但根據國外大樣本的研究資料[7]結果顯示,早產兒腦損傷(內出血和腦白質損傷)發生率無明顯降低。其中約10%患兒發生不同程度的腦性癱瘓(cerebral palsy,CP),25%~50%表現為輕度神經發育障礙,涉及到運動、認知和行為,從而引起學習障礙[8],嚴重的后遺癥給患兒、家庭和社會帶來嚴重負擔。
目前認為,引起早產兒腦損傷的因素很多,發病機制復雜,尚不完全清楚。有研究[9]表明,早產兒腦損傷與早產兒腦血管發育不完善而導致的易損性增加、圍產期窒息、缺氧缺血、宮內感染以及免疫學機制等有關,尤其是宮內感染后引起炎性細胞因子網絡反應是導致早產兒腦損傷的主要原因。有研究[10]通過對懷孕大鼠體內注入脂多糖建立動物模型發現,宮內感染能導致仔鼠腦損傷,表明腦損傷與宮內感染有密切的關系。
本研究以早產兒為研究對象,經胎膜、胎盤病理檢測,100例患兒中,40例被診斷為宮內感染,宮內感染患病率為40.0%;行頭顱超聲檢查,31例被診斷為腦損傷(早產腦損傷組),患病率為31.0%,其中19例宮內感染(61.3%)。宮內感染患兒腦損傷的患病率為47.5%(19/40),非宮內感染患兒腦損傷的患病率為20.0%(12/60)。宮內感染患兒腦損傷患病率顯著高于非宮內感染患者(χ2=8.485,P<0.05)。結果提示,宮內感染患兒其患腦損傷概率明顯增加,表明宮內感染與腦損傷關系密切。但宮內感染導致腦損傷的機制尚未完全明確。由于宮內感染時蛻膜、胎盤或羊水,以及局部和循環中有較高水平的炎性因子,因此被認為與胎膜早破和早產密切相關[11]。
本研究對2組患兒采用ELISA法檢測臍靜脈血血清中細胞因子水平,結果顯示:早產腦損傷組IL-1β、IL-6、TNF-α顯著高于早產無腦損傷組,IL-10低于早產無腦損傷組(均P<0.05)。提示細胞因子反應網絡在早產兒腦損傷的形成機制中產生了重要作用。可能是由于孕婦宮內感染后,激活機體產生大量炎性因子,臍血中與此相關的IL-1β、IL-6、TNF-α水平明顯增高,并造成早產兒腦損傷;同時作為抗炎分子的IL-10水平顯著降低,炎癥保護作用減弱,亦可能是早產兒腦損傷的機制之一。
綜上所述,本研究提示產婦宮內感染與早產兒腦損傷有較為顯著的關系,細胞因子網絡反應可能是早產兒腦損傷的重要機制。同時提示:可從抗細胞因子藥物著手進行干預,為防治早產兒腦損傷提供新的途徑,具有良好的科學價值以及社會效益。
[1] 陳慧金,范秀芳,高喜容,等.6家醫院147例腦損傷早產兒的多中心隨訪報告[J].中國當代兒科雜志,2009,11(3):166-172.
[2] 中華醫學會兒科學分會新生兒學組.早產兒腦室周圍-腦室內出血與腦室周圍白質軟化的診斷建議[J].中華兒科雜志,2007,45(1):34-36.
[3] 史學凱,農紹漢,高平明,等.胎盤組織炎癥對早產兒腦室內出血發病風險的影響[J].中國新生兒雜志,2010,25(3):139-141.
[4] Peled E,Eidelman M,Katzman A,et al.Neonatal incidence of hip dysplasia:ten years of experience[J].Clin Orthop Relat Res,2008,466(4):771-775.
[5] Morin C,Zouaoui S,Delvalle Fayada A,et al.Ultrasound assessment of the acetabulum in the infant hip[J].Acta Orthop Belg,2013,65(3):261-265.
[6] 陳惠金.新生兒缺氧缺血性腦損傷和顱內出血的B超診斷[J].中華婦幼臨床醫學雜志,2005,1(1):10-12.
[7] Herber Jonat S,Schulze A,Kribs A,et al.Survival and major neonatal complications in infants born between 22 0/7 and 24 6/7 weeks of gestation(1999—2003)[J].Am J Obstet Gynecol,2006,195(1):16-22.
[8] De Vries L S,van Haastert I C,Rademaker K J,et al.Ultrasound abnormalities preceding cerebral palsy in high-risk preterm infants[J].Pediatr,2004,144(6):815-820.[9] 姚裕家.早產兒腦損傷的病因及病理生理機制[J].臨床兒科雜志,2009,24(3):16-18.
[10] [劉艷,徐三清,豐利芳,等.宮內感染導致腦損傷幼鼠腦組織核因子-κB、腫瘤壞死因子-α表達的變化[J].實用醫學雜志,2010,26(23):4319-4322.
[12] Ennen C S,Huisman T A,Savage W J,et al.Glial fibrillary acidic protein as a biomarker for neonatal hypoxic-ischemic encephalopathy treated with whole-body cooling[J].Am J Obstet Gynecol,2011,205(3):251-257.
(責任編輯:周麗萍)
Premature Brain Damage and Intrauterine Infection Cause Cytokine Network Response
MO Kun-meia,LI Yuan-tuana,XIE Jian-honga,CHEN Yu-bina,LIANG Bo-quanb,CHEN Zhong-qic,DENG Lingd(a.DepartmentofPediatrics; b.DepartmentofClinicalLaboratories; c.DepartmentofPathology; d.DepartmentofObstetrics,FogangPeople’sHospital,Fogang511600,China)
Objective To explore the causality relationship between intrauterine infection and brain damage in premature infants,to observe the mechanism of brain damage in premature infants with intrauterine infection from the perspective of cytokine network response,and to provide a new way of preventing premature brain damage.Methods According to head ultrasound and CT results,100 premature infants were divided into brain damage group(n=31) and non-brain damage group(n=69).Intrauterine infection-induced premature brain damage was observed through pathological examinations of fetal membranes and placenta(mainly chorioamnionitis).In addition,serum levels of cytokines interleukin-1β(IL-1β),interleukin-6(IL-6),interleukin-10(IL-10) and tumor necrosis factor-α(TNF-α) were detected by ELISA.Results The prevalence of intrauterine infection was 40.0%(40/100).The incidence of brain damage in infants with intrauterine infection(47.5%,19/40) was significantly higher than that in infants without intrauterine infection(20.0%,12/60)(χ2=8.485,P<0.05).Moreover,infants with brain damage had higher levels of IL-1β,IL-6 and TNF-α and lower levels of IL-10 than infants with non-brain damage((6.33±2.17),(8.20±4.10),(1.46±0.25) and(5.35±2.00)μg·L-1vs(1.44±1.01),(1.58±2.33),(1.65±0.30) and(3.57±1.33)μg·L-1,respectively;P<0.05).Conclusion Premature brain damage is positively associated with intrauterine infection,and the cytokine network response may mediate the damage process.
preterm infants; brain damage; intrauterine infection; cytokine
2014-12-19
清遠市科技項目(2009B067)
莫坤梅(1979—),女,學士,主治醫師 主要從事新生兒重癥監護的研究。
R722
A
1009-8194(2015)09-0050-04
10.13764/j.cnki.lcsy.2015.09.022

