根霉脂肪酶系統分離優化實驗研究
孟 軍,張紅亞,張 勇,趙紀耀,王 濤,陳四華
(安徽建筑大學 環境與能源工程學院/水污染控制與廢水資源化省級重點實驗室,安徽 合肥 230022)
根霉脂肪酶系統分離優化實驗研究
孟 軍,張紅亞,張 勇,趙紀耀,王 濤,陳四華
(安徽建筑大學 環境與能源工程學院/水污染控制與廢水資源化省級重點實驗室,安徽 合肥 230022)
利用固態發酵法生產根霉脂肪酶,對影響此酶分離的多種條件進行了優化研究,其中包括浸提固液比、浸提時間、硫酸銨飽和度和分子排阻凝膠層析的洗脫流速。得出了優化后條件為浸提固液比為1∶3,浸提時間為120 min,硫酸銨飽和度為40%,洗脫流速為1.5 mL/min的結論。
脂肪酶;柱層析;系統分離
1 引言
脂肪酶是一類特殊的酯鍵水解酶,可將脂肪分解成甘油和脂肪酸,機理主要是脂肪酶對甘油三酸酯的催化水解反應是親核反應,脂肪酶也是一種弱的親核試劑[1]。脂肪酶廣泛應用于食品、輕紡、皮革、精細化工、有機合成、醫藥等領域[2~4]。根霉屬微生物是脂肪酶的重要生產菌,從根霉菌中已分離到30多種脂肪酶,且有多種根霉脂肪酶已被制成商品化酶制劑[5]。此外,根霉脂肪酶大多具有高度的1、3位置專一性,因而常用于油脂加工,以提高油脂的品質[6]。
目前,脂肪酶的分離純化方法主要有雙水相萃取分離法[7]、膜分離法[8]、硫酸銨—丙酮協同法[9]、免疫純化法[10]、界面親和層析法[11]。但這些方法都有各自的缺點,如雙水相萃取分離法的關鍵是找到與該種脂肪酶對應的雙水相;膜分離法存在易堵塞的現象,重復使用率不高;硫酸銨—丙酮協同法有酶回收率較低的現象;免疫純化法是一種價格較昂貴的方法;界面親和層析法的載體較昂貴,機械強度低[12]。
本實驗根霉脂肪酶成功篩選的基礎上進一步對該酶的分離純化方法進行研究,旨在找出一種分離步驟少,方法簡單,成本低廉,分離能力強的分離純化方法,為該類脂肪酶性質的研究開拓道路。
2 實驗的材料與方法
菌種:實驗室自篩根霉。
儀器與設備:蛋白質純化儀(GE公司)。
2.1 粗脂肪酶液制備
培養基:斜面培養基;產孢培養基;產酶基礎培養基[13]。
粗脂肪酶液的制備:根霉菌株接種于斜面培養基,置于28 ℃恒溫箱中培養96 h,轉至產孢培養基,置于28 ℃恒溫箱中培養96 h,轉至產酶基礎培養基,于250 mL三角燒瓶中,28 ℃培養96 h,后用離子濃度為1/15 mol/L的磷酸鹽緩沖液浸提后既得脂肪酶液。
2.2 酶活力的測定及活力單位定義
脂肪酶活力的測定及酶活定義參見Gandhi N N[14]等。
2.3 固液比的優化
稱量130 g經過發酵的固體發酵培養基并研碎后均分成五份,放在五個三角燒瓶中,分別按固液比1∶1、1∶2、1∶3、1∶4、1∶5順序加入pH值為7.5的磷酸鹽緩沖液浸提酶液,時間為4 h,然后測定各瓶浸提液中的酶活并記錄。
2.4 浸提時間的優化
稱量26 g的經過發酵的固體培養基并用將其研碎,后加入90 mL緩沖液浸提,開始計時,每隔0.5 h測一次浸提液的酶活力。
2.5 硫酸銨鹽析飽和度的優化
取五份脂肪酶液,每份為100 mL,分別按10%,20%,30%,40%,50%飽合度加入粉末狀的硫酸銨鹽后,攪拌均勻,在5 000 r/min離心15 min,沉淀用pH值為7.5的磷酸鹽緩沖液10 mL溶解。分別測定上清液和其對應的沉淀的酶活為U1,U2。
2.6 Sephacryl S-300 HR 柱層析洗脫流速的優化
粗分離得到的脂肪酶樣品經透析袋透析后取1 mL樣,在10 000 r/min下離心15 min,然后上樣進行分析,洗脫速度分別采用0.5 mL/min、1.0 mL/min、1.5 mL/min,2.0 mL/min,2.5 mL/min。在紫外280 nm下監測記錄峰形,收集最高峰對應的流出液,檢測其脂肪酶酶活。
3 結果與分析
3.1 脂肪酶粗分離的浸提固液比
從圖1中可以看出,隨著浸提固液比的增大,溶解在浸提液中脂肪酶的酶活力逐漸升高,固液比為1∶3時浸提液中脂肪酶的酶活力最高,以后隨著浸提固液比的增大,浸提液中酶活力逐漸變小,為了脂肪酶能夠最大程度的溶解在浸提液和減少脂肪酶下游分離的難度,該固體發酵脂肪酶的最佳浸提固液比為1∶3。
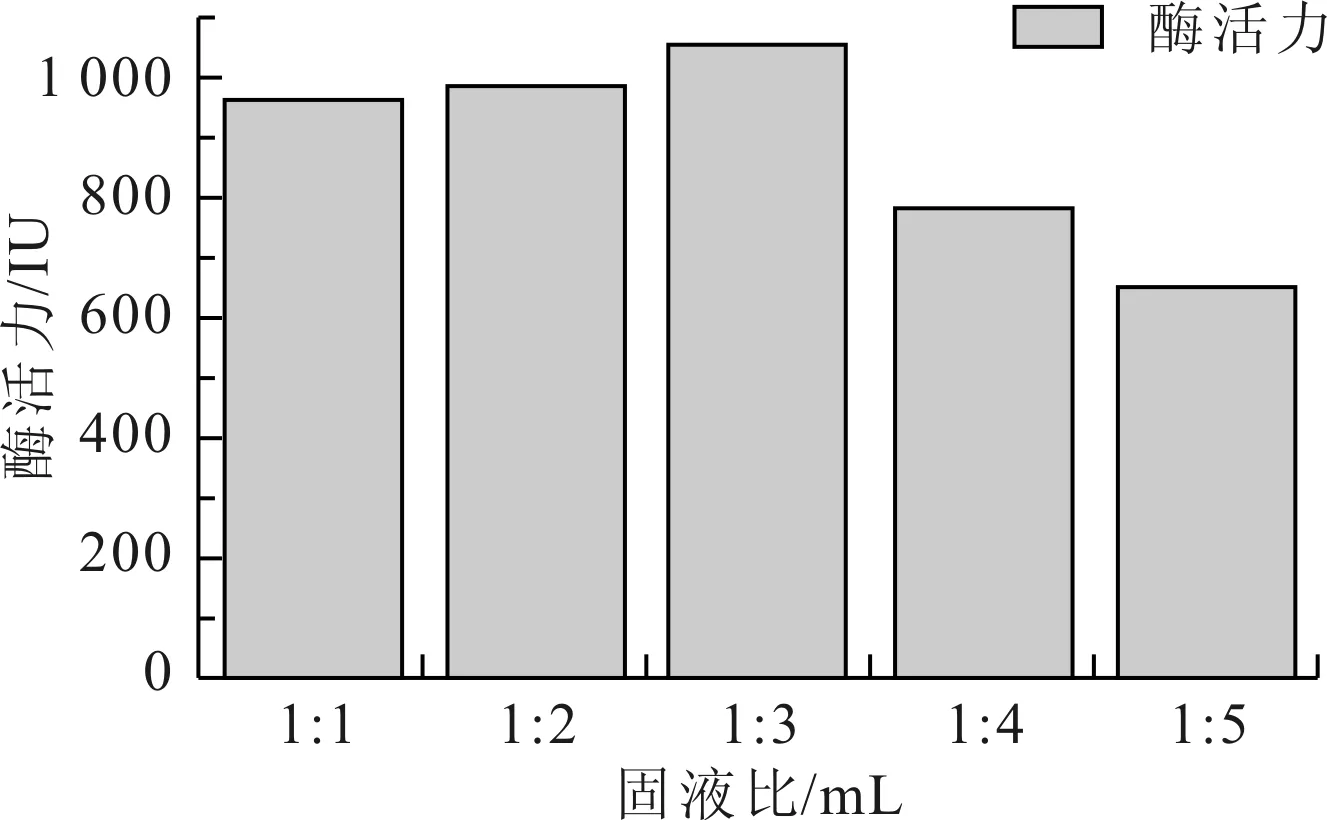
圖1 浸提固液比對提取脂肪酶的影響
3.2 脂肪酶粗分離的最優浸提時間
從圖2中可以看出從120 min起到180 min時,溶解在浸提液中脂肪酶的量已經穩定。在120 min后,浸提液中酶活力沒有變化,所以浸提120 min就可以提取培養基中的大部分脂肪酶,可定120 min浸提時間為最優浸提時間。

圖2 浸提時間對提取脂肪酶的影響
3.3 硫酸銨分級沉淀最佳飽和度的確定
在硫酸銨飽和度梯度下分離的脂肪酶液,所對應的上清液和沉淀的酶活力結果見圖3,由圖可知隨著硫酸銨飽和度的升高,上清液的酶活力逐漸降低,沉淀部分的酶活力逐漸升高,從40%硫酸銨飽和度開始,脂肪酶分離得到的上清液就未檢測到酶活,而沉淀部分的酶活趨于穩定,所以最佳硫酸銨飽和度為40%。
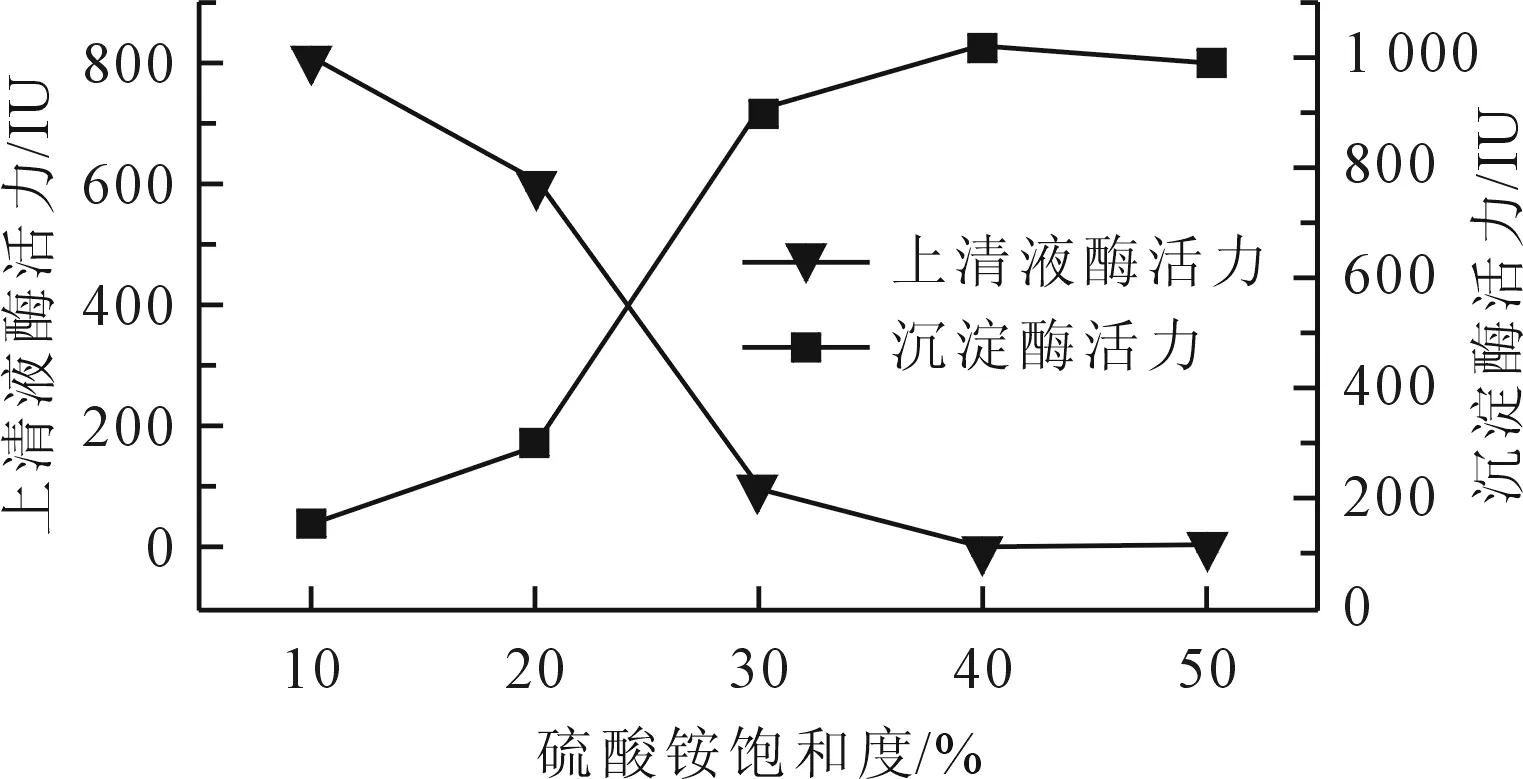
圖3 硫酸銨飽和度對分離脂肪酶的影響
3.4 Sephacryl S-300 HR柱層析分離脂肪酶最佳洗脫流速的測定
從圖4中可以看出,Sephacryl S-300 HR柱層析在選定的五個洗脫流速下都可以分離得到純的脂肪酶。隨著洗脫流速的增加,分離得到的酶液酶活力也是逐漸增高,在洗脫流速達到1.5 mL/min時,分離的酶液酶活力達到最高,后隨著洗脫流速的增大,分離的酶液酶活力反而變小,同時與光吸收的變化也是一致的。在洗脫流速為1.5 mL/min時,280 nm紫外光下收集的分離液不僅光吸收值最大,而且脂肪酶活力最高,從而可以得出洗脫流速為1.5mL/min時為Sephacryl S-300 HR柱層析純化粗脂肪酶的最佳洗脫流速。
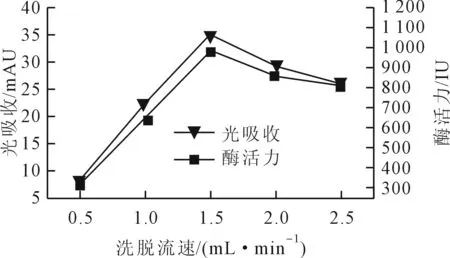
圖4 柱層析的洗脫流速對分離脂肪酶的影響
4 結語
本文對根霉脂肪酶分離實驗進行系統優化。經實驗測得最佳浸提固液比為1∶3,最優浸提時間為120 min,在40%飽和度的硫酸銨可使脂肪酶沉淀達到最大。最后選用美國GE公司的蛋白質純化儀配置的Sephacryl-S 300HR柱層析,優化了洗脫流速,最佳洗脫流速為1.5 mL/min。
從實驗中發現,該菌產酶量低,通過Sephacryl-S 300HR洗脫下來的脂肪酶不能直接檢測,只能采取冷凍干燥后檢測酶活。這也使得我們的實驗進展延遲,沒能繼續對純酶的性質進行研究。建議以后可以對根霉菌的發酵培養基進行優化提高產酶量,也可以嘗試通過各種誘變方法提高產酶量。
[1]Khare S K,Nakajima . Immobilization of Rhizopus japonicus lipase on celite and its application for enrichment of docosahexaenoic acid in soybean oil[J].Food Chemistry ,2000,68:153~157.
[2]彭立鳳.微生物脂肪酶的應用[J].生物工程進展,1999,19(5):61~65.
[3]馬歌麗,高建奇,張志剛,等.根霉脂肪酶產生菌篩選及發酵培養基研究[J]. 飼料工業,2006,27(22).
[4]Patel R. N., Biocatalysis: Synthesis of Chiral Intermediates for Pharmaceuticals[J].Current Org.Chem,2006(10):1289~1321.
[5]逄淑召,王 群,王 智,等.熒光假單孢菌Pseudomonas fluorescence 5963產脂肪酶條件的優化[J].生物加工過程,2004(1):62~65.
[6]顏興和,王 棟,徐 巖.根霉脂肪酶的研究進展[J].工業微生物,2005,35(3):45~49.
[7]楊建軍,馬曉迅.雙水相系統分離純化南極假絲酵母脂肪酶[J].化學工程,2009,37(5):49~52.
[8]鞠輝軍,汪學軍,劉均洪.微生物脂肪酶的純化方法[J].河南化工,2004(6):1~3.
[9]李燕妮,曹紅光.硫酸銨-丙酮協同沉淀法純化南極假絲酵母產脂肪酶[J].化學與生物工程,2006(5):36~37,48.
[10]閻金勇,丁 雙,楊江科,等.微生物酶分離純化研究進展[J].現代化工,2007(6):19~23.
[11]Baisida A,Sabuquilo P,Amisen P,etal A single step purification immobilization and hyperactivation of lipases via interfacial absorption on strongly hydrophobic supports[J].Biotechnol and Bioeng,1998,58(5):486~493.
[12]蘭立新,肖懷秋.微生物脂肪酶生物學特性及分離純化研究進展[J].江蘇調味副食品,2009(5):1~5.
[13]劉 斌,蔡敬民,吳茜茜,等.根霉產脂肪酶液態發酵條件及部分酶學性質研究[J].安徽農業科學,2003(6):992~993,1002.
[14]Gandhi N N,Sawant S B ,Joshi J B.Study on the lipozyme-catalyzed synthesis of butyl laurate[J].Biotechnol Bioeng,1995(46):1~12.
Research on the Optimization of SystematicSeparationof Rhizopus Chinensis Lipase
Meng Jun, Zhang Hongya, Zhang Yong, Zhao Jiyao, Wang Tao, Chen Sihua
((1.SchoolofEnvironmentandEnergyEngineering,AnhuiJianzhuUniversity/ProvincialKeyLaboratoryofWaterPollutionControlandwastewaterresourcesregeneration,Hefei230022,China)
By using solid state fermentation, the article aims to produce rhizopus lipases and researches on a variety of conditions that affect this enzyme separation, whichincludethe solid-to-liquidof extraction, time of extraction, saturation of ammonium sulfateand elution flow rate of molecular exclusion gel chromatography. After Optimization,theconditionsare that the solid-to-liquid ratiois 1∶3,time of extraction is 120 minutes,saturation of ammonium sulfate is 40% and elution flow rate is1.5mL/min.
lipase; column chromatography; systematic separation
2015-10-29
孟 軍(1988—),男,安徽合肥人,碩士研究生,主要從事水處理理論與技術研究。
Q556
A
1674-9944(2015)12-0277-02

