IL-28B基因多態性與HBeAg陽性的慢性乙型肝炎患者干擾素病毒學應答相關性的meta分析
滕巍,崔巍,劉沛
(中國醫科大學附屬第一醫院傳染科,沈陽 110001)
·論著·
IL-28B基因多態性與HBeAg陽性的慢性乙型肝炎患者干擾素病毒學應答相關性的meta分析
滕巍,崔巍,劉沛
(中國醫科大學附屬第一醫院傳染科,沈陽 110001)
目的研究白細胞介素28B(IL-28B)基因多態性與HBeAg陽性的慢性乙型肝炎患者應用干擾素病毒學應答的相關性。方法計算機檢索PubMed、Web of Science、China Bio Medicine(CBM)、萬方數據庫等,由2名評價員獨立檢索和提取資料并交叉核對,納入相關病例對照試驗。采用Cochrane協作網提供的RevMan 5.3軟件進行meta分析,應用Stata11.0軟件進行發表偏倚檢驗。結果共納入文獻7篇,包括1 345例患者,經過meta分析后發現與rs8099917 TG/GG等位基因相比,rs8099917 TT等位基因對于HBeAg陽性的慢性乙型肝炎患者應用干擾素的病毒學應答無明顯差異(P=0.20)。rs12979860 CC與CT/TT等位基因相比對于病毒學應答的發生沒有差異(P=0.75)。結論IL-28B(rs8099917、rs12979860)的基因多態性與HBeAg陽性慢性乙型肝炎患者應用干擾素達到持續病毒應答無相關性。
乙型肝炎;抗病毒治療;白細胞介素28B;基因多態性;meta分析
乙型肝炎病毒由于其傳播性強,傳播面廣且發病率高,而成為世界危害性很大的傳染病之一。根據世界衛生組織的調查,全球每年約有100萬人死于乙型肝炎病毒的感染,我國是乙型肝炎流行的高發區,感染率高達55.6%[1]。目前應用干擾素是治療慢性乙型肝炎的有效方法之一。國內外學者針對干擾素療效的應答因素做了大量的研究,包括性別、年齡、肝臟纖維化程度、病毒水平等,為患者應用干擾素個性化治療提供循證學依據。近年來,有學者研究表明[2]白細胞介素28B(interleukin-28B,IL-28B)基因多態性與丙肝患者應用干擾素治療的應答高度相關。隨著進一步的研究[3]還發現IL-28B基因多態性與丙肝病毒感染后的病毒自發清除及預后相關。但是IL-28B基因多態性與慢性乙型肝炎患者應用干擾素應答的關系目前尚無統一結論,有些研究結果甚至矛盾[4,5]。本研究運用Cochrane系統評價方法,選取國內外發表的IL-28B與HBeAg陽性的慢性乙型肝炎患者應用干擾素應答的相關文獻進行meta分析,旨在闡明兩者之間的關系。
1 材料與方法
1.1 檢索策略
計算機檢索PubMed、Web of Science、China Bio Medicine(CBM)、萬方數據庫等,并追查所有檢出文獻的參考文獻。檢索年限從建庫至2014年10月。
英文文獻檢索策略:(1)(il28b)AND hepatitis b virus;(2)(IL28B)OR ifn lambda OR genomics AND hepatitis b virus AND interferon。中文文獻檢索策略:(IL-28B OR白細胞介素28b)AND乙型肝炎
1.2 納入及排除標準
1.2.1 納入標準:(1)文獻內容涉及IL-28B與HBeAg陽性的慢性乙肝患者應用干擾素療效相關性的對照研究或橫斷面研究;(2)所有診斷為HBeAg陽性的慢性乙肝患者必須符合國際診斷標準;(3)所有文獻觀察終點為應用干擾素抗病毒治療48周時的病毒載量;(4)檢測多態性位點的實驗方法科學,如PCR,探針監測法等國際公認的基因監測方法;(5)研究位點符合Hardy-Weinberg平衡;(6)可獲得詳細的數據。
1.2.2 排除標準:(1)不符合納入標準;(2)樣本資料交代不清或不全;(3)無法獲取全文;(4)重復發表;(5)文獻類型為會議記錄、說明書、綜述、薈萃分析等。
1.3 文獻提取
由2人獨立進行文獻質量評價,意見不一致時通過討論解決分歧。數據提取由2位研究者獨立完成。
1.4 統計學方法
應用Cochrane協作網提供的RevMan 5.3軟件進行meta分析。以優勢比(odds rate,OR)表示,并給出95%可信區間(confidence interval,CI)。當試驗存在統計學異質性時,用隨機效應模型(random effects model,REM)進行合并分析,反之用固定效應模型(fixed effects model,FEM)計算。
應用Stata11.0軟件進行Begg’s檢驗,明確是否存在發表偏倚。
2 結果
2.1 納入研究的一般特征和質量評價
初檢得到478篇文獻,通過閱讀標題和摘要進行初篩,排除不符合納入標準的文獻。最終納入7篇[4~10]。7篇文獻共包括1 345例患者。
質量評價采用Cochrane協作網推薦的非隨機對照試驗質量評價量表進行。質量評價的項目包括研究基線相似性、診斷標準、分組方法、病例納入情況及混雜因素的控制,每個項目為0~2分,記分為0~10分,1~5分為低質量研究,6~10分為高質量研究。納入研究的特征見表1。
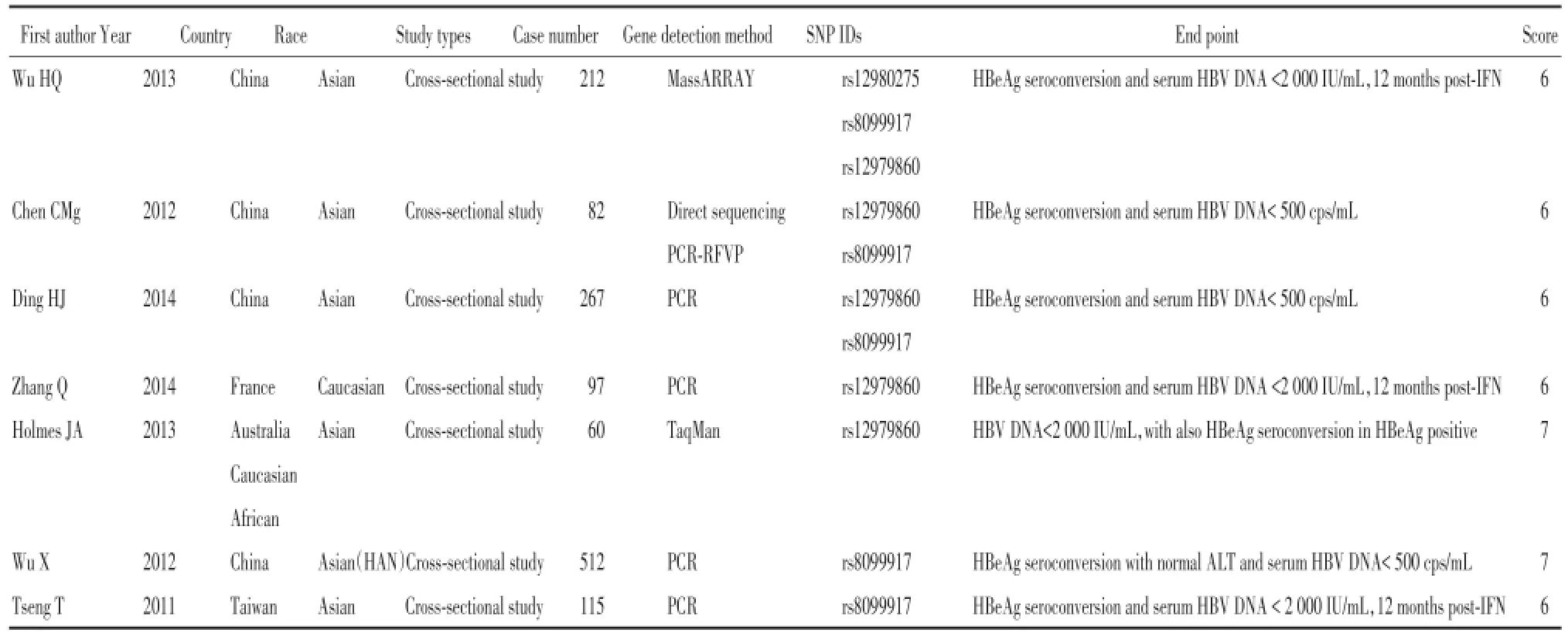
表1 納入研究的基本特征Tab.1 General characteristics of the included studies
2.2 Meta分析結果
2.2.1 rs8099917基因多態性與HBeAg陽性的慢性乙型肝炎患者應用干擾素病毒學應答的相關性:在納入的7篇文獻中,有5篇是針對rs8099917位點,異質性結果提示各研究間存在異質性(I2=84%)。應用隨機效應模型進行分析,與rs8099917TG/GG等位基因相比,rs8099917TT等位基因對于HBeAg陽性的慢性乙型肝炎患者應用干擾素獲得持續病毒應答無明顯差異(OR=0.46,95%CI 0.14~1.52,P= 0.20),見圖1。
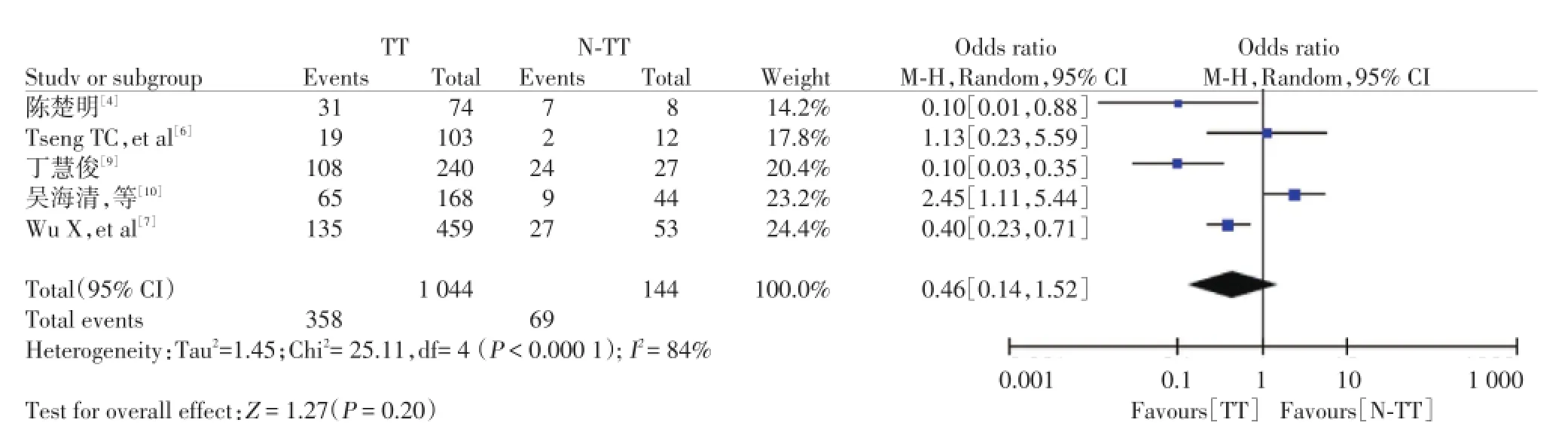
圖1 rs8099917基因多態性與HBeAg陽性的慢性乙型肝炎患者應用干擾素病毒學應答的相關性Fig.1 The association between the polymorphism in rs8099917gene and the interferon virological response in HBeAg-positive chronic hepatitis B
2.2.2 rs12979860基因多態性與HBeAg陽性的慢性乙型肝炎患者應用干擾素病毒學應答的相關性:對納入文獻中涉及rs12979860的5篇文獻進行異質性檢驗后提示各研究存在異質性(I2=65%),應用隨機效應模型進行分析后得出結論:rs12979860CC與CT/TT等位基因相比對于病毒學應答的發生沒有差異(OR=0.88,95%CI 0.41~1.91,P=0.75),見圖2。
2.3 發表偏倚評估
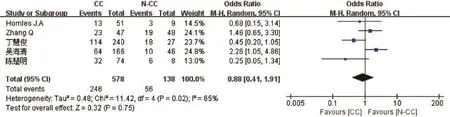
圖2 rs12979860基因多態性與HBeAg陽性的慢性乙型肝炎患者應用干擾素病毒學應答的相關性Fig.2 Association between the polymorphism in rs12979860 gene and the interferon virological response in HBeAg-positive chronic hepatitis B
觀察納入Meta分析的各組文獻漏斗圖發現,漏斗圖對稱性較好,提示相關研究發表偏倚較小。采用Begg法分別對各相關研究對稱性進行檢驗,rs8099917組文獻及rs12979860組文獻P值分別為0.462、0.221,見圖3、4。
3 討論
人IL-28B基因最早由Zymo Genetics公司于2003年發現,位于染色體19q13.13的ACO11445.6基因群上,屬于Ⅲ行干擾素家族,編碼IFN-λ3[11]。2009年9月,美國杜克大學人類基因組變異中心的Ge等[12]研究人員首次報道了患者IL-28B基因多態性與HCV清除之間的關系。此后大量研究表明IL-28B基因多態性不僅可以作為HCV病毒清除及HCV標準療法與三聯療法治療效果的預測指標,而且可能在HBV感染及治療領域存在重大價值。

圖3 rs8099917組文獻發表偏倚評價Fig.3 Publication bias of the rs8099917 group
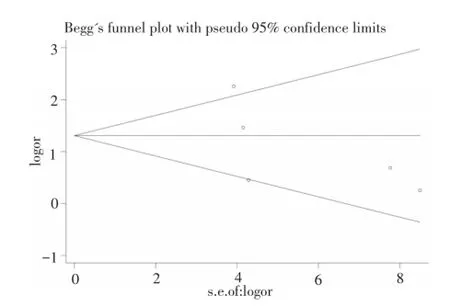
圖4 rs12979860組文獻發表偏倚評價Fig.4 Publication bias of the rs12979860 group
本文共納入文獻7篇,結果顯示IL-28B(rs12979860,rs8099917)與HBeAg陽性的慢性乙肝患者對干擾素的反應無明顯相關性。這一結果提示IL-28B(rs12979860,rs8099917)基因多態性對慢性乙肝患者干擾素應答無預測作用,不能以此為依據給予患者個體化治療。本次meta分析過程中文獻檢索盡量保證全面,嚴格遵循納入及排除標準,且各研究中等位基因的檢測均要求準確,極大程度地減少了各種偏倚的發生。但由于部分國外文獻所觀察的指標與國內文獻存在差異,仍存在原始文獻數據獲取失敗所造成的偏倚。同時各實驗室之間的檢測水平及檢測儀器的不同可能造成研究內偏倚。本研究由于樣本量較小,納入文獻數目有限,可能存在此meta分析結果的局限性。另外,本研究只針對IL-28B的2個位點進行分析,并未對其他位點(如rs10853728、rs12980275、rs4803219等)進行分析,因而存在一定局限性。
發表偏倚對于meta分析結果的真實性和可靠性有很大的影響,故現在有很多種方法來進行發表偏倚的檢驗,例如Egger’s檢驗,Begg’s檢驗等。由于本研究納入文獻數目較少,上述檢驗方法都存在局限性。有文獻表明[13]當meta分析納入研究的樣本含量明顯呈非正態分布時,Begg’s檢驗比Egger’s檢驗的結果更穩健,更加接近真實情況。故本研究綜合考慮實際情況,選用Begg’s檢驗進行發表偏倚的檢驗。通過結果分析,以α=0.05檢驗,P>0.05,在一定程度上可以認為無明顯發表偏倚。
綜上所述,IL-28B(rs12979860,rs8099917)基因多態性與HBeAg陽性的慢性乙肝患者應用干擾素病毒學應答無明顯相關性。由于本次納入文獻文獻數量有限,存在一定的局限性。故需要納入更多設計嚴格、樣本量大,多地區、多中心的研究,以獲得更明確的結論。
[1]陳建新.關于對乙型肝炎流行病學的分析研究[J].中國衛生產業,2012(21):171.
[2]徐輝,郭麗琳,何伶俐,等.宿主白介素28B基因多態性與慢性丙型肝炎抗病毒療效的研究分析[J].四川大學學報(醫學版),2012(6):855-859.
[3]許剛,任浩.IL-28B基因多態性在丙型肝炎患者治療中的作用[J].世界華人消化雜志,2011(7):661-666.
[4]陳楚明.IL28B基因多態性與慢性乙型肝炎患者對干擾素應答的關系[D].南方醫科大學,2012.
[5]Holmes JA,Nguyen T,Ratnam D,et al.IL28B genotype is not useful for predicting treatment outcome in Asian chronic hepatitis B patients treated with pegylated interferon-alpha[J].J Gastroenterol Hepatol,2013,28(5):861-866.
[6]Tseng TC,Yu ML,Liu CJ,et al.Effect of host and viral factors on hepatitis B e antigen-positive chronic hepatitis B patients receiving pegylated interferon-alpha-2a therapy[J].Antivir Ther,2011,16(5):629-637.
[7]Wu X,Xin Z,Zhu X,et al.Evaluation of susceptibility locus for response to interferon-alpha based therapy in chronic hepatitis B patients in Chinese[J].Antiviral Res,2012,93(2):297-300.
[8]Zhang Q,Lapalus M,Asselah T,et al.IFNL3(IL28B)polymorphism does not predict long-term response to interferon therapy in HBeAg-positive chronic hepatitis B patients[J].J Viral Hepat,2014,21(7):525-532.
[9]丁慧俊.IL-28B單核苷酸基因多態性與CHB干擾素療效的相關性[J].中國醫藥科學,2014(17):9-11.
[10]吳海清,趙鋼德,錢方興,等.IL28B基因多態性與HBeAg陽性慢性乙型肝炎患者聚乙二醇化干擾素α應答的關系[J].肝臟,2013(6):359-364.
[11]Sheppard P,Kindsvogel W,Xu W,et al.IL-28,IL-29 and their class II cytokine receptor IL-28R[J].Nat Immunol,2003,4(1):63-68.
[12]Ge D,Fellay J,Thompson AJ,et al.Genetic variation in IL28B predicts hepatitis C treatment-induced viral clearance[J].Nature,2009,461(7262):399-401.
[13]石修權,王增珍.Egger’s test與Begg’s test的功效差異比較與原因分析[J].華中科技大學學報(醫學版),2009(01):91-93.
(編輯 武玉欣)
Meta Analysisofthe Association ofPolymorphism in IL-28B Gene and VirologicalResponse to Interferon in HBeAg-positive Chronic Hepatitis B
TENG Wei,CUIWei,LIUPei
(DepartmentofInfectious Disease,The FirstHospital,China MedicalUniversity,Shenyang 110001,China)
Objective To explore the association between the polymorphism in IL-28B gene and the interferon virologicalresponse in HBeAg-positive chronic hepatitis B patients.MethodsA literature search was performed on PubMed,Web of Science,China Bio Medicine(CBM)and Wan-Fang database.The references was screened with the inclusion and exclusion criteria,and then data were extracted and methodological quality of the studies was judged.Statistical analysis was carried out with RevMan 5.3 and STATA 11.0.ResultsTotally 7 publications were recruited for the study,including 1 345 patients.The meta-analysis showed that there was no significant difference of interferon response between HBeAg-positive chronic hepatitis B patients with rs8099917TG/GG alleles and rs8099917TT alleles(P=0.20).There was no statistical difference between Rs12979860CC and CT/TT allele for the sustained virological response(P=0.75).ConclusionOur current meta-analysis suggests that there was no correlation of rs8099917,rs12979860 polymorphism in IL-28B with the sustained virological response to interferon in HBeAg-positive chronic hepatitis b.
hepatitis B;antiviral therapy;IL-28B;gene polymorphism;meta analysis
R512.6
A
0258-4646(2015)08-0749-04
滕巍(1987-),女,醫師,碩士研究生.
劉沛,E-mail:syliupei2013@163.com
2015-03-18
網絡出版時間:

