恩替卡韋聯合胸腺肽α1治療慢性乙型肝炎療效的Meta分析
渠亞超,田 洲,鮑旭麗,呂艷偉,閭 軍
(1.首都醫科大學附屬北京佑安醫院,北京 100069;2.北京市創傷骨科研究所,北京 100035)
論 著
恩替卡韋聯合胸腺肽α1治療慢性乙型肝炎療效的Meta分析
渠亞超1,田 洲1,鮑旭麗1,呂艷偉2,閭 軍1
(1.首都醫科大學附屬北京佑安醫院,北京 100069;2.北京市創傷骨科研究所,北京 100035)

目的 評價恩替卡韋聯合胸腺肽α1治療慢性乙型肝炎的療效。方法 檢索2005—2014年4月PubMed、Cochrane Library、OVID、SpringerLink、中國知網、中國生物醫學文獻數據庫、萬方數據醫學網及維普網,根據納入標準、排除標準,對入選的10篇隨機對照試驗(RCT)的研究結果采用RevMan5.2軟件進行分析。結果 與對照組相比,實驗組能更顯著地提高ALT復常率、HBV DNA轉陰率、HBeAg轉陰率和HBeAg血清轉換率,相對危險度(RR)分別為1.13[95%CI(1.06,1.21),Z=3.61,P=0.000 3],1.19[95%CI(1.09,1.30),Z=3.83,P=0.000 1]、2.25[95%CI(1.52,3.33),Z=4.04,P<0.0001]和2.31[95% CI (1.83,2.92),Z=7.06,P<0.000 01];且無明顯不良反應。結論 恩替卡韋聯合胸腺肽α1治療慢性乙型肝炎能有效增加恩替卡韋單藥抗病毒療效,但確切療效尚需更多臨床研究加以證實。
慢性乙型肝炎;恩替卡韋;胸腺肽α1; Meta分析
慢性乙型肝炎(慢乙肝)是目前全世界范圍內的難治疾病之一。目前使用任何一種藥物都無法控制或消滅慢性乙型肝炎病毒(HBV)感染,治療目的主要是防止或減少肝硬化、肝細胞癌及肝臟相關性死亡的發生。近年研究表明,抑制病毒的持續復制可使疾病進展的危險性減小[1-2],但長期單獨口服抗病毒藥物所引發的耐藥問題逐漸引起人們重視。將不同核苷(酸)類似物聯合應用可以降低耐藥的發生,但是早期相關研究結果并不令人滿意[3]。由于HBV感染所造成的損害由免疫反應引起,人們逐漸選擇將抗病毒藥物與免疫調節劑聯合應用來改善慢乙肝的臨床治療終點。有研究證實,將口服抗病毒藥與干擾素α(IFN-α)聯用可導致更高的HBeAg血清學轉換率,且可達到更持久的HBV-DNA抑制效果[4]。但INF注射面臨患者耐受性差及肝硬化失代償患者不適用等局限性[5]。胸腺肽α1是一種從胸腺組織中提取的28個氨基酸的多肽[6],是一種重要的免疫遞質,可以提高HBV病毒清除率。體外實驗證實,胸腺肽α1可以影響T細胞的成熟和抗原識別,可以刺激IFN和細胞內因子的生成,影響自然殺傷細胞介導的毒性細胞的活性[7-8]。目前涉及胸腺肽α1的臨床隨機對照實驗常樣本量較小,且結果不總是一致。雖然與IFN相比,胸腺肽的不良反應要溫和,但它的臨床效果仍然無法確定[9-10]。目前已有IFN聯合核苷類似物與單獨使用胸腺肽α1的療效報道。然而,將恩替卡韋與胸腺肽α1聯用的報道數據較少,因此,聯用比單獨使用恩替卡韋是否有更佳的治療效果值得研究。本研究收集當前使用恩替卡韋的上述隨機對照試驗,旨在客觀評價2種治療方案的臨床療效及應用價值。
1 研究資料
1.1 檢索策略 搜集所有采用恩替卡韋聯合胸腺肽α1與恩替卡韋對照治療慢乙肝的隨機對照試驗(randomized controlled trial,RCT)資料,2位評價者單獨檢索并交叉核對。檢索PubMed、Cochrane Library、OVID、SpringerLink、中國知網、中國生物醫學文獻數據庫(CBM-disk)、萬方數據醫學網及維普網, 時間控制在2005年恩替卡韋上市至2014年4月, 檢索詞為“HBV、hepatitis B、CHB、entecavir、ETV、thymosin、恩替卡韋、胸腺肽α1、病毒性肝炎、隨機對照試驗”。查閱所有檢出文獻的參考文獻作為補充。
1.2 納入標準 ①研究類型: RCT,無論是否采用盲法。②研究對象: HBeAg 陽性或HBeAg陰性且未應用過核苷類似物治療的慢乙肝患者,診斷符合《慢性乙型肝炎防治指南》[11]標準。男女不限,年齡16~70歲。篩選前HBsAg陽性至少6個月,篩選時ALT水平升高(≥1.3~10倍ULN),TBil≤42.75 μmol/L,HBV DNA≥104拷貝/mL。③干預措施:實驗組接受恩替卡韋 0.5 mg,1次/d口服,胸腺肽α1 1.6 mg,皮下注射,每周2次,治療48周;對照組單用恩替卡韋治療48周。④觀察指標:血清ALT復常率、HBV DNA陰轉率、HBeAg陰轉率、血清HBeAg/抗-HBe轉換率、纖維化指標、不良反應發生率。
1.3 排除標準 ①同時感染HIV、HCV、HDV者;②其他肝病, 如酒精性、自身免疫性、膽汁淤積性肝病或肝癌患者。
1.4 文獻篩選、資料提取和質量評價 2名作者獨立進行文獻篩選、數據提取、質量評價,如遇分歧討論決定或請第3位研究者裁決。文獻質量評價參照Jadad 量表,主要從受試者分組是否真正隨機、研究過程中是否使用盲法、對失訪者是否記錄等對入選文獻進行質量評價。Jadad積分≥3分為高質量研究。
1.5 統計學方法 對所有收集的資料采用Cochrane協作網RevMan 5.2軟件進行Meta分析。計數資料采用相對危險度(RR)為療效分析統計量;各效應量均以95%CI表示。為判斷聯合各試驗進行分析的合理性,采用卡方檢驗進行各試驗間的異質性檢驗。如同質性好(P>0.10,I2≤50%)則采用固定效應模型進行Meta分析;若同質性不好(P≤0.10,I2>50%)則分析產生異質性的原因,確定是否能采用隨機效應模型進行Meta分析。異質性可能源于低質量研究,進一步做敏感性分析。采用漏斗圖分析可能的發表偏倚。P<0.05為差異有統計學意義。
2 結 果
2.1 文獻檢索結果及納入研究特征 初檢共獲得93篇文獻,其中中國知網28篇、CBM 20篇、萬方26篇、維普網19篇。閱讀文題排除相同和無關的文獻后,初篩出15篇。進一步閱讀摘要和全文,排除5篇,最終納入10篇文獻[12-21],其中1篇[18]Jadad積分為5分,1篇[16]Jadad積分為3分,8篇[12-15,17-18,20-21]Jadad積分為2分。共計1 026例患者,其中實驗組503例,對照組523例。具體檢索策略見圖1,各納入研究的基本特征見表1。
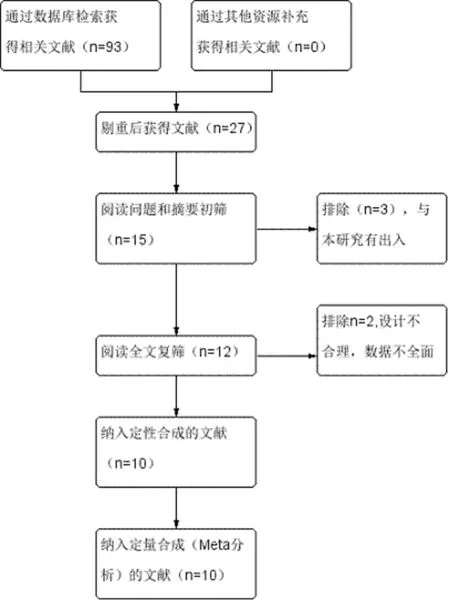
圖1 文獻篩選流程及結果

表1 納入研究的一般特征
注:①為血清ALT復常率;②為血清HBV DNA陰轉率;③為血清HBeAg陰轉率;④為血清HBeAg/抗-HBe血清學轉換率;⑤為不良反應;⑥為纖維化指標。
2.2 各觀察指標結果
2.2.1 血清ALT復常率 有8個研究[12-14,17-21]報道了治療48周時血清ALT復常率。研究結束時,實現ALT復常的共619例,其中實驗組321例,對照組298例。各研究間無統計學異質性(P=0.33,I2=13%),故采用固定效應模型進行合并分析,結果表明2組差異有統計學意義[RR=1.13,95% CI(1.06,1.21),Z=3.61,P=0.000 3],見圖2。倒漏斗圖顯示8項研究之間無明顯發表偏倚,見圖3。

圖2 2組血清ALT復常率比較的Meta分析
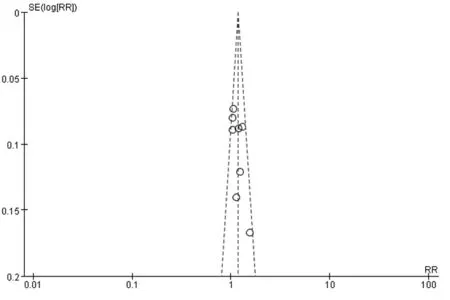
圖3 2組血清ALT復常率比較的漏斗圖
2.2.2 HBV DNA陰轉率 有10個研究[12-21]報道了治療48周時HBV DNA陰轉率。治療結束時實現HBV DNA轉陰(血清PCR法檢測HBV DNA<500拷貝/mL)共792例,其中實驗組428例,對照組364例。各研究間有統計學異質性(P=0.05,I2=48%),采用隨機效應模型進行合并分析,結果表明實驗組HBV DNA陰轉率明顯高于對照組[RR=1.19,95%CI(1.09, 1.30),Z=3.83,P=0.000 1],見圖4。去除1篇[17]進行敏感性分析,結果顯示2組HBV DNA陰轉率仍然有統計學意義[RR=1.17,95%CI(1.07,1.27)P=0.000 3],說明該組分析穩定性較好。
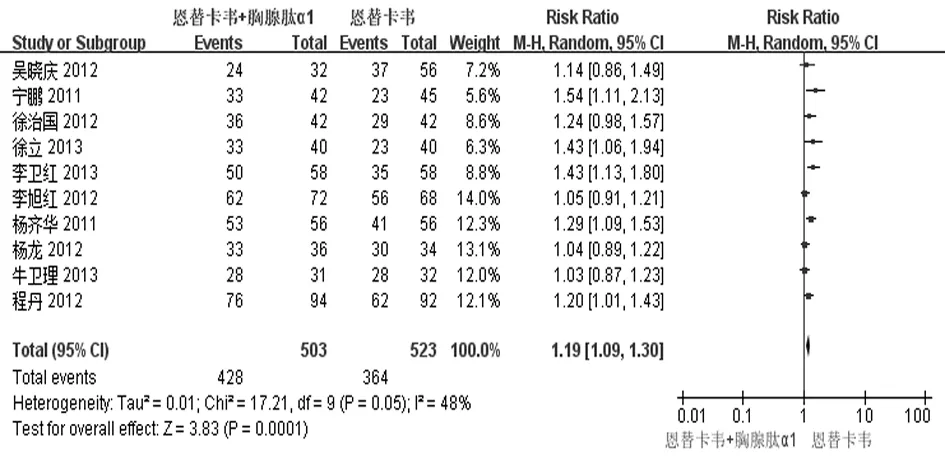
圖4 2組血清HBV DNA陰轉率比較的Meta分析
2.2.3 血清HBeAg陰轉率 有6個研究[13-15,18-19,21]報道了治療48周時血清HBeAg陰轉率。治療結束時實現血清HBeAg陰轉的共238例,其中實驗組166例,對照組72例。各研究間存在異質性(P=0.03,I2=59%),故采用隨機效應模型進行合并分析,結果表明2組差異有統計學意義[RR=2.25,95%CI(1.52,3.33),Z=4.04,P<0.000 1],見圖5。去除1篇[19]進行敏感性分析,結果顯示2組血清HBeAg陰轉率仍然有統計學意義[RR=1.95,95%CI(1.54,2.46),P<0.00001],說明該組分析穩定性較好,見圖6。倒漏斗圖顯示5項研究之間無明顯發表偏倚,見圖7。
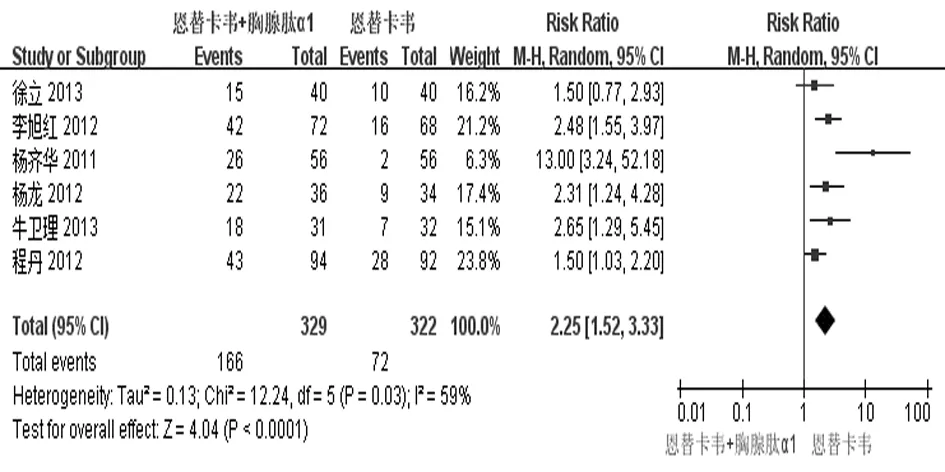
圖5 2組血清HBeAg陰轉率比較的Meta分析

圖6 2組血清HBeAg陰轉率比較敏感性分析

圖7 2組血清HBeAg陰轉率比較漏斗圖
2.2.4 血清HBeAg/抗-HBe轉換率 有10個研究[12-21]報道了治療48周時血清HBeAg/抗-HBe轉換率。治療結束時,實現血清HBeAg/抗-HBe轉換的共261例,其中實驗組180例,對照組81例。各研究間無統計學異質性(P=0.42,I2=2%),故采用固定效應模型進行合并分析,結果表明2組差異有統計學意義[RR=2.31,95% CI(1.83,2.92),Z=7.06,P<0.000 01],見圖8。倒漏斗圖顯示10項研究之間無明顯發表偏倚,見圖9。
2.2.5 不良反應發生率 僅有3項研究[12-13,18]報道治療過程中出現頭痛、疲勞、眩暈、惡心等不良反應,發生率均<6%,2組間比較均無統計學意義。由于發生率低,無法統計2組之間差異。
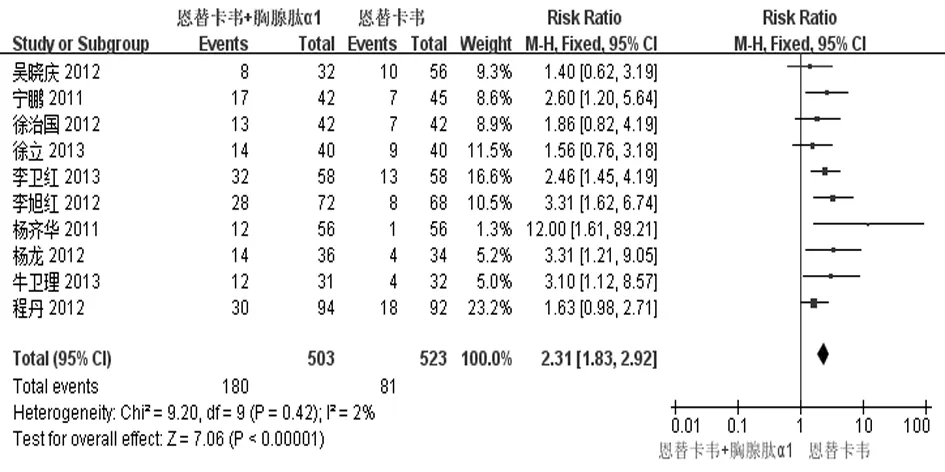
圖8 2組血清HBeAg/抗-HBe血清學轉換率比較的Meta分析
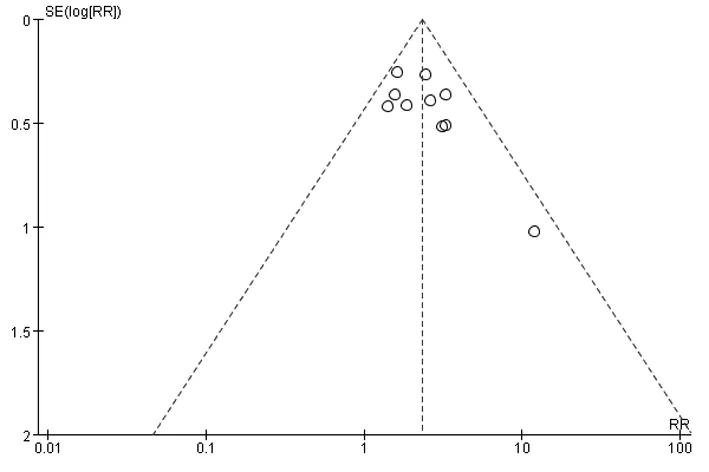
圖9 2組血清HBeAg/抗-HBe血清學轉換率比較漏斗圖
2.2.6 其他 僅有寧鵬[17]對2組治療前后患者的血清LN、HA、CⅣ、PCⅢ,用Fibroscan對肝纖維化程度進行定量檢測。經過48周,治療結果顯示對于肝纖維化的改善,聯合用藥組優于對照組。
3 討 論
恩替卡韋是2005年3月美國FDA批準上市的藥物,適用于有活動性復制和血清學或肝組織學炎癥指標的成年慢乙肝患者。恩替卡韋是鳥嘌呤核苷類藥物,能有效選擇性抑制HBV復制,阻斷復制的3個環節:抑制HBV多聚酶的啟動,抑制前基因組mRNA逆轉錄負鏈的形成,抑制DNA依賴的DNA合成,因此恩替卡韋抗病毒活性強,是現有國內市場上核苷類似物中抗病毒活性最強的化合物[22-23]。胸腺肽α1是胸腺提取物的主要活性成分,它與恩替卡韋有一定的協同作用,恩替卡韋可以快速抑制HBV的復制,胸腺肽α1則通過刺激機體細胞免疫,抑制HBV前基因組RNA的轉錄和反轉錄,有利于清除低水平復制的HBV,彌補恩替卡韋不能直接清除肝細胞核內HBV的不足,達到控制HBV感染、減少疾病復發的目的[22]。
目前,對于非肝硬化的肝病患者,干擾素、拉米夫定、阿德福韋酯和恩替卡韋都可以作為一線治療用藥,但是仍有許多問題,如IFN-α治愈率低且耐受性差;拉米夫定長期治療容易發生耐藥YMDD突變[24];單用核苷類似物治療還存在停藥后持續應答率低等局限性[25]。由于目前可選擇的藥物有限,導致人們開始研究新型藥物和新的聯合治療方案。鑒于HBV和HIV治療之間有相似性,根據治療HIV經驗可知,使用任何單一的藥物來永久控制或消除慢性HBV感染無法實現[26]。Economou等[27]與單獨使用拉米夫定相比,拉米夫定和聯合干擾素治療12個月可以防止或延緩YMDD變異的發生及病毒突破。胸腺肽α1與拉米夫定或干擾素聯用可增強療效[10]。Zhang等[28]已證實,胸腺肽α1與拉米夫定聯用可以提高ALT復常率、病毒學反應率及HBeAg血清學轉換率。本研究結果顯示,恩替卡韋和胸腺肽α1聯用可以提高血清ALT復常率、血清HBV DNA陰轉率、HBeAg陰轉率及HBeAg/抗-HBe轉換率,且無明顯不良反應,但由于胸腺肽α1長期用藥價格相對昂貴,且需要進行注射給藥,不利于經常出差或長時間在外地人員使用,存在患者長期應用時依從性欠佳等問題。另外,本分析收錄的10篇文獻均為國內研究,限制了結論的質量及科學性。因此,此種聯合治療方案的效果還需要大規模嚴謹的臨床隨機對照試驗加以驗證。
[1] Chen CF,Lee WC,Yang HI,et al.Changes in serum levels of HBV DNA and alanine aminotransferase determine risk for hepatocellular carcinoma[J].Gastroenterology,2011,141(4):1240-1248
[2] Chen CJ,Yang HI.Natural history of chronic hepatitis B REVEALed[J].J Gastroenterol Hepatol,2011,26(4):628-638
[3] Perrillo RP.Current treatment of chronic hepatitis B: benefits and limitations[J].Semin Liver Dis,2005,25 (Suppl1):20-28
[4] Santantonio TA,Fasano M.Chronic hepatitis B:Advances in treatment[J].World J Hepatol,2014,6(5):284-292
[5] Liaw YF,Kao JH,Piratvisuth T,et al.Asian-Pacific consensus statement on the management of chronic hepatitis B: a 2012 update[J].Hepatology international,2012,6(3):531-561
[6] Goldstein AL.From lab to bedside: emerging clinical applications of thymosin alpha 1[J].Expert Opin Biol Ther,2009,9(5):593-608
[7] Garaci E.Thymosin alpha1: a historical overview[J].Ann N Y Acad Sci,2007,9(1112):14-20
[8] Sugahara S,Ichida T,Yamagiwa S,et al.Thymosin-alpha1 increases intrahepatic NKT cells and CTLs in patients with chronic hepatitis B[J].Hepatol Res,2002,24(4):346-354
[9] Chien RN,Lin CY,Yeh CT,et al.Hepatitis B virus genotype B is associated with better response to thymosin alpha1 therapy than genotype C[J].J Viral Hepat,2006,13(12):845-850
[10] Lee HW,Lee JI,Um SH,et al.Combination therapy of thymosin alpha-1 and lamivudine for HBeAg positive chronic hepatitis B: A prospective randomized, comparative pilot study[J].J Gastroenterol Hepatol,2008,23(5):729-735
[11] 賈繼東,李蘭娟.慢性乙型肝炎防治指南(2010年版)[J].臨床肝膽病雜志,2011,27(1):113-128
[12] 李衛紅.恩替卡韋聯合胸腺肽α1治療HBeAg陽性慢性乙型肝炎116例療效分析[J].青海醫藥雜志,2013,43(5):18-19
[13] 徐立.胸腺肽α1對恩替卡韋治療HBeAg陽性慢性乙型肝炎療效的影響[J].中國當代醫藥,2013,20(11):40-41
[14]楊龍,蔣雪花,陳芳妹.恩替卡韋聯合胸腺肽α1治療慢性乙型肝炎臨床研究[J].肝臟,2012,17(6):445-446
[15] 程丹,劉文濤,黃新造.恩替卡韋聯合α1胸腺肽治療HBeAg陽性慢性乙型肝炎療效及安全性分析[J].實用肝臟病雜志,2012,15(4):350-351
[16] 徐治國,梁艷.恩替卡韋聯合胸腺肽α1治療HBeAg陽性慢性乙型肝炎的療效分析[J].中國醫藥指南,2012,10(29):264-266
[17] 寧鵬.恩替卡韋聯合胸腺肽α1治療慢性肝炎療效研究[D].青島:青島大學,2011
[18] 牛衛理.恩替卡韋聯合胸腺肽α1治療慢性乙型肝炎的臨床效果分析[J].中國當代醫藥,2013,20(27):58-59
[19] 楊齊華,鄭拓,童楚盛.恩替卡韋聯合胸腺肽治療HBeAg陽性的慢性乙型肝炎臨床觀察[J].海峽藥學,2011,23(5):88-90
[20] 吳曉慶,萬紅.恩替卡韋聯合胸腺肽α1治療慢性乙型肝炎近期療效觀察[J].實用肝臟病雜志,2012,15(6):568-569
[21] 李旭紅,賴江瓊,李奕鑫,等.恩替卡韋片聯合胸腺肽α1治療HBeAg陽性乙型肝炎療效分析[J].傳染病信息,2012,25(4):235-236
[22] 趙艷娟,高歌.干擾素α2b與苦參素、胸腺肽α1聯合序貫治療慢性乙型肝炎的實驗研究[J].臨床肝膽病雜志,2005,21(6):341-342
[23] 楊松.2009年恩替卡韋臨床應用專家共識[J/CD].中華實驗和臨床感染病雜志:電子版,2009,3(2):42-45
[24] Paik YH,Han KH,Hong SP,et al.The clinical impact of early detection of the YMDD mutant on the outcomes of long-term lamivudine therapy in patients with chronic hepatitis B[J].Antivir Ther,2006,11(4):447-455
[25] 謝雯,閆杰,趙紅.慢性乙型肝炎聯合抗病毒治療專家共識[J/CD].中華實驗和臨床感染病雜志:電子版,2011,13(2):224-233
[26] Locarnini S.Molecular virology and the development of resistant mutants: implications for therapy[J].Semin Liver Dis,2005,25 (Suppl 1):9-19
[27] Economou M,Manolakopoulos S,Trikalinos TA,et al.Interferon-alpha plus lamivudine vs lamivudine reduces breakthroughs, but does not affect sustained response in HBeAg negative chronic hepatitis B[J].World J Gastroenterol,2005,11(37):5882-5887
[28] Zhang YY,Chen EQ,Yang J,et al.Treatment with lamivudine versus lamivudine and thymosin alpha-1 for e antigen-positive chronic hepatitis B patients:a meta-analysis[J].Virol J,2009,25(6):63
Entecavir versus entecavir-thymosin alpha-1 combination therapy for chronic hepatitis B: a Meta analysis
QU Yachao1, TIAN Zhou1, BAO Xuli1, LYU Yanwei2, LYU Jun1
(1.Beijing Youan Hospital of Capital Medical University, Beijing 100069, China; 2.Beijing Institute of Trauma Department of Orthopedics, Beijing 100035, China)
Objective It is to value the effect of entecavir-thymosin alpha-1 combination therapy for chronic hepatitis B.Methods The papers were searched in the database of the PubMed, Cochrane Library, OVID, SpringerLink, CNKI, the Chinese Biomedical Database (CBM), Wanfangdata and CQVIP according to inclusion criteria and exclusion criteria from 2005 to April 2014.The findings of the selected ten randomized controlled trials (RCT) were analyzed by RevMan 5.2 Software.Results Compared with the control group, the ALT normalization rate, HBV DNA negative rate, HBeAg negative rate and HBeAg seroconversion rate of experimental group were significantly improved: RR were 1.13 [95%CI (1.06, 1.21),Z=3.61,P=0.000 3〗, 1.19 [95%CI (1.09, 1.30),Z=3.83,P=0.000 1], 2.25 [95%CI (1.52,3.33),Z=4.04,P<0.000 1] and 2.31 [95%CI (1.83, 2.92),Z=7.06,P<0.000 01].The injection of thymosin alpha-1 was no significant adverse events.Conclusion Entecavir-thymosin alpha-1 combination therapy is more effective in the HBV DNA reduction, increase of serum HBeAg negative rate, conversion rate and ALT normalization rate and without increasing drug adverse reactions compared with entecavir.More RCTs of high quality and large scale are required to verify this conclusion.
chronic hepatitis B; entecavir; thymosin alpha-1; Meta analysis
渠亞超,女,碩士研究生,主要從事肝病方面的研究。
閭軍,E-mail:lujun98@ccmu.edu.cn
北京市衛生系統高層次衛生技術人才培訓資助項目(2011-2-20);“十二五”重大科技專項基金資助項目(2014ZX10002002-001-002)
10.3969/j.issn.1008-8849.2015.09.001
R0512.62
A
1008-8849(2015)09-0913-05
2014-08-05

