HPLC-UV法測定人血漿及尿中多尼培南
秦永平梅亞君章 麗毛 銳南 峰向 瑾梁茂植余 勤
(1.四川大學華西醫院臨床藥理研究室,四川 成都 610041;2.成都中醫藥大學藥學院,四川 成都 611137)
HPLC-UV法測定人血漿及尿中多尼培南
秦永平1,梅亞君1,2,章 麗1,毛 銳1,南 峰1,向 瑾1,梁茂植1,余 勤1
(1.四川大學華西醫院臨床藥理研究室,四川 成都 610041;2.成都中醫藥大學藥學院,四川 成都 611137)
建立HPLC-UV法測定人血漿及尿中多尼培南(DP)的質量濃度,用于DP人體藥代動力學研究。采用Ultimate XB-C18(150 mm×4.6 mm×3 μm)色譜柱,血漿及尿樣測定用流動相分別為10 mmol/L醋酸鈉:乙腈:三乙胺(體積比94:6:0.1,冰乙酸調pH為4.51)和8mmol/L醋酸鈉:乙腈:三乙胺(體積比95.5:4.5:0.1,冰乙酸調pH值為4.99),流速均為1mL/min,檢測波長為297nm。血漿樣品經乙睛沉淀蛋白,再用二氯甲烷反洗后取上清液進樣,以美羅培南(MRP)做內標;尿樣直接用水稀釋后進樣,外標法定量。血藥濃度在0.0625~200μg/mL范圍內與峰面積線性關系良好,定量限為0.0625μg/mL,批內精密度在1.0%~6.0%之間,批間精密度在3.0%~6.7%之間,方法回收率在92.4%~104.5%之間,預處理回收率在91.2%~103.8%之間。尿藥濃度在0.625~4 800 μg/mL范圍內與峰面積線性關系良好,定量限為0.625μg/mL,批內精密度在0.7%~4.0%之間,批間精密度在1.1%~5.3%之間,方法回收率在94.1%~106.7%之間。該方法具有簡便、靈敏、準確等特點,適用于人血漿及尿中多尼培南質量濃度的測定。
多尼培南;高效液相色譜法;血藥濃度;尿藥濃度
0 引 言
多尼培南是一種新的1β甲基碳青霉烯類抗生素[1],其抗菌譜廣、抗菌活性強,對各種需氧、厭氧G+及G-菌均有很強的抗菌活性[2]。Sutherland C和Iked K等[3-4]分別采用固相萃取法和超濾法進行樣品預處理,采用HPLC-UV法對DP的血藥濃度進行測定。國內有多尼培南的臨床藥代動力學研究報道[5-6],但無多尼培南尿液濃度的相關測定。本實驗建立了人血漿及尿液中多尼培南濃度的HPLC-UV測定方法。
1 實驗部分
1.1 儀器與色譜條件
日本SHIMADZU公司2010-HPLC型高效液相色譜儀,采用Ultimate XB-C18分析柱(150 mm× 4.6mm×3μm),柱溫35℃,紫外檢測波長297nm。血漿和尿液樣品用流動相分別為10mmol/L醋酸鈉:乙腈:三乙胺(體積比94:6:0.1,冰乙酸調pH為4.51)和8mmol/L醋酸鈉:乙腈:三乙胺(體積比95.5:4.5:0.1,冰乙酸調pH為4.99),流量均為1mL/min。
1.2 藥品與試劑
多尼培南(Doripenem,DP)對照品(成都地奧九泓制藥廠,含量:91.79%,批號:20131001);美羅培南(Meropenem,MRP)對照品(中國藥品生物制品檢定所,含量:87.0%,批號:30506-200702)。乙腈、甲醇、三乙胺均為色譜純試劑;其余試劑為分析純;實驗用水由美國Millipore公司Milli-Q型超純水器制備所得。
1.3 溶液配制
1)血漿樣品測定用儲備液。精密稱取DP對照品21.79 mg(相當于DP20 mg)于25 mL容量瓶中,用純水溶解并定容至刻度,即得血漿樣品測定用DP儲備液(800μg/mL),分裝于EP管中-80℃冰箱保存。臨用前,用水稀釋得DP血樣測定標準系列工作液。
2)尿液樣品測定用儲備液。稱取DP對照品130.7mg(相當于DP120mg)于25mL的容量瓶中,用純水溶解并定容至刻度,即得尿液樣品測定用DP儲備液(4 800 μg/mL),分裝于EP管中-80℃冰箱保存。臨用前,用水稀釋得DP尿樣測定標準系列工作液。
3)內標(IS)儲備液及工作液。精密稱取MRP對照品22.99 mg(相當于MRP20 mg)于50 mL的容量瓶中,用甲醇溶解并定容至刻度即得MRP儲備液(400μg/mL),分裝于EP管中-80℃冰箱保存。臨用前,用水稀釋得MRP內標工作液(40μg/mL)。
1.4 樣品預處理
1)血漿樣品。取待測血漿樣品200μL,加入純水50 μL、加入內標工作液50 μL,混勻,再加入乙腈600μL,充分混合后離心10min(13000r/min,8℃);傾倒上清液于圓底管,加入2mL二氯甲烷反洗,渦旋5min,離心7min(3000r/min,8℃),取20μL上清液進樣。
2)尿液樣品。取待測尿液樣品100 μL,加入純水900μL,混勻后離心10 min(13000r/min,8℃),取20μL上清液進樣。
2 方法與結果
2.1 專屬性
空白血漿(6個)、對照品、空白血漿加對照品及血漿樣品色譜圖見圖1,DP(1)與IS(2)保留時間分別為5.3min和8.5min。結果顯示:血漿中的內源性雜質對藥物和內標峰均無干擾。
空白尿樣(6個)、對照品、空白尿樣加對照品及尿液樣品色譜圖見圖2,DP(1)保留時間為8.3 min。結果顯示:尿液中的內源性雜質對藥物峰無干擾。
2.2 線性及最低定量限考察
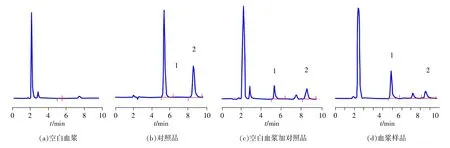
圖1 血漿測定色譜圖

圖2 尿液測定色譜圖
1)血漿。分別取200μL空白血漿9份,空白管補水50μL,其余各管依次加入血樣測定標準系列工作液50μL,使DP血漿質量濃度分別為0.0625,0.125,3.125,12.5,25,50,100,200μg/mL。按1.4項下1)自“加入內標工作液50μL”起操作,進樣20μL。記錄藥物及內標色譜峰面積,以二者峰面積之比(Y)對多尼培南血漿質量濃度(X)進行加權(1/x2)線性回歸,得DP的血漿標準曲線回歸方程:Y=0.090 73X+ 0.006 93(r2=0.999 8),結果顯示多尼培南血漿質量濃度在0.062 5~200 μg/mL范圍內標準曲線線性良好。定量限為0.062 5 μg/mL,測定5次的平均值為0.057 2μg/mL,RSD為9.16%,準確度和精密度均符合相關規定。
2)尿液。取空白尿11份,每份100μL,空白管補水900μL,其余管先依次加入尿液測定標準系列工作液100 μL,使其尿藥濃度分別為:0.625,1.25,5,20,100,400,800,1600,3200,4800μg/mL,再加水800μL,按1.4項下2)混勻離心處理后進樣。記錄藥物色譜峰面積,以峰面積(Y)對尿藥濃度(X)進行加權(1/x2)線性回歸,得DP的尿液標準曲線回歸方程:Y=2359.74X-485.866(r2=0.999 8),結果顯示多尼培南尿液質量濃度在0.625~4 800 μg/mL范圍內標準曲線線性良好。最低定量限為0.625μg/mL,測定5次的平均值為0.643μg/mL,RSD為2.73%,準確度和精密度均符合相關規定。
2.3 方法精密度和回收率
1)血漿樣品。取用空白血漿加DP工作液配成的低(0.125 μg/mL)、中(10 μg/mL)、高(160 μg/mL)3個質量濃度血漿樣品各5份,按1.4項下1)自“加入內標工作液50μL”起同法操作。以多尼培南與內標峰面積之比在當日血漿標準曲線上求出多尼培南質量濃度,于1d內連續測定5次,測得DP平均血藥濃度分別為0.121,10.277,152.533 μg/mL,對應的批內精密度RSD分別為5.98%,1.03%和2.58%。血漿方法回收率分別為(97.02±5.81)%、(102.77±1.06)%和(95.33±2.46)%。于7d內測定3批,每批5次,測得DP平均血藥濃度分別為0.121,10.673,158.518μg/mL,對應的批間精密度RSD分別為6.66%、2.98%和3.53%。
2)尿液樣品。用空白尿液加DP工作液配成的低(1.875μg/mL)、中(3.75μg/mL)、中高(240μg/mL)、高(3 840 μg/mL)4個質量濃度的尿液樣品各5份,按1.4項下2)處理進樣。以多尼培南峰面積在當日血漿標準曲線上求出多尼培南質量濃度,在1 d內連續測定5次,測得DP平均尿藥濃度分別為1.736,3.760,256.030,3 811.533μg/mL,對應的批內精密度RSD分別為3.99%、4.02%、0.72%和0.91%。方法回收率分別為(94.05±3.756)%、(103.09±5.612)%、(106.68±0.766)%和(99.26±0.902)%。于7d內測定3批,每批5次,測得DP平均尿藥濃度分別為1.699,3.536,254.702,3 811.598μg/mL,對應的批間精密度RSD分別為4.10%、5.25%、1.13%和1.15%。
2.4 血漿預處理回收率
取用空白血漿加DP工作液配成的低(0.125 μg/mL)、中(10 μg/mL)、高(160 μg/mL)3個質量濃度血漿樣品,每個濃度3份,按1.4項下1)自“加入內標工作液50μL”起同法操作,將所得藥物及內標峰面積與相應濃度的工作液直接進樣所得峰面積相比,得血漿樣品預處理平均回收率分別為118.35%、104.53%和101.32%,內標的預處理平均回收率為96.63%。
2.5 樣品穩定性考察
取用空白血漿加DP工作液配成的低(0.125 μg/mL)、中(10μg/mL)、高(160μg/mL)的3個質量濃度的血漿樣品及用空白尿液加DP工作液配成的低(1.875 μg/mL)、中(3.75 μg/mL)、中高(240μg/mL)、高(3 840μg/mL)4個質量濃度的尿液樣品各3份,分別考察-80℃長期放置、反復凍融、室溫放置、處理后樣品在進樣室(8℃)放置及重復進樣穩定性。結果顯示,所有穩定性試驗中實測值與理論值的相對偏差均小于15%。表明血漿樣品在-80℃條件下保存30d,反復凍融3次,室溫放置6h,進樣室放置16h,重復進樣1次均穩定;尿液樣品在-80℃條件下保存34d,反復凍融3次,室溫放置4h,進樣室放置14h、重復進樣2次均穩定。
2.6 尿樣稀釋因子考察
在尿液樣品測定中,有樣品質量濃度超過了標準曲線上限(4800μg/mL)的,進行4倍稀釋因子的考察。取空白尿液加DP對照品配成的尿液樣品(8000μg/mL)0.5mL,加入空白尿樣1.5mL稀釋,充分混勻后按尿液樣品預處理方法處理后進樣。將直接測得的質量濃度乘以4即為換算的實際質量濃度,其測定5次的平均質量濃度為7670.85μg/mL,與配制偏差為4.12%,RSD為0.85%,表明樣品稀釋4倍后測定結果準確可靠。
3 應 用
本文建立的方法已用于12名健康志愿者在3個周期里分別單次靜脈滴注多尼培南低(0.25 g)、中(0.5g)、高(1.0g)劑量的藥動學研究。其低、中、高劑量單次給藥的均值藥時曲線見圖3;尿液中多尼培南平均累積排泄率-時間曲線見圖4(低劑量12例,中劑量9例,高劑量8例)。由圖可知:多尼培南血藥濃度隨劑量增加而相應增加,低、中、高劑量尿中24h累積排泄率在70%以上。
4 討 論
4.1 流動相的選擇

圖3 12名健康受試者單次靜脈注射DP后的均值藥-時曲線
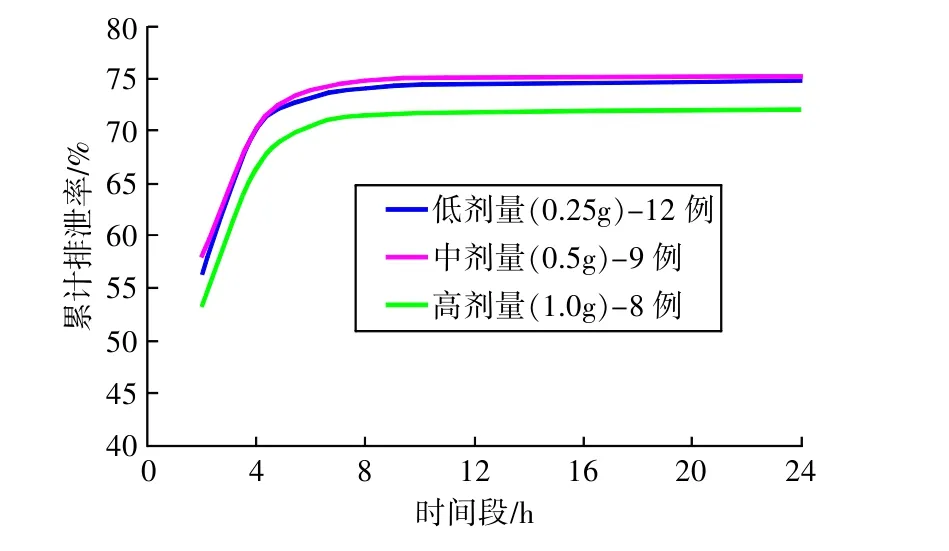
圖4 12名健康受試者單次靜脈注射DP后的均值尿藥累積排泄率曲線
由多尼培南的化學結構可知,多尼培南屬于極性較大的化合物。因此所需乙腈量較少,且乙腈量的微小改變對藥物及內標的保留時間影響很大。同時,pH對血漿和尿液中的雜質出峰也有較大的影響。流動相選擇時分別考察了不同乙腈比例和不同的pH值對出峰的影響,以確保藥物、內標與雜質峰能完全分開,并最終選定了本文所用流動相。
4.2 樣品預處理方法
DP和內標極性大,不溶于有機溶劑,無法使用液液萃取法。Sutherland C和Iked K等分別采用固相萃取法和超濾法進行樣品預處理,固相萃取法和超濾法成本高,重現性較差。本文根據對同類藥物樣品的預處理經驗[7],首先選擇用乙腈沉淀蛋白,再用二氯甲烷反洗去除脂溶性雜質和沉淀蛋白的乙腈,離心取上清液直接進樣,不僅操作簡便、成本低,而且樣品沒有被稀釋,測定的靈敏度高、精密度好。方法優化中考察了沉淀蛋白的乙腈用量以及反洗劑二氯甲烷的體積,確定了上述預處理方法。
4.3 尿液外標法定量
首先考慮采用血樣測定方法對尿樣進行測定,但由于尿液樣品中雜質較多,在DP與內標處均有雜質干擾。通過調節流動相比例及pH,在DP出峰處可避開雜質干擾,但在內標MRP出峰處仍有干擾。用水直接稀釋進樣,預處理過程簡單,操作誤差可控,經方法學評價,尿液樣品測定采用外標法定量完全符合生物樣本測定的相關要求。
5 結束語
本文建立的HPLC-UV法測定血漿及尿液中DP質量濃度,具有樣品具有儀器設備要求低、預處理簡便、測定結果靈敏準確等特點,適用于DP血藥濃度及尿藥濃度的測定及藥代動力學研究。
[1]朱雪焱.碳青霉烯類抗生素多尼培南及其臨床應用[J].世界臨床物,2006,27(9):537-551.
[2]Ge Y,Wikler M A,Sahm D F,et al.In vitro antimicrobial activity of doripenem,a new carbapenem[J]. Antimicrob Agents&Chemother,2004,48(4):1384-1396.
[3]Sutherland C,Nicolau DP.Development of an HPLC method for the determination of doripenem in human and mouse serum[J].J Chromatogr,2007,853(1-2):123-126.
[4]Ikeda K,Ikawa K,Morikawa N,et al.Quantification ofdoripenem in human plasma and peritoneal fluid by highperformance liquid chromatography with ultraviolet detection[J].J Chromatogr,2008,867(1):20-25.
[5]和佳鴛.注射用多利培南健康人體藥動學研究[J].中國抗生素雜志,2013,38(11):866-870.
[6]唐季紅.高效液相色譜-串聯質譜法測定人血漿中多尼培南的濃度[J].中國新藥與臨床雜志,2009,28(5):380-384.
[7]章麗.HPLC-UV法測定人血漿及尿中頭孢他美鈉的濃度[J].中國抗生素雜志,2013,38(10):756-759.
HPLC-UV determination of doripenem in human plasma and urine
QIN Yongping1,MEI Yajun1,2,ZHANG Li1,MAO Rui1,NAN Feng1,XIANG Jin1,LIANG Maozhi1,YU Qin1
(1.Laboratoryof ClinicalPharmacologyGCPCenterof WestChinaHospital,SichuanUniversity,Chengdu610041,China;2.College of Pharmacy,Chengdu University of TCM,Chengdu 611137,China)
To establish a HPLC-UV method for determining Doripenem(DP)in human plasma and urine to perform DPhuman pharmacokinetic studies.The assay was conducted on a HPLC-UV column of Ultimate XB-C18(150mm×4.6mm×3μm).Mobile phases were 10mmol/L natrium aceticumacetonitrile-triethylamine(94:6:0.1(ν:ν:ν),pH adjusted to be 4.51 with acetic acid)and 8 mmol/L natrium aceticum-acetonitrile-triethylamine(95.5:4.5:0.1(ν:ν:ν),pH adjusted to be 4.99 with acetic acid).The above mobile phases were pumped at the rate of 1mL/min through the column,with the detection wavelength set at 297nm.Plasma samples were deproteinized with acetonitrile,which was extracted and removed with dichloromethane.Meropenem(MRP)was used as the internal standard(IS). Urine samples were diluted in distilled water and then quantified with the external reference method. The plasma concentration was in a linear relationship with the calibration curve within the range of 0.0625-200μg/mL while the quantitation limit was 0.0625μg/mL.The within-run and between-run precisions were 1.0%-6.0%and 3.0%-6.7%,respectively.The method recovery was 92.4%-104.5% and the plasma pretreatment recovery was 91.2%-103.8%.The urine concentration had a linear correlation to the calibration curve in the range of 0.625-4 800 μg/mL while the quantization limit was 0.625 μg/mL.The within-run and between-run precision were 0.7%-4.0%and 1.1%-5.3%,respectively.The method recovery was 94.1%-106.7%.This method is simple and rapid,sensitive and accurate,suitable for determining DPconcentration in human plasma and urine.
doripenem;HPLC;plasma concentration;urine concentration
A
:1674-5124(2015)05-0054-04
10.11857/j.issn.1674-5124.2015.05.014
2014-11-08;
:2015-01-05
秦永平(1963-),男,四川長寧縣人,技師,碩士,主要從事體內藥物分析工作。

