Carfilzomib:從天然產(chǎn)物到藥物的研發(fā)歷程
鈕俊興,徐星宇,胡立宏
(中國科學(xué)院上海藥物研究所,中藥現(xiàn)代化中心,上海201203)
Carfilzomib:從天然產(chǎn)物到藥物的研發(fā)歷程
鈕俊興,徐星宇,胡立宏
(中國科學(xué)院上海藥物研究所,中藥現(xiàn)代化中心,上海201203)
摘要:天然產(chǎn)物及其衍生物是藥物的重要來源。Carfilzomib是一個(gè)以天然產(chǎn)物為先導(dǎo)通過結(jié)構(gòu)優(yōu)化得到的用于治療多發(fā)性骨髓瘤的藥物,其先導(dǎo)化合物Epoxomicin是從微生物中發(fā)現(xiàn)的具有抗癌活性的環(huán)氧酮肽類天然產(chǎn)物,能夠選擇性地抑制蛋白酶體,其環(huán)氧酮結(jié)構(gòu)以獨(dú)特的兩步反應(yīng)和蛋白酶體共價(jià)結(jié)合,因此克服了同類藥物的脫靶缺點(diǎn)。以Epoxomicin為先導(dǎo),通過結(jié)構(gòu)優(yōu)化得到活性更強(qiáng)、成藥性性更好的Carfilzomib,作為新一代蛋白酶體抑制劑于2012年上市。
關(guān)鍵詞:蛋白酶體抑制劑; Carfilzomib; Epoxomicin
1 簡(jiǎn)介
天然活性產(chǎn)物具有結(jié)構(gòu)新穎,藥理活性多樣的特點(diǎn),是新藥創(chuàng)制的重要來源,臨床上有約50%的藥物直接或間接來源于天然產(chǎn)物,但大多數(shù)天然產(chǎn)物存在活性弱、特異性低、類藥性差等缺點(diǎn),因此需要根據(jù)其不足,有針對(duì)性的進(jìn)行結(jié)構(gòu)優(yōu)化。本文通過總結(jié)文獻(xiàn),介紹以活性天然產(chǎn)物Epoxomicin為先導(dǎo)化合物,通過結(jié)構(gòu)優(yōu)化,得到上市藥物Carfilzomib的實(shí)例,從藥物化學(xué)的視角分析天然產(chǎn)物結(jié)構(gòu)改造的要點(diǎn)。
Carfilzomib(商品名Kyprolis) (結(jié)構(gòu)見圖1)是美國Onys制藥公司開發(fā)的新一代蛋白酶體抑制劑,于2012年7月20日獲得美國食品藥品監(jiān)督管理局(FDA)批準(zhǔn)上市,主要用于曾接受過兩種或以上過往治療方案(包括Bortezomib和免疫調(diào)節(jié)劑治療)的多發(fā)性骨髓瘤患者。多發(fā)性骨髓瘤是惡性漿細(xì)胞在骨髓中克隆增生性疾病,也是一種較為罕見的致命疾病。作為一種罕見病用藥,Carfilzomib是在美國FDA加速審批程序下獲得批準(zhǔn)的。

圖1 Epoxomicin和Carfilzomib的結(jié)構(gòu)圖
2 Epoxomicin的發(fā)現(xiàn)及作用機(jī)制
2.1作用靶點(diǎn)蛋白酶體是真核生物細(xì)胞內(nèi)降解蛋白質(zhì)的核心部分,是一類桶裝復(fù)合物,由1個(gè)20S核心顆粒和2個(gè)19S調(diào)節(jié)顆粒和許多多肽亞基組成。真核生物體中β1、β2、β5亞基具有水解蛋白的活性特點(diǎn),其中β5亞基(糜蛋白酶樣活性)負(fù)責(zé)大部分蛋白質(zhì)的水解。蛋白酶體水解蛋白質(zhì)時(shí),首先產(chǎn)生具有活性的蘇氨酸(Thr1),在水傳遞電子的作用下,Thr1Oγ親核進(jìn)攻肽鍵的羰基,發(fā)生水解反應(yīng)。
抑制蛋白酶體的水解活性會(huì)增加毒性蛋白、激活凋亡通路、導(dǎo)致細(xì)胞凋亡;在增殖活躍的腫瘤細(xì)胞中,由于異常蛋白的迅速積累致使蛋白酶體高表達(dá),蛋白酶體的活性比正常細(xì)胞中更強(qiáng)。因而腫瘤細(xì)胞對(duì)抑制蛋白酶體活性導(dǎo)致的凋亡作用更敏感,因此,蛋白酶體被認(rèn)為是治療腫瘤的靶標(biāo)。
2.2 Epoxomicin的發(fā)現(xiàn)來源于微生物的天然產(chǎn)物Epoxomicin(見圖1)是一個(gè)具有環(huán)氧酮結(jié)構(gòu)的天然線性多肽,于20世紀(jì)90年代,由百時(shí)美施貴寶(BMS)的東京研發(fā)部從編號(hào)Q996-17的放線菌菌株中首次分離得到[1]。盡管它在體內(nèi)、體外均表現(xiàn)出很強(qiáng)的抗腫瘤活性(對(duì)鼠源黑色素瘤B16-F10和白血病P388細(xì)胞株增殖抑制的IC50均為2 ng·mL-1;對(duì)BDF1小鼠B16黑色素瘤靜脈給藥的有效劑量為每天0.13 mg·kg-1),但BMS認(rèn)為其有不穩(wěn)定的環(huán)氧酮結(jié)構(gòu)和較差的類藥性質(zhì),加之抗腫瘤機(jī)制不明確,因此放棄了進(jìn)一步的研究。
2.3 Epoxomicin的作用機(jī)制與此同時(shí),耶魯大學(xué)的Crews小組對(duì)Epoxomicin很感興趣:一方面其體外體內(nèi)抗癌活性很強(qiáng);另一方面其環(huán)氧結(jié)構(gòu)可能與蛋白通過共價(jià)鍵結(jié)合,易于獲得靶蛋白,從而解釋其抗癌的作用機(jī)制。Crews小組通過全合成得到了Epoxomicin,并利用生物素標(biāo)記原理合成了分子探針[2,3],通過探針確立靶蛋白為蛋白酶體β1、β2i和β5i亞基。合成的Epoxomicin能選擇性地抑制蛋白酶體活性,不抑制其他蛋白酶如木瓜蛋白酶、糜蛋白酶、胰蛋白酶等。
為了解釋Epoxomicin高度選擇性的原因,確定其與蛋白酶體結(jié)合的機(jī)理,Crews與慕尼黑理工大學(xué)的Groll合作得到了Epoxomicin和酵母菌蛋白酶體的晶體復(fù)合物[4]。通過晶體復(fù)合物發(fā)現(xiàn)Epoxomicin的羰基部分被蛋白酶體的Thr1Oγ進(jìn)攻后形成半縮醛結(jié)構(gòu)復(fù)合物,這個(gè)復(fù)合物分子中親核性的Thr1N繼而親核進(jìn)攻環(huán)氧,生成了6-exo-tet的嗎啉環(huán)。這樣的兩步反應(yīng)使Epoxomicin和蛋白酶體通過共價(jià)鍵不可逆地緊密結(jié)合在一起(見圖2)。
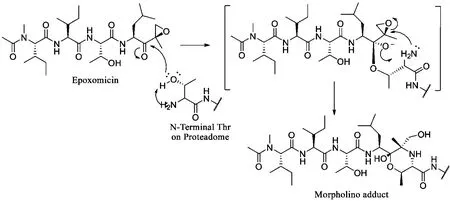
圖2 Epoxomicin和蛋白酶體的結(jié)合機(jī)制
當(dāng)時(shí)在研的蛋白酶體抑制劑如醛肽類、烯砜肽類、硼酸肽類等,除了和蛋白酶體以共價(jià)鍵結(jié)合外,還與其他具有親核性基團(tuán)的蛋白酶如絲氨酸蛋白酶、半胱氨酸蛋白酶結(jié)合,有不同程度的脫靶作用,使得療效較差,毒副作用較大[5]。而Epoxomicin這種通過兩步反應(yīng)形成共價(jià)鍵的機(jī)制,決定了它對(duì)具有獨(dú)特Thr1結(jié)構(gòu)的蛋白酶體有特異選擇性,優(yōu)于以往的蛋白酶體抑制劑,具有潛在成藥性。
3 Epoxomicin的結(jié)構(gòu)優(yōu)化
因?yàn)镋poxomicin表現(xiàn)出了很強(qiáng)的蛋白酶體β5亞基的選擇性抑制活性,所以Crews小組期望通過結(jié)構(gòu)優(yōu)化,得到蛋白酶體抑制活性和抗癌活性更強(qiáng)、成藥性更好的候選藥物。Epoxomicin的結(jié)構(gòu)可分為兩個(gè)部分(見圖3) :環(huán)氧酮部分和四肽部分(四肽部分根據(jù)與蛋白酶體水解位點(diǎn)的距離分別為P1~P4),下面分別對(duì)它們進(jìn)行結(jié)構(gòu)優(yōu)化。

圖3 多肽結(jié)構(gòu)示意圖
3.1環(huán)氧酮部分的改造由上文的作用機(jī)制可以看出,Epoxomicin的環(huán)氧結(jié)構(gòu)是進(jìn)行共價(jià)結(jié)合的活性必須基團(tuán)。同時(shí)早期研究也表明,環(huán)氧結(jié)構(gòu)為2R構(gòu)型時(shí)有活性,而為2S構(gòu)型時(shí)則活性降低或消失[6],說明具有一定立體構(gòu)型的環(huán)氧片段是保持活性所必需的,因而不對(duì)該部分進(jìn)行改造。
3.2肽鏈的長度與活性的關(guān)系相關(guān)研究表明:蛋白酶體的20S催化亞基中的多個(gè)口袋,可以與多肽的側(cè)鏈發(fā)生相互作用,而P1片段是該類4肽衍生物與蛋白酶體結(jié)合的關(guān)鍵位置[7]。當(dāng)P1區(qū)域?yàn)榱涟彼峄虮奖彼釙r(shí),可以有效提高對(duì)β5亞基的選擇性;而為堿性片段如賴氨酸和精氨酸時(shí),β5亞基的選擇性降低[8,9]。
因此,研發(fā)人員首先將R1~R4的取代基都改為異丁基,設(shè)計(jì)并合成化合物1~4,考察活性與鏈長的關(guān)系(見表1)。
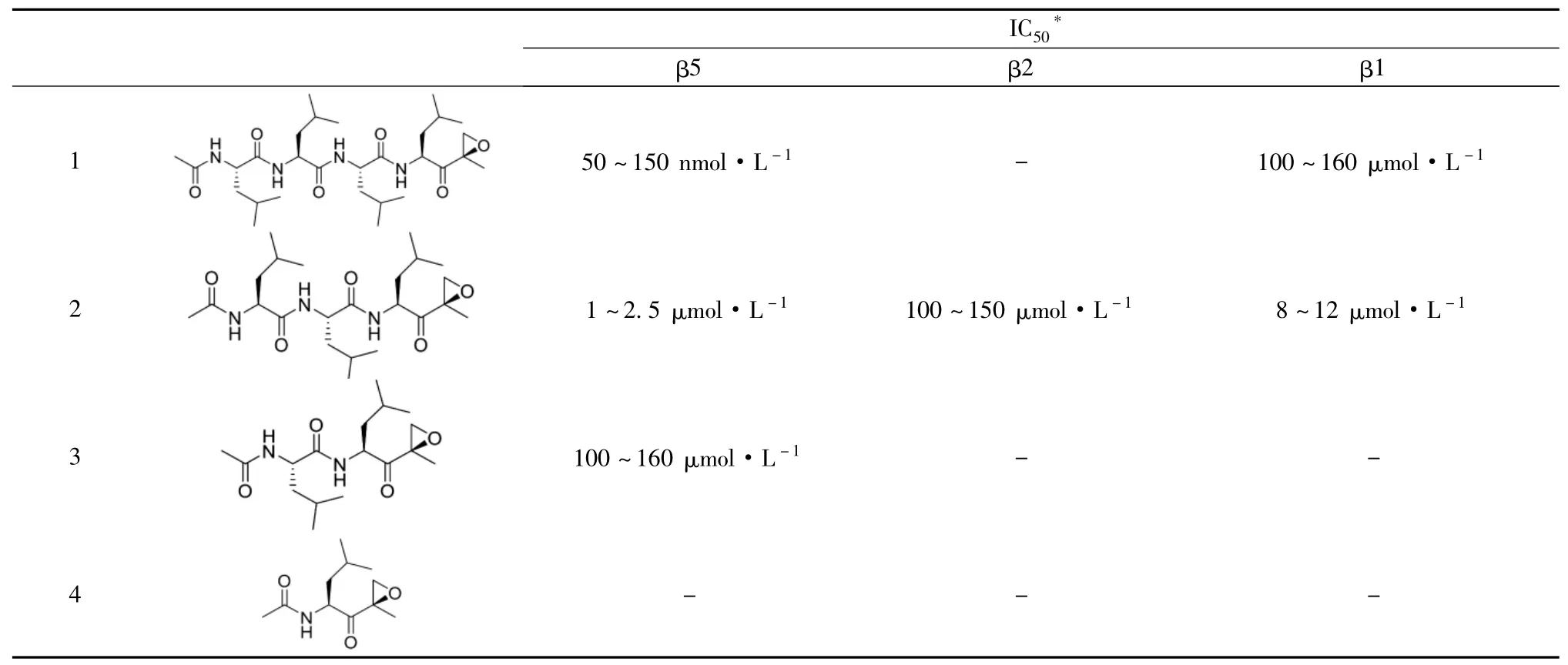
表1 肽鏈長度與蛋白酶體不同亞基抑制活性關(guān)系
結(jié)果表明,肽鏈為四肽長度時(shí),選擇性和活性都最佳,肽鏈長度的縮短將導(dǎo)致活性和選擇性的下降,推測(cè)可能與蛋白酶體催化位點(diǎn)口袋尺寸有關(guān)。
3.3 R2~R4取代基的優(yōu)化在確定了四肽環(huán)氧酮為基本骨架后,研究人員以化合物1為基礎(chǔ),通過改變P2、P3、P4片段的氨基酸種類來探究其對(duì)活性的影響(見表2)。
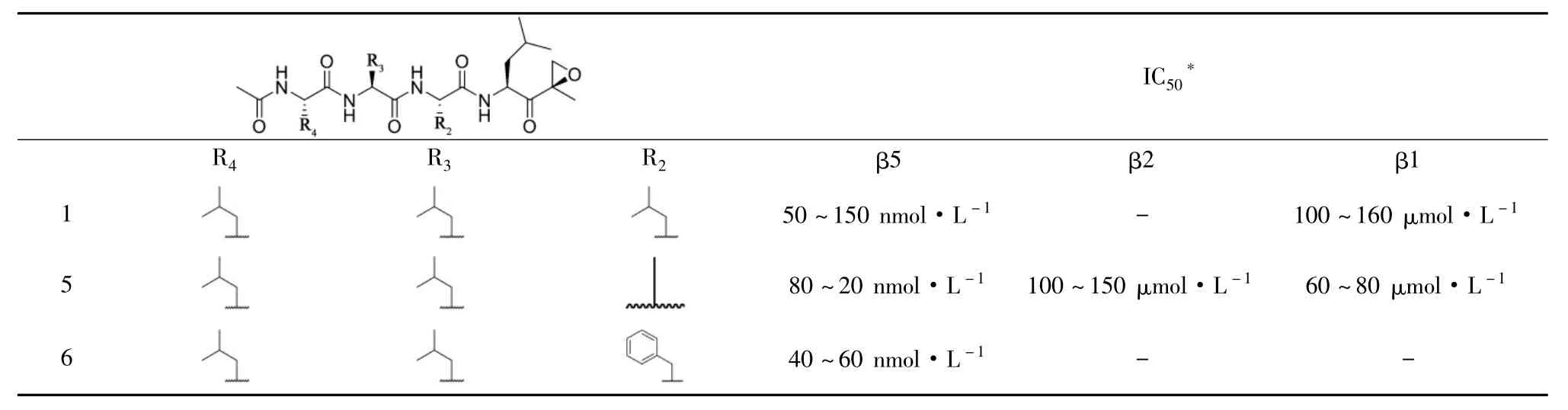
表2 化合物5~15對(duì)蛋白酶體不同亞基抑制活性
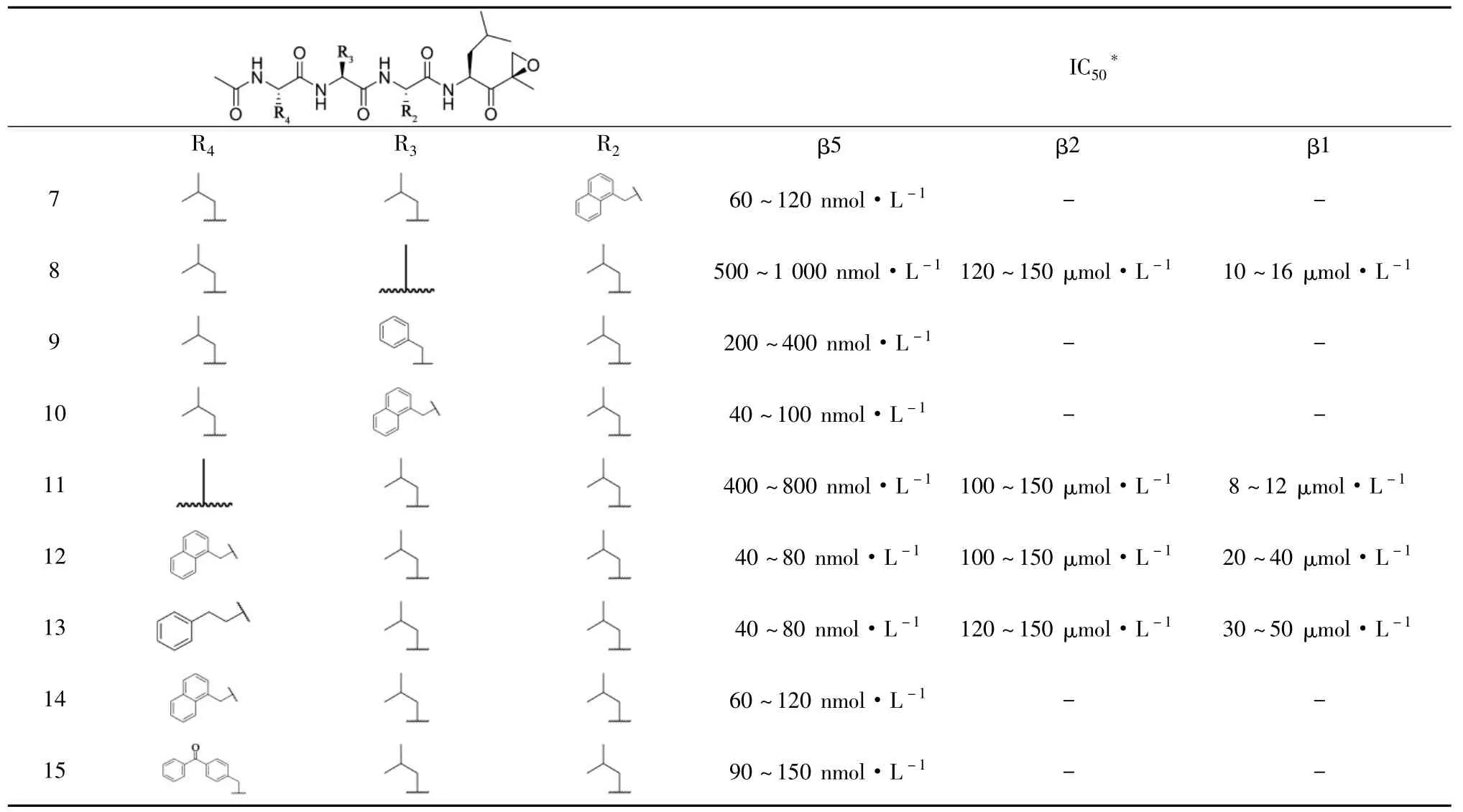
續(xù)表2:
首先保持R3、R4都為異丁基,改變R2的取代基,得到化合物5~7。體外活性測(cè)試表明,R2基團(tuán)為脂肪族取代基,活性較差;為芳香性取代基時(shí),對(duì)酶的抑制效果以及選擇性都有顯著提高,尤其以苯乙基取代時(shí),結(jié)果最優(yōu)。
其次保持R2、R4取代基為異丁基不變,改變R3取代基,獲得化合物8~10,發(fā)現(xiàn)將化合物1的R3取代基改為其他疏水性片段后,對(duì)酶抑制效果與選擇性都降低了,所以R3取代基仍舊保持為異丁基。
隨后再保持R2、R3取代基不變時(shí),改變R4取代基的結(jié)構(gòu),獲得化合物12~15,發(fā)現(xiàn)為芳香取代時(shí),活性普遍較好,且以苯乙基取代時(shí),選擇性與活性最優(yōu)。
基于以上結(jié)果,科研人員將R2、R3、R4的最優(yōu)基團(tuán)結(jié)合在一起,得到了化合物16(YU-101) (見圖4),以及其N-去乙酰基衍生物17。活性測(cè)試顯示(見表3),化合物17的活性、選擇性均較弱; 16的活性、選擇性更佳,其抑制蛋白酶體β5亞基的活性明顯強(qiáng)于Epoxomicin和Bortezomib等蛋白酶體抑制劑,并且在體內(nèi)具有強(qiáng)抗炎活性。
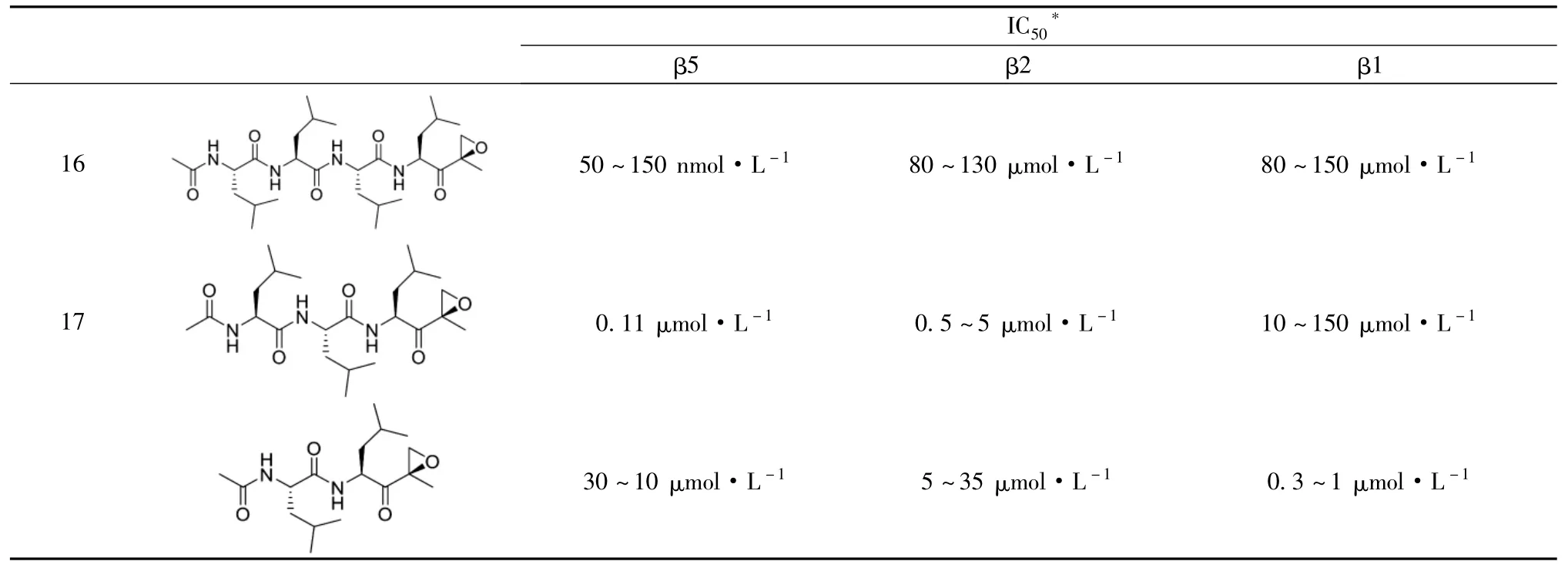
表3 化合物16、17對(duì)蛋白酶體不同亞基抑制活性
3.4候選化合物PR171的確定Crews將YU-101轉(zhuǎn)讓給了Proteolix制藥公司(后被Onyx收購), Proteolix繼續(xù)進(jìn)行改造得到了上百個(gè)化合物,但活性都不如YU-101。盡管YU-101抗腫瘤效果顯著,但Proteolix公司很快發(fā)現(xiàn)YU-101的水溶性差,難以成藥,因此引入嗎啉環(huán),合成了活性保持而水溶性增加幾個(gè)數(shù)量級(jí)的化合物PR-171(見圖4),并以此作為候選化合物進(jìn)入臨床研究。

圖4 Carfizomib的優(yōu)化過程
4 Epoxomicin的上市
在Crews小組進(jìn)行結(jié)構(gòu)改造的同時(shí),硼酸二肽類藥物Bortezomib作為第一個(gè)蛋白酶體抑制劑成功上市,用于治療多發(fā)性骨髓瘤。但臨床研究發(fā)現(xiàn)Bortezomib不僅會(huì)出現(xiàn)血小板減少、周圍神經(jīng)炎等副作用,而且易產(chǎn)生耐藥,分析可能是由于其脫靶作用造成的[10]。而環(huán)氧酮肽類化合物Carfilzomib因其特殊的共價(jià)結(jié)合方式對(duì)蛋白酶體的選擇性高、結(jié)合力強(qiáng),與Bortezomib相比能克服其脫靶作用,毒副反應(yīng)較小。
對(duì)Carfilzomib的臨床前研究[11,12]也證實(shí)其對(duì)蛋白酶體以及免疫蛋白酶體β5亞基的抑制活性與Bortezomib相當(dāng),并且對(duì)其他的蛋白酶都沒有抑制活性;同時(shí)對(duì)Bortezomib耐藥的病人也十分有效。因此,Carfilzomib作為第二代蛋白酶體抑制劑被FDA批準(zhǔn)上市,用于此前至少經(jīng)過兩個(gè)優(yōu)先療法,包括Bortezomib和免疫調(diào)節(jié)劑治療的多發(fā)性骨髓瘤患者。
5 總結(jié)
Carfilzomib從具有抗癌活性的天然產(chǎn)物Epoxomicin的發(fā)現(xiàn),到其抑制蛋白酶體活性作用機(jī)制的闡明,再到通過結(jié)構(gòu)改造發(fā)現(xiàn)活性更強(qiáng)化合物YU-101,最終到水溶性更好的Carfilzomib上市,這一研發(fā)歷程對(duì)我們啟示頗多。
5.1生物界的次生代謝產(chǎn)物是為了自身的生長和種群的繁衍而產(chǎn)生的,生來不是為了給人類治病,毒性、成藥性等方面的缺陷決定了需要對(duì)它們進(jìn)行結(jié)構(gòu)改造。面對(duì)作用機(jī)制不明,類藥性差等問題,應(yīng)根據(jù)所研究的天然產(chǎn)物的性質(zhì),進(jìn)行個(gè)性化、量體裁衣式地改造,有針對(duì)性地優(yōu)化藥效、藥代、安全性等性質(zhì)。
5.2明確作用機(jī)制有利于進(jìn)一步的修飾改造。Epoxomicin獨(dú)特的兩步形成共價(jià)結(jié)合的機(jī)制的闡明,不僅明確了作用靶標(biāo)為蛋白酶體,同時(shí)提示了環(huán)氧酮基團(tuán)的必要性,為接下來的改造工作提供了便利。
5.3研發(fā)的新藥必須要比上市或準(zhǔn)上市藥物更具有優(yōu)勢(shì)。在Epoxomicin的改造過程中,首個(gè)蛋白酶體抑制劑Bortezomib進(jìn)入臨床并批準(zhǔn)上市,這對(duì)其他蛋白酶體抑制劑的開發(fā)也帶來了更大的挑戰(zhàn)和壓力。但Bortezomib由于其可逆結(jié)合的機(jī)制,毒副作用較大且易耐藥;而Epoxomicin作用機(jī)制獨(dú)特:它選擇性不可逆抑制蛋白酶體,以其為基礎(chǔ)研發(fā)的第二代蛋白酶體抑制劑Carfilzomib克服了Bortezomib毒副作用大的缺點(diǎn),同時(shí)對(duì)Bortezomib耐藥的病人也有效果,故而得以在Bortezomib之后上市。
參考文獻(xiàn):
[1]Hanada M,Sugawaras K,Kaneta K,et al.Epoxomicin,a new antitumor agent of microbial origin[J].J Antibiot (Tokyo),1992,45(11) : 1746-1752.
[2]Sin N,Kim KB,Elofsson M,et al.Total synthesis of the potent proteasome inhibitor epoxomicin: a useful tool for understanding proteasome biology[J].Bioorg Med Chem Lett,1999,9(15) : 2283-2288.
[3]Meng L,Mohan R,Kwok BH,et al.Epoxomicin,a potent and selective proteasome inhibitor,exhibits in vivo antiinflammatory activity[J].Proc Natl Acad Sci U S A,1999,96(18) : 10403-10408.
[4]Groll M,Kim KB,Kairies N,et al.Crystal structure of epoxomicin: 20S proteasome reveals a molecular basis for selectivity of α',β'-epoxyketone proteasome inhibitors [J].J Am Chem Soc,2000,122(16) : 1237-1238.
[5]Borissenko L,Groll M.20S proteasome and its inhibitors: crystallographic knowledge for drug development[J].Chem Rev,2007,107(3) : 687-717.
[6]Kim KB,Myung J,Sin N,et al.Proteasome inhibition by the natural products epoxomicin and dihydroeponemycin: insights into specificity and potency[J].Bioorg Med Chem Lett,1999,9(23) : 3335-3340.
[7]Adams J,Behnke M,Chen S,et al.Potent and selective inhibitors of the proteasome: dipeptidyl boronic acids[J].Bioorg Med Chem Lett,1998,8(4) : 333-338.
[8]Bogyo M,Shin S,McMaster JS,et al.Substrate binding and sequence preference of the proteasome revealed by active-site-directed affinity probes[J].Chem Biol,1998,5(6) : 307-320.
[9]Lynas JF,Harriott P,Healy A,et al.Inhibitors of the chymotrypsin-like activity of proteasome based on di-and tri-peptidyl α-keto aldehydes (glyoxals)[J].Bioorg Med Chem Lett,1998,8(4) : 373-378.
[10]Elofsson M,Splittgerber U,Myung J,et al.Towards subunit-specific proteasome inhibitors: synthesis and evaluation of peptide α',β'-epoxyketones[J].Chem Biol,1999,6(11) : 811-822.
[11]Arastu-Kapur S,Anderl JL,Kraus M,et al.Nonproteasomal targets of the proteasome inhibitors bortezomib and carfilzomib: a link to clinical adverse events[J].Clin Cancer Res,2011,17(9) : 2734-2743.
[12]Demo SD,Kirk CJ,Aujay MA,et al.Antitumor activity of PR-171,a novel irreversible inhibitor of the proteasome [J].Cancer Res,2007,67(13) : 6383-6391.
·制劑研究·
·實(shí)驗(yàn)研究·
專家簡(jiǎn)介
胡立宏,男,中國科學(xué)院上海藥物研究所研究員、研究組長、博士生導(dǎo)師,研究工作主要涉及“基于中草藥資源的藥物發(fā)現(xiàn)”研究領(lǐng)域。現(xiàn)任世界中醫(yī)藥學(xué)會(huì)聯(lián)合會(huì)中藥分析專業(yè)委員會(huì)理事、中國植物學(xué)會(huì)民族植物學(xué)分會(huì)理事、上海市藥學(xué)會(huì)天然藥化專業(yè)委員會(huì)委員、上海市口腔醫(yī)學(xué)重點(diǎn)實(shí)驗(yàn)室學(xué)術(shù)委員會(huì)委員,以通訊作者身份在Journal of Neuroscience,Chemistry&Biology,Journal of Medicinal Chemistry,Diabetes,Green Chemistry,Organic Letters等國際主流刊物上發(fā)表研究論文190余篇,獲得發(fā)明專利授權(quán)10余項(xiàng)。2009年以“天然藥物化學(xué)”研究方向獲得“國家杰出青年基金”資助,并入選“中國科學(xué)院百人計(jì)劃”,2012年獲得了“上海市優(yōu)秀學(xué)科帶頭人”稱號(hào)。
Carfilzomib: from natural product to drug
NIU Jun-xing,XU Xing-yu,HU Li-hong
(Shanghai Research Center for Modernization of Traditional Chinese Medicine,Shanghai Institute of Materia Medica,Chinese Academy of Sciences,Shanghai 201203,China)
Abstract:Natural products and their derivatives have been invaluable as a source of therapeutic agents.Carfilzomib,a potential chemotherapy drug for patients with multiple myeloma,was developed from a microbial natural product Epoxomicin.Epoxomicin was found to exhibit potent anti-cancer activity,which might attribute to its inhibitory activity against proteasome.Because of its unique two -step binding mode,Epoxomicin has a clear advantage compared to other proteasome inhibitors with their substantial off-target activity.With a more pontecy and better drug-like properties,Carfilzomib was developed from the lead compound Epoxomicin and approved by FDA as a second-generation proteasome inhibitor in 2012.
Key words:Proteasome inhibitor; Carfilzomib; Epoxomicin
基金項(xiàng)目:國家自然科學(xué)基金面上項(xiàng)目(No.81473110)
中圖分類號(hào):R979.1
文獻(xiàn)標(biāo)識(shí)碼:A
文章編號(hào):2095-5375(2015) 10-0559-006

