家族性腺瘤性息肉病伴發硬纖維瘤2例并文獻復習
?
家族性腺瘤性息肉病伴發硬纖維瘤2例并文獻復習
黃晉熙,王程虎,原偉偉,陳貝貝,周一※
(鄭州大學附屬腫瘤醫院普外科,鄭州 450003)
關鍵詞:家族性腺瘤性息肉病;硬纖維瘤;大腸息肉基因
家族性腺瘤性息肉病(familial adenomatous polyposis,FAP)是一種遺傳性疾病,現階段的主要治療方法是手術,而硬纖維瘤是FAP患者的一種腸外病變。現收集鄭州大學附屬腫瘤醫院收治的2例FAP合并硬纖維瘤患者的臨床資料,結合有關文獻探討FAP合并硬纖維瘤的發生、發展、診斷以及治療,現報道如下。
1臨床資料
例1,男,李某,31歲,因“大便帶血3個月余”于2009年8月就診。患者既往無腹部手術史。入院后行纖維腸鏡檢查發現,全大腸息肉近百枚,直腸肛管處有一巨大潰瘍,活組織檢查提示為腺癌。考慮為“FAP惡變”。追問其家族史,其母因結腸癌去世。完善術前準備后行“全大腸切除術+回腸造瘺術”。術中發現空腸系膜有一巨大腫物,因侵犯腸系膜根部血管,考慮切除后短腸綜合征可能性大,因此未予切除,僅行活組織檢查,提示侵襲性纖維瘤。患者手術順利,術后恢復
良好,術后病理分期:pT4aN0M0。隨訪4年,腹腔硬纖維瘤緩慢生長(圖1),患者無明顯臨床癥狀,目前給予環加氧酶2抑制劑治療。術后建議患者直系家屬行腸鏡檢查,其四姐妹均未發現結腸息肉,但其弟發現多發腸息肉(圖2),但因經濟原因當時未予治療。
例2,男,李某,28歲,例1患者的弟弟,因“大便帶血4個月余”于2012年12月入院。患者既往無腹部手術病史。入院后行結腸鏡及活組織檢查提示:直腸肛管癌合并多發性結腸息肉(鏡下見數千枚息肉)。CT提示腹腔內實性占位,下段直腸腸壁增厚。考慮FAP合并硬纖維瘤,遂行手術探查,并行“全大腸切除術+回腸造瘺術+腸系膜腫瘤切除術”治療。術后病理證實為“FAP(pT4aN0M0)并硬纖維瘤”,見圖3~5。患者術后恢復良好,給予氟尿嘧啶類方案化療并口服環加氧酶2抑制劑維持治療,隨訪無臨床癥狀。術后患者行大腸息肉基因(adenomatous polyposis gene,APC)分析,基因測序顯示患者為外顯子12的1605~1606 TG缺失的移碼突變(圖6)。
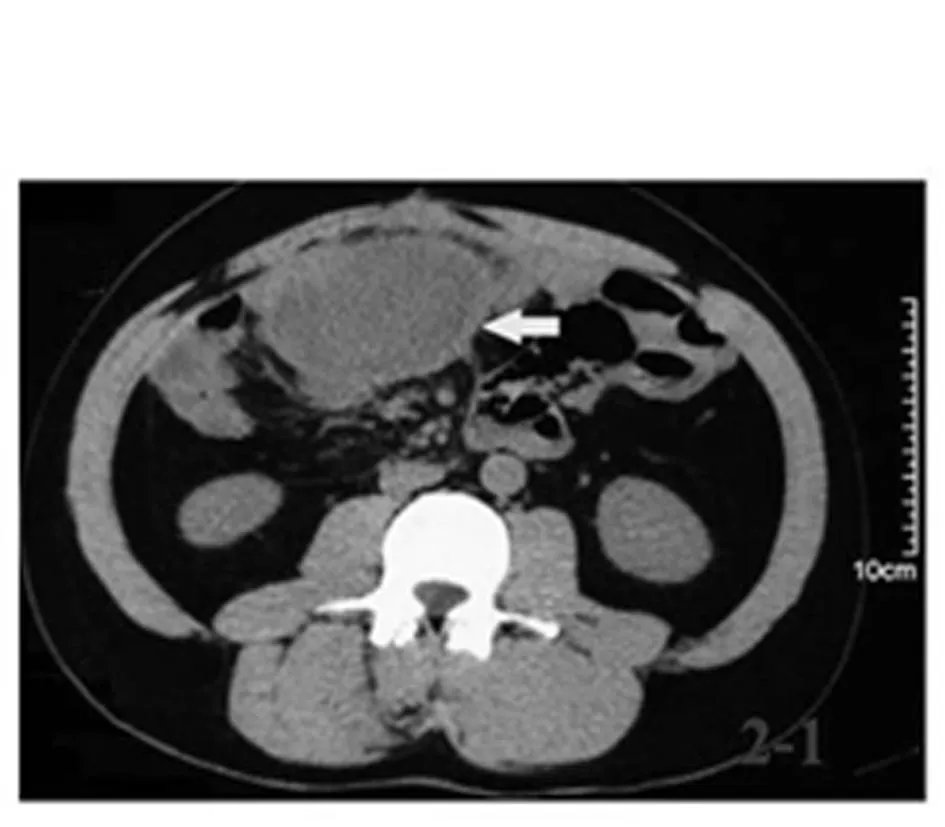
圖1 例1家族性腺瘤性息肉 病患者伴硬纖維瘤CT 圖像腹腔硬纖維瘤 侵犯小腸系膜

圖2 家族性腺瘤性息肉病患者伴硬纖維瘤患者家系系譜圖

圖3 例2家族性腺瘤性 息肉病患者伴硬纖維 瘤患者CT圖像提示 腹腔硬纖維瘤侵犯 小腸系膜

圖4 例2家族性腺瘤性息肉病患者伴硬纖維瘤患者,術中切除的部分肛管直腸及小腸系膜硬纖維瘤大體標本

圖5例2家族性腺瘤性息肉病患者伴硬纖維瘤患者,小腸系膜硬纖維瘤病理切片,可見大量膠原纖維細胞形成,部分可見梭形纖維細胞,其間可見血管增生5a.HE×40; 5b.HE×100

圖6例2家族性腺瘤性息肉病患者伴硬纖維瘤患者APC基因分析6a.例2患者的APC基因分析圖; 6b.野生型對照圖
2討論
2.1流行病學及概述FAP是一種常染色體顯性遺傳性疾病,2009年歐盟國家報道的FAP的發病率為3/10萬~10/10萬,且年輕男女的患病比例基本相同[1]。FAP的典型過程是患者在20歲左右時發現結腸和直腸上出現數百至數千個腺瘤,如果診斷和治療不及時幾乎所有的患者都會發展成結直腸癌[2]。約50%典型FAP患者會在15歲時發生結腸腺瘤,約95%患者在35歲時發生結腸腺瘤[3]。
除了結直腸的腺瘤,胃底、十二指腸、壺腹部及小腸也會發生腺瘤性病變,其中胃底和小腸的腺瘤發生癌變的概率較低,但十二指腸與壺腹部的腺瘤發生癌變的概率為5%,較正常人高出數百倍[4-7]。
FAP患者一般都會有一些腸外表現,如骨瘤、皮膚疾病、牙齒異常、先天性視網膜色素上皮肥厚、硬纖維瘤及其他腸外臟器的惡性腫瘤(如甲狀腺、肝臟、膽管及中樞神經系統的腫瘤)[2]。另一種輕表型FAP(attenuated FAP,AFAP)結腸內息肉數量較少(通常>10個,但<100個),且腺瘤出現的年齡(平均44歲)及惡變時間(平均56歲)較典型FAP患者晚[8]。
硬纖維瘤是一種罕見的良性腫瘤,其在人群中的發病率為0.03%,但FAP患者發生硬纖維瘤的危險系數是正常人的825倍,發病率為10%~20%,男女比例為1∶1.4,可發生于任何年齡段,最常見于20~40歲[9-10]。約81.5%的患者在確診FAP后又發生硬纖維瘤,僅7%的患者FAP與硬纖維瘤同時發生[10]。本研究的兩例患者為同一家系,結直腸內均見大量腺瘤,發病年齡在30歲左右,為典型的FAP患者,其結腸外表現為同時發生的腹腔內小腸系膜硬纖維瘤。患者的母親也是FAP患者,但因去世多年,無法查證是否同時合并硬纖維瘤。同一家族多例患者同時合并FAP與硬纖維瘤,在國內外均屬罕見。
2.2病因學APC基因是位于第5號常染色體長臂q21內的抑癌基因,是含有15個外顯子的編碼區,編碼的蛋白主要是調節細胞的黏附、信號轉導及轉錄,是Wnt通路的重要分子,在結直腸腫瘤的發生、發展中起重要作用[11]。目前認為,APC基因的突變導致了FAP的發生。突變的類型主要是無義突變,其導致了截短蛋白的形成,引起了染色體不穩或錯配修復功能缺失,最終導致結直腸癌的發生。密集型FAP的APC基因突變多位于中心區域(1284~1580密碼子間),又稱突變密集區[12],而AFAP的APC基因突變一般位于4、5、9及15號外顯子的3′端[13]。
非FAP患者的硬纖維瘤是因為β聯蛋白的突變,而FAP患者的硬纖維瘤是APC基因的突變,其突變位點一般位于1309~1580密碼子[14]。FAP患者發生硬纖維瘤的危險因素包括生育期女性、妊娠、口服避孕藥[15]、手術史和家族史等。Bertario等[16]發現,APC基因1444~1578密碼子的突變更易導致硬纖維瘤發生。本研究兩例患者都為男性,表現為家族聚集性,其基因突變是位于12外顯子1605~1606的移碼突變。
2.3臨床表現與診斷大部分硬纖維瘤發生于腹部,且多位于腹腔內(小腸系膜多見),但也可以發生于腹壁(如瘢痕),約10%的患者可發生在腹外器官[17-18]。雖然硬纖維瘤在病理學上表現為良性,幾乎不出現遠處轉移,但其呈浸潤性生長,可侵及鄰近臟器。根據所在部位,硬纖維瘤可無任何臨床表現或表現為疼痛或胃腸道癥狀,特別是發生在系膜的硬纖維瘤,可引起腸梗阻、輸尿管梗阻、小腸缺血、膿腫形成、甚至小腸穿孔或小腸瘺等[19]。對于腹腔外的硬纖維瘤,可用細針穿刺細胞學診斷,而腹腔內的病變可在多普勒超聲或CT引導下細針穿刺診斷。當CT或MRI發現有FAP家族史或手術史的患者出現進行性增長的實性腫瘤,排除惡性腫瘤復發后,應考慮硬纖維瘤。
2.4治療有研究報道,有5%~10%的硬纖維瘤可自發緩解消失,30%出現緩解與發展交替,50%診斷后無變化,只有10%會持續生長并浸潤其他器官[18,20]。因此,只有當硬纖維瘤引起癥狀、對周圍組織有浸潤風險或影響美觀的情況下才需要治療[19]。
由于大部分對于硬纖維瘤的研究都是基于與FAP相關或散發病例,因此現階段暫無有效控制硬纖維瘤的方法[21]。對于腹壁或腹外的硬纖維瘤,手術治療可作為一線方案[18],術后可給予輔助放療[22];而對于腹腔內的硬纖維瘤,舒林酸(非甾體類消炎藥)和(或)選擇性雌激素受體抑制劑(如他莫昔芬或托瑞米芬)是一線治療方案[10,21]。對于有臨床癥狀但手術無法切除或其他治療方法無效但呈浸潤性生長的硬纖維瘤,細胞毒藥物化療藥物,如阿霉素加卡鉑[23]或阿霉素+達卡他嗪[24]也是可以選擇的方案。對于腹腔內的硬纖維瘤,因高復發及死亡風險,手術并不是一線治療方案,但對于藥物治療失敗且有臨床癥狀的患者手術仍為可選擇的治療方法之一[25]。
2.5監測雖然未對FAP患者行硬纖維瘤監測形成共識,但因篩查的普及而導致FAP患者結直腸癌的病死率降低及硬纖維瘤發生率升高,進行腹腔CT或MRI掃描還是有必要的,特別是對于突變位點在密碼子1444~1578或有硬纖維瘤家族史的患者[19]。此外,對于存在硬纖維瘤高危因素的高齡患者來說,是否需要手術治療或采用什么類型的手術需要慎重考慮[26-27]。
3小結
對于大部分的FAP患者,硬纖維瘤多發生在手術后,同時合并FAP和腹腔硬纖維瘤的較少見,因而國內外暫無統一治療意見。本研究例1患者雖未行腹腔硬纖維瘤切除,但至今仍無明顯臨床癥狀,正常生存;例2患者雖行硬纖維瘤切除,術后也未發生明顯的并發癥,但術中發生并發癥的風險及術后復發風險均較高,是否將術中手術切除硬纖維瘤視為標準治療方案還有待商榷。
參考文獻
[1]Church JM,Xhaja X,Warrier SK,etal.Desmoid tumors do not prevent proctectomy following abdominal colectomy and ileorectal anastomosis in patients with familial adenomatous polyposis[J].Dis Colon Rectum,2014,57(3):343-347.
[2]Half E,Bercovich D,Rozen P.Familial adenomatous polyposis[J].Orphanet J Rare Dis,2009,4(6):22.
[3]Ngamruengphong S,Boardman LA,Heigh RI,etal.Gastric adenomas in familial adenomatous polyposis are common,but subtle,and have a benign course[J].Hered Cancer Clin Pract,2014,12(1):4.
[4]Bianchi LK,Burke CA,Bennett AE,etal.Fundic gland polyp dysplasia is common in familial adenomatous polyposis[J].Clin Gastroenterol Hepatol,2008,6(2):180-185.
[5]Tajika M,Niwa Y,Bhatia V,etal.Risk of ileal pouch neoplasms in patients with familial adenomatous polyposis[J].World J Gastroenterol,2013,19(40):6774-6783.
[6]Groves CJ,Saunders BP,Spigelman AD,etal.Duodenal cancer in patients with familial adenomatous polyposis (FAP):results of a 10 year prospective study[J].Gut,2002,50(5):636-641.
[7]Aihara H,Kumar N,Thompson CC.Diagnosis,surveillance,and treatment strategies for familial adenomatous polyposis:rationale and update[J].Eur J Gastroenterol Hepatol,2014,26(3):255-262.
[8]Plawski A,Banasiewicz T,Borun P,etal.Familial adenomatous polyposis of the colon[J].Hered Cancer Clin Pract,2013,11(1):15.
[9]Church J,Lynch C,Neary P,etal.A desmoid tumor-staging system separates patients with intra-abdominal,familial adenomatous polyposis-associated desmoid disease by behavior and prognosis[J].Dis Colon Rectum,2008,51(6):897-901.
[10]Knudsen AL,Bülow S.Desmoidtumour in familial adenomatous polyposis.A review of literature[J].Fam Cancer,2001,1(2):111-1119.
[11]Groden J,Thliveris A,Samowitz W,etal.Identification andcharacterization of the familial adenomatous polyposis coli gene[J].Cell,1991,66(3):589-600.
[12]Zhang J,Cao H,Zhang B,etal.Berberine potently attenuates intestinal polyps growth in ApcMin mice and familial adenomatous polyposis patients through inhibition of Wnt signalling[J].J Cell Mol Med,2013,17(11):1484-1493.
[13]Laurent S,Franchimont D,Coppens JP,etal.Familial adenomatous polyposis:clinical presentation,detection and surveillance[J].Acta Gastroenterol Belg,2011,74(3):415-420.
[14]Bertario L,Russo A,Sala P,etal.Multiple approach to the exploration of genotype-phenotype correlations in familial adenomatous polyposis[J].J Clin Oncol,2003,21(9):1698-1707.
[15]Lazar AJ,Tuvin D,Hajibashi S,etal.Specific mutations inthe beta-catenin gene ( CTNNB1) correlate with local recurrence inspo-radic desmoid tumors[J].Am J Pathol,2008,173(5):1518-1527.
[16]Bertario L,Russo A,Sala P,etal.Genotype and phenotype factors as determinants of desmoid tumors in patients with familial adenomatous polyposis[J].Int J Cancer,2001,95(2):102-107.
[17]Li M,Gerber DA,Koruda M,etal.Hepatocelluar carcinoma associated with attenuated familial adenomatous polyposis:a case report and review of the literature[J].Clin Colorectal Cancer,2012,11(1):77-81.
[18]Claes E,Renson M,Delespesse A,etal.Psychological implications of living with familial adenomatous polyposis[J].Acta Gastroenterol Belg,2011,74(3):438-444.
[19]Lahat G,Nachmany I,Itzkowitz E,etal.Surgery for sporadic abdominal desmoid tumor:is low/no recurrence an achievable goal?[J].Isr Med Assoc J,2009,11(7):398-402.
[20]Barrow P,Khan M,Lalloo F,etal.Systematic review of the impact of registration and screening on colorectal cancer incidence and mortality in familial adenomatous polyposis and Lynch syndrome[J].Br J Surg,2013,100(13):1719-1731.
[21]Sturt NJ,Phillips RK,Clark SK.High-dose tamoxifen and sulindac as first-line treatment for desmoid tumors.[J]Cancer,2004,101(3):652.
[22]Bülow S,Sφndergaard JO,Moesgaard F.Familial adenomatous polyposis[J].Ugeskr Laeger,1990,152(37):2628-2632.
[23]Garbay D,Le Cesne A,Penel N,etal.Chemotherapy in patients with desmoid tumors:a study fromthe French Sarcoma Group (FSG)[J].Ann Oncol,2012,23(6):182-186.
[24]Kim B,Giardiello FM.Chemoprevention in familial adenomatous polyposis[J].Best Pract Res Clin Gastroenterol,2011,25(4/5):607-622.
[25]Middleton SB,Phillips RK.Surgery for large intra-abdominal desmoid tumors:report of four cases[J].Dis Colon Rectum,2000,43(12):1759-1762.
[26]Heinrich MC,McArthur GA,Demetri GD,etal.Clinical and molecular studies of theeffect of imatinib on advanced aggressive fibromatosis (desmoid tumor)[J].J Clin Oncology,2006,24(7):1195-1203.
[27]Tudyka VN,Clark SK.Surgical treatment in familial adenomatous polyposis[J].Ann Gastroen terol,2012,25(3):201-206.
《醫學綜述》雜志被美國化學文摘社收錄
美國化學文摘社(CAS)是全球最大、最全面的化學和科學信息數據庫提供機構,是美國化學學會(ACS)的分支機構。美國《化學文摘》是涉及學科領域最廣、權威性最高、影響力最大、實用性最強、收集文獻類型最全、提供檢索途徑最多、部卷也最為龐大的一種著名的世界性檢索工具。
《醫學綜述》雜志接到美國化學文摘社(CAS)中國文獻處理中心通知,經過嚴格評估,本刊被列入美國化學文摘社2012年中國期刊收錄名單,進入國際著名文摘數據庫。由此,標志著本刊辦刊水平和學術地位得到了國際化學文獻檢索權威機構的認可。這是廣大作者和全體編審人員的榮耀,是億萬讀者的福音,也是我們跨出了與國際交流的第一步,實現了成為國際權威數據庫來源期刊的工作目標。
《醫學綜述》歡迎您閱讀,歡迎您賜稿,歡迎您指導。
Familial Adenomatous Polyposis Superimposed Desmoid Tumor:A Report of Two Cases and Review of the LiteraturesHUANGJin-xi,WANGCheng-hu,YUANWei-wei,CHENBei-bei,ZHOUYi.(DepartmentofGeneralSurgery,theCancerHospitalAffiliatedofZhengzhouUniversity,Zhengzhou450003,China)
Key words:Familial adenomatous polyposis; Desmoid tumor; Colorectal polyposis gene
收稿日期:2014-12-27修回日期:2015-07-02編輯:辛欣
doi:10.3969/j.issn.1006-2084.2015.20.073
中圖分類號:R735.3
文獻標識碼:A
文章編號:1006-2084(2015)20-3839-03

