腦出血灶周HIF-1α 的表達與腦水腫的實驗研究
董 靜,劉 群
缺氧誘導因子-1(hypoxia inducible factor-1,HIF-1)是由低氧所誘導細胞產生的一種轉錄因子,于1992 年由Semenza 和Wang 在研究缺氧誘導的EPO 基因時,從細胞核中提取發現,參與氧穩態失衡調節的一個核轉錄因子[1]。HIF-1 的生理活性主要取決于HIF-1α 亞基的活性和表達[2]。HIF-1α 常氧條件下由于快速降解而無法檢測到,缺氧條件下,HIF-1α 與HIF-1β 形成有活性的HIF-1 二聚體,誘導其下游靶基因的表達,通過調節一系列靶基因來調節血管舒張和新生血管生成、紅細胞生成和抗炎癥反應,從而改善腦組織缺氧和損傷。近年來研究已證實,HIF-1α 在腦缺血的保護性反應中起重要的作用,但有學者推測ICH 后,HIF-1α 的過量表達可能參與神經細胞凋亡等的病理過程,并加重了腦出血(ICH)后腦損傷的過程。近期有學者在動物研究中發現,HIF-1α 與ICH 后水腫密切相關。本研究采用人腦出血灶周組織,應用免疫組化SP 法觀察血腫周邊神經組織中HIF-1α 蛋白的表達情況,并探討腦水腫程度與HIF-1α 蛋白表達之間的關系。
1 材料和方法
1.1 一般資料 2013 年1 月~2013 年12 月在吉林醫藥學院附屬醫院神經外科收治的高血壓腦出血患者24 例,均行開顱經顳葉入路血腫清除術。均符合全國第四屆腦血管病學術會議制定的ICH診斷標準,全部為基底節區出血。
1.2 標本的抽取 全部患者在經顳葉皮質“造瘺”清除血腫時,將入路通道范圍內緊鄰血腫的腦組織保存下來,做為病例組標本,大小約0.1~0.15 mm3,病例組按發病時間分為<6 h、6~24 h、24 h~3 d、>3 d 組。將部分患者皮質“造瘺”起始處即遠離血腫2~3 cm 左右腦組織保留下來,做為對照組標本,共6 例。將所取的腦組織分兩部分,一部分用液氮運送至-70 ℃冰箱凍存,一部分組織于10%福爾馬林固定液中浸泡固定后石蠟包埋。連續切片進行HE 染色和HIF-1α 免疫組化染色。另取血腫周邊腦組織約100 mg 進行腦組織含水量測定。
1.3 HIF-1α 免疫組化SP 法檢測 鼠抗人HIF-1α 多克隆抗體購于北京博奧森生物技術有限公司,DAB 顯色試劑盒、SP-9710 試劑盒均購于福州邁新生物技術開發限公司。免疫組化過程按試劑盒說明進行,以PBS 代替一抗作陰性對照。免疫組化染色細胞質陽性為棕黃色結果,胞核呈藍色,胞漿呈紅色,紅細胞呈桔紅色,其它成分呈深淺不同紅色。數碼相機拍照,在血腫周圍和對照組隨機各取5 個視野,圖像采用Motic Images advanced 3.2 彩色圖像分析系統,所測得的灰度值越大陽性越弱,灰度值越小陽性越強。
1.4 RT-PCR 方法檢測HIF-1αmRNA 定量Rtizol 裂解細胞后抽提總RNA,取1 ml 測光密度值,DNA 消化。使用日本Toyobo 公司試劑盒逆轉錄體系進行cDNA 合成.引物由北京鼎國昌盛生物技術有限公司設計合成,序列如下:HIF-1α 上游:CCTATGTAGTTGTGGAAGTTTATGC;HIF-1α 下 游:ACTAGGCAATTTTGCTAAGAATG。PCR 體系:cDNA:2 μl,Taq 酶0.25 μl,總反應體系:25 μl。PCR循環參數:94℃預變性,2 min,94 ℃變性,30 s,30 次循環,55 ℃退火,30 s,30 次循環,72 ℃延伸,1 min,30 次循環。反應后將制備好的cDNA 放-20 ℃冷凍保存。擴增產物經瓊脂糖凝膠電泳分析。通過凝膠成像系統進行拍照,記錄結果。產物定量分析:利用ABI PRISM 7700 Sequence Detector,臨測每個循環的熒光強度,通過Ct 值和標準曲線的分析對起始模板進行定量分析。
1.5 腦組織含水量測定 采用干濕重法測定腦組織含水量,取腦組織約150 mg,電子天平稱濕重后置于100 ℃烤箱烘烤24 h 至恒重,稱取干重。計算公式:按Blliot 公式腦組織含水量(%)=(濕重-干重)/濕重×100%,精確度為0.11 mg。
2 結果
2.1 免疫組化檢測HIF-1α HIF-1α 主要在神經元、神經膠質細胞的胞核中表達,其中胞核染色陽性的細胞多聚集在靠近血腫邊緣的壞死區及血管相對稀少的區域,胞質中也有表達,DAB 染色成棕褐色(見圖1、圖2)。對照組及出血灶周人腦組織中HIF-1α 的灰度值測定(見表1),對照組與6 h 組相比無差異(P >0.05),對照組與出血組各組相比均有統計學意義(P <0.05),且出血組各組之間亦有差異(P <0.05)。在出血6 h 后,HIF-1α 的陽性細胞增加,灰度值減少,24 h~3 d 陽性細胞數最多,灰度值最低,之后逐漸上升。

圖1 6~24 h 組HIF-1α 陽性表達細胞(SP×400)
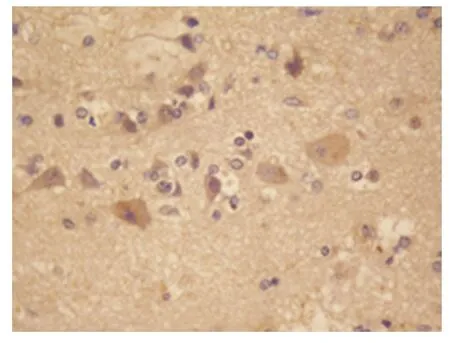
圖2 24 h~3 d HIF-1α 陽性表達細胞(SP×400)
表1 各組HIF-1α 灰度值的比較(,n=5)

表1 各組HIF-1α 灰度值的比較(,n=5)
與對照組相比,aP >0.05;與<6 h 組比較,bP <0.05;與6~24 h 組比較,cP <0.05;與24 h~3 d 組比較,dP <0.05
表2 ICH 后HIF-1α mRNA 表達()

表2 ICH 后HIF-1α mRNA 表達()
與對照組比較* P <0.05

表3 各組腦組織含水量的比較
2.2 RT-PCR 經PCR 擴增后,在近145bp 處出現HIF-1α mRNA 表達產物,分別于各時間點觀察對照組及出血組HIF-1α mRNA 的表達,HIF-1α 的PCR 產物相對定量分析結果(見表2、圖3),結果可見對照組中有少量表達,血腫灶周6 h 出現HIF-1α陽性細胞,24 h 進一步增加,24 h~3 d 時HIF-1α 陽性細胞表達達高峰,3 d 后仍可見HIF-1α 的表達,但較3 d 時下降(兩組相比均有統計學意義,P <0.05)。
2.3 ICH 后腦組織含水量變化 見表3,在出血6 h 內含水量即開始增高,24 h 后較明顯增高,3 d左右達到峰值,之后減輕(P <0.05)。
2.4 ICH 組HIF-1α 灰度值與腦組織水含量關系 用直線回歸進行分析顯示(見圖4):ICH 后各時間點HHIF-1α 灰度值與腦組織水含量的變化呈負的直線相關關系(r=-0.85849,P <0.001),24 h~3 d 顯著降低(P <0.05);3 d 達到最低;HIF-1α 含量與腦組織含水量均表現出一致的時相依賴性變化,即隨著HIF-1α 表達的增加腦組織水含量也增加,且相關關系非常密切。
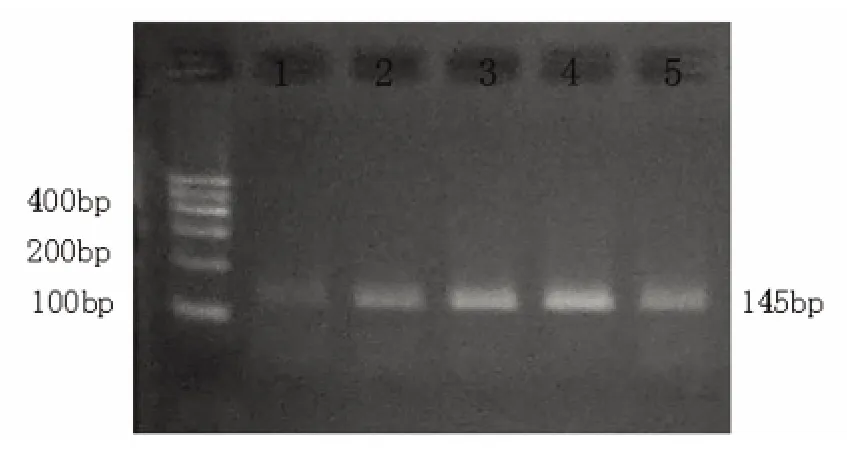
圖3 HIF-1α 的PCR 產物相對定量分析

圖4 出血灶周腦組織含水量與HIF-1α 灰度值表達
3 討論
本研究發現:HIF-1α 在ICH 出血灶邊緣及壞死區均有明顯表達,主要表達于神經細胞核,胞質中也有表達,這和國外一些學者的研究結果基本一致[3],且隨著出血時間的延長,HIF-1α 表達的陽性率及表達強度也逐漸增加,3 d 達高峰,后逐漸下降,出血后不同時間點陽性表達率比較(P <0.05),有顯著性差異,提示HIF-1α 的表達與神經細胞缺血、缺氧的時間密切相關[4,5]。腦組織缺血、缺氧均可誘導ICH周圍缺血區HIF-1α 表達增加[6]。
近二十余年來,動物實驗已經證實,ICH 后血腫形成分泌的凝血酶可導致ICH 后腦水腫的形成和神經功能的損傷[7]。1999 年,Xi 等[8]在實驗中再一次證實凝血酶可導致ICH 后大鼠腦組織水腫。綜上所述,現已達成專家共識。凝血酶本身是引起ICH 早期腦水腫的重要因素。近年來,有學者證明在ICH過程中,凝血酶大量釋放,能刺激HIF-1α 蛋白的表達[9]。Richard 等[10]在體外平滑肌細胞培養的研究中發現,在正常氧分壓下,凝血酶可以上調HIF-1α的表達。凝血酶導致ICH 后腦水腫的病理生理機制較為復雜,目前已進行了一些相關動物實驗研究,提出凝血酶對BBB 的破壞和對神經細胞的毒性作用可能是ICH 后腦水腫形成的重要機制,也有動物實驗表明,凝血酶及HIF-1α 共同參與ICH 后腦水腫的形成。
以往的研究表明,ICH 6 h 后,血腫周圍開始出現水腫,24 h~3 d 內腦水腫的程度加重,一般認為,ICH 后3 d 水腫程度達到高峰。我們在實驗中也觀察到,HIF-1αmRNA 在ICH 后3 d 陽性表達,顯著高于其它時間點。而且我們經過對ICH 后不同時間HIF-1α 表達的情況與腦水腫的程度進行相關性分析,結果顯示HIF-1α 的表達與腦水腫的程度成正相關。國內個別研究有類似發現[11],HIF-1α 表達主要位于出血血腫壞死邊緣區域的腦組織,24 h 后HIF-1α 陽性表達率為94.4%,明顯高于其它時間,提示HIF-1α 的表達與腦組織水腫程度關系密切。ROS已被證實與腦組織受損后神經細胞發生水腫有直接關系,因而HIF-1α 表達增加的情況與腦水腫的程度有相關性可能與此機制有關。
一般認為低氧環境是誘導HIF-1α 表達增強的一個重要因素[12]。在常氧條件下,細胞漿內HIF-1α的表達水平很低,但在低氧條件下,HIF-1α 卻大量集聚并轉移至細胞核中。我們的實驗也證實ICH 后HIF-1α 主要表達于灶周神經細胞胞核,染色陽性的細胞多聚集在靠近血腫邊緣的壞死區及血管相對稀少的區域,和國內某些研究一致。本實驗研究結果顯示:ICH 后采用RT-PCR 法能明顯的檢測到HIF-1α 的表達,而對照組未見HIF-1α 蛋白信號,提示在ICH 過程中,存在其他調節HIF-1α 表達的因素,低氧可能并非誘導HIF-1α 蛋白表達增強的唯一機制。
據近年的研究,認為HIF-1α 對出血性卒中有一定的保護作用。HIF-1α 激活轉錄多種靶基因,增加缺氧組織的氧氣供應,維持內環境穩定,對機體形成保護作用。ICH 后,HIF-1α 可以通過靶基因促進VEGF 表達,促使新生血管生成[13,14],改善腦血流動力學,使腦缺血得以迅速恢復,保護腦細胞。ICH后,出血灶周邊腦組織處于持續的缺血缺氧狀態,而缺氧可使多種基因差異表達,引起相關蛋白及細胞因子變化的連鎖反應,導致腦水腫,顱內壓增高且啟動腦組織細胞的抗損傷和修復反應[15]。HIF-1α 是缺氧狀態下血管生成的核心調控因子,通過影響其他生長因子的表達,而直接參與血管生成的全過程[16,17],在這一過程中因對缺氧的適應性可能是腦組織抗損傷和修復的關鍵。而細胞對缺氧的適應性主要靠HIF-1α 調節[18],它能減少細胞發生凋亡的數目有助于神經功能的恢復。
Papandreou 等[19]研究發現,低氧時HIF-1α 可通過誘導丙酮酸脫氫酶激酶-1 的表達,使得細胞內氧張力增高,改善ICH 后的能量供應,腦損傷減輕。另外,Helton 等[20]通過敲除大鼠大腦HIF-1α 基因發現,不僅未增加腦缺氧缺血損傷,反而減輕了缺氧缺血后腦損傷,這一結果使我們對HIF-1α 的腦保護作用仍有待進一步探討。普遍認為,輕度缺氧時,HIF-1α 產生缺氧耐受性,發揮神經保護作用;長期重度缺氧時,誘導神經細胞凋亡,具有神經毒性作用[21,22]。實驗表明[23]嚴重長時間缺氧能使HIF-1α去磷酸化,去磷酸化的HIF-1α 導致p53 穩定性增加,介導缺氧誘導的細胞凋亡。綜上可見,HIF-lα 具有雙重調節作用,在不同的缺氧狀態、對細胞發揮著保護或促凋亡的作用,兩者誰占主導與缺氧嚴重程度有關[24]。
目前HIF-1α 在神經系統疾病中的研究正在成為熱點,HIF-1α 在ICH 中所發揮的作用,是繼發性缺血損傷還是誘導血管新生來促進缺血周邊組織的側枝循環以改善供血,在ICH 時如何調控HIF-1α 的表達值得今后研究。
[1]Flashman E,McDonough MA,Schofield CJ.OS-9:another piece in the HIF complex story[J].Mol Cell,2005,17(4):472-473.
[2]Brown JM,Wilson WR.Exploiting tumor hypoxia in cancer treatment[J].Net Raw Cancer,2004,4(6):437-447.
[3]Sharp ER,Bergeron M,Bemaudin M.Hypoxia-inducible factor in brain[J].Adv ExpMed Biol,2001,502:273-291.
[4]Bemaudin M,Nedelec AS,Divoux D,et al.Normobaric hypoxia induces tolerance to focal cerebral ischemia in association with all increased expression of hypoxia-inducible factor-l and its target genes,erythropoietin in and VEGF in the adult mouse brain[J].J Cerebra Blood Flow Metal,2002,22(47):393-403.
[5]Chevez JC,Lamanna JC.Activation of hypoxia-inducible factor-1 in the rest cerebral cortex after transient global ischemia:potential role insulin like growth factor-1ɑ[J].J Neurosis,2002,22(20):8922-8931.
[6]Marti HJ,Bemaudin M,Bellail A,et al.Hypoxia-induced vascular endothelial growth factor expression precedes neovascularization after cerebral ischemia[J].Am J Pathos,2000,156(3):965-976.
[7]Hua Y,Xi G,Keep RF,et al.Complement activation in the brain after experimental intracerebral hemorrhage[J].Neurosurg,2000,92:1016-1622.
[8]Xi G,Hua Y,Bhasin RR,et al.Mechanisms of edema formation after intracerebral hemorrhage,effects of extravasated red blood cells Ollblood flow and blood-brain barrier integrity[J].Stroke,2001,32:2932-2938.
[9]Jiang Y,Wu J,Keep RF,et al.Hypoxia-Inducible Factor-1 a Accumulation in the Brain After Experimental Intracerebral Hemorrhage[J].Cerebral Blood Flow Metab,2002,22(6):689-696.
[10]Richard DE,Berra E,Pouyssegur J.Nonhypoxic pathway mediates the induction of hypoxia-inducible factor lalpha in vascular smooth muscle cells[J].J Biol Chem,2000,275(35):26765-26771.
[11]Du F,Wu XM,Gong Q,et al.Hyperthermia conditioned atrocity-cultured medium protects neurons from ischemic injury by the up-regulation of HIF-1 alpha and the increased anti-apoptotic ability[J].Euro J Pharmacology,2011,666(1/2/3):19-25.
[12]Schumacker PT.Hypoxia-inducible factor-1 (HIF-1)[J].Crib Care Med,2005,33(12):4232-4251.
[13]Yeh SH,Ou LC,Gean PW,et al.Selective inhibition of early but not late-expressed HIF-1α is neuroprolective in rats after focal ischemic brain damage[J].Brain Pathos,2011,2(3):249-262.
[14]Chen C,Ostrwski RP,Zhou C,et al.Suppression of hypoxia inducible factor-1 alpha and its downstream genes reduces acute hyperglycemia hemorrhagic transformation in a rat model of cerebral ischemic[J].J Neurosis Res,2010,89(9):2046-2055.
[15]Piret JP,Mottet D,Raes M,et al.Is HIF-l alpha a proof all antiapoptotic protein7[J].Brioche Pharmacology,2002,64(5/6):889-892.
[16]Hirota K.Hypoxia-indelible factor l,amasser transcription factor of cellular hypoxic gene expression[J].J Amnesty,2002,16(2):150-159.
[17]Huang LE,BunnHF.Hypoxia-indelible factor and its biomedical relevance[J].J Biol Chem,2003,278(22):19575-19578.
[18]Hammond EM,Garcia AJ.The role 0f p53 in hypoxia-induced apoptosis[J].Brioche Biolphys Ras Common,2005,331(3):718-725.
[19]Papandreou I,Cairns RA,Fontana L,et al.HIF-I mediates adaptation to hypoxia by actively down regulating mitochondrial oxygen consumption[J].Cell Metal,2006,3(3):187-197.
[20]Helton R,Cui J,Scheele JR,et al.Brain-specific knock-ore 0f hypoxia-inducible factor-1 alpha reduce rather than increases hypoxicischemic damage[J].J Neuroses,2005,25(16):4099-4107.
[21]Matsuda T,Abe T,Wu JL,et al.Hypoxia-inducible factor-1 DNA induced angling gneiss in a rat cerebral ischemia model[J].Neural Res,2005,27(5):503-508.
[22]Liu J,Narasimhan P,Yu F,et al.Neumprotection by hypoxic preconditioning involves oxidative stress-mediated expression of hypoxia-inducible factor and erythropoietin[J].Stoke,2005,36(6):1264-1269.
[23]Hammond EM,Garcia AJ.The role of p53 in hypoxia-induced apoptosis[J].Brioche Biolphys Raps Common,2005,331(3):718-725.
[24]Chen W,Ostrowski RP,Obenaus A,et al.Prudent or prosurvival:two facets of hypoxia inducible fator-1 in prenatal brain injury[J].Exp Neural,2009,16:7-15.

