醒腦靜輔助卡馬西平治療腦卒中后繼發性癲癇的臨床療效及安全性評價
王 麗,唐冬云,阮玉泉
(恩施市中心醫院神經內科,湖北 恩施 445000)
醒腦靜輔助卡馬西平治療腦卒中后繼發性癲癇的臨床療效及安全性評價
王麗※,唐冬云,阮玉泉
(恩施市中心醫院神經內科,湖北 恩施 445000)
摘要:目的探討醒腦靜輔助卡馬西平治療腦卒中后繼發性癲癇(PSE)的臨床療效及安全性。方法將2010年12月至2013年12月恩施市中心醫院收治的80例繼發性癲癇患者按照隨機數字表法分為兩組,各40例。對照組僅給予卡馬西平進行治療,每次0.1 mg,口服,每日3次;觀察組在此基礎上給予醒腦靜進行治療,20 mL醒腦靜注射液與100 mL葡萄糖溶液進行靜脈滴注,每日1次。7 d為1個療程,連續治療4個療程。比較兩組患者的臨床療效,治療前后癇樣放電和累及導聯數,生活質量及不良反應發生率。結果觀察組總有效率為92.5%(37/40),對照組為70.0%(28/40),差異有統計學意義(P<0.05)。治療后對照組癇樣放電與累及導聯數分別為(11.2±4.4) t/180 s、(5.4±1.4)/180 s,觀察組分別為(6.9±1.3) t/180 s、(3.0±0.6)/180 s,均較治療前顯著降低,且治療后觀察組上述指標均顯著小于對照組(P<0.01)。治療后觀察組生活質量評分顯著優于對照組(P<0.01);觀察組不良反應發生率和對照組分別為10.0%(4/40)和20.0%(8/40),差異無統計學意義(P>0.05)。結論醒腦靜輔助卡馬西平治療繼發性癲癇療效顯著,安全性高。
關鍵詞:腦卒中后繼發性癲癇;醒腦靜;卡馬西平;臨床療效;安全性
腦卒中后繼發性癲癇(post stroke pilepsy,PSE)屬于我國癲癇患者中最為常見的一種臨床類型,多發于中老年人群[1]。據相關統計數據顯示,我國PSE患者約占全部癲癇患者的10%,這與國外報道結果較為接近[2]。當PSE發生后,不僅會在腦卒中的基礎上額外加劇患者的腦損傷程度,還會誘發患者出現高血壓及高血糖等多系統全身性疾病,起病之前多伴隨前驅癥狀,其臨床表現為頭痛頭暈、短暫性肢體麻木以及眩暈等不良癥狀,對患者正常生活造成了極大影響。目前,臨床治療PSE的最常見方法仍為藥物治療。本研究將醒腦靜輔助卡馬西平用于PSE治療,取得了較為滿意的臨床效果,報道如下。
1資料與方法
1.1一般資料選擇2010年12月至2013年12月恩施市中心醫院收治的PSE患者80例,均符合我國第四屆腦血管會議中制訂的腦卒中及國際抗癲癇聯盟所提出的癲癇發作與癲癇綜合征的診斷標準[3]。排除具有其他疾病或合并癥、接受可影響效應觀測指標治療、嚴重心、肝、腎損害、精神病等患者。將上述患者按照隨機數字表法分為對照組和觀察組,每組40例,年齡37~79歲,病程1~8年。對照組中男22例、女18例,平均年齡(60±7)歲,平均病程(5.4±0.4)年;觀察組中男24例、女16例,平均年齡(60±6)歲,平均病程(5.4±0.3)年。兩組PSE的發生情況:對照組,早發性21例、遲發性19例;缺血性18例、出血性22例;觀察組,早發性22例、遲發性18例;缺血性17例、出血性23例。兩組患者在性別、年齡、病程及PSE的發生情況等方面比較差異均無統計學意義(P>0.05),具有可比性。本研究經醫院倫理委員會批準,患者知情同意并簽署知情同意書。
1.2治療方法兩組患者均給予腦卒中常規治療,包括抗凝、抗血小板聚集、活血化痰、腦保護以及擴張血管等方面的治療策略。對照組在此基礎上給予卡馬西平(上海復旦復華藥業有限公司生產,批號:20040123)治療,每次0.1 mg,口服,每日3次;觀察組在對照組治療的基礎上聯合20 mL醒腦靜注射液(河南天地藥業股份有限公司生產,批號:20140519)加入100 mL葡萄糖溶液進行靜脈滴注,每日1次。兩組7 d為1個療程,連續治療4個療程。比較兩組臨床療效、治療前后癇樣放電、累及導聯數、生活質量及不良反應發生率。
1.3臨床療效判定標準控制:未出現任何癲癇發作;顯效:癲癇發作頻率減少75%~90%;有效:癲癇發作頻率減少50%~74%;無效:癲癇發作頻率減少<50%[4-5]。總有效率=(控制+顯效+有效)例數/總例數×100%。
1.4生活質量評價方法主要根據SF-36生活質量評價量表對患者術后生活質量進行評價,具體方法見表1[6]。

表1 SF-36健康量表維度分計算公式

2結果
2.1兩組患者臨床療效比較經治療,觀察組總有效率為92.5%,高于對照組的70.0%(χ2=6.458,P=0.043),觀察組臨床療效顯著優于對照組,差異有統計學意義(Z=5.373,P<0.05),見表2。

表2 兩組腦卒中后繼發性癲癇
對照組:僅給予卡馬西平進行治療;觀察組:在對照組基礎上給予醒腦靜進行治療
2.2兩組患者治療前后癇樣放電與累及導聯數比較治療前兩組癇樣放電與累及導聯數比較差異無統計學意義(P>0.05),兩組治療后癇樣放電與累及導聯數較治療前均顯著降低(P<0.01),且治療后觀察組上述指標均顯著小于對照組(P<0.01),見表3。
2.3兩組患者術后生活質量比較根據SF-36評分標準,觀察組術后生活質量各評分顯著高于對照組(P<0.01),見表4。
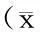
表3 兩組腦卒中后繼發性癲癇患者治療前后癇樣放電與累及導聯數比較 ±s)
對照組:僅給予卡馬西平進行治療;觀察組:在對照組基礎上給予醒腦靜進行治療

表4 兩組腦卒中后繼發性癲癇患者術后生活質量比較 ±s,分)
對照組:僅給予卡馬西平進行治療;觀察組:在對照組基礎上給予醒腦靜進行治療
2.4兩組患者不良反應發生率比較對照組出現頭暈、頭痛、惡心、嘔吐發生例數分別為2、1、3、2例,總發生率為20.0%(8/40);觀察組分別為1、1、0、2例,總發生率為10.0%(4/40),兩組不良反應發生率比較差異無統計學意義(χ2=1.569,P=0.210)。
3討論
PSE可發生于腦卒中后的任何時間段內,然而臨床上多以早發性PSE患者居多,據相關統計數據顯示,早發性PSE患者約占PSE總患者數的60%以上[7]。腦卒中后,即可在急性期出現腦組織缺血及血氧狀態,同時還伴隨腦細胞鈉泵衰竭,當Na+大量內流后則會在一定程度上改變神經元細胞膜的穩定性,且神經元除了極化過度,或區域性缺血部位的神經元喪失了部分與周圍神經細胞間產生關聯的功能,最終導致癲癇性放電現象的發生[8]。
在先行積極治療腦卒中的基礎上再合理選擇藥物進行抗癲癇治療是當前臨床上普遍認可治療PSE的流程及途徑[9]。常規抗癲癇藥物,如卡馬西平可使70%~80%的癲癇發作頻數得到有效控制,然而臨床實踐研究表明[10],仍然有約25%的患者治療效果不理想。此外,還有報道顯示[11],卡馬西平用于抗癲癇治療,可導致血常規及肝腎功能出現異常,進而使患者的治療依從性偶爾出現不理想的狀況。另外,對部分性發作的癲癇患者而言,采用新型抗癲癇類藥物醒腦靜輔助卡馬西平治療的臨床研究結果表明,醒腦靜不僅表現出了較為理想的患者耐受度、低程度的不良反應以及更少藥物間的相互反應等,甚至對某些難治性癲癇患者的治療效果也較為理想[12]。醒腦靜可對腦細胞的電壓依賴性通道產生阻斷作用,不僅能很好地阻止神經元發生放電反應,有效降低突觸傳遞的興奮沖動,促使K+內流以糾正神經元細胞膜的穩定性,同時還能有效緩解神經元過度發生極化現象[13]。
本研究結果顯示,兩組治療后癇樣放電與累及導聯數較治療前均顯著降低(P<0.01),且治療后觀察組上述指標均顯著小于對照組(P<0.01)。兩組不良反應發生率差異無統計學意義(P>0.05)。綜上所述,醒腦靜輔助卡馬西平治療PSE療效顯著,安全性較高。
參考文獻
[1]王慶祝,李搖宇,司有偉,等.83例腦卒中后癲癇臨床分析[J].安徽醫藥,2013,17(1):83-84.
[2]萬繼峰,陸尤,任歆,等.不同類型卒中后癲癇的發病特點[J].中國腦血管病雜志,2012,9(5):248-252.
[3]Kilpairict CJ,Davis SM,Hopper JL,etal.Early seizures after acute stroke risk of late seizurss[J].Arch Neurol,1992,49(5):507-510.
[4]蘇凌瓔,狄晴,余年,等.癲癇患者撤藥的研究現狀[J].中華神經科雜志,2012,45(4):268-270.
[5]吳月鵬,張顏波,李美藝,等.卒中后癲癇研究進展[J].中華神經醫學雜志,2010,9(11):1186-1188.
[6]孫家躍,孟現奇.393例抗癲癇藥物血藥濃度監測結果分析[J].安徽醫藥,2012,16(9):1363-1364.
[7]國家藥典委員會.臨床用藥須知[S].北京:中國醫藥科技出版社,2011:685.
[8]孟清,覃娜,饒家敏,等.拉莫三嗪治療腦卒中后繼發癲癇的療效及不良反應觀察[J].中國現代醫藥雜志,2013,15(5):48-50.
[9]羅榕,劉凌,司洋,等.拉莫三嗪治療癲癇的療效及安全性分析[J].現代預防醫學,2011,16(21):761-762.
[10]趙秀麗,李志一,劉宇,等.拉莫三嗪引起不良反應[J].中國誤診學雜志,2011,23(36):599-603.
[11]夏莉,何瑜玢,顏起文,等.拉莫三嗪治療成人部分性發作癲癇的臨床療效與安全性研究[J].卒中與神經疾病,2011,9(2):143-144.
[12]王艷,趙新利,吳新艷,等.奧卡西平與卡馬西平治療腦卒中后繼發性癲癇療效比較[J].新鄉醫學院學報,2014,31(4):312-313.
[13]侯蘊祈.奧卡西平與卡馬西平單藥治療腦梗死后遲發型癲癇的對照研究[J].中國當代醫藥,2010,17(15):52-53.
Clinical Efficacy and Safety Evaluation of Xingnaojing Injection Assisted Carbamazepine Therapy for Post Stroke EpilepsyWANGLi,TANGDong-yun,RUANYu-quan.(DepartmentofNeurology,CenterHospitalofEnshi,Enshi445000,China)
Abstract:ObjectiveTo explore the clinical efficacy and safety of Xingnaojing assisted carbamazepine in the treatment of post stroke epilepsy(PSE).MethodsTotal of 80 secondary epilepsy patients admitted to Enshi Center Hospital from Dec.2010 to Dec.2010 were randomly divided into two groups:control group(40 cases) receiving carbamazepine treatment(0.1 mg/time,oral,3 times per day),observation group(40 cases) receiving Xingnaojing(i.v.20 mL with 100 mL glucose solution) treatment on the basis of the control group′s treatment.The clinical efficacy,epilepsy discharge and involved lead number and quality of life before and after treatment and the incidence of adverse reactions of the two groups were compared.ResultsThe clinical curative effect of the observation group was 92.5%(37/40),of the control group was 70.0%(28/40),the differences was statistically significant(P<0.05).After treatment,epileptiform discharge and the number of involved leads of the control group were (11.2±4.4) t/180 s,(5.4±1.4)/180 s,of the observation group were (6.9±1.3) t/180 s,(3.0±0.6)/180 s,which were all significantly lower than before treatment,and the observation group′s data were significantly less than that of the control group after treatment(P<0.01).After treatment,quality of life of the observation group was significantly better than the control group(P<0.01).The incidence of adverse reaction of the observation group and control group were 10.0%(4/40) and 20.0%(8/40),the difference was not statistically significant(P>0.05).ConclusionXingnaojing assisted carbamazepine treating PSE has obvious therapeutic effect and high safety.
Key words:Post stroke epilepsy; Xingnaojing; Carbamazepine; Clinical efficacy; Safety
收稿日期:2014-08-11修回日期:2015-03-18編輯:伊姍
doi:10.3969/j.issn.1006-2084.2015.17.066
中圖分類號:R741.05
文獻標識碼:A
文章編號:1006-2084(2015)17-3243-03

