負壓封閉引流術治療四肢軟組織嚴重擠壓傷的效果
楊 威 劉 楊 趙鳴雁
1.哈爾濱醫科大學附屬第一醫院ICU,黑龍江哈爾濱 150001;2.哈爾濱醫科大學附屬第一醫院骨科,黑龍江哈爾濱 150001
隨著工業文明的不斷進步,交通事故、建筑意外以及大型機械碾壓等使軟組織擠壓傷的發病率逐年增高。 軟組織擠壓傷常伴有開放性骨折,除造成局部組織感染、壞死外,組織溶解及壞死物質的吸收還會導致全身多器官功能障礙[1],包括急性腎損傷(AKI)、膿毒癥、全身炎癥反應綜合征(SIRS)以及多器官功能障礙綜合征(MODS)等,嚴重威脅患者的生命安全。負壓封閉引流術(VSD)是近年來廣泛用于控制感染的外科引流技術[2],但對于應用VSD 技術在軟組織擠壓傷后清除壞死組織,減輕全身中毒癥狀的報道較少。為此,本研究選取哈爾濱醫科大學附屬第一醫院(以下簡稱“我院”)收治的四肢軟組織擠壓傷患者,清創后行VSD 引流,觀察其對全身中毒癥狀的改善作用,取得滿意療效,現報道如下:
1 資料與方法
1.1 一般資料
選取我院2012 年10 月~2014 年10 月收治的四肢Gustilo Ⅲ型軟組織擠壓傷患者62 例。根據清創術后選擇VSD 引流或常規換藥治療分為觀察組(35 例)和對照組(27 例)。 兩組年齡、性別等一般資料比較,差異均無統計學意義(P >0.05),具有可比性。 見表1。本研究經醫院醫學倫理委員會批準,所有患者和/或家屬均知情同意并簽署知情同意書。
納入標準:①診斷明確的四肢擠壓傷外傷史;②受傷至清創開始時在6 h 以內;③軟組織損傷GustiloⅢ型[3],即皮膚、皮下組織和肌肉的廣泛損傷,合并或不合并重要血管神經的損傷;④患者年齡>18 周歲。排除標準:①伴有致死性合并傷,包括顱腦外傷、頸脊髓損傷以及重要的內臟器官損傷;②既往有周圍血管病變;③合并糖尿病、甲亢等內分泌系統疾病;④伴有腎小球腎炎、尿毒癥等泌尿系統疾病;⑤伴有凝血功能異常的血液系統疾病。

表1 兩組一般資料比較
1.2 治療方法
1.2.1 手術治療 入院時出現休克患者積極抗休克治療,待休克糾正后給予清創術,無休克患者急診行清創術。術中由淺至深,切除污染和失去活力的皮膚、皮下組織、筋膜、肌肉,對于肌腱、血管、神經盡量予以保留,避免遺漏死角和無效腔。 骨折端根據患者情況給予外固定架固定或鋼板內固定,清創結束后再次用生理鹽水、3%過氧化氫溶液及0.1%活力碘清洗傷口。對照組患者清創術后選擇常規換藥治療,觀察組患者清創術后選擇VSD 治療。 對照組患者用骨折周圍軟組織覆蓋骨折處,傷口敞開,用無菌敷料濕敷,術后根據傷口情況每日換藥1~2 次。 觀察組患者應用VSD技術,將明膠泡沫剪成與創腔相同形狀,略大于創腔,確保充分填入,避免留有空隙,兩根硅膠引流管從正常皮膚處穿出,并用4-0 縫合線固定,創口用生物半透膜覆蓋。 接通負壓-125~-450 mmHg(1 mmHg =0.133 kPa),觀察到明膠癟陷,半透膜下液體被迅速抽走為負壓有效標志。 VSD 每周期為5~7 d,到期后取出VSD,根據肉芽生長狀況決定更換VSD 或行皮瓣轉移術閉合傷口。兩組患者中對于局部傷口感染難以控制,雖經積極治療但全身狀況仍不斷惡化者,采用截肢術根除感染灶。
1.2.2 全身治療 術后除對受傷部位行局部治療外,還進行積極的全身治療,包括:①根據組織液的藥敏檢查結果全身應用敏感抗生素;②脫水、利尿減輕患肢腫脹;③維持水、電解質、酸堿平衡;④堿化尿液,保護腎功能,積極應用血液凈化腎臟替代治療;⑤合理的營養支持治療。
1.3 觀察指標
1.3.1 實驗室檢測指標 兩組患者均在術后48 h 抽取靜脈血,檢測白細胞(WBC)計數,鉀離子(K+)濃度,血肌酐(Scr)、尿素氮(BUN)水平。 留取尿液通過半定量方法,以(-)、(±)、(1+)、(2+)、(3+)表示尿蛋白水平,分別記為0、1、2、3、4 分。
1.3.2 并發癥發生率及病死率 術后觀察患者并發AKF、SIRS、膿毒癥及MODS 的比率,并計算患者病死率。 AKI 采用2005 年急性腎損傷網絡(AKIN)診斷標準[4]:48 h 內Scr 升高≥26.5 μmol/L,或Scr 達到基線水平的1.5 倍,或6 h 尿量持續<0.5 mL/(kg·h)。SIRS、膿毒癥、MODS 采用2012 年美國危重病學會(SCCM)和歐洲危重病學會(ESICM)推出的膿毒癥治療指南診斷標準[5],由2 名高年資醫生根據患者一般特點、炎癥參數、組織灌注參數和器官功能障礙參數進行綜合評定。1.3.3 預后指標 患者出院時統計患者清創術至二期皮瓣轉移術閉合傷口時間,住院時間,血液凈化次數,以及截肢率。 截肢率=(組內截肢例數/組內患者數)×100%。
1.4 統計學方法
應用SPSS 20.0 統計軟件對結果進行分析,正態分布計量資料以均數±標準差()表示,兩組間比較采用t 檢驗;計數資料以率表示,采用χ2檢驗。 以P <0.05 為差異有統計學意義。
2 結果
2.1 兩組實驗室檢測指標比較
兩組實驗室檢測指標比較,觀察組WBC 計數、血清K+濃度、Scr、BUN 及尿蛋白水平均優于對照組,差異有統計學意義(P <0.05)。 見表2。
表2 兩組實驗室檢測指標比較()

表2 兩組實驗室檢測指標比較()
注:WBC:白細胞計數;K+:鉀離子;Scr:血肌酐;BUN:血尿素氮
?
2.2 兩組并發癥發生率及病死率比較
兩組并發癥及病死率比較,觀察組AKF、SIRS、膿毒癥及MODS 的發生率均低于對照組,差異有統計學意義(P <0.05);兩組病死率比較,差異無統計學意義(P >0.05)。 見表3。
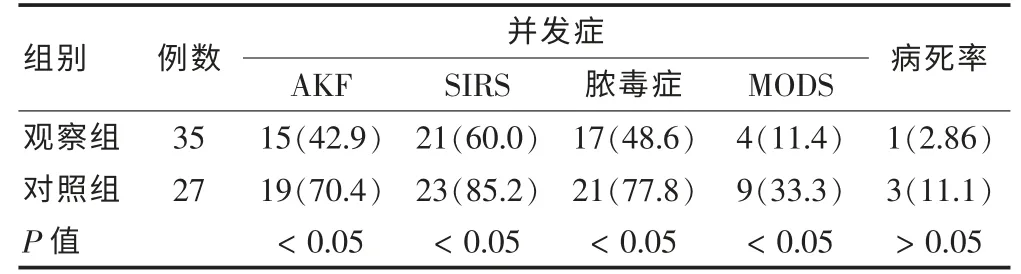
表3 兩組并發癥發生率及病死率比較[n(%)]
2.3 兩組預后指標比較
兩組因患者死亡,共4 例脫落,其中觀察組1 例和對照組3 例。 兩組預后指標比較,觀察組傷口閉合時間、血液凈化次數及住院天數均優于對照組,差異有統計學意義(P <0.05);兩組截肢率比較,差異無統計學意義(P >0.05)。 見表4。
表4 兩組預后指標比較()
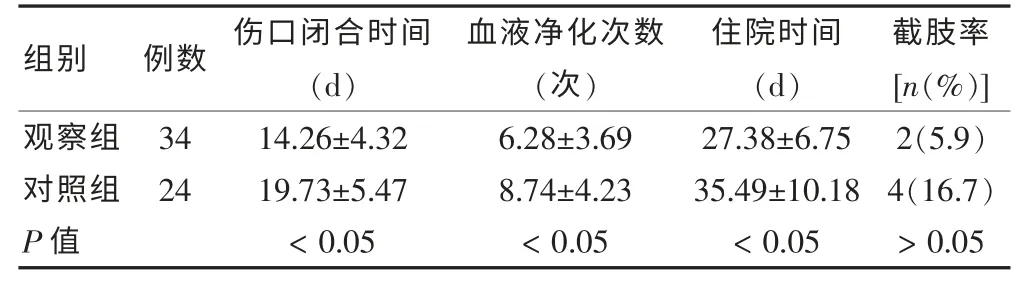
表4 兩組預后指標比較()
組別 例數 傷口閉合時間(d)血液凈化次數(次)住院時間(d)截肢率[n(%)]觀察組對照組P 值34 24 14.26±4.32 19.73±5.47<0.05 6.28±3.69 8.74±4.23<0.05 27.38±6.75 35.49±10.18<0.05 2(5.9)4(16.7)>0.05
3 討論
隨著軟組織擠壓傷發病率的上升,國內外學者對擠壓傷所致全身病理生理變化的研究也不斷深入。軟組織擠壓傷后,局部組織因缺血缺氧發生壞死,致壓物解除后缺血再灌注損傷導致局部橫紋肌溶解,使得局部有害物質進入血液循環, 患者出現以高鉀血癥、代謝性酸中毒為主要表現的水電失衡,同時出現肌紅蛋白尿、氮質血癥等急性腎衰竭表現,甚至發展為MODS,臨床上稱之為擠壓綜合征[6]。 有研究表明[7],雖然軟組織擠壓傷發展為擠壓綜合征的概率僅為10%,但導致急性腎衰竭的概率高達50%。 本研究中AKF的發生率明顯高于50%,可能與研究對象均為GustiloⅢ型重度軟組織損傷有關。 因此,軟組織擠壓傷后維持內環境的穩態成為亟待解決的問題。
VSD 技術是近年來用于控制外科感染的重要方法之一,其主要作用是通過灌洗清除局部代謝產物,利用半透膜提供一個密閉空間,使得肉芽組織盡快在明膠泡沫周圍生長,降低二次感染率[8]。對于軟組織擠壓傷,VSD 除能控制局部感染外,還能持續清除局部壞死組織。 國外研究表明[9],在軟組織損傷后,即使行擴大清創術,術后局部壞死產物也會增多,這是由于缺血再灌注后氧化應激所致的遲發型組織損傷,在清創術后正常組織還會發生壞死或者凋亡。 因此,即使對局部進行徹底清創,術后單純換藥治療仍難以降低毒素的吸收,局部的好轉并不能改善全身多器官的惡化[10]。 本研究結果分析,觀察組術后血鉀濃度和氮質血癥程度均較對照組有所降低(P <0.05),說明了VSD 技術能夠通過持續清除局部壞死物質從而降低毒素的吸收,改善全身中毒癥狀。 這與林武[11]應用VSD 治療骨筋膜室綜合征的報道結果相一致。
根據SCCM/ESICM 指南標準,SIRS、膿毒癥、MODS是序貫發生的病理過程。 由于SIRS 的診斷標準比較寬泛,因此從結果看兩組SIRS 的發病率均較高,但近年來普遍認為SIRS 并不是單一疾病,而是一種病理狀態用于判斷疾病的嚴重程度[12-13],兩組SIRS 的高發病率也提示在臨床中對于嚴重擠壓傷患者應早期由重癥監護病房(ICU)進行觀察和治療。 膿毒癥的治療原則是控制感染灶和全身支持治療[14-16]。 本研究中在局部應用VSD 治療的同時積極應用血液凈化治療,在術后48 h 即將血鉀降至正常水平,并且由膿毒癥發展為MODS 的比率明顯降低,說明了血液凈化治療在改善全身中毒癥狀中的重要作用。 在控制感染方面,除根據細菌培養和藥敏結果選用敏感抗生素外,還要注意VSD 半透膜可能形成的局部缺氧環境,防止厭氧菌感染[17-20]。 兩組患者病死率和截肢率比較差異無統計學意義(P >0.05),可能與樣本量較少有關,尚需擴大樣本量進一步研究。
綜上所述,負壓封閉引流技術能夠有效降低軟組織損傷后局部有害物質的吸收,減輕全身中毒癥狀,提高治療效果。
[1] 楊帆.物理負壓促進創面愈合機制的研究[D].武漢:華中科技大學,2010.
[2] Wang J,Zhang H,Wang S. Application of vacuum sealing drainage in the treatment of internal fixation instrument exposure after early postoperative infection [J]. Minerva Chir,2015,70(1):17-22.
[3] Fochtmann A,Mittlb?ck M,Binder H,et al. Potential prognostic factors predicting secondary amputation in thirddegree open lower limb fractures [J]. J Trauma Acute Care Surg,2014,76(4):1076-1081.
[4] Strametz R,Pachler C,Kramer JF,et al. Laryngeal mask airway versus endotracheal tube for percutaneous dilatational tracheostomy in critically ill adult patients [J].Cochrane Database Syst Rev,2014,6:CD009901.
[5] 岳金鳳,吳大瑋,李琛,等.以急性腎損傷網絡標準評估重癥監護病房患者急性腎損傷的發病率、 預后及死亡相關危險因素[J].中華醫學雜志,2011,91(4):260-264.
[6] Chunguang Z,Rigao C,Fuguo H,et al. Characteristics of crush syndrome caused by prolonged limb compression longer than 24h in the Sichuan earthquake [J]. Emerg Med J,2010,27(8):627-630.
[7] Smith J,Greaves I. Crush injury and crush syndrome:a review [J]. J Trauma,2003,54(5 Suppl):S226-S230.
[8] 林愛華,孫海軍.封閉負壓吸引治療重度多發傷合并盆腔嚴重感染[J].中 華急診醫學雜志,2013,22(6):581-582.
[9] Nishikata R,Kato N,Hiraiwa K. Oxidative stress may be involved in distant organ failure in tourniquet shock model mice [J]. Leg Med (Tokyo),2014,16(2):70-75.
[10] Demirkiran O,Dikmen Y,Utku T,et al. Crush syndrome patients after the Marmara earthquake [J]. Emerg Med J,2003,20(3):247-250.
[11] 林武.封閉負壓引流在骨筋膜室綜合征切開減壓中的應用觀察[J].中華危重癥醫學雜志:電子版,2012,5(5):36-38.
[12] 羅瓊湘,徐小強,陳贊美,等.降鈣素原在重癥患者合并膿毒癥早期診斷中的臨床價值[J].實用臨床醫藥雜志,2014,18(11):40-42.
[13] 吳安華,李春輝.重癥感染的診斷與治療[J].中華急診醫學雜志,2011,20(3):334-336.
[14] 楊曉明,蔣衛平,韋冰丹,等.封閉式負壓引流治療四肢創傷性軟組織缺損的臨床體會[J].臨床和實驗醫學雜志,2013,12(19):1556-1557.
[15] 張富軍,張建亮,宋戰鋒,等.負壓封閉引流-B 技術治療肢體碾挫傷21 例臨床觀察[J].疑難病雜志,2013,12(12):957-958,960.
[16] 呂濤,周潘宇,許碩貴,等.外固定支架聯合負壓封閉引流術治療下肢開放性粉碎性骨折合并嚴重軟組織損傷[J].中國醫藥導報,2012,9(2):150-151,154.
[17] 張耿明,李浩瑜.負壓封閉引流術治療四肢骨折合并嚴重軟組織損傷的臨床療效觀察[J].河北醫學,2013,19(5):713-715.
[18] 丁峰.膿毒癥合并急性腎損傷的治療[J].中國血液凈化,2010,9(7):352-356.
[19] 童偉林,唐芙蓉,項舟,等.負壓封閉引流術治療四肢骨折合并嚴重軟組織損傷的臨床效果觀察[J].中國醫藥導報,2013,10(29):62-64,67.
[20] 田恒進,盛輝,張治家,等.負壓封閉引流技術在治療復雜性軟組織缺損創面中的臨床應用[J].實用臨床醫藥雜志,2009,13(21):41-42.

