離子液體水溶液吸收模擬煙氣中SO2
王晨星,任樹行,侯玉翠,王一鳴,田士東,吳衛澤
(1北京化工大學化學工程學院,化工資源有效利用國家重點實驗室,北京 100029;2太原師范學院化學系,山西 太原 030031;3中南大學化學化工學院,湖南 長沙 410083)
引言
我國是多煤少油的能源消耗大國,一次能源消費中煤炭占據了70%左右,并且其中約有80%用于直接燃燒,為我國提供電力和熱能。然而,燃煤煙氣中含有大量的污染物,如粉塵、SO2、NOx、CO2,其中SO2的影響更為嚴重。SO2不僅會形成酸雨對環境造成污染[1],而且對人身體健康也會造成傷害。與此同時,SO2又是一種重要的化工原料。因此,對SO2的控制及回收具有重要意義。目前成熟的濕法脫硫技術有:鈣法脫硫技術[2]、氨法脫硫技術[3-4]、鈉法脫硫技術[5-6]等。雖然這些技術能解決一定的脫硫問題,但或多或少存在一些問題。如鈣法脫硫技術中,使用的石灰石脫硫會生產出大量的副產品石膏,易出現結垢、堵塞等問題[7],并且產生的石膏品位低,沒有回收利用的價值,從而形成二次污染[8];氨法脫硫技術中,使用的氨水本身就具有揮發性,在吸收過程中,不免會有氨以氣態形式進入大氣造成資源浪費和二次污染[9];鈉法脫硫技術中,長時間運行后,系統中的Na2SO4結晶易堵塞管道,而且在處理吸收后的富液時會產生大量的廢水[10]。研究發現,離子液體具有很多優良的性質,如蒸氣壓低、熱穩定性好、可設計性等[11-13],這使得離子液體在各個領域都有廣泛的應用。離子液體作為一種新型吸收劑,在煙氣脫硫方面也具有很強的優勢,具有處理 SO2濃度低、脫硫效率高、吸收速度快等優點[14]。Wu等[15]首次以四甲基胍和乳酸為原料,經過中和得到四甲基胍乳酸鹽[TMG]L,并進行SO2吸收實驗。研究發現,在常壓、45℃時,[TMG]L對體積分數為8%的SO2飽和吸收量可達0.982 mol SO2·(mol IL)-1。Wu等[16]研究了水對TMGL吸收SO2的影響,發現離子液體在吸收 SO2的過程中不斷吸收水分,使得離子液體黏度降低,增加了傳質效果。Yuan等[17]合成了一系列醇胺類離子液體,并考察了其對 SO2的吸收性能以及離子液體的再生循環利用情況,發現醇胺類離子液體可以有效地吸收SO2,并可以在較溫和的條件下進行再生。然而,目前離子液體還很少用于工業吸收SO2,缺少必要的放大數據。
本研究以乙醇胺和乳酸為原料,通過中和法制備了乙醇胺乳酸鹽[MEA]L,將所制[MEA]L稀釋配制成一定濃度的水溶液,直接用于放大脫硫實驗。建立了一套放大裝置,在裝置中進行脫硫實驗,考察了吸收劑含水量、煙氣中SO2濃度、氣液比、煙氣成分等對吸收過程的影響,以此獲得最佳實驗條件,并在此條件下進行吸收-解吸循環實驗,為工業應用提供放大數據。
1 實驗材料和方法
1.1 材料
乙醇胺,AR,阿拉丁試劑有限公司提供,質量分數 >99.0%;乳酸,AR,阿拉丁試劑有限公司提供,質量分數85.0%~90.0%;二氧化硫,北京海普氣體有限公司提供,體積分數 >99.95%;二氧化碳,北京海普氣體有限公司提供,體積分數 >99.995%;去離子水,化工資源有效利用國家重點實驗室提供,電導率σ<1.5 μS·cm-1。
1.2 實驗裝置
脫硫實驗裝置如圖1所示,主要包括:模擬煙氣制備系統、吸收系統、解吸系統、煙氣分析系統以及尾氣吸收系統。模擬煙氣通過空氣泵和SO2鋼瓶提供原料氣體,在混合罐中進行混合,由轉子流量計控制流量;吸收系統中吸收塔為316 L不銹鋼材質(高1.8 m,內徑46 mm),內裝陶瓷拉西環填料(填料層高1.0 m),富液罐為316 L不銹鋼材質(容積12 L);解吸塔為316 L不銹鋼材質(高1.5 m,內徑50 mm),內裝陶瓷拉西環填料(填料層高0.5 m),解吸塔塔釜通過內置加熱器進行加熱,貧液罐為316 L不銹鋼材質(容積12 L);煙氣分析系統中,通過綜合煙氣分析儀(Kane International limited 公司生產,KM9106型,SO2測量范圍 0~14285 mg·m-3,精度15 mg·m-3,對模擬煙氣及尾氣中的 SO2進行測定;尾氣吸收系統中用濃度為 1.0 mol·L-1NaOH進行尾氣處理。
1.3 實驗方法
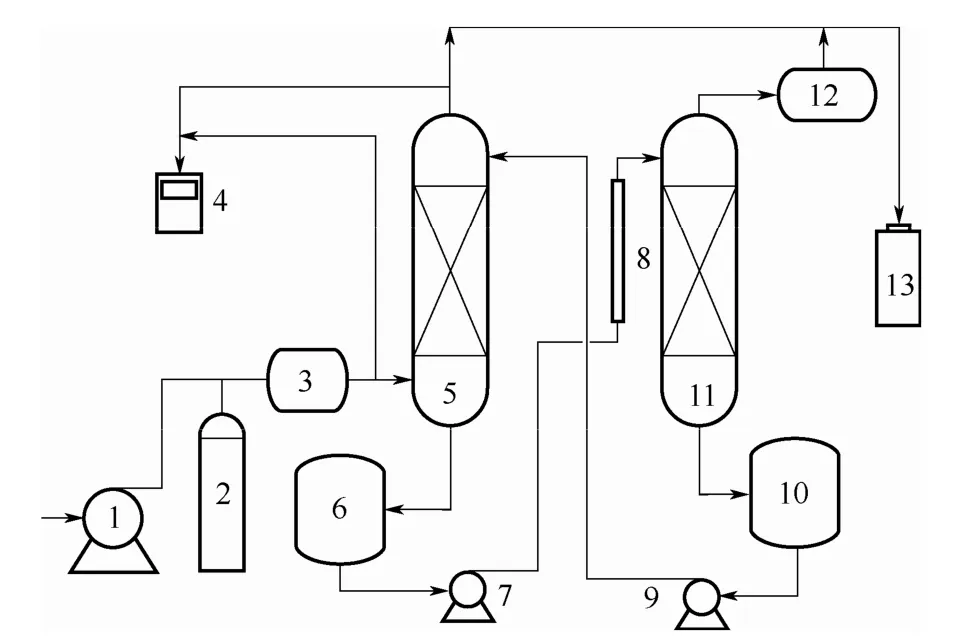
圖1 實驗裝置Fig.1 Schematic diagram of experiment apparatus
1.3.1 乙醇胺乳酸鹽吸收劑的制備 乙醇胺乳酸鹽([MEA]L)通過將乙醇胺與等物質的量的乳酸中和制備,具體合成方法見文獻[18]。將合成的[MEA]L與去離子水混合,配制成不同含水量的吸收劑。實驗中用到的離子液體水溶液均為新鮮配制。離子液體和去離子水按一定比例混合后,通過水分滴定儀進行水分測定,每個數值重復測試3次,取其平均值。
1.3.2 SO2吸收實驗 儲存在貧液罐中的吸收劑由隔膜泵以一定流量從吸收塔塔頂進入,空氣和SO2經混合罐混合成模擬煙氣,從吸收塔塔底進入,吸收劑與模擬煙氣逆流接觸并吸收。吸收后的富液儲存于富液罐中,尾氣中SO2濃度,由綜合煙氣分析儀跟蹤測定。富液由隔膜泵從富液罐中抽出,經預熱進入解吸塔,由解吸塔塔釜加熱產生的蒸汽對其進行再生。再生的貧液經冷卻進入貧液罐,再次打入吸收塔進行循環吸收。解吸塔出口的SO2經尾氣吸收系統處理后排空。
1.3.3 分析測試 模擬煙氣中 SO2濃度和尾氣中SO2濃度由綜合煙氣分析儀測定。SO2的去除率η(%)由式(1)進行計算

式中,Cin為模擬煙氣中SO2的濃度, mg·m-3,Cout為尾氣中SO2濃度,mg·m-3。
吸收后富液中 SO2含量根據國標 GB/T 11198.12—1989提供的方法進行測定。
2 實驗結果與討論
2.1 吸收劑中水含量對吸收的影響
合成好的離子液體與去離子水混合成不同含水量的吸收劑,根據式(2)計算出最小液氣比,以此得到離子液體的最小用量,并得到在保持離子液體用量一定的條件下吸收劑用量。
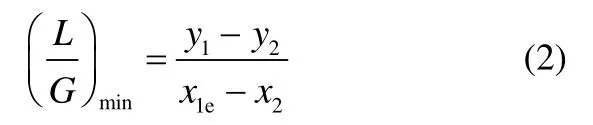
式中,G為模擬煙氣的摩爾流量;L為[MEA]L的摩爾流量;y1為模擬煙氣中 SO2的摩爾分數;y2為出口排放的SO2摩爾分數,根據《鍋爐大氣污染物排放標準》GB 13271—2014中燃煤鍋爐的 SO2排放濃度定為 300 mg·m-3;x1e為平衡時[MEA]L中 SO2的摩爾分數,該數據從文獻[19]中獲得;x2定為0。
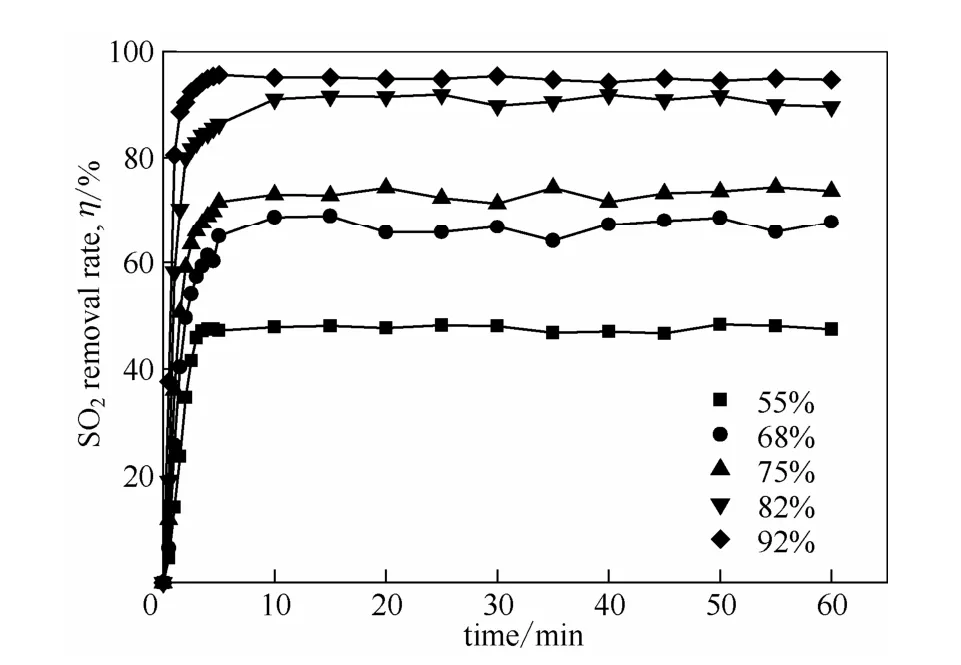
圖2 在40℃、常壓下不同含水量[MEA]L水溶液對SO2的去除率隨時間的變化關系Fig.2 Removal rate of SO2as a function of time with different mass fractions of water in [MEA]L solution
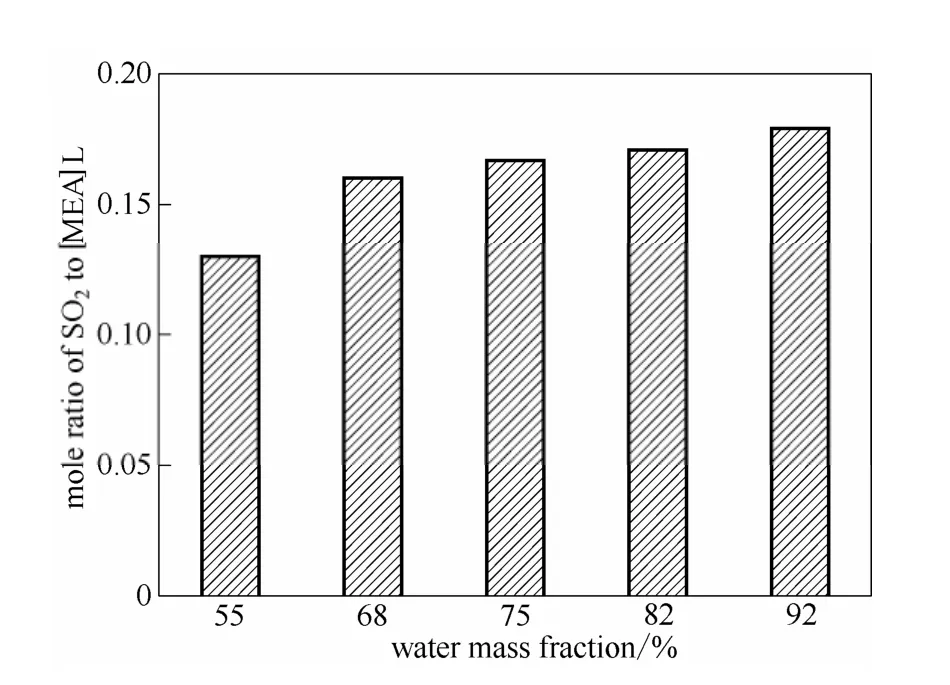
圖3 在40℃、常壓下不同含水量[MEA]L水溶液對SO2的摩爾吸收量Fig.3 Mole ratio of SO2to [MEA]L with different water contents in [MEA]L solution
如圖2和圖3所示,吸收劑對煙氣中SO2的去除率隨含水量的增加而增加,與之相對應,從塔頂到塔釜這一過程中[MEA]L對SO2的摩爾吸收量也隨著水分的增加而增加。這與之前離子液體對SO2的飽和吸收實驗結果相符合,這是由于 SO2不斷通入體系中,水含量的增加不會引起亞硫酸的濃度改變,只會使其他成分的濃度下降,根據勒夏特列原理,平衡向正方向移動,從而增加了離子液體對SO2的吸收量[20]。與此同時,水含量的增加也降低了吸收劑的黏度,增強了流動性和分散性,從而提高了傳質效果。然而,在應用時,含水量并不是越高越好,因為含水量越大,吸收劑中的有效成分離子液體越少,需要輸送的動力消耗就越大,因此,含水量在 70%左右即可滿足操作需求。
2.2 吸收劑用量(氣液比)對吸收的影響
配制含水量為 75%的[MEA]L溶液作為吸收劑,在不同的氣液體積比進行吸收SO2實驗,結果如圖4、圖5所示。發現在SO2濃度為10000 mg·m-3時,隨著吸收劑用量的增加(氣液比的減少)出口SO2的濃度是下降的,在氣液比為420時就能滿足排放標準(≤300 mg·m-3)。在更低的氣液比時,雖然SO2的濃度達到排放標準,但是從塔頂到塔釜這一過程中[MEA]L對SO2的摩爾吸收量卻不是很高。因此,在此條件下選擇氣液比為420時,既滿足排放標準,離子液體的利用率也比較高,消耗的動力也相對較少。
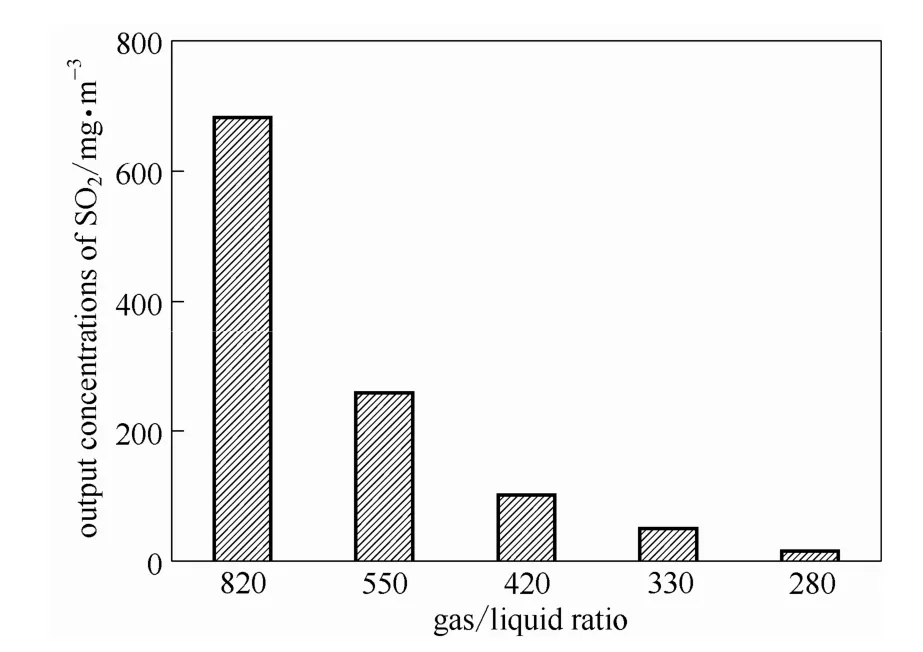
圖4 在40℃、常壓下含水量75%[MEA]L水溶液吸收SO2后出口濃度的變化Fig.4 Output concentration of SO2as a function of vapor/liquid ratio after SO2absorption
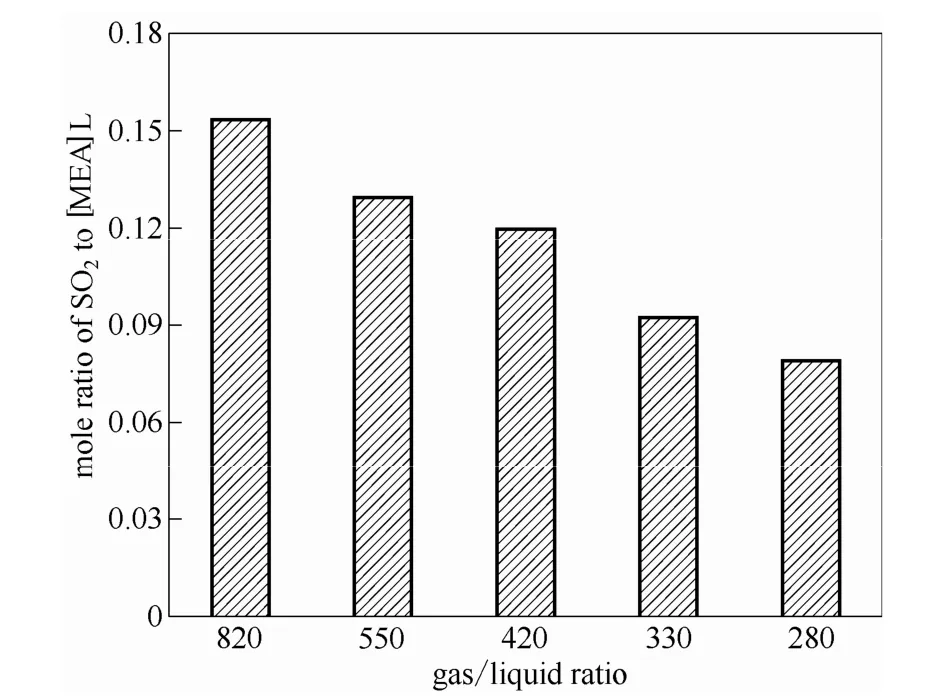
圖5 在40℃、常壓下不同氣液比時[MEA]L對SO2的摩爾吸收量Fig.5 Mole ratio of SO2to [MEA]L with different vapor/liquid ratios
2.3 煙氣中SO2濃度對吸收的影響
煙氣中SO2濃度對吸收的影響結果如圖6、圖7所示。在氣液比為420時,含水量為75%的[MEA]L溶液,對不同濃度SO2的去除率隨著SO2濃度的變化沒有顯著的變化,這是因為在濃度較低時,雖然傳質推動力較低,但是對應的吸收劑量比較大,吸收得比較徹底。在濃度較高時,傳質推動力比較大,因此也具有較高的去除率。然而,由于吸收劑的吸收能力有限,出口SO2的濃度卻有明顯的增加。在此操作條件下,煙氣中 SO2濃度為 2850~14280 mg·m-3時,出口濃度小于300 mg·m-3,滿足排放標準。
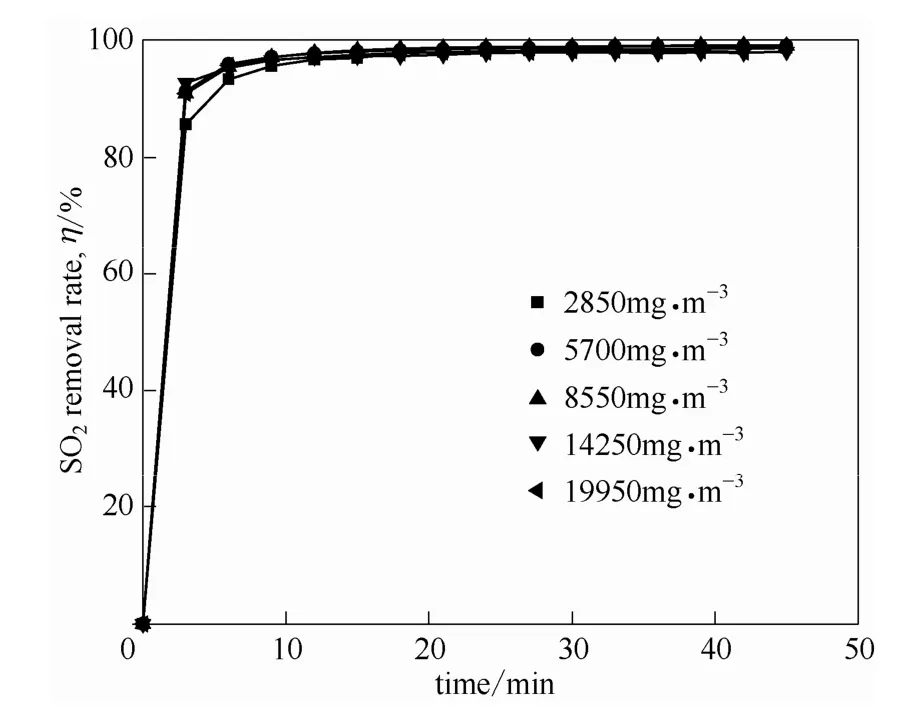
圖6 在40℃、常壓下含水量75%[MEA]L水溶液吸收對不同濃度SO2去除率隨時間的變化Fig.6 Removal rate of SO2as a function of time with different SO2concentrations in flue gas
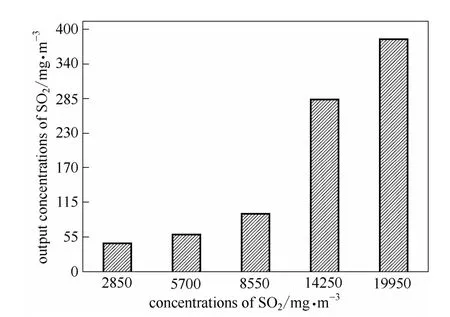
圖7 在40℃、常壓下含水量75%[MEA]L水溶液吸收不同濃度SO2后出口SO2濃度的變化Fig.7 Output concentration of SO2as a function of SO2concentration
2.4 煙氣中CO2對吸收的影響
燃煤煙氣中含有10%~15%的CO2,因此需要考慮CO2對吸收的影響。實驗測定了吸收劑對含有體積濃度為11% CO2的模擬煙氣的吸收效果。如圖8所示,煙氣中的CO2對SO2的去除率沒有影響。并且,使用 TOC對吸收前后吸收劑的分析可以知道,吸收前吸收劑中的CO2為20.68 mg·m-3,吸收后吸收劑中CO2為17.72 mg·m-3,即吸收前后吸收劑中 CO2的含量沒有變化,這說明吸收劑對CO2沒有吸收,僅對煙氣中的SO2進行選擇性吸收。
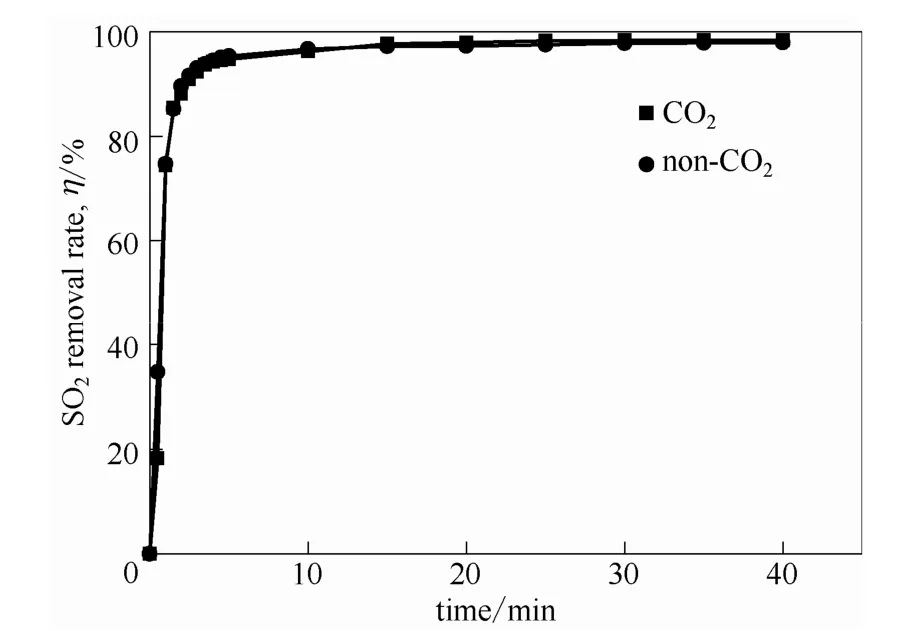
圖8 在40℃、常壓下含水量75%[MEA]L水溶液吸收對SO2去除率隨時間的變化Fig.8 Removal rate of SO2as a function of time
2.5 再生對吸收的影響
通過前幾組實驗,可確定出一個最佳吸收實驗條件,在此條件下進行吸收-解吸循環實驗。結果如圖9所示,在沒有進行解吸時,循環到220 min時SO2脫除率即下降至95%以下,然而,進行解吸再生后,SO2脫除率保持在95%以上的時間延長了一倍,通過在解吸塔塔釜加熱,產生蒸氣對吸收后的富液進行氣提再生,可以顯著提高離子液體的使用時間。說明該脫硫劑可以解吸再生,并且再生后仍具有很好的吸收能力。然而,由于解吸塔的高度不足,致使富液沒有完全解吸,吸收劑逐漸積累SO2,因此,隨著時間的增加,SO2去除率逐漸下降,如在500 min時,SO2的脫除率為94%。在后續的工作中,將提高解吸塔高度,使富液解吸比較完全,實現高效的SO2吸收-解吸循環。
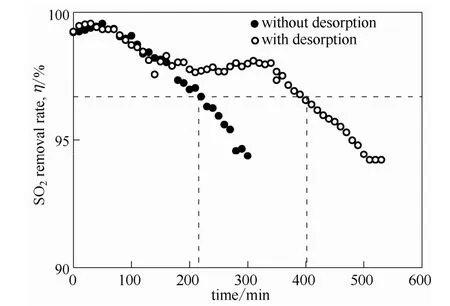
圖9 40℃,常壓下含水量75%[MEA]L水溶液吸收對SO2去除率隨時間的變化Fig.9 Removal rate of SO2as a function of time without desorption and with desorption
3 結 論
通過研究[MEA]L水溶液在放大裝置中對 SO2的吸收行為,可以得到以下結論。
[MEA]L水溶液對SO2的脫除率隨著含水量的增加而增加,最合適的含水量為70%~80%;隨著氣液比的下降而增加,最合適的氣液比為 420,對于濃度為2850~14280 mg·m-3SO2有著很強的去除率,并且出口濃度保持在300 mg·m-3之下,滿足國家排放標準;煙氣中的CO2對[MEA]L吸收SO2沒有影響,[MEA]L選擇性吸收SO2。
[MEA]L水溶液作為吸收劑,可以有效地吸收低濃度的 SO2,而且通過蒸氣氣提,達到再生的目的,并可以進行循環使用,可實現吸收-解吸循環脫硫的過程。
[1] Xu Y. Improvements in the Operation of SO2scrubbers in China’s coal power plants [J].Environ. Sci. Technol., 2011, 45(2):380-385.
[2] Tan Xin(譚鑫), Zhong Rugang(鐘儒剛), Zhen Yan(甄巖),et al.Progresses in research on calcium-based processes for flue gas desulfurization [J].Environmental Protection of Chemical Industry(化工環保), 2003, 23(6):322-328.
[3] Wang Jiaming(汪家銘). Use of desulfurization with ammonia in treatment of tail gas from manufacture of acid based on sulfur [J].Journal of the Chemical Fertilizer Industry(化肥工業), 2010, 37(4):14-17.
[4] Ge Nengqiang(葛能強), Shao Yongchun(邵永春). Application of wet ammonia desulphurization process [J].Sulphuric Acid Industry(硫酸工業), 2006, (6):10-15.
[5] Erga O. SO2recovery by a sodium citrate solution scrubbing [J].Chem. Eng. Sci., 1980, 35(1):162-169.
[6] Liu Y, Bisson T M, Yang H Q,et al. Recent developments in novel sorbents for flue gas clean up [J].Fuel Process Technol., 2010, 91(10):1175-1197.
[7] He Zhiqiang(禾志強), Qi Liming(祁利明), Ma Qingshu(馬青樹).The study of demister blocking in lmiestone-gypsum desulfurization technology [J].Boiler Technology(鍋爐技術), 2010, 41(1):77-80.
[8] Hansen B B, Fogh F, O K N,et al. Performance of a wet flue gas desulfurization pilot plant under oxy-fuel conditions [J].Ind. Eng.Chem. Res., 2011, 50(8):4238-4244.
[9] Bao Jingjing(鮑靜靜), Yin Huabin(印華斌), Yang Linjun(楊林軍),et al. Removal of fine aerosol particles formed in wet ammonia flue gas desulfurization process by heterogeneous condensation [J].Journal of Power Engineering(動力工程), 2009, 29(2):178-183.
[10] Xia Yuzheng(夏宇正), Du Shimao(杜士帽), Wei Jiaming (魏甲明),et al. Preparation of poly (1,1,3,3-tetramethylguanidine acrylate) and its absorption-desorption properties to SO2[J].The Chinese Journal of Process Engineering(過程工程學報), 2012, 12(4):583-589.
[11] Li Ruxiong(李汝雄), Wang Jianji(王建基). Research and application on green solvent——the ionic liquid [J].Chemical Industry and Engineering Progress(化工進展), 2002, 21(1):43-48.
[12] Dupont J, de Souza R F, Suarez P A Z. Inoic Liquid (molten salt)phase organometallic catalysis [J].Chem. Rev., 2002, 102:3667-3692.
[13] Fredlake C P, Crosthwaite J M, Hert D G,et al. Thermophysical properties of imidazolium-based ionic liquids [J].J. Chem. Eng. Data.,2004, 49(4):954-964.
[14] Lei Z G, Dai C N, Chen B H. Gas solubility in ionic liquids [J].Chem.Rev., 2014, 114(2):1289-1326.
[15] Wu W Z, Han B X, Gao H X,et al. Desulfurization of flue gas:SO2absorption by an ionic liquid [J].Angew. Chem. Int. Ed., 2004, 43(18):2415-2417.
[16] Ren S H, Hou Y C, Wu W Z,et al. Effect of H2O on the desulfurization of simulated flue gas by an ionic liquid [J].Ind. Eng.Chem. Res., 2009, 48(10):4928-4932.
[17] Yuan X L, Zhang S J, Lu X M. Hydroxyl ammonium ionic liquids:synthesis, properties, and solubility of SO2[J].J. Chem. Eng. Data,2007, 52(2):596-599.
[18] Zhai L Z, Zhong Q, He C,et al.Hydroxyl ammonium ionic liquids synthesized by water-bath microwave:synthesis and desulfurization[J].J. Hazard. Mater., 2010, 177:807-813.
[19] Jin M J, Hou Y C, Wu W Z,et al.Solubitions and thermodynamic properties of SO2in inoic liquids [J].J. Phys. Chem. B, 2011, 115(20):6585-6591.
[20] Qian J G, Ren S H, Tian S D. Highly efficient and reversible absorption of SO2by aqueous triethyleneteramine tetralactate solutions [J].Ind. Eng. Chem. Res., 2014, 53(39):15207-15212.

