鈦精礦碳熱還原制備碳氮化鈦的研究
肖 玄,陳 敏
(攀枝花學院材料工程學院,四川 攀枝花 617000)
鈦精礦碳熱還原制備碳氮化鈦的研究
肖 玄,陳 敏
(攀枝花學院材料工程學院,四川 攀枝花 617000)
以鈦精礦和石墨為原料,在氮氣氣氛下通過碳熱還原法制備出碳氮化鈦(TiCN)粉體。結合XRD、SEM、化學成分分析和TG-DSG綜合熱分析研究了配碳量及反應溫度對鈦精礦碳熱還原進程的影響。研究結果表明,配碳量的增加影響逐級還原反應溫度以及反應總失重,當配碳量達到23%時碳氮化鈦產物中出現游離碳。鈦精礦碳熱還原過程中鐵氧化物優先還原,鈦氧化物經逐級還原形成TiCN,還原順序為TiO2→Ti4O7→Ti3O5→TiN→Ti(C,N,O)→TiCN。得到的碳氮化鈦粉體呈微米級不規則形狀。
鈦精礦;碳熱還原;碳氮化鈦
0 引言
碳氮化鈦基硬質合金具有高強度、高熔點、耐磨、耐腐蝕以及抗氧化等特性,可用于制備刀具材料以及密封環類等耐磨材料[1-3]。碳氮化鈦的制備方法較多,包括傳統的制備工藝以及近年來發展的新工藝,其中碳熱還原法是最經濟有效且容易實現規模化生產的方法[4-9]。我國鈦資源儲量居世界第一,其中攀西地區最為豐富。鈦精礦碳熱還原法可得到含鐵的碳氮化鈦復合粉,既可以直接制備鐵基碳氮化鈦復合材料,也可經鹽酸浸取后得到碳氮化鈦粉用于制備密封環、陶瓷噴嘴等耐磨材料,而含有FeCl2的浸出液可用氧化焙燒的方法制取鐵紅粉和HCl,再通過水淋洗回收制取再生稀鹽酸。鈦精礦碳熱還原法制備碳氮化鈦的過程中,配碳量是重要的工藝參數,配碳量偏低導致產物中碳氮化鈦的氧含量偏高,配碳量偏高則產物中存在游離碳,游離碳和氧都將嚴重影響后續制備材料的力學性能。本實驗以攀枝花鈦精礦為原料,研究了配碳量及反應溫度對鈦精礦碳熱還原進程的影響,探索了鈦精礦碳熱還原法制備碳氮化鈦的演變規律。
1 實驗
1.1 制備方法
實驗以攀枝花鈦精礦和市售石墨為原料。鈦精礦由鈦鐵氧化物主體成分及雜質組成,主體成分約占88%,其中 TiO2為 47.48%,FeO為 33.01%,Fe2O3為7.36%,粒度約為150 μm。市售石墨為微米級石墨粉,粒度約為30 μm。鈦精礦與石墨以一定的配比混料后進行球磨。選用QM-1SP2行星式球磨機混合粉料,球料比為20∶1,球磨轉速為350 r/min,球磨時間為4 h。將混合均勻的粉料裝入石墨坩堝,然后放置在碳管爐內,碳管爐抽真空后通入流動氮氣,氮氣流量為0.2 L/min。碳管爐從室溫加熱至1 400℃,混合粉料經高溫燒結合成含鐵的碳氮化鈦復合粉體。復合粉體經鹽酸浸取、過濾、洗滌后,繼續在氫氟酸溶液中酸浸,反應完成后再經過濾、洗滌干燥得到碳氮化鈦粉。鹽酸質量分數為25%,水浴加熱溫度為90℃,液固比為10∶1,加熱時間為6 h。氫氟酸質量分數為20%,液固比為10∶1,反應時間為4 h。
1.2 測試方法
采用D/MAX-1200型X射線衍射儀進行物相分析。檢測參數:Cu靶,X射線波長0.154 056 nm,工作電壓40 kV,工作電流30 mA,單色器濾波,掃描范圍10°~90°,掃描速度2°/min。綜合熱分析由STA449C型熱分析儀測定,測定過程中升溫速度為20℃/min,升溫范圍為25~1 400℃,氮氣流量為60 mL/min。采用TESCAN VEGAⅡLMU型掃描電子顯微鏡觀察粉體形貌。
2 結果和討論
2.1 配碳量對鈦精礦還原過程的影響
以鈦精礦為鈦源制備碳氮化鈦的總反應式如下:

熱力學計算表明,選擇適宜的配碳量制備TiN、TiC以及一系列C/N可調的TiCN的反應吉布斯自由能均為負值,說明這些反應在熱力學上均是可進行的,并且隨著溫度的升高,反應趨勢均增大[10]。實驗中通過計算有效配碳量進行配料。圖1為燒結溫度1 400℃時碳管爐內鈦精礦還原反應總失重隨配碳量的變化曲線。當配碳量(質量分數)從18.5%增加到21.8%時,還原反應總失重接近線性增加,從35.48%增加到42.55%。當配碳量繼續增加到23%時,反應總失重增幅減小。當配碳量超過21.8%時檢測到的反應失重高于理論失重(42%),一方面由于球磨后粉料的吸附氣體在燒結過程中脫除所致,另一方面說明該配碳范圍能夠反應形成碳氮化鈦[11-12]。

圖1 不同配碳量的鈦精礦碳熱還原失重圖Fig.1 Mass loss graph of carbothermic reduction of ilmenite with different carbon contents
為了研究鈦精礦的還原進程,分別選擇配碳量為20%、21.5%及23%的樣品進行了TG-DSC綜合熱分析,結果見圖2、圖3。從圖2和圖3可以看出,鈦精礦碳熱還原反應過程中有兩個明顯的吸熱峰,不同配碳量所得綜合熱分析曲線峰形相似,說明在實驗配碳范圍內配碳量的改變不會引起還原過程的物相演變,但是對逐級還原反應溫度以及總失重有較大的影響。當配碳量從20%增加到23%時,碳熱還原反應總失重從27.6%增加到40%,有利于降低最終產物中的氧含量。鈦精礦碳熱還原反應的熱重曲線結果比燒結爐內的反應失重偏低,這是由于燒結爐內升溫速度和熱分析相比要慢,且球磨粉料吸附氣體較多,導致失重偏高。

圖2 不同配碳量的TG曲線Fig.2 TG curves of different carbon contents

圖3 不同配碳量的DSC曲線Fig.3 DSC curves of different carbon contents
隨著配碳量的增加,DSC曲線中第一個主要吸熱峰的開始反應溫度從1 120℃降低到1 091℃,說明提高配碳量可使逐級還原反應提前進行。結合圖2和圖3可以看出,當配碳量從21.5%增加到23%時,鈦精礦碳熱還原反應的TG曲線和DSC曲線變化一致,說明當配碳量達到21.5%后鈦精礦的碳熱還原反應完成。
分別對配碳量為21.5%和23%的反應產物進行XRD物相分析,結果見圖4。由圖4可以看出,當配碳量為21.5%時,反應產物中TiCN和Fe為主相。當配碳量增加到23%時,產物中檢測到明顯的石墨峰,石墨相的存在會導致產物中游離碳增多,影響后續制備材料的力學性能。因此適宜的配碳量應低于23%。
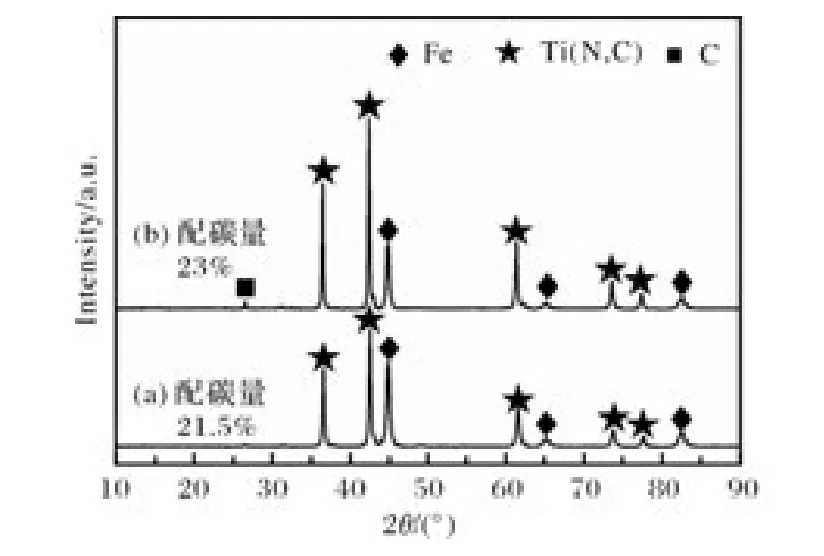
圖4 不同配碳量的反應產物XRD圖譜Fig.4 XRD patterns of reaction products with different carbon content
2.2 反應溫度對鈦精礦還原過程的影響
流動氮氣氣氛下,當配碳量為21%時鈦精礦還原過程中不同溫度下所得燒結產物的物相分析結果如圖5所示。反應爐內溫度從800℃開始隨著溫度的升高,鈦精礦實現逐級還原。鐵氧化物優先還原,二氧化鈦被分離出來,產物中檢測到TiO2峰出現。900℃時大部分鐵被還原出來,鐵相成為主峰。此外,TiO2逐級還原反應開始,Ti4O7形成,TiO2和FeTiO3相衍射峰消失,反應產物中鐵和Ti4O7中間氧化物為主相。當反應溫度達到1 000℃時,TiN和Ti3O5形成,Ti4O7還原為穩定的中間鈦氧化物Ti3O5。氮氣氣氛下 Ti3O5向 TiN的轉化更容易進行[10]。當反應溫度達到1 100℃時,Ti4O7消失,鈦氧化物為Ti3O5。鈦氧化物的逐級還原過程內TiO2完成了向低階鈦氧化物的轉變后消失,Ti4O7物相經歷了從開始形成到先增強后消失的過程。當反應溫度增加到1 200℃時,石墨峰消失,立方相TiN先形成Ti(C,N,O)后轉化為TiCN,衍射峰逐漸向高角度偏移。還可以檢測到少量的Fe3C相。當反應溫度達到1 300℃時,反應產物以TiCN和鐵為主。氮氣氣氛下鈦精礦碳熱還原過程中的物相演變未檢測到TiC相,說明隨著溫度的升高,TiN形成后向TiC的轉化存在一個動態平衡,兩者形成固溶體并以TiCN的形式穩定存在。

圖5 不同反應溫度下鈦精礦還原產物的XRD圖譜Fig.5 XRD patterns of reduction products of ilmenite at different temperatures
將1 400℃的燒結產物經鹽酸浸取、過濾、洗滌干燥后得到的碳氮化鈦粉體形貌如圖6所示。對碳氮化鈦粉體進行化學分析,結果如表1所示。氮氣氣氛下鈦精礦碳熱還原制備的碳氮化鈦為微米級不規則形狀粉體,純度接近95%。游離碳和氧含量是碳氮化鈦制備后續材料的重要參數,產物中碳氮化鈦的氧含量(2.62%)偏高是由于鈦精礦中的氧化鋁高溫燒結后形成剛玉,剛玉不溶于酸和堿所致。

圖6 碳氮化鈦粉的SEM照片Fig.6 SEM micrograph of TiCN powder

表1 碳氮化鈦粉的化學成分(w/%)Table 1 Chemical composition of TiCN powder
3 結論
(1)鈦精礦碳熱還原過程中,配碳量的增加影響還原反應溫度以及反應總失重。當配碳量從20%增加到23%時,鈦精礦碳熱還原反應總失重從27.6%增加到40%,DSC曲線中第一個主要吸熱峰的開始反應溫度從1 120℃降低到1 091℃。
(2)當配碳量從21.5%增加到23%時,鈦精礦碳熱還原TG曲線和DSC曲線變化一致。當配碳量為21.5%時,反應產物中TiCN和Fe為主相。當配碳量增加到23%時,產物中檢測到明顯的石墨峰。
(3)鈦精礦碳熱還原制備碳氮化鈦過程中,當溫度低于900℃時反應以鐵氧化物還原為主。鈦氧化物經逐級還原形成碳氮化鈦,當反應溫度達到1 200℃后中間氧化物和石墨峰消失,還原順序為TiO2→Ti4O7→Ti3O5→TiN→Ti(C,N,O)→TiCN。碳氮化鈦粉體呈微米級不規則形狀。
[1]Kim Sungwon,Min Kyoung-hoon,Kang Shinhoo.Rim Structure in Ti(C0.7N0.3)-WC-Ni Cermets[J].Journal of the American Ceramic Society,2003,86(10):1761-1766.
[2]Liu Ning,Xu Yudong,Li Zhenhong,et al.Influence of molybdenum addition on the microstructure and mechanical properties of TiC-based cermets with nano-TiN modification [J].Ceramics International,2003,29(8):919-925.
[3]鄭勇,熊惟皓,宗校軍,等.Ti(C,N)基金屬陶瓷氮化處理后的表面組織結構及形成機理[J].硅酸鹽學報,2003,31(3):262-267.
[4]Yeh C L,Chen Y D.Direct formation of titanium carbonitrides by SHS in nitrogen [J].Ceramics International,2005,31(5):719-729.
[5]Lichtenberger O,Pippel E,Woltersdorf J,et al.Formation of nanocrystalline titanium carbonitride by pyrolysis of poly(titanylcarbodiimide)[J].Materials Chemistry and Physics,2003,81(1):195-201.
[6]Feng Xin,Shi Li-Yi.Novel chemical metathesis route to prepare TiCN nanocrystallites at low temperature[J].Materials Chemistry and Physics,2005,94(1):58-61.
[7]Chen Xilai,Li Yuanbing,Li Yawei,et al.Carbothermic reduction synthesis of Ti(C,N)powder in the presence of molten salt[J].Ceramics International,2008,34(5):1253-1259.
[8]陳幫橋,葉金文,劉穎,等.碳熱還原法制備碳氮化鈦粉末[J].硬質合金,2009,26(2):98-101.
[9]鮑春艷,鄭永挺,赫曉東.配碳量對自蔓延鎂熱還原反應制備 TiCN 粉末的影響[J].粉末冶金技術,2006,24(1):36-39.
[10]Welham N J,Berbenni V,Chapman P G.Effect of extended ball milling on graphite [J].JournalofAlloys and Compounds,2003,349(1):255-263.
[11]Welham N J,Berbenni V,Chapman P G.Increased chemisorption onto activated carbon after ball-milling[J].Carbon,2002,40(13):2307-2315.
[12]Monteverde Frederic,Medri Valentina,Bellosi Alida.Synthesis of ultrafine titanium carbonitride powders[J].Applied Organometallic Chemistry,2001,15(5):421-429.
Investigation on the Carbothermal Reduction Process of Titanium Carbonitride Prepared by Ilmenite
Xiao Xuan,Chen Min
(Materials Engineering College of Panzhihua University,Panzhihua 617000,China)
TiCN powders were synthesized by ilmenite and graphite in nitrogen atmosphere.The effects of carbon contents and reaction temperature on the process of reduction were investigated with X-Ray Diffraction(XRD),scanning electron microscope(SEM),chemical analysis and thermal analysis.The results show that increasing carbon contents influences the reaction temperature of gradual deoxidizing and total mass loss.When the carbon content is 23%,free carbon exists in the products.Iron oxides are reduced prior to titanium oxides in the reduction process,TiCN forms via gradual deoxidizing of titanium oxides,and the order is TiO2→Ti4O7→Ti3O5→TiN→Ti(C,N,O)→TiCN.
ilmenite;carbothermal reduction;TiCN
10.13567/j.cnki.issn1009-9964.2015.04.010
2015-05-07
四川省應用基礎研究項目(2014JY0132);攀枝花市科技支撐項目(2013CY-G-7;2014CY-G-26-1);攀枝花學院校級科研專案(2013YB28)
肖玄(1986—),男,碩士。

