異步控制Varicol工藝分離愈創(chuàng)木酚甘油醚對(duì)映體過(guò)程研究
龔如金,林小建,李平,于建國(guó)
(華東理工大學(xué)化學(xué)工程聯(lián)合國(guó)家重點(diǎn)實(shí)驗(yàn)室,上海 200237)
引 言
手性對(duì)映體藥物進(jìn)入生物體后往往在藥效學(xué)、藥代動(dòng)力學(xué)等方面呈現(xiàn)很大的差異,因此美國(guó)、歐共體、日本等許多國(guó)家相繼頒布關(guān)于手性藥物生產(chǎn)的法規(guī),這些舉措極大地促進(jìn)了手性藥物拆分技術(shù)的發(fā)展。獲得光學(xué)純度高且毒副作用小的單一對(duì)映體已經(jīng)成為醫(yī)藥研究的發(fā)展方向。模擬移動(dòng)床(SMB)色譜具有成本低、分離效率高、固定相利用率高、流動(dòng)相循環(huán)使用、自動(dòng)化連續(xù)操作等優(yōu)勢(shì),已被國(guó)際上公認(rèn)為制備規(guī)模拆分手性藥物的最有效手段[1-4]。
為了提高模擬移動(dòng)床的分離效率,適應(yīng)更復(fù)雜的分離體系,在傳統(tǒng)的模擬移動(dòng)床技術(shù)基礎(chǔ)上發(fā)展出了一些新的技術(shù),主要包括梯度模擬移動(dòng)床(溶劑、溫度)[5-6]、超臨界模擬移動(dòng)床[7]、各區(qū)色譜柱數(shù)量變化Varicol工藝[8]、進(jìn)料濃度可變的Modicon工藝[9]、流動(dòng)相流速可變的Powerfeed工藝[10]、 三區(qū)SMB[11]、五區(qū)SMB[12],此外還有模擬移動(dòng)床串聯(lián)技術(shù)[13]、模擬移動(dòng)床技術(shù)與結(jié)晶耦合[14]等。工藝的不斷發(fā)展和創(chuàng)新使得 SMB技術(shù)更加完善,在分離技術(shù)領(lǐng)域更有競(jìng)爭(zhēng)力。
Varicol工藝是對(duì)傳統(tǒng)SMB技術(shù)的一種改進(jìn),操作原理基于循環(huán)周期內(nèi)進(jìn)出口位置的不同步切換。與傳統(tǒng)模擬移動(dòng)床相比,Varicol工藝各區(qū)中的色譜柱分布隨時(shí)間變化,而且柱數(shù)不受整數(shù)的限制,從而提高各區(qū)中固定相的利用率,節(jié)省手性固定相的使用,降低分離成本。與使用相同數(shù)量色譜柱的SMB工藝相比[15],Varicol工藝分離效果更好,而且在設(shè)計(jì)和操作上靈活性更高。然而,由于Varicol過(guò)程離散的動(dòng)態(tài)切換對(duì)分離區(qū)域有很強(qiáng)的影響,并且該工藝對(duì)實(shí)驗(yàn)設(shè)備自動(dòng)化控制要求較高,目前研究工作大多是基于數(shù)值計(jì)算,實(shí)驗(yàn)研究相對(duì)較少[8,15-21],而國(guó)內(nèi)理論和實(shí)驗(yàn)研究報(bào)道更少。黃永東等[22]采用傳統(tǒng)SMB、Varicol、Partial-discard工藝通過(guò)實(shí)驗(yàn)分離純化ECG和EGCG,結(jié)果表明:同傳統(tǒng)SMB相比,Varicol工藝具有提高產(chǎn)品純度和回收率的優(yōu)點(diǎn)。Lu[23]通過(guò)建立異步切換SMB模型,利用文獻(xiàn)數(shù)據(jù)驗(yàn)證了模擬結(jié)果,并理論分析了異步切換過(guò)程的優(yōu)勢(shì),模型和數(shù)值方法可以用來(lái)確定 Varicol工藝合適的操作條件。肖迪等[24]設(shè)計(jì)了16種典型的Varicol運(yùn)行模式,并通過(guò)數(shù)值方法從軸向濃度分布曲線分析了Varicol工藝的優(yōu)勢(shì)。
在前期工作中[25],通過(guò)實(shí)驗(yàn)和理論計(jì)算比較了SMB和Varicol兩種工藝分離愈創(chuàng)木酚甘油醚對(duì)映體的效率,結(jié)果發(fā)現(xiàn)Varicol工藝分離效果更好,更適用于手性藥物分離,但是對(duì)于Varicol工藝的設(shè)計(jì)及分離過(guò)程并沒(méi)有進(jìn)行詳細(xì)的理論研究。本研究采用 Varicol工藝的數(shù)學(xué)模型計(jì)算了愈創(chuàng)木酚甘油醚對(duì)映體在系統(tǒng)內(nèi)濃度分布的時(shí)間進(jìn)程曲線,分析Varicol工藝的分離過(guò)程,并設(shè)計(jì)了5柱 (1-1.5-1.5-1)構(gòu)態(tài)的 Varicol工藝分離愈創(chuàng)木酚甘油醚對(duì)映體的操作區(qū),通過(guò)Varicol實(shí)驗(yàn)進(jìn)行了驗(yàn)證。
1 數(shù)學(xué)模型
模擬移動(dòng)床以逆流連續(xù)操作方式,通過(guò)同步切換物料進(jìn)出口位置實(shí)現(xiàn)吸附劑向下移動(dòng)而物料向上移動(dòng)的效果,提高了固定床的生產(chǎn)能力和分離效率,同時(shí)避免了移動(dòng)床中吸附劑移動(dòng)產(chǎn)生的磨損。而Varicol工藝與SMB工藝區(qū)別在于:
(1)SMB的切換周期為ts,而本研究采用的5柱(1-1.5-1.5-1)Varicol工藝在ts內(nèi)又分為二步,在整個(gè)循環(huán)內(nèi)Varicol工藝增加了切換步驟;
(2)SMB工藝在循環(huán)內(nèi)每個(gè)區(qū)內(nèi)柱數(shù)不變,而Varicol隨切換過(guò)程每個(gè)區(qū)內(nèi)的柱數(shù)會(huì)發(fā)生改變,提高了SMB的分離效率。
模擬移動(dòng)床色譜數(shù)學(xué)模型是由色譜柱模型和柱與柱之間起銜接作用的節(jié)點(diǎn)模型所構(gòu)成。模型的基本假設(shè)為:
(1)整個(gè)過(guò)程溫度恒定,沒(méi)有熱效應(yīng),并且忽略吸附熱對(duì)譜帶的影響;
(2)不考慮色譜柱內(nèi)部徑向濃度、速度分布,只考慮軸向上的質(zhì)量、動(dòng)量傳遞過(guò)程;
(3)填料及床層空隙率分布均勻,忽略手性固定相顆粒內(nèi)部的傳質(zhì)過(guò)程;
(4)假設(shè)色譜柱內(nèi)流動(dòng)為平推流,忽略流動(dòng)相的可壓縮性,組分在色譜柱內(nèi)以恒定的線速度運(yùn)動(dòng);
(5)組分在流動(dòng)相中傳播時(shí),分子擴(kuò)散和渦流擴(kuò)散綜合為軸向擴(kuò)撒,而且擴(kuò)散系數(shù)恒定。
為了能夠描述分離的動(dòng)態(tài)過(guò)程以及進(jìn)出口的異步切換,采用模擬移動(dòng)床模型的建模方法。Varicol工藝使用的模型方程與模擬移動(dòng)床一樣,區(qū)別在于Varicol工藝考慮了進(jìn)出口位置的異步切換模式,同時(shí)也考慮了軸向擴(kuò)散和傳質(zhì)阻力的影響,并且采用線性驅(qū)動(dòng)力模型描述固定相顆粒上的傳質(zhì)過(guò)程[18,19,26-28],模型方程見(jiàn)表1。
2 數(shù)學(xué)模型求解
在實(shí)際操作中 5柱(1-1.5-1.5-1)Varicol工藝的運(yùn)行方式為:0~0.5ts時(shí)間內(nèi)按照SMB(1-1-2-1)運(yùn)行,0.5ts~ts時(shí)間內(nèi)按照 SMB(1-2-1-1)運(yùn)行,如圖1所示。所以在數(shù)值求解過(guò)程中一個(gè)切換周期可以看成 SMB(1-1-2-1)和 SMB(1-2-1-1)的耦合。
表1中的偏微分方程和代數(shù)方程構(gòu)成了Varicol工藝過(guò)程的數(shù)學(xué)模型。Varicol工藝過(guò)程中,由于進(jìn)出口位置的異步切換,每根色譜柱在切換周期內(nèi)表現(xiàn)為不同的功能區(qū),節(jié)點(diǎn)位置處的邊界條件也隨之發(fā)生改變。在gPROMS編程環(huán)境下,通過(guò)直線數(shù)值方法對(duì)Varicol工藝數(shù)學(xué)模型進(jìn)行數(shù)值求解。以時(shí)間作為連續(xù)變量,采用有限元正交配置法對(duì)空間變量進(jìn)行離散,沿色譜柱軸向方向?qū)⒋矊臃譃?50個(gè)單元,每個(gè)單元采用3個(gè)配置點(diǎn),將偏微分方程組轉(zhuǎn)化為常微分方程組。兩相鄰有限元通過(guò)相鄰配置點(diǎn)的連續(xù)條件關(guān)聯(lián)得到,邊界條件上的配置點(diǎn)代入邊界條件。使用DASOLV求解器對(duì)常微分方程組和代數(shù)方程組進(jìn)行求解,迭代過(guò)程中絕對(duì)誤差限為10?5。此外, 對(duì)比有限元正交配置法和有限元差分法發(fā)現(xiàn)離散方法對(duì)模擬結(jié)果影響不大。

表1 Varicol工藝數(shù)學(xué)模型方程Table 1 Mathematical model equations for Varicol process
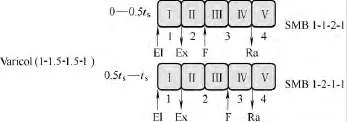
圖1 Varicol(1-1.5-1.5-1)工藝分離過(guò)程的數(shù)值求解方法Fig.1 Numerical solution method of Varicol process(1-1.5-1.5-1)
3 結(jié)果討論
前期工作[29]已經(jīng)測(cè)定了愈創(chuàng)木酚甘油醚對(duì)映體(R-GUA,S-GUA)在Chiralcel OD固定相上的吸附平衡以及模型參數(shù)(表 2),其中組分 R-GUA為弱保留組分,組分 S-GUA為強(qiáng)保留組分,流動(dòng)相為正己烷/乙醇=70:30(體積比),柱溫為25℃。本研究采用的Varicol工藝由5根色譜柱串聯(lián),填充的固定相粒徑為20 μm,柱構(gòu)態(tài)為1-1.5-1.5-1,進(jìn)料質(zhì)量濃度為 4 mg·ml?1。
3.1 進(jìn)出料口異步切換對(duì)多柱內(nèi)R-GUA和S-GUA濃度分布的影響
本研究通過(guò)數(shù)值方法考察初始循環(huán)內(nèi) Varicol工藝異步切換模式對(duì)R-GUA和S-GUA濃度分布的影響,如圖2所示,模型參數(shù)和工藝條件見(jiàn)表2。橫坐標(biāo)反映了 Varicol工藝進(jìn)出料口在循環(huán)內(nèi)異步切換的過(guò)程。從初始狀態(tài)開(kāi)始需要總共經(jīng)過(guò) 10步切換,才能完成一次5柱(1-1.5-1.5-1)Varicol工藝完整的循環(huán)。在系統(tǒng)進(jìn)料前,吸附分離過(guò)程尚未開(kāi)始,所有色譜柱處在初始狀態(tài)即濃度為零(t=0)。隨后系統(tǒng)通過(guò)進(jìn)料口開(kāi)始連續(xù)不斷地進(jìn)料,組分在床層內(nèi)發(fā)生吸附脫附過(guò)程,在第一次切換之前系統(tǒng)內(nèi)瞬態(tài)內(nèi)部濃度曲線如圖所示(t=0.5ts)。隨著進(jìn)出料口位置的不斷切換,強(qiáng)吸附組分 S-GUA逐漸移動(dòng)到萃取液口位置,而弱吸附組分 R-GUA逐漸移動(dòng)到萃余液口位置,兩組分實(shí)現(xiàn)分離。

表2 Varicol工藝操作條件和模型參數(shù)Table 2 Operating conditions and model parameters of Varicol process
在表 2的操作條件下,通過(guò)數(shù)學(xué)模型預(yù)測(cè) 20個(gè)循環(huán)內(nèi)愈創(chuàng)木酚甘油醚對(duì)映體內(nèi)部濃度曲線,如圖3所示。經(jīng)過(guò)5次循環(huán)后循環(huán)開(kāi)始趨于穩(wěn)定,此時(shí)內(nèi)部濃度曲線隨循環(huán)數(shù)增加不再發(fā)生變化。結(jié)果表明Varicol工藝分離R-GUA和S-GUA對(duì)映體時(shí)系統(tǒng)能夠快速達(dá)到穩(wěn)定狀態(tài)。此外,通過(guò)數(shù)學(xué)模型還預(yù)測(cè)了萃取液和萃余液兩個(gè)出口中溶質(zhì)的濃度曲線隨時(shí)間的變化,如圖4所示。在一次切換周期內(nèi),萃余液出口 R-GUA組分濃度隨時(shí)間增大,萃取液出口 S-GUA組分濃度隨時(shí)間降低,并且在一個(gè)循環(huán)內(nèi)呈周期性變化。
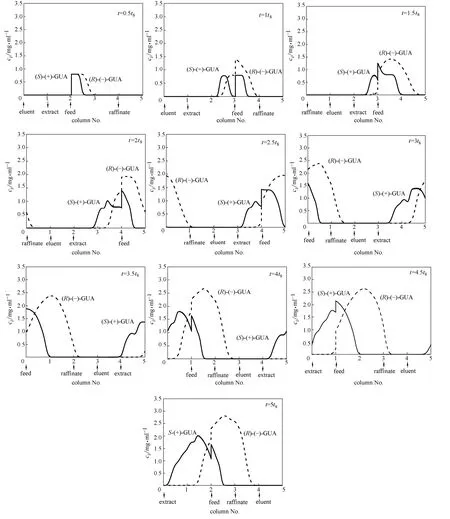
圖2 初始循環(huán)階段Varicol工藝的柱內(nèi)R-GUA和S-GUA瞬間濃度分布Fig.2 Transient internal concentration profile for R-GUA and S-GUA in first cycle of Varicol process
3.2 分離區(qū)設(shè)計(jì)及實(shí)驗(yàn)驗(yàn)證
通過(guò)在數(shù)學(xué)模型中考慮進(jìn)出料口位置的異步切換模式,三角形操作區(qū)可以指導(dǎo)Varicol工藝的分離過(guò)程[17,30]。為了保證 1區(qū)內(nèi)強(qiáng)吸附組分 S-GUA從吸附劑上全部脫附,同時(shí)在4區(qū)內(nèi)保證弱吸附組分R-GUA全部被吸附,m1和m4必須滿足一定的約束條件。對(duì)于Langmuir型吸附等溫線,一種簡(jiǎn)化的方法可以用來(lái)確定m的約束值[31-32],見(jiàn)式(1)和式(2)。本實(shí)驗(yàn)設(shè)計(jì)中選取m1=5.79,m4=1.61。通過(guò)數(shù)值方法,在滿足99.0%產(chǎn)品純度要求的前提下設(shè)計(jì)的Varicol工藝分離操作區(qū)如圖5所示,設(shè)計(jì)條件以及模型參數(shù)見(jiàn)表 2。在理論上認(rèn)為此區(qū)域內(nèi)均能獲得至少99.0%的產(chǎn)品純度。
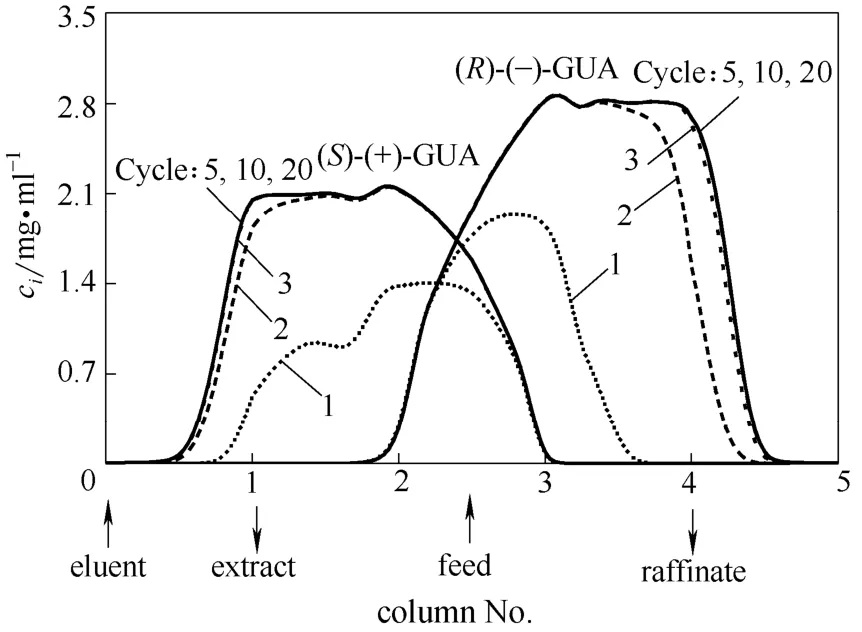
圖3 不同循環(huán)內(nèi)Varicol工藝內(nèi)部濃度曲線(操作條件見(jiàn)表2)Fig.3 Internal concentration profile of Varicol process at half switch time with different cycles (operating conditions shown in Table 2)
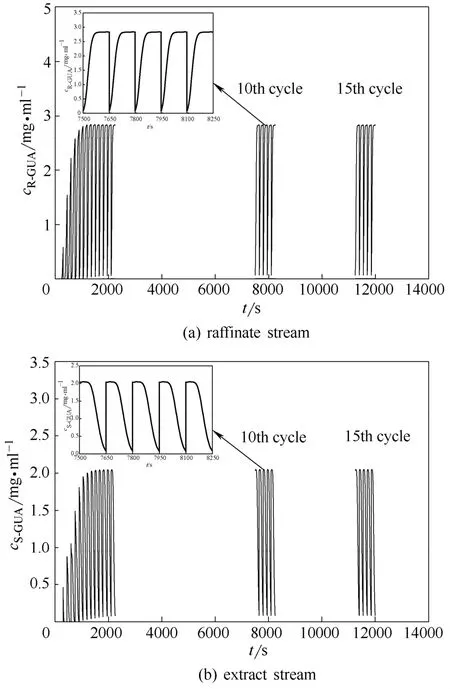
圖4 Varicol工藝15個(gè)循環(huán)內(nèi)產(chǎn)品流出曲線Fig.4 Concentration profile of Varicol process for 15 cycles in raffinate stream and extract stream (top left corner is outlet streams during the 10th cycle)
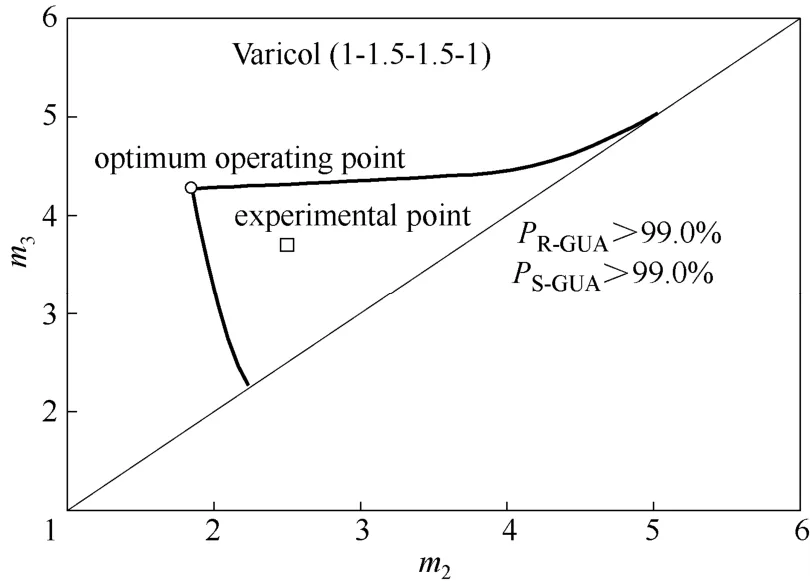
圖5 Varicol工藝(1-1.5-1.5-1)分離愈創(chuàng)木酚甘油醚對(duì)映體的操作區(qū)Fig.5 Separation region of 1-1.5-1.5-1 Varicol process for guaifenesin enantiomers
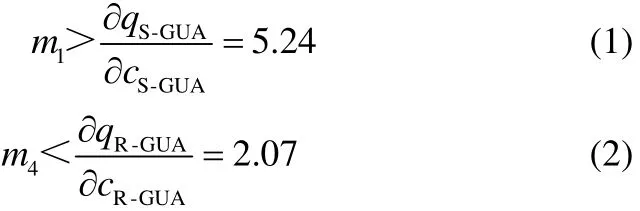
參數(shù)mj為液相凈流速和固相凈流速之比,定義見(jiàn)式(3)。
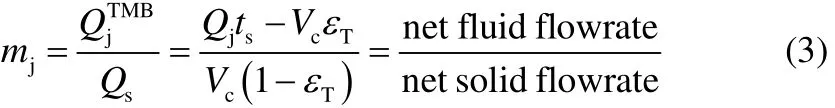
為了驗(yàn)證設(shè)計(jì)的分離操作區(qū),在其內(nèi)部選取實(shí)驗(yàn)操作條件,在 MICRO-VARICOL儀器上進(jìn)行Varicol實(shí)驗(yàn)。相應(yīng)的實(shí)驗(yàn)操作條件和實(shí)驗(yàn)結(jié)果見(jiàn)表3[25]。比較實(shí)驗(yàn)和模擬結(jié)果,雖然實(shí)驗(yàn)結(jié)果略低于理論預(yù)測(cè)的純度,但是仍然滿足設(shè)計(jì)的99.0%純度要求。數(shù)學(xué)模型能夠較好地預(yù)測(cè)Varicol工藝分離過(guò)程,而且設(shè)計(jì)的分離操作區(qū)可以用來(lái)指導(dǎo) Varicol(1-1.5-1.5-1)工藝分離愈創(chuàng)木酚甘油醚對(duì)映體的設(shè)計(jì)與優(yōu)化。
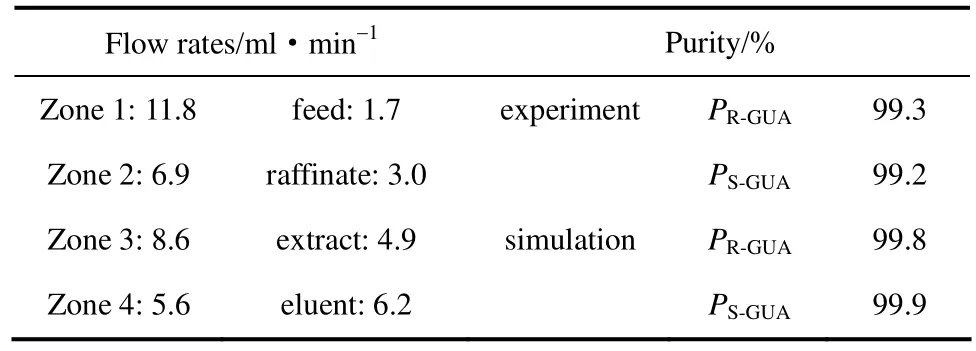
表3 Varicol工藝各區(qū)的流速及分離愈創(chuàng)木酚甘油醚對(duì)映體的實(shí)驗(yàn)和模擬結(jié)果比較Table 3 Flow rates in each zone of Varicol process and comparison of separation results between experiment and simulation for separation of guaifenesin enantiomers
選擇實(shí)驗(yàn)點(diǎn)居于三角形區(qū)域中心主要是考慮到此位置相對(duì)于區(qū)域邊緣部分的抗干擾性較強(qiáng),選擇這樣的操作點(diǎn)對(duì)于初始設(shè)計(jì)能夠獲得比較理想的實(shí)驗(yàn)結(jié)果。理論上,三角形頂點(diǎn)位置的分離性能最好,產(chǎn)率最高,并且溶劑消耗量最低。但是在實(shí)際分離中,由于死體積以及模型參數(shù)等因素的影響,該操作點(diǎn)的最佳分離性能往往難以實(shí)現(xiàn),因而操作點(diǎn)往往會(huì)選擇靠近該頂點(diǎn)的位置。
在實(shí)際過(guò)程中除了擴(kuò)散作用還有傳質(zhì)阻力的影響,這些都影響三角分離區(qū)的變化。Pais等[31]報(bào)道了傳質(zhì)阻力對(duì)模擬移動(dòng)床操作分離區(qū)的影響,結(jié)果證明隨傳質(zhì)阻力增大操作分離區(qū)的區(qū)域減小。另外,系統(tǒng)死體積會(huì)引起三角操作區(qū)位置的偏移[33]。針對(duì)本研究選擇的分離體系,吸附分離因子較大,約為 2.6。當(dāng)進(jìn)料濃度較低時(shí),非線性競(jìng)爭(zhēng)型Langmuir吸附作用不強(qiáng),設(shè)計(jì)的三角形操作區(qū)域較大,如圖5所示,采用Varicol工藝很容易分離愈創(chuàng)木酚甘油醚。增加進(jìn)料濃度,非線性作用變強(qiáng),實(shí)際的操作區(qū)域變得越窄,愈創(chuàng)木酚甘油醚分離操作條件選擇越嚴(yán)格。
4 結(jié) 論
針對(duì)Chiralcel OD為手性固定相、乙醇/正己烷為流動(dòng)性相的 Varicol工藝分離愈創(chuàng)木酚甘油醚對(duì)映體體系,建立了異步切換的Varicol過(guò)程的數(shù)學(xué)模型,采用有限元正交配置法對(duì)模型進(jìn)行數(shù)值求解。該模型能夠較好地預(yù)測(cè)愈創(chuàng)木酚甘油醚對(duì)映體在模擬移動(dòng)床多個(gè)色譜柱內(nèi)的濃度曲線分布。隨著進(jìn)出料口位置的不斷切換,強(qiáng)吸附組分(S)-對(duì)映體(S-GUA)逐漸移動(dòng)到萃取液口位置,弱吸附組分(R)-對(duì)映體(R-GUA)逐漸移動(dòng)到萃余液口位置。當(dāng)多次循環(huán)操作(如10次)后,系統(tǒng)達(dá)到穩(wěn)定狀態(tài),優(yōu)化工藝條件,在萃取液口位置能夠回收高純度的S-GUA,在萃余液口位置能夠回收高純度的R-GUA。
由動(dòng)態(tài)切換的 Varicol工藝的數(shù)學(xué)模型計(jì)算愈創(chuàng)木酚甘油醚分離操作區(qū),選擇高純度對(duì)映體(99%R-GUA和99% S-GUA)分離條件。基于設(shè)計(jì)的操作條件,進(jìn)行5柱Varicol工藝(1-1.5-1.5-1)的分離愈創(chuàng)木酚甘油醚對(duì)映體實(shí)驗(yàn)。結(jié)果表明,S-GUA和 R-GUA兩個(gè)組分實(shí)現(xiàn)了 99.0%的高純度的分離結(jié)果,滿足設(shè)計(jì)要求,與理論預(yù)測(cè)基本吻合。因此建立的數(shù)學(xué)模型能夠較好地預(yù)測(cè)愈創(chuàng)木酚甘油醚對(duì)映體的Varicol工藝分離過(guò)程,為工業(yè)化設(shè)計(jì)提供基礎(chǔ)理論依據(jù)。
符 號(hào) 說(shuō) 明
ci,k——組分i在第k根色譜柱中的液相質(zhì)量濃度,kg·m?3
Dax,i——軸向擴(kuò)散系數(shù),m2·s?1
F——相比[F= ( 1 ?εT)/εT],m2·s?1
j——區(qū)數(shù)(j=1,2,3,4)
KL——傳質(zhì)系數(shù),m·s?1
k——柱子數(shù)目(k=Ⅰ,Ⅱ,Ⅲ,Ⅳ,Ⅴ)
Lk——第k根色譜柱長(zhǎng)度,m
mj——第j區(qū)凈流速比
qeq,i,k——組分在固相中的質(zhì)量濃度,kg·m?3
——與液相濃度平衡時(shí)的固相質(zhì)量濃度,kg·m?3
t——時(shí)間,s
ts——切換時(shí)間,s
u——線速度,m·s?1
Vc——色譜柱體積,m3
v1,v2,v3,v4——1~4 區(qū)內(nèi)的間隙流速,m·s?1
z——軸向坐標(biāo),m
εT——總孔隙率
[1]Li Ling (李凌), Jing Yuanwei (井元偉), Yuan Decheng (袁德成).Simulated moving bed adsorption separation technology and its applications [J].Computers and Applied Chemistry(計(jì)算機(jī)與應(yīng)用化學(xué)), 2007, 24 (4): 441-444
[2]Cai Yujie (蔡宇杰), Ding Yanrui (丁彥蕊), Zhang Dabing (張大兵),Dai Jun (戴軍), Shi Guiyang (石貴陽(yáng)), Xu Wenbo (須文波).Simulated moving bed technology and its applications [J].Chinese Journal of Chromatography(色譜), 2004, 22 (2): 111-115
[3]Wei Feng (危風(fēng)),Shen Bo (沈波),Chen Mingjie (陳明杰),Zhou Xianbo (周先波),Wu Pingdong (吳平東). Omeprazole resolution by simulated moving bed chromatography [J].Journal of Chemical Industry and Engineering(China)(化工學(xué)報(bào)), 2005, 56 (9):1699-1702
[4]Rajendran A, Paredes Galatea, Mazzotti M. Simulated moving bed chromatography for the separation of enantiomers [J].Journal of Chromatograpy A, 2009, 1216: 709-738
[5]Li P, Xiu G H, Rodrigues A E. Proteins separation and purification by salt gradient ion-exchange SMB [J].AIChE Journal, 2007, 53:2419-2431
[6]Migliorini C, Wendlinger M, Mazzotti M, Morbidelli M. Temperature gradient operation of a simulated moving bed unit [J].Industrial Engineering Chemistry Research, 2001, 40: 2606-2617
[7]Peper S, Lubbert M, Johannsen M, Brunner G. Separation of ibuprofen enantiomers by supercritical fluid simulated moving bed chromatography [J].Separation Science and Technology, 2002, 37:2545-2566
[8]Toumi A, Hanisch F, Engell S. Optimal operation of continuous chromatographic processes: mathematical optimization of the VARICOL process [J].Industrial & Engineering Chemistry Research,2002, 41: 4328-4337
[9]Schramm H, Kaspereit M, Kienle A, Seidel-Morgenstern A.Simulated moving bed process with cyclic modulation of the feed concentration [J].Journal of Chromatography A, 2003, 1006: 77-86
[10]Zhang Z Y, Mazzotti M, Morbidelli M. Power feed operation of simulated moving bed units: changing flow-rates during the switching interval [J].Journal of ChromatographyA, 2003, 1006: 87-99
[11]Shen B, Chen M J, Jiang H L, Zhao Y X, Wei F. Modeling study on a Three-zone simulated moving bed without zone Ⅰ [J].Separation Science and Technology, 2011, 46: 695-701
[12]Wang X, Ching C B. Chiral separation of beta-blocker drug (nadolol)by five zone simulated moving bed chromatography [J].Chemical Engineering Science, 2005, 60: 1337-1347
[13]Wankat P C. Simulated moving bed cascades for ternary separations[J].Industrial & Engineering Chemistry Research,2001, 40:6185-6193
[14]Lorenz H, Sheehan P, Seidel-Morgenstern A. Coupling of simulated moving bed chromatography and fractional crystallization for efficient enantioseparation [J].Journal of Chromatography A, 2001,908: 201-214
[15]Ludemann-hombourger O, Nicoud R M. The “varicol” process: a new multicolumn continuous chromatographic process [J].Separation Science and Technology, 2000, 35: 1829-1862
[16]Ludemann-Hombourger O, Pigorini G, Nicoud R M, Terfloth G.Application of the ‘VARICOL’ process to the separation of the isomers of the SB-553261 racemate [J].Journal of Chromatography A, 2002, 947: 59-68
[17]Toumi A, Engell S, Ludemann-Hombourger O, Nicoud R M, Bailly M. Optimization of simulated moving bed and Varicol processes [J].Journal of Chromatography A, 2003, 1006: 15-31
[18]Zhang Y, Hidajat K, Ray A K, Morbidelli M. Multiobjective optimization of SMB and Varicol process for chiral separation [J].AIChE Journal, 2002, 48: 2800-2816
[19]Zhang Y, Hidajat K, Ray A K. Multi-objective optimization of simulated moving bed and Varicol processes for enantio-separation of racemic pindolol [J].Separation and Purification Technology, 2009,65: 311-321
[20]Da Silva A C, Salles A C, Perna R F, Correia C R D, Santana C C.Chromatographic separation and purification of mitotane racemate in a Varicol multicolumn continuous process [J].Chemical Engineering Technology, 2012, 35: 83-90
[21]Rodrigues R C R, Araujo J M M, Eusebio M F J, Mota J P B.Experimental of assessment of simulated moving bed and Varicol processes using a single-column setup [J].Journal of Chromatography A, 2007, 1142: 69-80
[22]Huang Yongdong (黃永東), Jiang Heyuan (江河源), Jiang Yongwen(江用文), Zhang Jianyong (張建勇), Wang Bin (王斌), Bai Yan (白艷), Wen Zhihao (文志浩), Wang Weiwei (王偉偉). Comparison of Varicol and partial-discard process with traditional process to purify ECG and EGCG from green tea polyphenols using simulated moving bed chromatography [J].Journal of Tea Science(茶葉科學(xué)), 2011, 31(3): 201-210
[23]Lu J G. Numerical simulation of asynchronous simulated moving bed chromatography [J].Chinese Journal of Chemical Engineering, 2004,12: 415-420
[24]Xiao Di (肖迪), Ge Qicheng (葛啟承), Lin Jinguo (林錦國(guó)).Dynamic simulation of simulated moving bed based on Vericol [J].Computers and Applied Chemistry(計(jì)算機(jī)與應(yīng)用化學(xué)), 2012, 29:567-570
[25]Gong R J, Lin X J, Li P, Yu J G, Rodrigues A E. Experiment and modeling for the separation of guaifenesin enantiomers using simulated moving bed and Varicol units [J].Journal of Chromatography A,2014, 1363: 242-249
[26]Yang Minglei (楊明磊), Wei Min (魏民), Hu Rong (胡蓉), Ye Zhencheng (葉貞成), Qian Feng (錢峰). Modeling of simulated moving bed for xylene separation [J].CIESC Journal(化工學(xué)報(bào)),2013, 64 (12): 4335-4341
[27]Wu Xiandong (吳獻(xiàn)東), Jin Xiaoming (金曉明), Su Hongye (蘇宏業(yè)).Multi-objective optimization of simulated moving bed chromatography separation based on NSGA-Ⅱ algorithm [J].Journal of Chemical Industry and Engineering(China)(化工學(xué)報(bào)), 2007, 58 (8):2038-2044
[28]Li Ling (李凌), Yuan Decheng (袁德成), Jing Yuanwei (井元偉).Simulated moving bed process modeling and performance analysis [J].Computers and Applied Chemistry(計(jì)算機(jī)與應(yīng)用化學(xué)), 2013, 30(11): 1289-1293
[29]Gong R J, Lin X J, Li P, Yu J G, Rodrigues A E. Adsorption equilibrium and kinetic study of guaifenesin enantiomers on cellulose tris 3,5-dimethylphenylcarbamate packed column [J].Chemical Engineering Journal, 2014, 244: 128-136
[30]Pais L S, Rodrigues A E. Design of simulated moving bed and Varicol processes for preparative separations with a low number of columns[J].Journal of Chromatography A, 2003, 1006: 33-44
[31]Pais L S, Loureiro J M, Rodrigues A E. Separation of enantiomers of a chiral epoxide by simulated moving bed chromatography [J].Journal of Chromatography A, 1998, 827: 215-233
[32]Zhang Y, Hidajat K, Ray A K. Enantio-separation of racemic pindolol onα1-acid glycoprotein chiral stationary phase by SMB and Varicol[J].Chemical Engineering Science, 2007, 62: 1364-1375
[33]Migliorini C, Mazzotti M, Morbidelli M. Simulated moving-bed units with extra-column dead volume [J].AIChE Journal, 1999, 45:1411-1421

