抗栓小肽RWR的毒理學試驗研究
鄭海鋒,趙海霞,王少華,楊濤,楊利軍
(山西醫科大學 生物化學與分子生物學學科 省部共建細胞生理學教育部重點實驗室,山西 太原 030001)
?
抗栓小肽RWR的毒理學試驗研究
鄭海鋒,趙海霞,王少華,楊濤,楊利軍Δ
(山西醫科大學 生物化學與分子生物學學科 省部共建細胞生理學教育部重點實驗室,山西 太原 030001)
目的 對具有自主知識產權的抗栓小肽RWR進行毒理學研究和安全性評價。方法 分別對RWR進行小鼠急性毒性試驗、小鼠骨髓細胞微核形成試驗、小鼠精子畸形試驗和大鼠30d喂養試驗。結果 急性毒性試驗動物經腹腔注射MTD大于120 mg/kg;骨髓細胞微核試驗、精子畸形試驗結果均為陰性;大鼠30 d喂養試驗對大鼠體質量、食物利用率、臟器系數、血生化等各項指標均未見不良影響。病理組織學觀察肺、肝、脾、腎、心臟均未見明顯與注射樣品有關的組織學病理改變。結論 在本試驗條件下,RWR對動物的生長發育、造血功能、肝腎功能、器官組織均無明顯毒性作用。
RWR;毒理學;安全性
心腦血管疾病是嚴重危害人類健康的常見病,特別是心肌梗死、腦梗塞等血栓性疾病危害更大。纖維蛋白原α鏈中的RGD(Arg-Gly-Asp)序列與血小板表面整合素αIIbβ3(GPⅡb/Ⅲa)特異性結合是血栓形成的最終途徑[1-3]。阻斷此過程即可阻斷各種病理性的血栓形成。含有RGD序列的多肽可以競爭性抑制纖維蛋白與血小板結合,從而抑制血栓形成[4-6]。本課題組根據含RGD序列多肽的抗栓特性及血栓性疾病研究現狀,在RGD序列的基礎上,設計合成了一種新型小肽RWR(Arg-Gly-Asp-Trp-Arg)[7]。初步藥效學研究表明RWR通過與血小板表面整合素αIIbβ3受體結合,抑制血小板聚集從而起到抗栓作用,其分子量小,免疫原性低,抗血小板活性強[8]。為探討RWR作為抗血栓藥物的可行性,給臨床用藥提供合理、可靠的科學依據,本文旨在對RWR進行毒理學安全性研究。
1 材料與方法
1.1 藥物 小肽RWR由上海強耀生物科技有限公司合成(純度≧95.10%);環磷酰胺(cyclophosphamide,monohydrate)購自Sigma公司。
1.2 儀器 Beckman AU5800生化儀2;KDC-2046低速冷凍離心機;美國Thermo冷凍切片機;日本Olympus IX51光學顯微鏡。
1.3 實驗動物 試驗用昆明小鼠、SD大鼠均從北京維通利華實驗動物技術有限公司購買,許可證號:SCXK(京)2012-0001。
1.4 實驗方法
1.4.1 急性毒性試驗:昆明小鼠50只,雌、雄各半,體質量18~22 g,隨機分為5組。①陰性對照組:生理鹽水組;②RWR 24 mg/kg組;③RWR 48 mg/kg組;④RWR 96 mg/kg組;⑤RWR 120 mg/kg組。給藥組每組用生理鹽水配置相應的RWR溶液,濃度分別為0.12%、0.24%、0.48%、0.6%,2次腹腔注射給藥,間隔3 h,每次腹腔注射0.2 mL/10 g,對照組注射相應體積的生理鹽水,所用小鼠注射體積范圍為0.36~0.44 mL。連續觀察14 d動物反應情況,記錄動物外觀、活動狀態,大、小便性狀及顏色、被毛、呼吸、鼻、眼、口腔分泌物及死亡情況。
1.4.2 小鼠骨髓細胞微核形成試驗:昆明小鼠50只,雌、雄各半,體質量25~30 g,隨機分為5組。①陽性對照組:環磷酞胺(40 mg/kg);②陰性對照組:生理鹽水組;③RWR 24 mg/kg組;④RWR 96 mg/kg組;⑤RWR 120 mg/kg組。給藥組每組用生理鹽水配置相應的RWR溶液,濃度分別為0.12%、0.48%、0.6%,2次腹腔注射給藥,間隔24 h,每次腹腔注射0.15 mL/10 g,所用小鼠注射體積范圍為0.37~0.45 mL。第2次給相同劑量受試藥物后6 h頸椎脫臼處死小鼠,取胸骨骨髓細胞制片。觀察骨髓多染性紅細胞微核并計算微核發生率,以千分數(‰)表示。
1.4.3 小鼠精子畸形試驗:昆明小鼠25只,體質量25~30 g。分組同小鼠骨髓細胞微核生成率實驗,給藥組每組用生理鹽水配置相應的RWR溶液,濃度分別為0.12%、0.48%、0.6%,每天腹腔注射1次,每次注射0.15 mL/10 g,所用小鼠注射體積范圍為0.37~0.45 mL。連續5 d。于首次給藥后第35天處死小鼠,取兩側附睪精子濾液按常規制片、鏡檢。每只小鼠計數5000個結構完整的精子,計算精子畸變率(以百分率計)。
1.4.4 30d喂養試驗:SD大鼠80只,雌、雄各半,體質量70~75 g,隨機分為4組。①陰性對照組:生理鹽水組;②RWR 4.5 mg/kg組;③RWR 18.8 mg/kg組;④RWR 75.0 mg/kg組(分別為有效劑量的6倍、25倍和100倍),每組用生理鹽水配置相應的RWR溶液,濃度分別為0.09%、0.376%、1.5%,連續給藥30 d,每次注射0.5 mL/100g,所用大鼠注射體積范圍為0.35~1.5 mL。給藥前及給藥期間每周記錄1次大鼠體質量和進食量,給藥結束后空腹過夜,眼眶采血檢測血液生化學指標,稱取體質量及其肝、腎、脾、卵巢(睪丸)的重量,計算臟體比,并取肝、脾、腎、心臟、肺組織作HE染色,觀察其組織形態學變化。

2 結果
2.1 急性毒性試驗 在14 d的觀察過程中,RWR按照24、48、96、120 mg/kg注射給藥,陰性對照組注射相應體積的生理鹽水,觀察小鼠無一死亡,無明顯的中毒癥狀,無不良反應,外觀健康,行為活潑,被毛光滑、體質量、呼吸及大小便正常,鼻、眼和口腔未發現異常分泌物。可以認為RWR藥物的小鼠經腹腔1天最大耐受量大于120 mg/kg(高出前期藥效學有效劑量的100多倍),則可認為該藥物在給藥有效劑量條件下安全性較好。
2.2 RWR對小鼠骨髓微核形成的影響 隨著RWR濃度的增大,骨髓多染紅細胞微核形成率差異無統計學意義,各劑量組與陰性對照組比較差異無統計學意義,陽性對照組與陰性對照組比較,骨髓多染紅細胞微核形成率顯著性增大(P<0.01)。見表1。

表1 RWR對小鼠骨髓細胞微核形成試驗Tab.1 The assay of RWR on MN formation of PCE
*P<0.01,與各性別下陰性對照組比較,compared with negative control group in each gender
2.3 RWR對小鼠精子畸變率的影響 隨著RWR濃度的增大,各劑量組精子畸變率差異無統計學意義,各劑量組精子畸形率與陰性對照組比較,均差異無統計學意義,陽性對照組與陰性對照組比較,精子畸變率有顯著增大(P<0.01)。見表2。
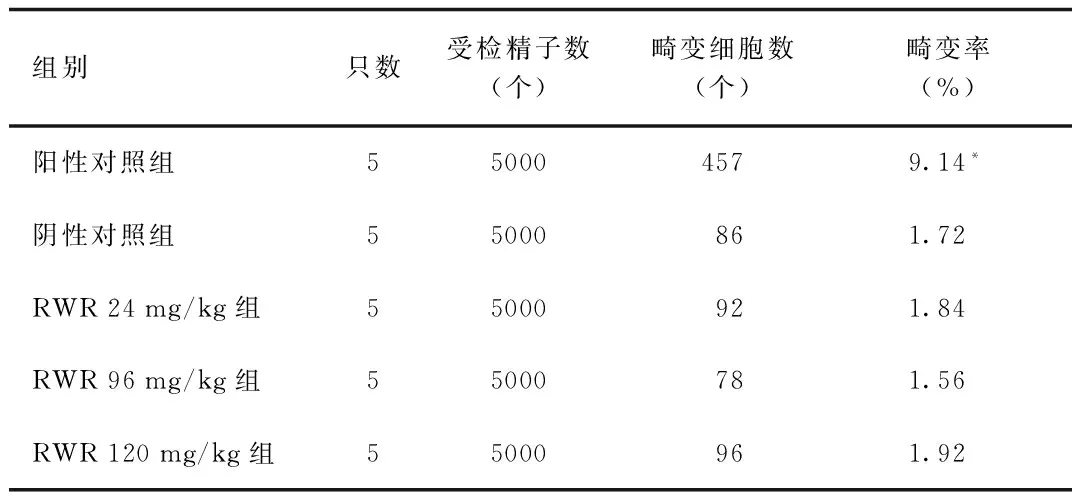
表2 RWR對小鼠精子畸形試驗Tab.2 The assay of RWR on mice sperm aberration rate
*P<0.01,與陰性對照組比較,compared with negative control group
2.4 30 d喂養試驗
2.4.1 RWR對大鼠體質量、食物利用率的影響 在30 d喂養試驗過程,各組動物狀況良好,未發現有中毒癥狀,亦無動物死亡。隨著RWR濃度增大,大鼠每周平均體質量、每周食物利用率和總的食物利用率差異無統計學意義,且各給藥組與生理鹽水組間差異無統計學意義。見表3、表4。

表3 RWR對SD大鼠體質量的影響Tab.
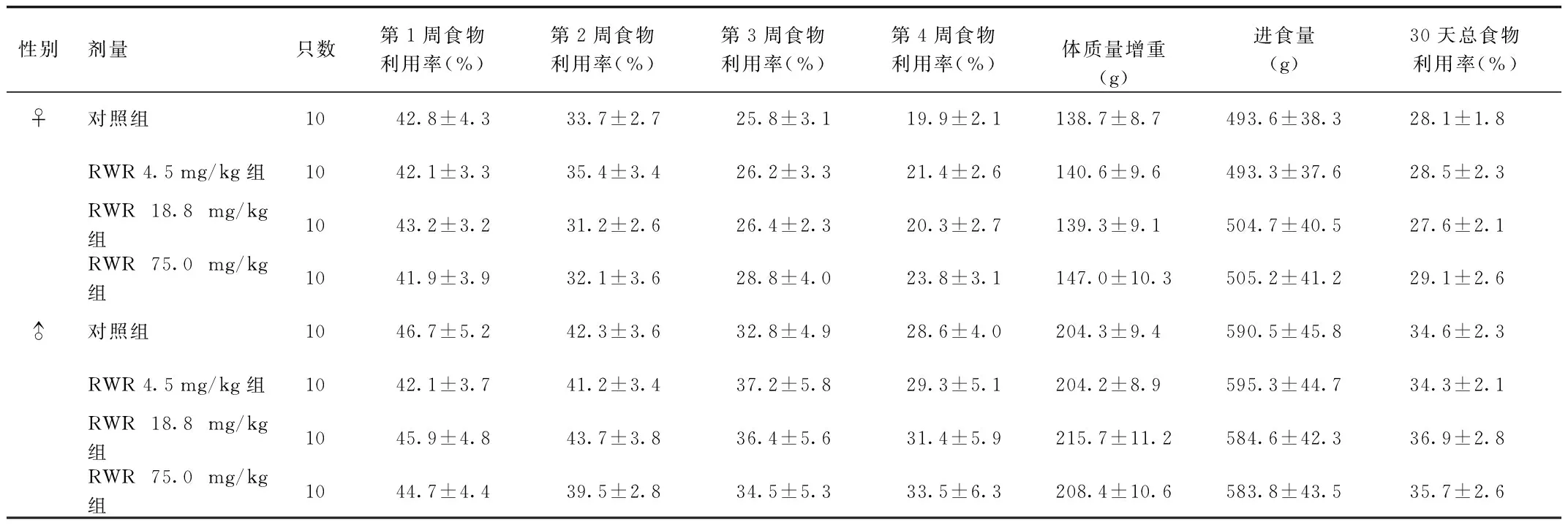
表4 RWR對大鼠食物利用率和體質量增重的影響Tab.4 Effect of RWR on rat food utilization rate and the increase of body weight
2.4.2 RWR對血液各生化指標的影響:在大鼠30 d喂養試驗中,隨著RWR濃度的增大,各劑量組間相比較,各生化指標均差異無統計學意義,且各劑量組與對照組相比較,各生化指標均差異無統計學意義,且均在生理正常范圍內。見表5。

表5 RWR靜脈注射給藥30 d對大鼠血液生化學指標的影響Tab.5 Effect of RWR on rats blood biochemical indexes among 30 day intravenous RWR
2.4.3 RWR對大鼠臟體比的影響:隨著RWR濃度的增大,各劑量組間的臟器系數均無明顯差異;且各劑量組與對照組比較,臟器系數差異均無統計學意義。見表6。

表6 RWR靜脈注射給藥30 d對大鼠臟器系數的影響Tab.6 Effect of RWR on the organ coefficient of rats among 30 day intravenous RWR
2.4.4 RWR對各臟器組織結構的影響,組織病理學觀察:RWR注射30 d后,各臟器外形、色澤、位置、大小未見明顯異常;取各組大鼠肝、脾、腎、心臟、肺組織,做HE染色。結果均未見明顯異常。見圖1、圖2。

圖1 雌性大鼠臟器HE染色組織形態學(HE,×400)Fig.1 HE stained with tissue morphology of organs in the female rat(HE, ×400)
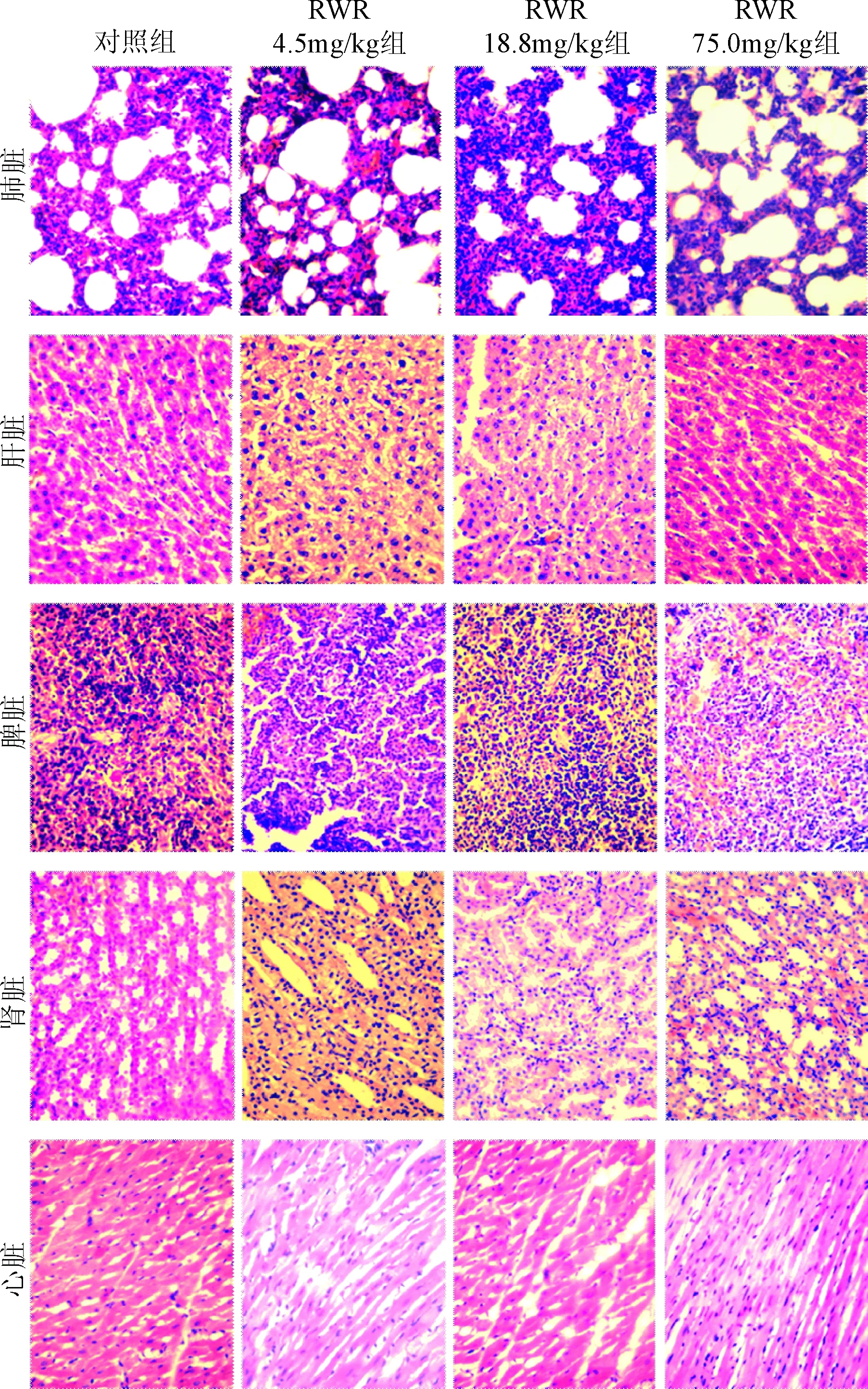
圖2 雄性大鼠臟器HE染色組織形態學(HE,×400)Fig.2 HE stained with tissue morphology of organs in the male rat (HE,×400)
3 討論
RGD序列為人纖維連接蛋白與其受體的結合點,能與αIIbβ3受體特異性結合[9,10]。血栓形成時,纖維蛋白α鏈的兩個RGD肽序可被活化的血小板αIIbβ3受體特異性識別[11-12],在相鄰的血小板之間形成橫橋,而一個血小板又可與多個纖維蛋白原結合,使血小板通過整合素αIIbβ3受體與纖維蛋白原“橋聯”黏聚成團,促使血小板聚集,介導纖維蛋白與血小板的結合,該過程猶如鏈條,把相鄰的血小板連在一起,形成血栓[13-14]。含RGD序列的小肽或藥物也可與纖維蛋白原的RGD序列競爭性結合活化的血小板膜整合素αIIbβ3 受體,從而抑制整合素αIIbβ3介導的生物學效應從而抑制血栓形成。因此含RGD序列的多肽衍生物作為抗栓劑受到廣泛重視。
RGD小肽僅能與血栓部位活化的血小板整合素αIIbβ3受體特異性結合,而對循環血小板無影響,這正是RGD小肽發揮血栓靶向性作用的基礎[15],另外整合素αIIbβ3在休眠的內皮細胞和其他正常組織中低表達甚至不表達[16],因此RGD小肽主要藥效以外的作用更弱,即對藥效學以外的組織器官毒性更低,為治療血栓性疾病提供了一種新的途徑,而且其獨特的抗血小板聚集、抑制血栓形成的作用具有其它抗血栓藥物無法比擬的優點,使得治療血栓性疾病靶向性用藥有了更好的發展前景。如果能證實其毒副作用很小,符合多肽類藥物的毒理學標準,將為進一步進入臨床研究奠定基礎。本研究即是在其基礎上進行的毒理學研究和評價。
RWR急性毒性實驗LD50>120 mg/kg,小鼠骨髓細胞微核生成率實驗、小鼠精子畸變率試驗、30 d喂養試驗均為陰性結果,可說明RWR小肽毒性很低。這是由于本實驗所用藥品RWR與纖維蛋白原相比,其分子量僅為689.7,而纖維蛋白原的分子量為45000,小分子量的RWR受到空間干擾的因素更小,可以更加有效的阻斷纖維蛋白原與整合素αIIbβ3受體的相互作用,并且由于其分子量相對小,代謝產物組成種類相對少,這也可以有效減少其藥效以外的毒性作用。
考慮到RWR的藥用有效劑量,在本實驗條件下,并未測出其LD50值,這與肽類物質本身穩定性相對較低、易于受到生物體代謝酶的降解有關外,還與含RGD序列的肽類衍生物的靶向性有關,特別是課題組在RGD序列的基礎上引入疏水性極強的疏水氨基酸W,同時引入R,使其與受體的結合力更強,作用效果更好[7,17],進而使其用藥相對有效劑量降低、在生物體內單位體積分布下降,這個也是其毒性相對較低的一個因素。本試驗條件下,RWR符合藥品安全性毒理學評價標準對藥品的要求,作為藥用,RWR有進一步開發利用價值。
[1] Badimon L,Vilahura G.Coronary atherothrombotic disease: progress in antiplatelet therapy[J].Rev Esp Cardiol,2008,61(5):501-513.
[2] 徐偉,曹蘅.IIb/IIIa受體抑制劑治療急性冠脈綜合征的最新研究進展[J].心臟雜志,2014,26(2):233-235.
[3] Wang Y,Zhao Y,Sun R,et al.Discovery of novel antagonists of glycoprotein IIb/IIIa-mediated platelet aggregation through virtual screening[J].Bioorg Med Chem Lett,2015,25(6):1249-1253.
[4] Rognoni A,Lupi A,Secco GG,et al.Update on glycoprptein IIb/IIIa:role in primary coronary intervention[J].Cordiovasc Hemotal Agents Med Chem,2011,9(2):106-112.
[5] Haubner R,Bruchertseifer F,Bock M,et al.Synthesis and biological evaluation of a (99m)Tc-labelled cyclic RGD peptide for imaging the alphavbeta3 expression[J].Nuklearmedizin,2004,43(1):26-32.
[6] Lu WF,Mo W,Liu Z ,et al.The antithrombotic effect of a novel hirudin derivative after reconstruction of carotid artery in rabbits[J].Thrombosis Res,2010,126(4):e339-e443.
[7] 楊利軍,楊濤,孫海飚,等.一種特異性識別血小板αIIbβ3的抗栓藥物RWR[P].中國專利:CN201110321825.X,2012-2-15.
[8] 趙海霞,楊濤,楊利軍.RWR通過與血小板表面整合素αIIbβ3受體作用對血栓形成的影響[J].中國生物制品學雜志,2013,26(8):1126-1129.
[9] Hass TA.Allosteric regulation of alpha (IIb)beta(3)by beta(3)95-105.Thromb Haemost[J].2008,99(4):701-710.
[10] Willmann JK,Kimura RH,Deshpande N,et al.Targeted contrast-enhanced ultrasound imaging of tumor angiogenesis with contrast microbubbles conjugated to integrin-binding knottin peptides[J].J Nucl Med,2010,51(3):433-440.
[11] Avraamides CJ,Garmy-Susini B,Varner JA.Integrins in angiogenesis and lymphangiogenesis[J].Nat Rev Cancer,2008,8(8):604-617.
[12] Shanley DK,Kiely PA,Golla K,et al.Pregnancy-specific glycoproteins bind integrin αIIbβ3 and inhibit the platelet-fibrinogen interaction[J].PLoS One,2013,8(2):e57491.
[13] Cho J,Mosher DF.Enhancement of thrombogenesis by plasma fibronectin cross-linked to fibrin and assembled in platelet thrombi[J].Blood,2006,107(9):3555-3563.
[14] Mehrbod M,Trisno S,Mofrad MR.On the activation of integrin αIIbβ3: outside-in and inside-out pathways[J].Biophys ical Journal,2013,105(6):1304-1315.
[15] Sun YH, Rolán HG,Den Hartigh AB,et al.Brucella abortus virB12 is expressed during infection but is not an essential component of the type IV secretion system[J].Infect Immun,2005,73(9):6048-6054.
[16] Somanath PR,Malinin NL,Byzova TV.Cooperation between integrin alphavbeta3 and VEGFR2 in angiogenesis[J].Angiogenesis,2009,12(2):177-185.
[17] Zhang JG,Krajden OB,Kainthan RK,et al.Conjugation to hyperbranched polyglycerols improves RGD-mediated inhibition of platelet function in vitro[J].Bioconjug Chem,2008,19(6):1241-1247.
(編校:譚玲)
Toxicological assessment of antithrombotic small peptide RWR
ZHENG Hai-feng, ZHAO Hai-xia, WANG Shao-hua, YANG Tao, YANG Li-junΔ
(Department of Biochemistry and Molecular Biology, Key Laboratory of Cellular Physiology of Ministry of Education, Shanxi Medical University, Taiyuan 030001, China)
ObjectiveTo evaluate the toxicological safety of antithrombotic small peptide RWR with independent intellectual property right.MethodsToxicity test in mice, mice bone marrow micronucleus assay, mice sperm abnormality test, and 30-day feeding test in rats were carried out in this study.ResultsThe MTD of acute toxicity test for rats was larger than 120 mg/kg.The results of bone marrow micronucleus assay, mice sperm abnormality test were all negative.Thirty-day feeding test had no adverse effects on body weight, food utility rate, organ coefficient, blood routine index of rats.There was also no histological changes related to RWR in lung, liver, spleen, kidney and heart of rats.ConclusionRWR had no obvious toxicity on animal growth, hematopoietic function, kidney function and organ tissue and so on.
RWR; toxicology; safety
國家科技部重大新藥創制計劃(2012ZX09103301-010);山西省自然科學基金(2012011041-5);國家自然科學基金青年基金(81101895);山西省高等學校優秀青年學術帶頭人支持計劃[晉教科(2012)10號]
鄭海鋒,男,碩士,研究方向:含RGD小肽的設計合成及功能研究,E-mail:zhenhaifeng215@foxmail.com;楊利軍,通訊作者,男,博士,副教授,研究方向:系列蛋白多肽藥物的設計合成和生物學活性研究,E-mail:yanglijunmm@126.com。
R996.3
A
1005-1678(2015)08-0006-05

