動物胰島素與人胰島素在中國糖尿病患者中的安全性和有效性對比:Meta分析
趙家軍 張賀娜 王柯 楊軍
1山東大學附屬省立醫院內分泌科;2禮來蘇州制藥有限公司上海分公司
1 前言
糖尿病在全球范圍內給人類健康和社會經濟發展帶來嚴重的危害。在我國,糖尿病也是一個日益嚴峻的公共衛生問題[1-4]。近年來隨著生活方式和飲食習慣的改變以及人口的老齡化,中國人群中糖尿病的患病率急速升高[1-3,5]。據估計,中國成年人中糖尿病的患病率已經由1980年的0.67%[5]增至2008年的9.7%[1]。
胰島素治療對于糖尿病及其并發癥的照護非常重要。糖尿病的發病機理是由于胰島β細胞胰島素分泌缺陷(1型糖尿病)和/或機體對胰島素不敏感(2型糖尿病),從而導致碳水化合物、脂肪和蛋白質代謝的缺陷[6]。長期患糖尿病將導致視網膜、周圍神經和腎臟等組織和器官的病變,以及增加心血管系統病變的風險[6]。1型糖尿病患者必須進行胰島素注射治療,而2型糖尿病患者隨著其胰島β細胞功能的不斷惡化,僅通過改變生活方式和口服降糖藥常無法有效控制血糖,大約50%的患者在啟用口服降糖藥6年后即需胰島素注射治療[7]。因此,胰島素治療對于控制血糖和防治糖尿病長期并發癥尤為重要。針對胰島素的長期臨床應用已經充分證明了使用胰島素控制血糖的安全性和有效性。由牛、豬和羊的胰腺組織提純的動物胰島素曾經被廣泛用于臨床治療糖尿病。當前,動物胰島素在一些地區仍有應用。重組人胰島素自上個世紀八十年代開始被用于治療糖尿病[8]。與動物胰島素相比,重組人胰島素的免疫原性較低,誘導產生的胰島素抗體較少[9]。但是,重組人胰島素對于控制高血糖癥的安全性和有效性是否優于動物胰島素仍有爭議[10,11]。
現有的系統評價和M eta分析[12,13]顯示,在白種人糖尿病患者中,人胰島素和動物胰島素有相似的安全性和有效性。在白種人糖尿病患者中,與牛或豬胰島素相比,人胰島素對于降低血漿糖化血紅蛋白(hemoglobin A 1c,HbA1c)的效果更好一些,但是其差異未達到統計學的有效意義[12]。動物胰島素和人胰島素在空腹血糖濃度和注射部位不良反應的發生率方面無差異[12,13],在低血糖的發生率方面無差異,在血糖達到滿意控制時的每日劑量無差異[12]。但研究顯示,當患者由動物胰島素轉換為人胰島素治療后, 其血漿胰島素抗體濃度有輕度降低[12]。然而,在中國糖尿病患者中尚缺乏類似的系統評價和M eta分析。
在全球范圍內,動物胰島素正逐漸被重組人胰島素所代替,但是在中國,動物胰島素仍然被廣泛使用[14]。過去,有一系列的研究[15-37]比較了動物胰島素和人胰島素在中國糖尿病患者中的安全性和有效性。但這些研究的樣本多數都較小,因此缺乏足夠的統計學效力。基于上述原因,我們對文獻進行了系統的檢索并對有關研究進行Meta分析。本Meta分析比較了動物胰島素和人胰島素在中國糖尿病患者中的安全性和有效性。
2 資料與方法
2.1 檢索策略
以人胰島素(或優泌林、諾和靈、甘舒霖)和動物胰島素(或豬胰島素、牛胰島素、羊胰島素)為主題詞檢索中國期刊全文數據庫(1994~2013.11)、V IP維普數據庫(1989~2013.11)、中國生物醫學文獻數據庫(1 9 7 8 ~2 0 1 3.11)、萬方數據庫(1997~2013.11);以hum an insu lin(或Humu lin、 Novolin、Gansulin)、animal insulin(或porcine insulin、 pork insulin、beef insulin、sheep insulin)和China(或Chinese、Taiw an、Taiw anese、Hong Kong)檢索MEDLINE(1966~2013.11)。
2.2 納入和排除標準
同時符合以下條件的文獻被納入:①研究為隨機對照試驗(random izedcontrolledtrial,RCT)、非隨機對照試驗(non-random izedcontrolledtrial,NRCT)和由動物胰島素治療轉換為人胰島素治療的轉換試驗(sw itch studies,SW)。②對動物胰島素和人胰島素在中國糖尿病患者中的使用進行平行比較或前后比較。③至少報告接受動物胰島素或人胰島素治療后一項臨床結局指標:空腹血糖濃度(fasting blood glucose,FBG),餐后2h血糖濃度((2h-postprandial plasma glucose,2h-PBG),達到滿意控制血糖時的每日胰島素用量和HbA1c水平,不良反應如低血糖癥、過敏反應和注射部位局部反應的發生率。
排除標準:①重復研究;②動物試驗;③非最終試驗報告;④會議論文或摘要。
2.3 文獻篩選和數據提取
由一位研究者檢索文獻、閱讀標題和摘要并按照納入和排除標準對文獻進行篩選,對無法確定的文獻進行全文閱讀并與另一位研究者討論決定是否納入。對有關系統評價的參考文獻部分進行手工檢索以發現符合納入標準的研究。納入研究中的數據由一位研究者提取并經另一位研究者確認,提取的數據主要包括:①一般資料:題目、作者、發表日期和文獻來源。②研究特征:包括隨機方法、對照、治療時間和樣本大小。③治療前后的臨床結局指標:FBG、2h-PBG、達到滿意控制血糖時的每日胰島素用量和HbA1c。④接受胰島素治療前后的不良反應發生率:低血糖癥、過敏反應和注射部位局部反應。當RCT 和NRCT中部分患者由動物胰島素轉為人胰島素治療且具有其基線數據時,則該部分患者也將并入SW進行分析。
基于不同劑型或不同方案胰島素的選擇對胰島素療效和安全性的可能影響[38],我們對納入研究中明確表明對使用相同劑型的動物或人胰島素的試驗數據進行了亞組分析。
2.4 數據質量評估
使用Jadad[39]評分標準對納入的研究的質量(包括隨機序列的產生方法、隨機化隱藏、盲法和試驗退出或撤出)進行評估。
2.5 統計分析
采用統計計算R項目(http://www.r-project.org)提供的R軟件(2.15.1版本)進行M eta分析。對于某一臨床結局指標,如有3篇或3篇以上文獻進行了報告則進行M eta分析。計量數據采用均數差(MD),計數數據采用相對危險度(RR),各效應量以95%置信區間(95%CI)表示。各研究的異質性采用Cochran Q檢驗。當各研究有統計學同質性時,采用固定效應模型進行合并分析。當各研究有明顯統計學異質性時(P<0.05),采用隨機效應模型進行合并分析。對于采用相對危險度報告的臨床結局指標,在固定效應模型下采用Mantel-Haenzsel Chi2檢驗進行比較;或在隨機效應模型下采用Dersimonian-Laird檢驗進行比較。動物胰島素組與人胰島素組間采用雙側t分布檢驗進行比較,P<0.05為存在明顯統計學差異。若研究中僅報告了患者的個體數據時,則由本文作者匯總計算出各組的平均值后合并其他研究進行Meta分析。
3 結果
3.1 文獻檢索結果
檢索中國期刊全文數據庫、VIP維普數據庫、中國生物醫學文獻數據庫、萬方數據庫和MEDLINE總計獲得597篇相關文獻(圖1)。根據納入標準,閱讀標題和摘要排除非比較性研究和未報告相關臨床結局指標的研究總計521篇。對余下76篇文獻進行全文閱讀,排除個案報告、綜述和無關研究,最終納入23個研究。其中 6個為NRCT[15-20]、7個為RCT[21-27]、10個為SW研究[28-37](表1)。納入的研究報告了至少一項臨床結局指標,多數研究沒有描述隨機分配方法和盲法。大多數的RCT和NRCT的樣本小于100,大多數SW研究的樣本小于50。約30%的研究的療程為3個月,約有50%的研究沒有描述療程長短(表1)。使用JADAD評分標準對研究進行質量評價顯示多數研究為低質量(結果未示出)。
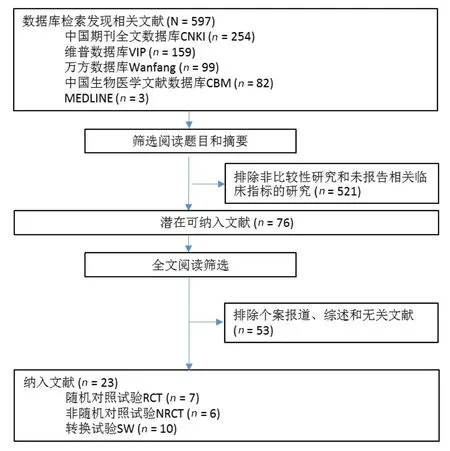
圖1 文獻檢索和篩選流程及結果
3.2 結局指標
3.2.1 總體分析結果
⑴每日胰島素用量:有7 個R C T[21-27],4 個NRCT[15,16,18,20],及10個SW[28-37]報告了達到血糖滿意控制時的胰島素用量。NRCT中有2個研究[17,19]未報告這一指標,因此未被納入Meta分析。對上述各組研究數據Meta分析顯示,使用胰島素治療高血糖癥,當血糖達到滿意控制時,所需人胰島素用量明顯低于動物胰島素(圖2)。
⑵低血糖反應發生率:有3個RCT[22-24],4個NRCT[15,16,19,20],及3個SW[30,31,34]報告了胰島素治療期間患者低血糖反應的人數[22-24]或次數[15,16,19,20,30,31,34]。Meta分析上述各組數據顯示,接受人胰島素治療的患者在治療期間發生低血糖癥的風險明顯低于接受動物胰島素治療的患者(圖3)。RCT 中有4個研究[22,24-26],NRCT中有2個研究[17,18],SW中有7個研究[28,29,32,33,35-37]未報告這一指標, 因此未被納入Meta分析。
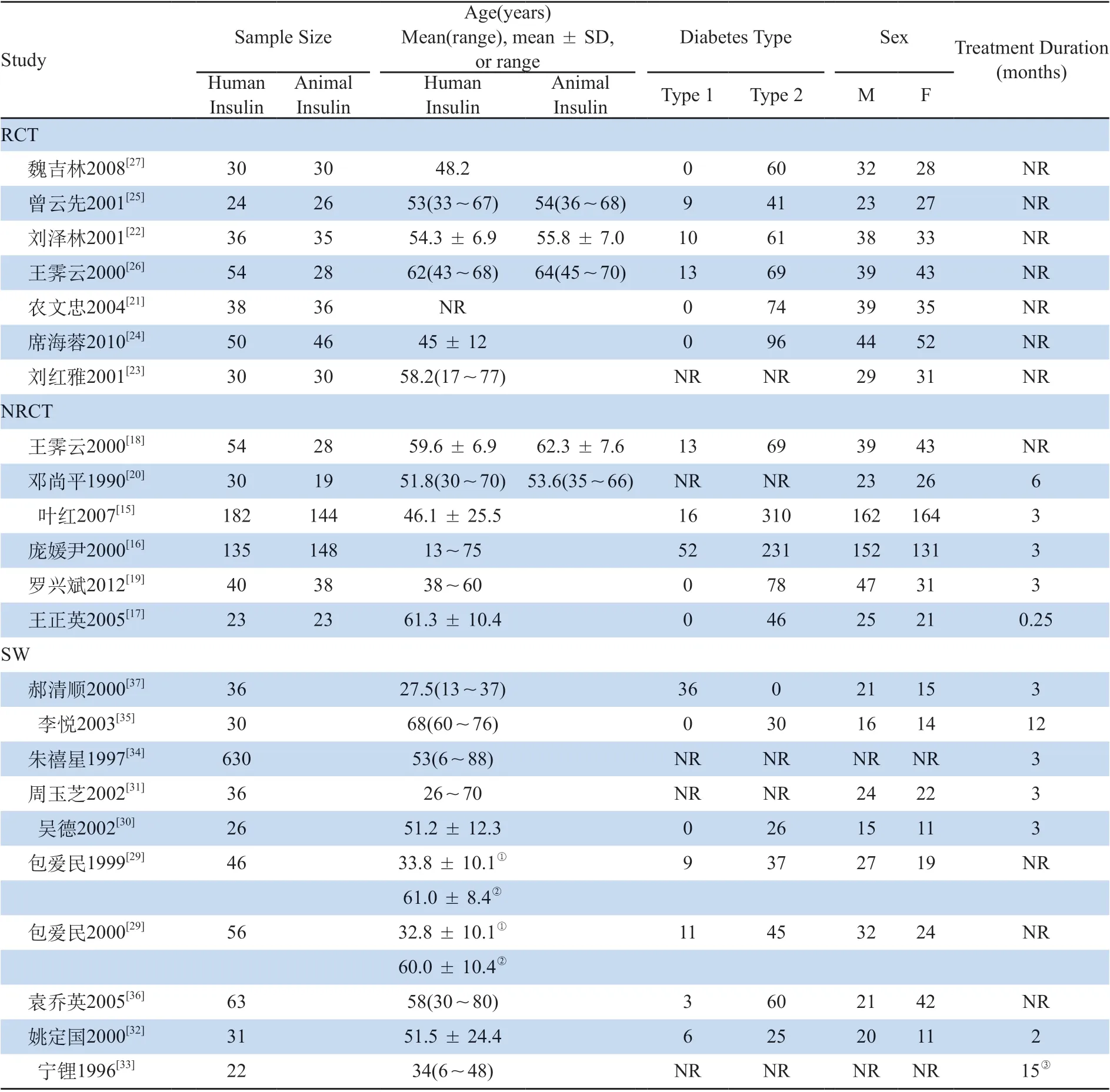
表1 納入研究的特征
⑶HbA1c:有5個SW[30,32,34,35,37]研究報告了胰島素治療達到血糖滿意控制后,患者HbA1c變化情況。M eta分析上述SW研究中患者HbA1c變化情況顯示,患者由動物胰島素治療轉為人胰島素治療后,其HbA1c明顯下降(圖4)。同時,患者的每日胰島素用量也明顯下降(圖1)。其他5個SW研究未報告HbA1c變化[28,29,31,33,36]。RCT和NRCT中報告了HbA1c變化的研究不足3個,未進行Meta分析。

圖2 中國糖尿病患者達到血糖理想控制時每日人胰島素或動物胰島素用量比較的Meta分析
⑷注射部位紅腫硬結:有3個RCT[21,23,27]研究報告了患者接受人胰島素或動物胰島素治療后,注射部位紅腫硬結發生率。Meta分析上述RCT顯示,與接受動物胰島素治療的患者相比,接受人胰島素治療的患者發生注射部位局部反應的風險明顯較低(圖5)。其他RCT研究未報告注射部位局部反應發生情況[22,24-26]。NRCT和SW中報告了注射部位局部反應發生率的研究不足3個,未進行Meta分析。
⑸過敏反應:有3個RCT[21,22,27]研究報告了患者接受人胰島素或動物胰島素治療后過敏反應的發生率。Meta分析上述RCT研究顯示,與接受動物胰島素治療的患者相比,接受人胰島素治療的患者發生過敏反應的風險無明顯差異[RR=0.19, 95%CI(0.03, 1.09)]。其他RCT、NRCT和SW研究未報告過敏反應發生情況。
3.2.2 亞組分析結果
Giugliano等[38]于2011年發表的一篇Meta分析報告了不同劑型的胰島素(基礎胰島素、餐時胰島素和雙相胰島素)在7759名2型糖尿病患者中的有效性和不良反應發生率存在差異。與餐時胰島素和雙相胰島素比較,基礎胰島素治療的患者達到HbA1c<7%的比例較低,發生低血糖癥的風險也較低。我們對納入文獻中明確表明了胰島素劑型(例如短效或中效人或動物胰島素)的研究進行了亞組分析以比較相同劑型的人胰島素和動物胰島素的安全性和有效性。
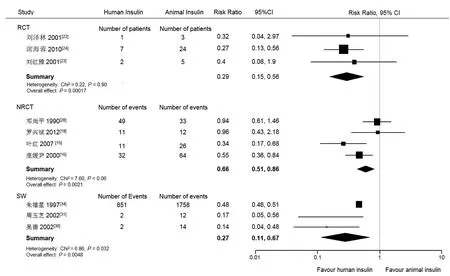
圖3 中國人糖尿病患者使用人胰島素或動物胰島素治療發生低血糖反應的發生率的比較的Meta分析
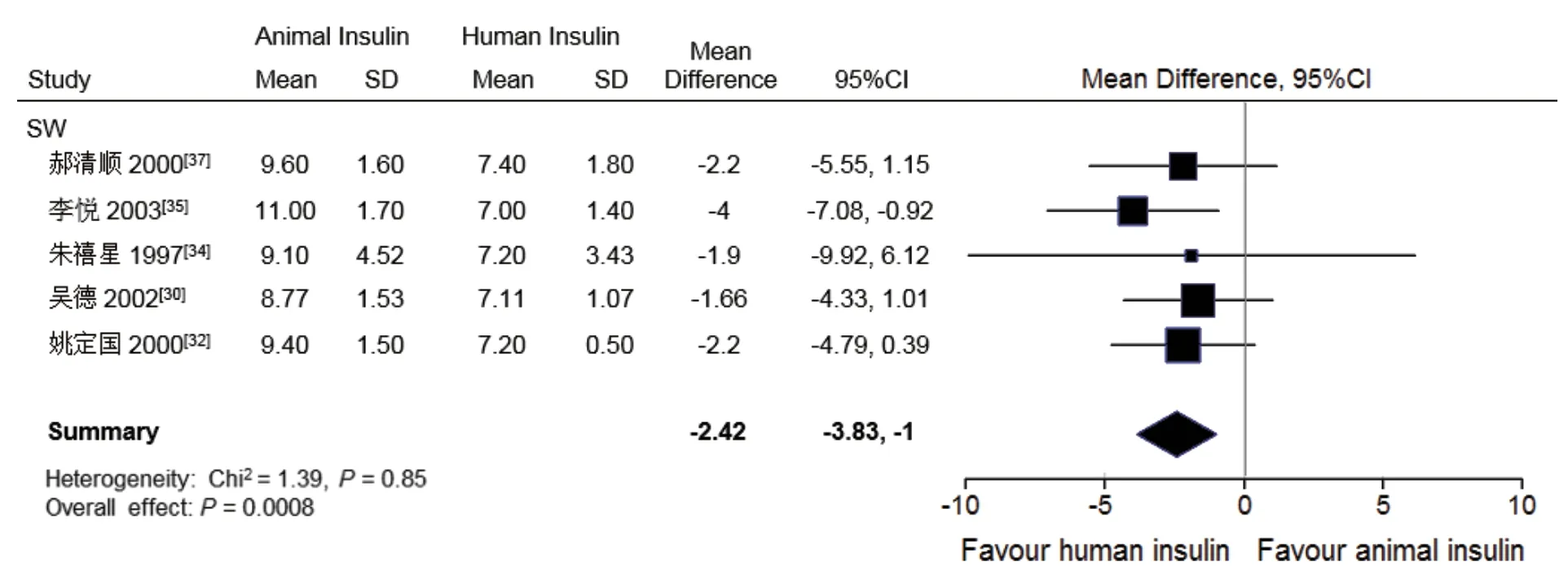
圖4 中國糖尿病患者由動物胰島素轉換為人胰島素治療前后糖化血紅蛋白百分比的比較的Meta分析
⑴空腹血糖濃度(FBG):有4個RCT[21,25-27]研究報告了患者接受短效或中效人胰島素或動物胰島素治療后FBG濃度。Meta分析上述研究數據顯示,患者接受人胰島素與接受動物胰島素治療后FBG濃度無明顯差異[MD=0.06,95%CI(-0.54,0.66)],但是患者的每日胰島素用量明顯下降。
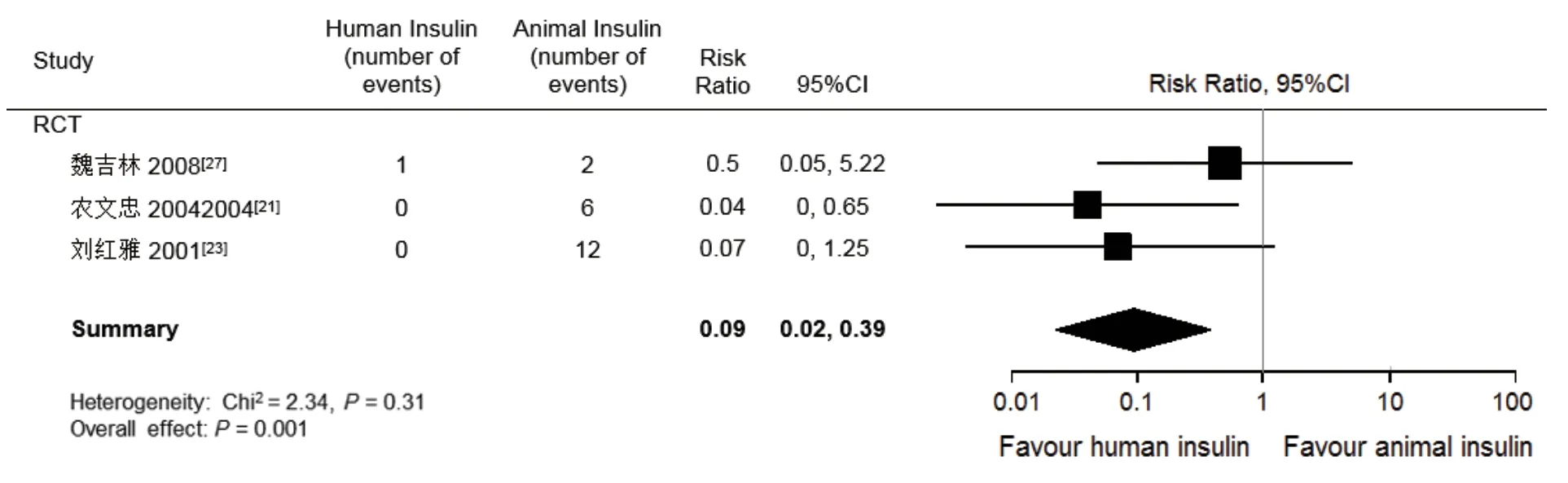
圖5 中國糖尿病患者接受人胰島素或動物胰島素治療局部不良反應發生率比較的Meta分析
⑵餐后2h血糖濃度(2h-PBG):有3個RCT[25-27]研究報告了患者接受短效或中效人胰島素或動物胰島素治療后2h-PBG濃度。M eta分析上述研究顯示,患者接受人胰島素與接受動物胰島素治療后2h-PBG濃度無明顯差異[MD=-0.36, 95%CI(-1.4, 0.69)],但是患者的每日胰島素用量明顯下降。
由于FBG和2h-PBG對于胰島素劑型較敏感,對于此兩項指標的分析僅限于明確表明了胰島素劑型的研究的亞組分析。對其他臨床結局指標(每日胰島素用量、低血糖反應發生率和注射部位紅腫硬結)進行亞組分析顯示其結果與總體分析結果一致(數據未示出)。對于HbA1c這一臨床結局指標,由于缺少足夠的數據,無法進行亞組分析。
4 討論
本文首次采用M eta分析的方法對文獻中有關人胰島素和動物胰島素在中國糖尿病患者中的安全性和有效性進行了比較。我們分析發現在中國糖尿病患者中,人胰島素比動物胰島素在多個臨床結局指征上顯示出較好的安全性和有效性。對于中國糖尿病患者,由動物胰島素治療轉為人胰島素治療具有額外的益處。
本M eta分析表明,人胰島素在中國糖尿病患者中較動物胰島素具有更好的安全性和有效性。我們分析發現中國糖尿病患者在接受胰島素治療達到血糖滿意控制后,接受人胰島素治療的患者所需每日胰島素劑量明顯低于接受動物胰島素治療的患者。這一結果與先前一項在白種人糖尿病患者中進行的研究的Meta分析的結果不同。Richter等[12]的Meta分析結論表明,在療程(平均5.8個月,介于1至24個月之間)結束時每日所需人胰島素的劑量與動物胰島素劑量無明顯差異。Richter等Meta分析報告的每日所需胰島素的劑量與本M eta分析結論不一致可能是由于患者的種族差異所致。另外,可能的原因包括由于中國藥典對胰島素的質量標準的規定與歐美國家有所不同,從而導致測定胰島素品質和胰島素效價所使用的方法上的差異。重組人胰島素于1993年進入中國市場,本文納入的研究對于人胰島素和動物胰島素的比較絕大部分發表于1996~2010年間,在此期間,由于胰島素的多組分前提,中國藥典對動物胰島素一直采用生物效價測定法,存在一定的誤差,其準確性較低;且對胰島素原,熾灼殘渣,微生物限度及細菌內毒素均無檢查要求,而對人胰島素測定項目與歐美藥典類似,采用儀器分析法。同時期,國外歐美藥典對動物胰島素則多采用儀器分析法[40,41]。另外,療程的長短也可能對胰島素的療效和安全性造成影響。本Meta分析所納入的研究中超過50%的研究沒有報告療程的長短。
我們發現在中國糖尿病患者中,人胰島素同動物胰島素相比能更加有效地降低HbA1c,同時患者每日所需人胰島素的劑量比動物胰島素的劑量明顯降低。Richter等[12]的Meta分析報告了人胰島素降低HbA1c的效果較動物胰島素更好,雖然其差別未達到明顯的統計學差異,但與本文的結論基本一致。另外,同動物胰島素治療相比,人胰島素治療對患者的FBG和2h-PBG沒有明顯的差異,但使患者達到相似的FBG和2h-PBG每日所需的人胰島素劑量明顯低于所需的動物胰島素劑量。以上結果提示,人胰島素控制高血糖癥的療效可能較動物胰島素更好。
我們發現在中國糖尿病患者中,同使用動物胰島素治療相比,使用人胰島素治療發生低血糖反應的幾率較低。Airey等[13]在一項系統評價中報告了在白種人糖尿病患者中,使用人胰島素治療與使用動物胰島素治療相比,低血糖癥發生率無明顯差異。同樣,Richter等[42]的Meta分析也報告了白種人糖尿病患者中的類似結論。但是,有多項研究顯示人胰島素治療可伴有無癥狀低血糖反應以及發生嚴重低血糖的風險增加[43-45]。以上研究主要是在白種人糖尿病患者中進行,本研究結論與上述文獻不一致可能是由于遺傳背景差異所致(中國人與白種人),因為有證據顯示遺傳背景的差異對亞裔糖尿病患者和白種人糖尿病患者在接受人胰島素治療時發生嚴重低血糖反應的幾率有影響[46]。
本次M eta分析顯示在中國糖尿病患者中,與動物胰島素治療相比,人胰島素治療發生局部不良反應的幾率較低。有文獻報告顯示,較高的胰島素抗體濃度與較高的局部不良反應發生率相關[12]。與動物胰島素相比,重組人胰島素因其氨基酸序列與內源性胰島素完全一致,其免疫原性較低。有研究發現當由動物胰島素轉換為人胰島素后,胰島素抗體的濃度降低[12]。另外,同豬胰島素相比,牛胰島素治療伴有較高的胰島素抗體濃度[12],這可能是由于同豬胰島素相比,牛胰島素與人胰島素的化學結構差異較大。由于人胰島素具有較低的免疫原性,以此可以解釋人胰島素的局部反應發生率較低。但是本Meta分析中的研究沒有報告胰島素抗體的濃度的變化。
本研究的優點在于納入研究的病例來自于日常臨床實踐,研究結果反映日常臨床工作的實際情況。本研究同時采用了多個臨床結局指標用于比較人胰島素和動物胰島素的安全性和有效性,因此結論具有較好的臨床實際意義。本研究的局限性在于,國內多數研究的樣本較小,多數試驗沒有報告隨機分配方法和盲法。重要的臨床指標,如療程的長短沒有被詳細地描述。另外須指出,各納入研究間對患者達到血糖滿意控制的標準不完全相同,但由于動物胰島素和人胰島素的療效和安全性是按照相同的標準進行比較的,因而不會對研究的結論造成明顯影響。
本文首次對在中國糖尿病患者中對比人胰島素與動物胰島素安全性和有效性的研究進行了M eta分析。本Meta分析結果顯示,人胰島素和動物胰島素能夠有效地控制高血糖癥。而且,達到理想血糖控制后,所需人胰島素的平均每日劑量明顯低于動物胰島素。同時,人胰島素比動物胰島素能更有效地降低HbA1c。人胰島素治療的低血糖反應和局部不良反應都比動物胰島素低。
綜上所述,在中國糖尿病患者中,與使用動物胰島素相比,使用人胰島素可能具有較好控制血糖、每日用量較低和不良反應較少的優點。但是須指出的是,上述結論還需要更多具有良好試驗設計的前瞻性研究來加強對這一結論的支持。
[1] Yang W, Lu J, Weng J, et al. Prevalence of diabetes among men and women in China[J]. N Engl J Med, 2010, 362(12): 1090-1101.
[2] Yang ZJ, Liu J, Ge JP, et al. Prevalence of cardiovascular disease risk factor in the Chinese population: the 2007-2008 China National Diabetes and Metabolic Disorders Study[J]. Eur Heart J, 2012, 33(2): 213-220.
[3] He J, Gu D, Wu X, et al. Major causes of death among men and women in China[J]. N Engl J Med, 2005, 353(11): 1124-1134.
[4] Xu Y, Wang L, He J, et al. Prevalence and control of diabetes in Chinese adults[J]. JAMA, 2013, 310(9): 948-959.
[5] National diabeties research group. Diabetes mellitus survey of 300,000 in fourteen provinces and cities of China[J]. Chinese Journal of Internal Medicine(中華內科學雜志), 1981, 20: 678-681.
[6] Melmed S, Willams R. W illiams textbook of endocrinology(12th Ed.)[M]. Philadelphia: Elsevier/Saunders. 2011: 1371-1435.
[7] UK prospective diabetes study(UKPDS)group. Intensive bloodglucose control w ith su lphony lureas or insu lin com pared w ith conventional treatment and risk of complications in patients w ith type 2 diabetes(UKPDS 33)[J]. Lancet, 1998, 352(9131): 837-853.
[8] Vajo Z, Faw cett J, Duckworth WC. Recombinant DNA technology in the treatment of diabetes: insulin analogs[J]. Endocr Rev, 2001, 22(5): 706-717.
[9] Gregory R, Tattersall RB. Bovine and human NPH insulins as T cell immunogens[J]. Diabetes Res Clin Pract, 1993, 20(2): 139-146.
[10] A ltman JJ, Feldman S, Bonnemaire M, et al. No increase of hypoglycaem ia upon transfer of aged longstanding type 1 diabetic patients to human insulin: a prospective random ized study. The Investigators of the Transfert Study[J]. Diabetes M etab, 1998, 24(5): 419-423.
[11] Schernthaner G. Immunogenicity and allergenic potential of animal and human insulins[J]. Diabetes Care, 1993, 16(Suppl 3): 155-165.
[12] Richter B, Neises G. 'Human' insulin versus animal insulin in people w ith diabetes mellitus[J]. Cochrane Database Syst Rev, 2005(1): CD003816.
[13] Airey CM, Williams DR, Martin PG, et al. Hypoglycaem ia induced by exogenous insulin-'human' and animal insulin compared[J]. Diabet Med, 2000, 17(6): 416-432.
[14] 胰島素市場研究報告(2010版)[EB]. http://w enku.baidu.com/view/d53ddde9aeaad1f346933ff0.htm l.
[15] Ye H, Li HQ. Human and porcine insulin in the treatment of diabetes, a clinical analysis[J]. Modern M ed J China(中國現代醫藥雜志), 2007 9(10): 114.
[16] Pang YY. Comparison of human insulin and animal insulin in the treatment of diabetes[J]. J GuangXi M ed Uni( 廣西醫科大學學報), 2000, 17(4): 676-677.
[17] Wang ZY. Efficacy of Novolin 30R in diabetes, an observation in 30 cases[J]. J Guiyang Med College(貴陽醫學院學報), 2005, 30(4): 358-359.
[18] Wang JY, Zhang LH, Jin JM, et al. Clinical analysis of human insulin and animal insulin in the treatment of diabetes[J]. Liaoning J Pract Diabetol(遼寧實用糖尿病雜志), 2000, 8(1): 47.
[19] Luo XB, RAN QM. App lication of protam ine zinc insulin 30R in primary hospital[J]. Chin J Mod Drug App(中國現代藥物應用), 2012, 6(6): 82-83.
[20] Deng SP, Duo ZZ, Wu W, et al. Ef f i cacy of semisynthetic human insulin in diabetes[J]. Chin J Endocrinol Metab(中華內分泌代謝雜志), 1990, 6(2): 75-76.
[21] Nong WZ. Ef f i cacy of recombinant human insulin and animal insulin in diabetes[J]. J GuangXi Med Uni(廣西醫科大學學報), 2004, 21(4): 591-592.
[22] Liu ZL, Zou WH, Lai XY, et al. Clinical analysis of treatment of diabetes w ith human and porcine insulins[J]. Pract Clini Med(實用臨床醫學), 2001, 2(3): 46-47.
[23] Liu HY. Efficacy of recombinant human insulin in the treatment and care of diabetes[J]. J Huanan Uni-Med Edition(南華大學學報?醫學版), 2001, 29(3): 324-325.
[24] Xi HR. Novolin30R in the treatment and care of type 2 diabetes[J]. Chin Med Herald(中國醫藥導報), 2010. 7(9): 58-59.
[25] Zeng XY. Com paring the efficacies of two types of insulin in the treatment of diabetes[J]. Clin Focus(臨床薈萃), 2001, 16(15): epub.
[26] Wang JY, Zhang LH, Jin JM, et al. Efficacy of synthetic insulin and animal insulin, a comparison[J]. New Med(新醫學), 2000, 31(5): 285.
[27] Wei JL. Comparing ef f i cacy of Isophane insulin 30R and Novolin 30R in diabetes[J]. Heilongjiang Med J(黑龍江醫藥), 2008, 21(6): 78.
[28] Bao AM, Yang MG, Liu SQ. Clinial observation of prem ixed insulin in the treatment of patients w ith diabetes[J] J Clin Healthcare(臨床中老年保健醫學), 1999, 2(1): 16-17.
[29] Bao AM, Wang YH, Liu SQ, et al. Ef f i cay of premixed human insulin in 56 cases of diabetes[J]. Anhui Med J(安徽醫學), 2000, 21(2): 11-12.
[30] Wu D, Zhang W, Wu SL, et al. efficacy of Novolin 30R and regular animal insulin, a comparison[J]. Liaoning J Pract Diabetol (遼寧實用糖尿病雜志), 2002, 9(2): 62.
[31] Zhou YZ. Sw itching from porcine insulin to human insulin treatment, a clinical observation[J]. Liaoning J Pract Diabetol (遼寧實用糖尿病雜志), 2002, 9(2): 46.
[32] Yao DG, Pan RJ. Recombinant human insulin in insulin antibody positive patients, a clinical observation(重組人胰島素治療胰島素抗體陽性的糖尿病患者臨床觀察)[J]. Zhejiang Med J(浙江醫學), 2000, 22(3): 83.
[33] Ning L. Recombinant human insulin treatment in 48 cases of diabetes[J]. J Jiangxi Med College(江西醫學院學報), 1996, 36(4): 64.
[34] Zhu XX. Clinical observation of human insulin(Novolin), ef f i cay and safety[J]. Shangdong Med J(山東醫藥), 1997, 37(12): 13.
[35] LI Y. Ef f i cacy of human insulin in elderly diabetic patients, an observation of 30 cases[J]. Chengdu Med J(成都醫藥), 2003. 29(4): 204.
[36] Yuan QY. Recombinant human insulin, efficay in 63 patients w ith diabetes - an observational study[J]. Central Plains Med J(中原醫刊), 2005, 32(5): 41.
[37] Hao QS, Yang CM, Zhou J. Human insulin in the treatment of type 1 diabetes, a report from 38 cases[J]. Shangdong Med J(山東醫藥), 2000, 40(6): 63.
[38] Giuglianon D, Maiorino M I, Bellastella G, et al. Efficacy of insulin analogs in achieving the hemoglobin A 1c target of<7% in type 2 diabetes: meta-analysis of random ized controlled trials[J]. Diabetes Care, 2011, 34(2): 510-517.
[39] Jadad AR, Moore RA, Carroll D, et al. Assessing the quality of reports of randomized clinical trials: is blinding necessary?[J]. Control Clin Trials, 1996, 17(1): 1-12.
[40] Wang YM. Quality standards and preparations of insulin in China[J]. Chinese Pharm A ffairs(中國藥事), 2012,. 26(9): 5.
[41] Wang WX, Liu W, Zhou Y, et al. Insulins in pharmacopoeia of China, US and UK, a comparison[J]. Jiangsu Pharm and Clini Res(江蘇藥學與臨床研究), 2005, 13(5): 2.
[42] Richter B, Neises G . 'Human' insulin versus animal insulin in people w ith diabetes mellitus[J]. Cochrane Database Syst Rev, 2002,(3): CD003816.
[43] M aran A, Lomas J, A rchibald H, et al. Double blind clinical and laboratory study of hypoglycaemia w ith human and porcine insulin in diabetic patients reporting hypoglycaemia unawareness after transferring to human insulin[J]. Bri Med J, 1993, 306(6871): 167-171.
[44] Cryer PE. Hypoglycem ia unawareness in IDDM[J]. Diabetes Care, 1993, 16 Suppl 3: 40-47.
[45] Egger M, Sm ith GD, Teuscher A. Human insulin and unawareness of hypoglycaem ia: need for a large random ised trial[J]. Bri Med J, 1992. 305(6849): 351-3555.
[46] Davidson JA, Lacaya LB, Jiang H, et al. Impact of race/ethnicity on the ef f i cacy and safety of commonly used insulin regimens: a post hoc analysis of clinical trials in type 2 diabetes mellitus[J]. Endocr Pract, 2010, 16(5): 818-828.

