蜈蚣草莖葉收獲物“水熱液化”脫除重金屬及生物油轉化
鄧自祥,楊建廣,李焌源,張緒亮
?
蜈蚣草莖葉收獲物“水熱液化”脫除重金屬及生物油轉化
鄧自祥,楊建廣,李焌源,張緒亮
(中南大學 冶金與環(huán)境學院,湖南 長沙,410083)
以重金屬超富集植物之一的蜈蚣草莖葉收獲物為對象,以實現(xiàn)其中重金屬高效分離及生物油轉化為目標,開展蜈蚣草莖葉收獲物“水熱液化”后處理工藝研究,考察粒度、溫度、液固比、壓力、反應時間和催化劑等工藝參數(shù)對蜈蚣草莖葉中重金屬分離和生物油轉化的影響。研究結果表明:在粒度為75 μm、液固比為40:1、壓力為23 MPa、溫度為380 ℃、反應時間為30 min、催化劑為0.1 mol/L K2CO3條件下可將蜈蚣草莖葉中99%以上的主要重金屬分離到水溶液中,83.76%的生物質(zhì)轉化成粗生物油。生物油經(jīng)GC-MS等測定表明其主要由11.81%苯類、42.85%酮類、14.7%醇類、15.28%烯類及11.8%酯類組成,相對分子質(zhì)量分布為94~282,碳數(shù)分布為6~18,熱值為32.72 MJ/kg。
蜈蚣草;生物質(zhì);水熱液化;重金屬;超富集植物
1977年,Brooks等[1]提出了超富集植物(hyperaccumulator)的概念,之后,McGrath等[2?3]提出利用超富集植物清除土壤重金屬污染的思想,并將這種思想引入到環(huán)境領域,形成了重金屬污染土壤的植物修復(phytoremediation)技術[4]。如今,經(jīng)過近30年的發(fā)展,植物修復技術以其治理效果的永久性、治理過程的原位性、治理成本的低廉性和環(huán)境美學的兼容性等特點,已逐漸成為土壤污染治理的主要途徑之一,并開始進入產(chǎn)業(yè)化實施階段[5]。但實現(xiàn)植物修復產(chǎn)物的減量化、無害化處置及能源化、資源化利用,卻是植物修復技術在產(chǎn)業(yè)規(guī)模化過程中,必須面對和迫切需要解決的重要問題之一。這一方面是由于積累了大量重金屬等有害成分的植物往往會通過腐爛、落葉等途徑使有害成分重返土壤,因此,必須在植物落葉前收割植株,并及時進行無害化處理。另一方面,為降低植物修復技術的成本甚至從中創(chuàng)造經(jīng)濟效益,達到植物采礦(phytomining)[6]的目的,也需要實現(xiàn)對這些植物修復產(chǎn)物進行資源化、能源化利用。Nicks等[7]認為:能否以一種環(huán)保、經(jīng)濟的方法分離回收植物修復產(chǎn)物中所含的有價金屬及生物質(zhì)能(bioenergy)是植物修復及植物采礦技術能否順利發(fā)展下去的關鍵因素之一。迄今為止,現(xiàn)有的植物修復產(chǎn)物后處理方法主要有焚燒法[8]、堆肥法[9?10]、壓縮填埋法[11]、高溫分解法[12]、灰化法[13]、液相萃取法[14]等。但實踐已證明:這些處理方法存在二次污染環(huán)境、重金屬元素分離率低、工藝流程長、設備投資大、資源化及能源化利用率不高的缺點。考慮到目前植物修復產(chǎn)物生物量巨大,而采用現(xiàn)有的處理方法對人類造成的潛在危險并未消除、且鑒于環(huán)境保護的日益嚴格及廢物資源化利用趨勢日益加強等方面的原因,研究新的植物修復產(chǎn)物減量化、無害化處置及資源化、能源化后處理技術具有非常重要的實際意義。采用“水熱液化”(hydrothermal upgrading process, HTU)技術處理各種植物修復產(chǎn)物,該技術的原理就是利用水在亞臨界或超臨界狀態(tài)下(374 ℃,22.1 MPa)的熱能,打斷生物質(zhì)中相對分子質(zhì)量較大的有機物的分子鍵,使之轉變?yōu)橄鄬Ψ肿淤|(zhì)量較小的物質(zhì)。同時,有機分子與重金屬離子間的螯合鍵也被打斷,各種重金屬也被釋放進入水溶液中,這些進入溶液中的重金屬成分可輕易通過萃取、沉淀等方法實現(xiàn)分離。已開展的研究結果表明[15?16]:采用水熱液化技術處理重金屬超富集植物收獲物,可高效分離出其中富集的重金屬成分并產(chǎn)出粗生物油,消除現(xiàn)有處理方法存在的“二次污染環(huán)境、重金屬元素分離率低、工藝流程長、設備投資大、資源化及能源化利用率不高”等缺點。有望突破限制植物修復技術大規(guī)模應用的技術障礙,實現(xiàn)重金屬富集、超富集植物收獲物的安全化、減量化處置及資源化、能源化利用。蜈蚣草是由陳同斌等[17]發(fā)現(xiàn)的砷超富集植物。蜈蚣草,鳳尾蕨科植物,多年生草本,高1.3~2.0 m;是一種對砷富集能力很強的植物,而且這種植物生長范圍廣泛,生命力頑強,生長速度快,生物量大且修復砷污染土壤時每年可以收割3次。蜈蚣草是有應用前景的修復砷污染土壤的植物材料,蜈蚣草有較強的耐鉛、鋅毒能力,可用于修復被As,Pb和Zn等重金屬復合污染土壤[18]。本文作者以“水熱液化”工藝處理典型重金屬超富集植物即蜈蚣草的莖葉收獲物為例,介紹“水熱液化”處理重金屬超富集植物收獲物的工藝過程及產(chǎn)物表征,由此揭示“水熱”條件下重金屬超富集植物中重金屬解離及生物油轉化特征。
1 試驗
1.1 試驗原料
試驗所用蜈蚣草莖葉來自云南某礦區(qū)砷污染土壤植物修復技術示范區(qū),采集的蜈蚣草莖葉首先清水洗滌去除其中的一些泥土等雜質(zhì),再在真空干燥箱中105 ℃干燥30 min,之后于65 ℃烘干至恒質(zhì)量,烘干后利用植物粉碎機將其粉碎至特定粒度后備用;試驗中用到的其他原料如丙酮、無水乙醇等均從市場直接購得。
1.2 試驗方法
將一定量的蜈蚣草粉末與一定量的蒸餾水混合浸泡6 h后加入到高壓釜中(FD?500系列間歇式高壓反應釜,大連通產(chǎn)公司制造),在一定溫度及壓力下反應至設定時間,反應完成后停止加熱并通入冷凝水,使反應釜快速冷卻。待反應釜冷卻至室溫,得到水熱液化產(chǎn)物,氣體用氣體收集袋收集稱重;打開反應釜,用丙酮清洗管線,洗液與液相產(chǎn)物合并進行固液分離;得到濾液和固體殘渣,固體殘渣用約20 mL丙酮沖洗3次,洗液并入濾液中。濾液用旋轉蒸發(fā)儀分餾出丙酮和水分后得到濃縮粗生物油;粗生物油以環(huán)己烷萃取并分餾,獲得生物油產(chǎn)品,試驗工藝流程如圖1所示。
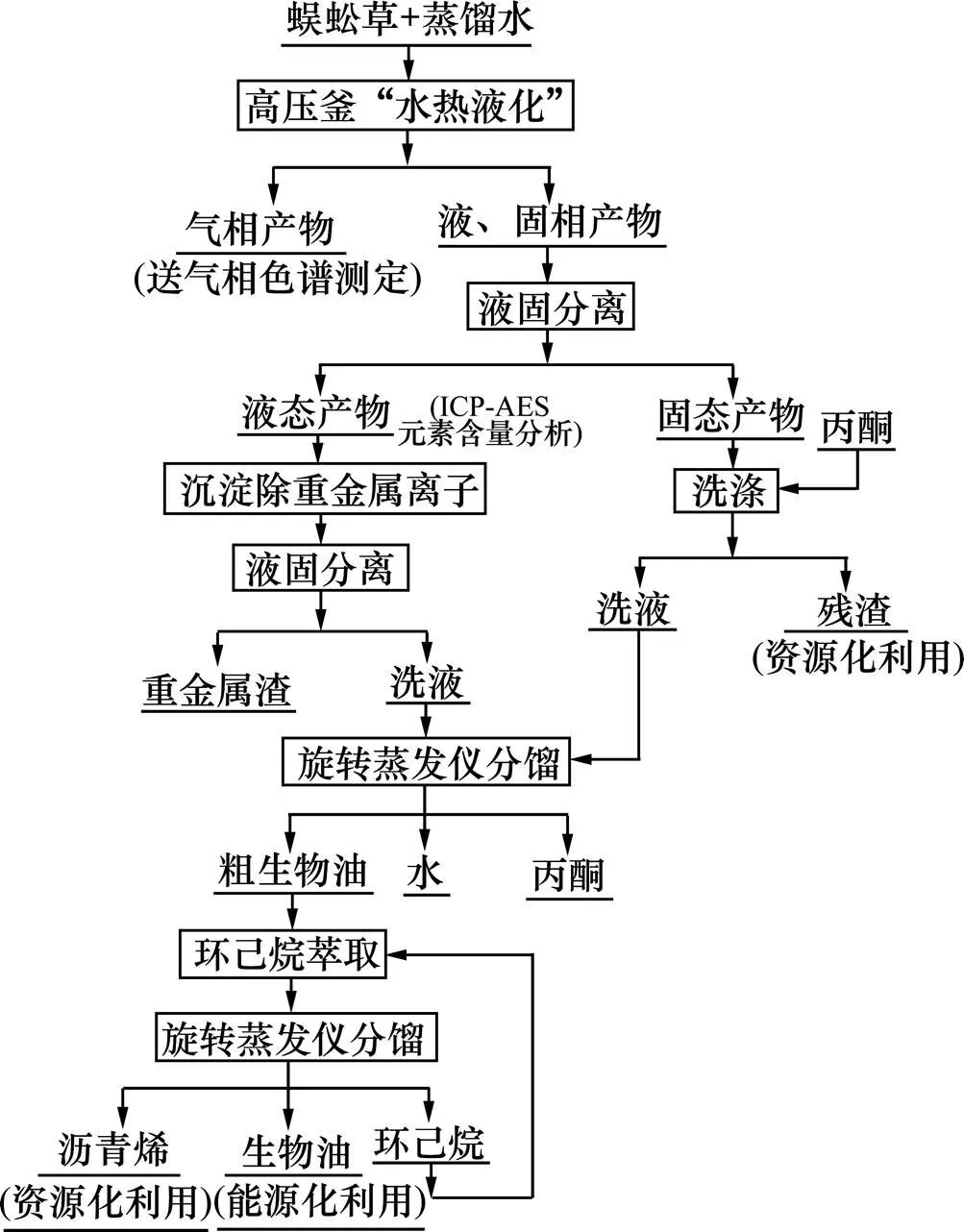
圖1 蜈蚣草莖葉“水熱液化”后處理工藝流程示意圖
試驗結束后,固體殘渣在100℃下干燥3 h,送ICP-AES分析其中重金屬元素含量。
氣體產(chǎn)物收率為氣體質(zhì)量與干基原料質(zhì)量之比;殘渣收率為固體殘渣質(zhì)量與干基原料質(zhì)量之比;粗生物油收率為干基原料質(zhì)量減去氣體質(zhì)量和殘渣質(zhì)量的差值與干基原料質(zhì)量之比;生物油收率為環(huán)己烷相油質(zhì)量與干基原料質(zhì)量之比。
1.3 原料分析及產(chǎn)物表征
蜈蚣草莖葉元素成分和含量采用英國Oxford instruments公司生產(chǎn)的X射線熒光分析儀(X?Met5000) 分析,所得結果如表1所示;C,H,O和N 含量采用氮/氧/氫測定儀(TCH600)和碳硫測定儀(CS?300)進行測定,所得結果如表2所示;“水熱液化”處理前后蜈蚣草粉末表面形貌變化采用日本日立公司生產(chǎn)的S?450掃描電子顯微鏡進行掃描,所得結果如圖2所示;“水熱液化”處理后,溶液中重金屬元素含量分析采用美國Thermo公司的等離子體發(fā)射光譜儀(ICP-AES,IntrepidII XSP Radial)檢測;獲得的生物油由美國Thermo Finigan公司的液相色譜/質(zhì)譜聯(lián)用儀(GC-MS)測定表征等。

表1 蜈蚣草莖葉樣品主要元素XRF分析結果(質(zhì)量分數(shù))

表2 蜈蚣草莖葉樣品氮/氧/氫/碳/硫分析結果(質(zhì)量分數(shù))

圖2 “水熱液化”處理前蜈蚣草粉末SEM圖像
2 結果及表征
2.1 粒度優(yōu)化試驗
取5 g不同粒度的蜈蚣草莖葉粉末與200 mL蒸餾水混合浸泡6 h后加入到高壓釜中,用真空泵將高壓釜內(nèi)空氣抽空。在380 ℃(升溫速率為10 ℃/min)、22.3 MPa條件下反應30 min。反應結束后通水冷卻,按如圖1所示操作流程獲得瀝青烯、粗生物油等產(chǎn)品。圖3所示為試驗獲得的粒度與各產(chǎn)物收率關系。表3所示為不同粒度條件下“水熱液化”處理后蜈蚣草莖葉粉末中重金屬分離率。
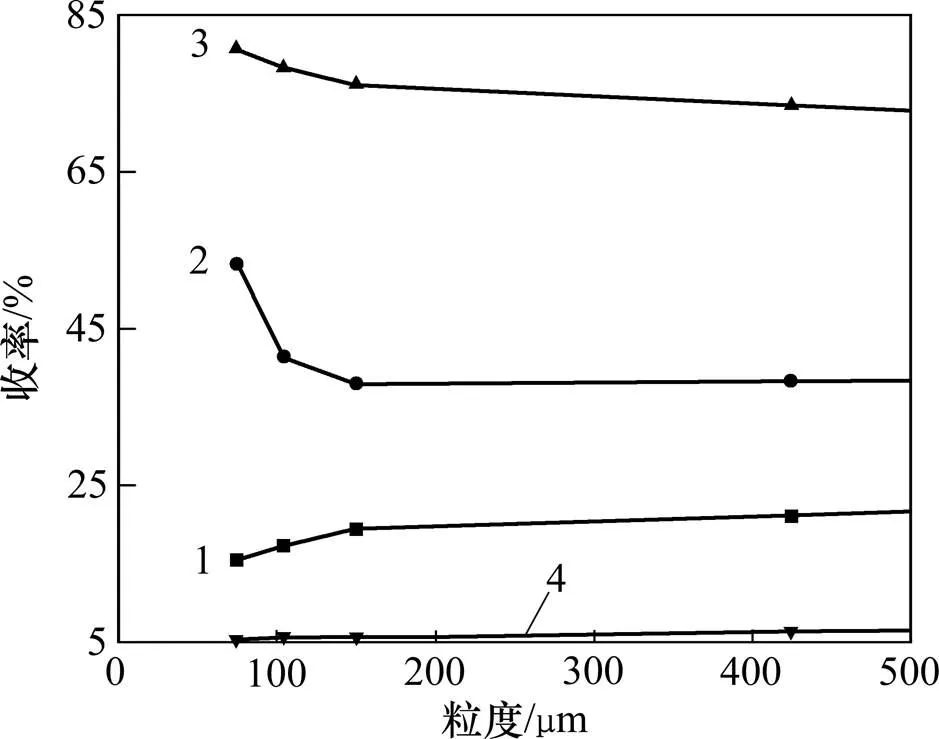
1—殘渣收率;2—生物油收率;3—粗生物油收率;4—氣體收率
圖3 蜈蚣草莖葉“水熱液化”粒度?產(chǎn)物收率關系曲線
Fig. 3 Granularity?yield curves of Pteris vittata harvest using hydrothermal upgrading process
表3 不同粒度下蜈蚣草中主要重金屬元素的分離率
Table 3 Pteris vittata main heavy metals separation rate with different particle sizes %
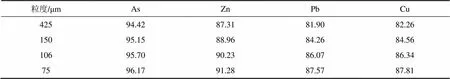
粒度/μmAsZnPbCu 42594.4287.3181.9082.26 15095.1588.9684.2684.56 10695.7090.2386.0786.34 7596.1791.2887.5787.81
由圖3可知:在同一條件下,隨著蜈蚣草莖葉收獲物粒度由425 μm向75 μm 變小,蜈蚣草莖葉經(jīng)“水熱液化”處理后得到的氣體收率由6.78%逐漸降低到5.20%,而反應殘渣則由22.36%逐漸降低到15.36%,粗生物油收率由70.86%升高到79.44%,對應的生物油收率也從38.46%升高到53.22%。尤其是在粒度達到106 μm 后,粗生物油及生物油收率增加幅度更為明顯。因此,從生物油收率的角度來看,蜈蚣草莖葉收獲物粒度越細,越有利于生物油的轉化。另外,從表3可知:隨著粒度變細,蜈蚣草莖葉砷、鉛、鋅、銅等重金屬被解離程度加大,As,Zn,Pb和Cu的分離率逐漸增大。粒度優(yōu)化試驗結果表明,粒度越小,越有利于蜈蚣草莖葉生物油轉化及重金屬的分離。但是考慮到粒度大于75 μm后,對粉碎設備要求越來越高,能耗加大,綜合考慮,選定“水熱液化”處理粒度為75 μm。
2.2 溫度優(yōu)化試驗
在蜈蚣草粉末粒度為75 μm分別在溫度為275,340,355,373和385℃條件下反應30 min。圖4所示為“水熱液化”工藝處理蜈蚣草莖葉試驗獲得的溫度與產(chǎn)物收率關系圖。表4所示為不同溫度條件下的重金屬分離率。
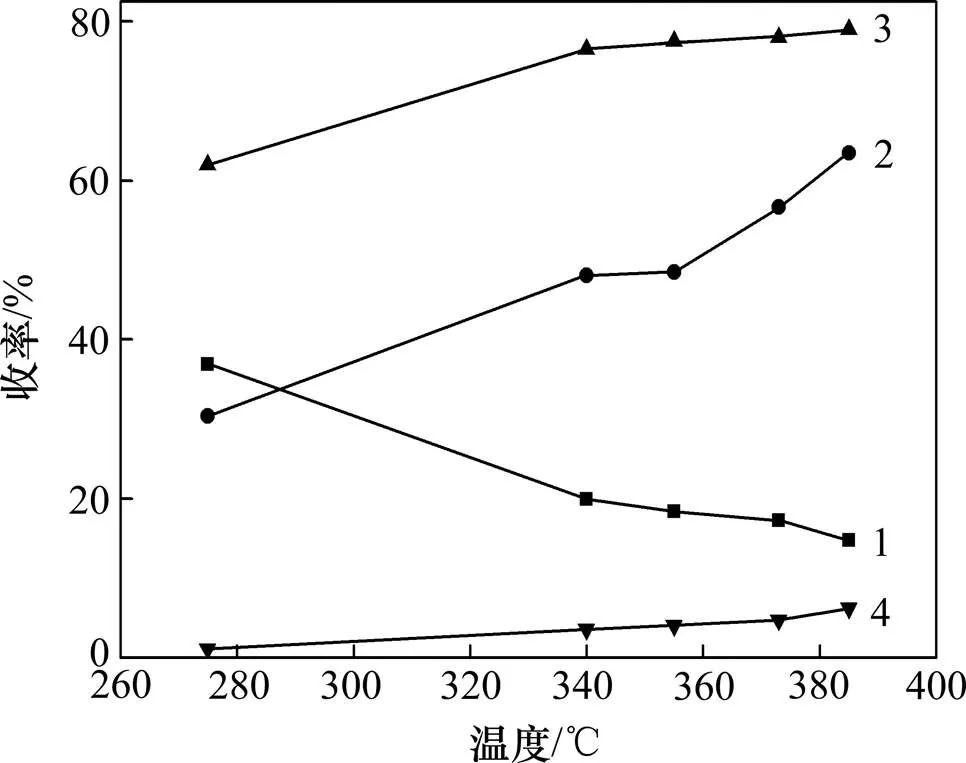
1—殘渣收率;2—生物油收率;3—粗生物油收率;4—氣體收率
圖4 蜈蚣草莖葉“水熱液化”溫度?產(chǎn)物收率關系曲線
Fig. 4 Temperature?yield curves of Pteris vittata harvest using hydrothermal upgrading process

表4 不同溫度下蜈蚣草中主要重金屬元素的分離率
由圖4可知:在同一條件下,隨著反應溫度由275 ℃升高到385 ℃,蜈蚣草莖葉經(jīng)“水熱液化”處理后所得的氣體收率由1.12%逐漸升高到6.26%,而反應殘渣則由32.90%逐漸降低到14.76%,粗生物油收率由61.98%升高到78.98%,對應的生物油收率也從30.41%升高到63.46%。尤其是在處理溫度達到水的臨界點374 ℃后,生物油收率升高幅度更為明顯。因此,從生物油收率的角度來看,“水熱液化”溫度越高,越有利于生物油的轉化。另外,從表4可知:隨著處理溫度的升高,蜈蚣草莖葉中富集的重金屬被解離程度加大,As,Zn,Pb和Cu的分離率升高。但是隨著處理溫度的升高,消耗能量越高,對處理設備的要求越來越高,綜合考慮,選定 “水熱液化”處理溫度為385 ℃。
2.3 液固比優(yōu)化試驗
在蜈蚣草粉末粒度為75 μm、溫度為385 ℃、壓力為24 MPa條件下進行蜈蚣草莖葉“水熱液化”液固比優(yōu)化試驗,液固比(mL:g)分別為60:1,40:1,25:1和15:1,反應時間為30 min。圖5所示為試驗結束后獲得的液固比與各產(chǎn)物收率關系圖。表5所示為不同液固比條件下蜈蚣草莖葉主要重金屬元素的分離率。

1—殘渣收率;2—生物油收率;3—粗生物油收率;4—氣體收率
圖5 蜈蚣草莖葉“水熱液化”液固比?產(chǎn)物收率關系曲線
Fig. 5 Liquid-solid ratio?yield curves of Pteris vittata harvest using hydrothermal upgrading process
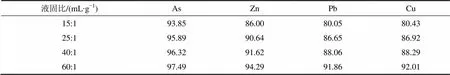
表5 不同液固比下蜈蚣草中主要重金屬元素的分離率
由圖5可知:在同一條件下,隨著反應液固比由15:1升高到60:1,蜈蚣草莖葉經(jīng)“水熱液化”處理后得到的氣體收率先由6.12%逐漸升高到8.53%,從液固比為25:1后又逐漸下降到5.37%。反應殘渣也由24.66%逐漸降低到10.07%,粗生物油收率則由69.22%升高到84.54%,對應的生物油收率則從40.82%升高到63.46%達到極值后又下降到61.11%。因此,從生物油收率的角度來看,“水熱液化”液固比在40:1時所得的生物油收率最大。另外,從表5可知:隨著液固比的升高,蜈蚣草莖葉中富集的重金屬被解離程度加大,As,Zn,Pb和Cu的分離率升高,但是在液固比40:1和60:1差別不是很大。但是隨著處理液固比的升高,“水熱液化”工藝處理蜈蚣草莖葉的效率降低。因此,綜合考慮,選定“水熱液化”處理液固比為40:1。
2.4 壓力優(yōu)化試驗
在蜈蚣草粉末粒度為75 μm、溫度為385 ℃、液固比為40:1、反應時間為30 min條件下進行蜈蚣草莖葉“水熱液化”壓力優(yōu)化試驗。反應壓力主要選擇在亞臨界及超臨界區(qū)間,分別為21,23,24和25 MPa。圖6所示為反應壓力與各產(chǎn)物收率關系。表6所示為不同反應壓力條件下蜈蚣草莖葉主要重金屬元素的分離率。
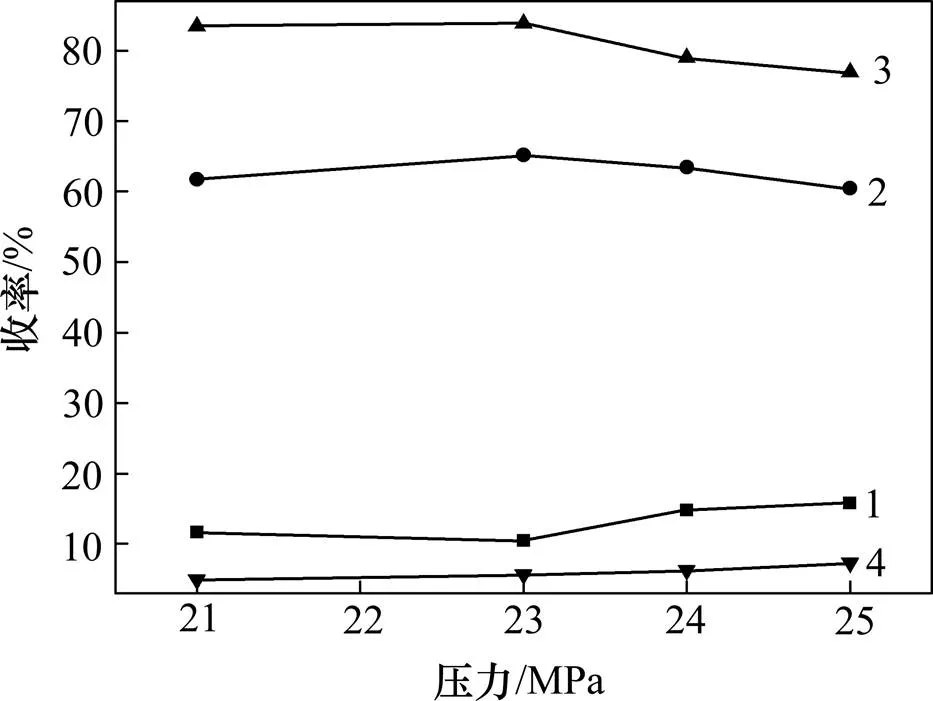
1—殘渣收率;2—生物油收率;3—粗生物油收率;4—氣體收率
圖6 蜈蚣草莖葉“水熱液化”反應壓力?產(chǎn)物收率關系曲線
Fig. 6 Reaction pressure?yield curves of Pteris vittata harvest using hydrothermal upgrading process
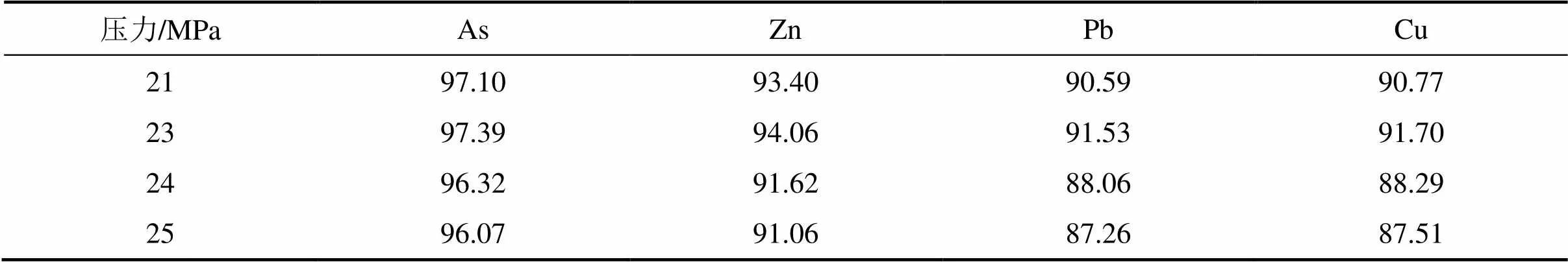
表6 不同壓力下蜈蚣草中主要重金屬元素的分離率
由圖6可知:在同一條件下,隨著反應壓力由21 MPa升高到25 MPa,蜈蚣草莖葉經(jīng)“水熱液化”處理后得到的氣體收率由4.92%逐漸升高到7.33%。反應殘渣由11.63%逐漸降低到10.47%,在23 MPa時殘渣量降到最低。之后,隨著反應壓力的增大又逐漸上升到15.74%。而粗生物油收率則由83.45%微升到83.87%后開始下降到76.93%。對應的生物油收率也從61.72%升高到65.15%達到極值后又下降到60.47%。因此,從生物油收率的角度來看,“水熱液化”反應壓力在23 MPa,生物油收率最高。另外,從表6可知:隨著反應壓力的升高,蜈蚣草莖葉中富集的重金屬被解離程度先升高后下降,As,Zn,Pb和Cu的分離率先升高到反應壓力超過23 MPa后,隨著反應壓力的增大,“水熱液化”殘渣率升高,蜈蚣草莖葉粉末焦炭化程度增大,有害重金屬元素解離到水溶液中的量反而減小。因此,綜合考慮,選定“水熱液化”處理反應壓力為23 MPa。
2.5 反應時間優(yōu)化試驗
在蜈蚣草粉末粒度為75 μm、溫度為385 ℃、液固比為40:1、反應壓力為23 MPa條件下進行反應時間優(yōu)化試驗,反應時間分別為5,15,30和60 min。圖7所示為反應時間與各產(chǎn)物收率關系。表7所示為不同反應時間下“水熱液化”處理后蜈蚣草莖葉中重金屬的分離率。
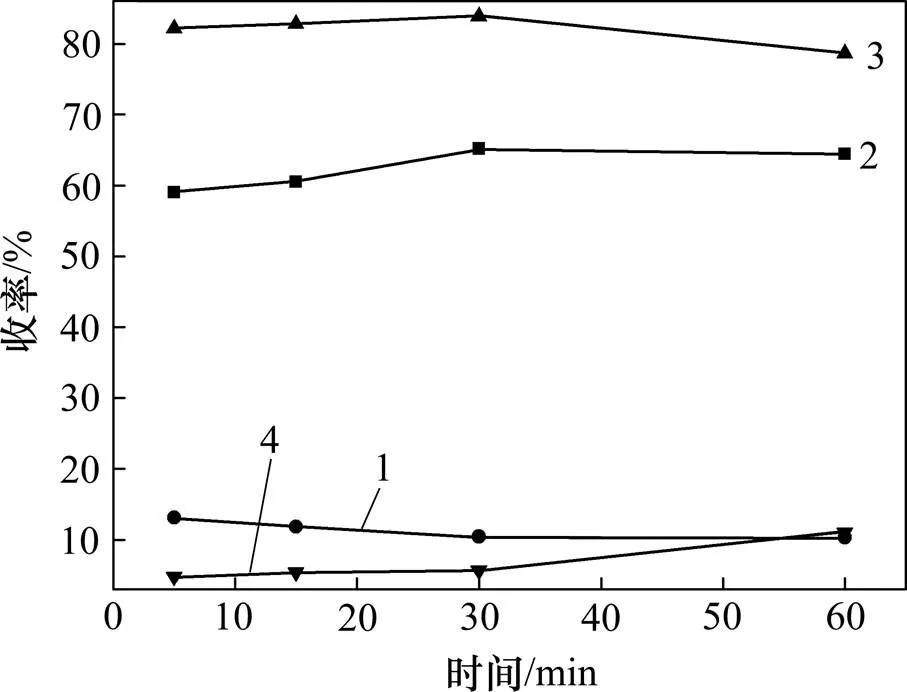
1—殘渣收率;2—生物油收率;3—粗生物油收率;4—氣體收率
圖7 蜈蚣草莖葉“水熱液化”反應時間?產(chǎn)物收率關系曲線
Fig.7 Reaction time?yield curves of Pteris vittata harvest using hydrothermal upgrading process
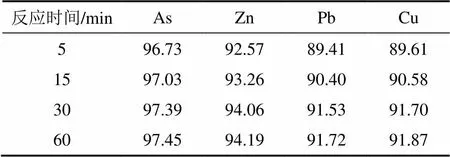
表7 不同反應時間下蜈蚣草中主要重金屬元素的分離率
由圖7可知:在同一條件下,隨著反應時間由5 min增加到60 min,蜈蚣草莖葉經(jīng)“水熱液化”處理后得到的氣體收率由4.77%逐漸增加到11.03%。反應殘渣則由13.09%逐漸降低到10.31%,粗生物油收率則先由82.14%增加到83.87%,在30 min以后,又開始下降到76.93%。對應的生物油收率也從61.72%升高到65.15%之后又下降到64.40%。從生物油收率角度看,隨著反應停留時間延長,生物油收率增大,在30 min時達到最大,繼續(xù)延長,氣體收率增大,生物油收率逐漸減小。同時,從表7可知:隨著反應停留時間延長,蜈蚣草莖葉中富集的重金屬被解離程度加大,As,Zn,Pb和Cu的分離率升高。反應時間30 min后,重金屬分離率變化不大。因此,綜合考慮,選定本“水熱液化”處理反應時間為30 min。
2.6 催化劑優(yōu)化試驗
在蜈蚣草粉末粒度為75 μm、溫度為385 ℃、壓力為23 MPa、反應時間為30 min條件下考察不同催化劑對蜈蚣草莖葉“水熱液化”處理效果的影響。圖8所示為不同催化劑與各產(chǎn)物收率關系圖。表8所示為不同催化劑作用下蜈蚣草莖葉中各重金屬的分離率。
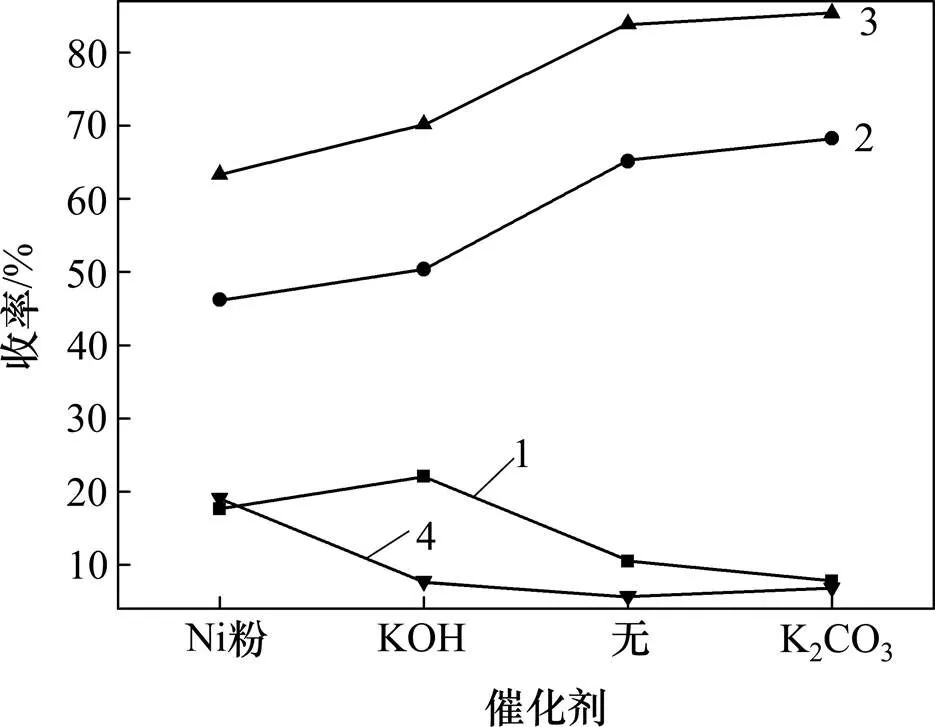
1—殘渣收率;2—生物油收率;3—粗生物油收率;4—氣體收率
圖8 蜈蚣草莖葉“水熱液化”催化劑?產(chǎn)物收率關系曲線
Fig. 8 Catalyst?yield curves of Pteris vittata harvest using hydrothermal upgrading process
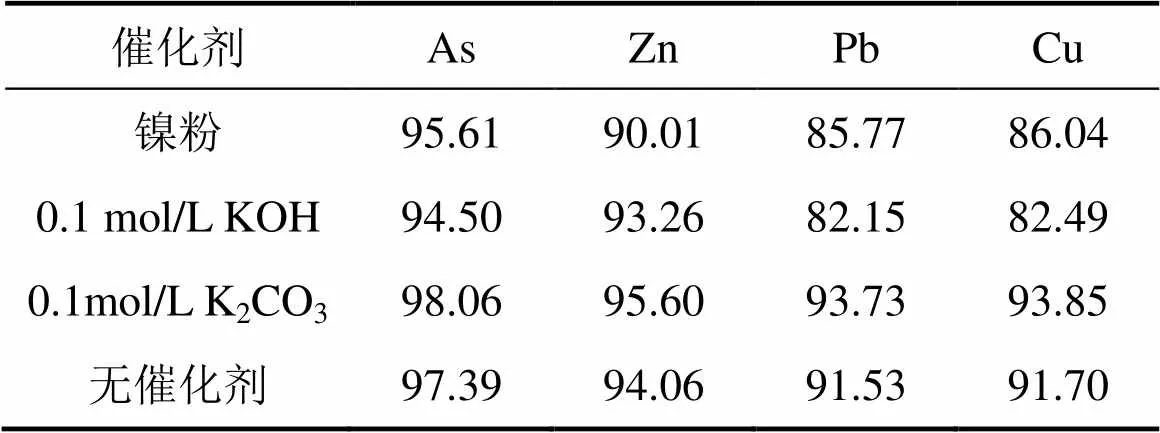
表8 不同催化劑下蜈蚣草中主要重金屬元素的分離率
由圖8可知:不同催化劑催化作用下,蜈蚣草莖葉經(jīng)“水熱液化”處理效果差別很大。相比較而言,K2CO3做催化劑催化下,氣體收率和殘渣得率更低,粗生物油收率和生物油收率都最高,分別達到85.39%和68.28%。相比于不加催化劑,添加(0.1 mol/L) K2CO3為催化劑后對蜈蚣草莖葉“水熱液化”處理效果明顯,不僅提高了生物油得率,同時蜈蚣草莖葉中富集的重金屬被解離程度進一步加大,As,Zn,Pb和Cu的分離率更高。因此,綜合考慮,選定本“水熱液化”處理催化劑為0.1 mol/L K2CO3。
2.7 綜合條件試驗
經(jīng)優(yōu)化試驗,獲得蜈蚣草莖葉“水熱液化”處理的最佳試驗條件為:粒度75 μm、液固比40:1、反應溫度380 ℃、反應壓力23 MPa、反應時間30 min、催化劑為0.1 mol/L K2CO3。在此優(yōu)化條件下,開展“水熱液化”處理蜈蚣草莖葉收獲物綜合條件試驗,試驗規(guī)模為7.5 g/次。按圖1所示的操作流程獲得瀝青烯、粗生物油等產(chǎn)品,表9所示為綜合條件實驗各產(chǎn)物收率。表10所示為綜合實驗“水熱液化”處理后蜈蚣草中主要重金屬元素的分離率。表11所示為綜合試驗所獲得生物油及固體殘渣中氮/氧/氫及碳/硫元素分析結果。表12所示為綜合條件試驗所得殘渣主要元素XRF分析結果。

表9 綜合實驗的各產(chǎn)物收率

表10 綜合實驗溶液中主要重金屬元素的分離率
表11 綜合實驗生物油和固體殘渣氮/氧/氫及碳/硫元素分析結果(質(zhì)量分數(shù))
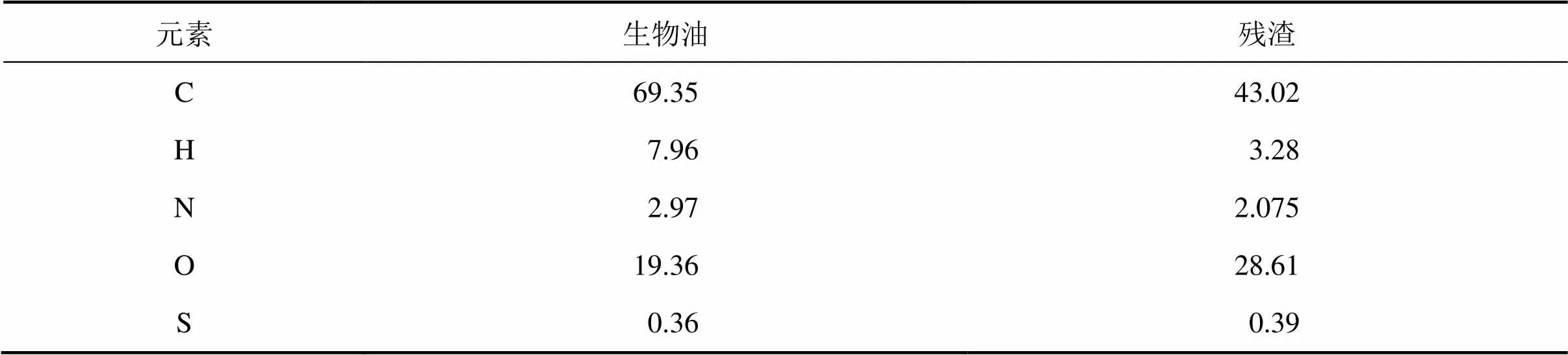
Table 11 N/H/O/C/S analysis result of bio-oil and residue in comprehensive experiment %
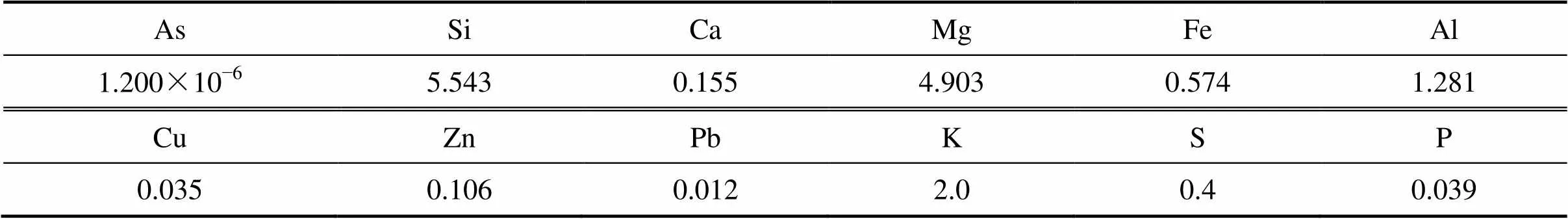
表12 綜合實驗殘渣主要元素XRF分析結果(質(zhì)量分數(shù))
圖9所示為“水熱液化”處理后蜈蚣草莖葉固體殘渣SEM像。由圖9可以看出:蜈蚣草莖葉收獲物經(jīng)“水熱液化”處理后,木質(zhì)素、纖維素及半纖維素等大分子構成的組織結構遭到嚴重的破壞,由處理前的致密塊狀的結構(圖2)變得疏松、類海綿絲狀結構(圖9)。說明超臨界水的非極性特性和所含熱能打斷蜈蚣草莖葉生物質(zhì)中相對分子質(zhì)量較大的有機物及所含的重金屬有機螯合物的分子鍵,使之轉變?yōu)橄鄬Ψ肿淤|(zhì)量較小的物質(zhì),同時使得其中所含的重金屬元素被解離進入水溶液中,也即“水熱液化”過程處理蜈蚣草莖葉收獲物既能實現(xiàn)蜈蚣草生物質(zhì)高效轉化為生物油,又使得其中所含重金屬成分有效脫除。另外,蜈蚣草莖葉收獲物中細胞壁等抗降解、難處理物質(zhì)殘留則形成為少量碳渣。

圖9 “水熱液化”處理后蜈蚣草莖葉固體殘渣SEM像
蜈蚣草莖葉收獲物經(jīng)“水熱液化”處理后獲得的生物油呈黑褐色黏稠狀液體,蒸餾過程中結焦的瀝青烯呈黑色。對綜合試驗獲得的生物油進行GC-MS測定,利用NIST譜庫自動檢索各峰質(zhì)譜,根據(jù)各類化合物的質(zhì)譜裂解規(guī)律對檢索結果進行人工核對。主要有機物成分及含量如表13所示。由表13可知:所得生物油成分較為復雜,含有 11.81%的苯類、42.85%酮類,14.7%醇類、15.28%烯類及11.8%酯類和2.37%的醚類和3.88%的苯酚和其他有機物,相對分子質(zhì)量分布為94~282,碳數(shù)分布為6~18。
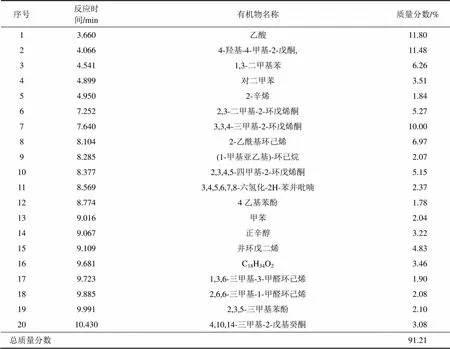
表13 綜合實驗生物油成分及含量
3 結論
1) 典型重金屬超富集植物即蜈蚣草莖葉收獲物經(jīng)“水熱液化”處理后,83.76%的生物質(zhì)轉化為粗生物油,通過萃取?蒸餾后,獲得68.51%的生物油,同時,99.95%的砷,94.92%的鋅,95.43%的鉛及95.48%的銅從蜈蚣草中分離進入水溶液。
2) 重金屬超富集植物蜈蚣草莖葉收獲物經(jīng)“水熱液化”處理獲得的生物油中,C含量明顯升高,O和S含量明顯降低。制得的生物油能量密度較原蜈蚣草粉末提高1.7倍,有利于后續(xù)的能量化利用。但還可以進一步進行改性處理,提高能量密度或制備成高分子產(chǎn)品,以便更好地實現(xiàn)蜈蚣草莖葉收獲物的資源化,能源化利用;另外,試驗獲得的少量固體殘渣重金屬含量低,熱值高,達到中國固體廢棄物排放標準,也可以用于燃料等資源化利用。
3) 重金屬超富集植物蜈蚣草莖葉收獲物經(jīng)“水熱液化”處理獲得的生物油成分較為復雜,主要含有苯類、酮類、醇類、烯類及酯類等有機物。
[1] Brooks R R, Lee J, Reeves R D, et al. Detection of nickeliferous rocks by analysis of herbarium specimens of indicator plants[J]. Journal of Geochemical Exploration, 1977, 7: 49?57.
[2] Brooks R R. Plants that hyperaccumulate heavy metals[M]. Wallingford, Oxen, UK: CAB International, 1998: 261?287.
[3] Robinson B H, Leblanc M, Petit D, et al. The potential of Thlaspi caerulescens for phytoremediation of contaminated soils[J]. Plant and Soil, 1998, 203(1): 47?56.
[4] Salt D E, Blaylock M, Kumar N P B A, et al. Phytoremediation: A novel strategy for the removal of toxic metals from the environment using plants[J]. Nature Biotechnology, 1995, 13(5): 468?474.
[5] Hanikenne M, Talke I N, Haydon M J, et al. Evolution of metal hyperaccumulation required cis-regulatory changes and triplication of HMA4[J]. Nature, 2008, 453(7193): 391?395.
[6] Anderson C W N, Brooks R R, Stewart R B, et al. Harvesting a crop of gold in plants[J]. Nature, 1998, 395(6702): 553?554.
[7] Nicks L J, Chambers M F. Farming for metals[J]. Mining Environmental Management, 1995, 3(3): 15?18.
[8] Reijnders L. Disposal, uses and treatments of combustion ashes: A review[J]. Resources, Conservation and Recycling, 2005, 43(3): 313?336.
[9] Tandy S, Healey J R, Nason M A, et al. Remediation of metal polluted mine soil with compost: Co-composting versus incorporation[J]. Environmental Pollution, 2009, 157(2): 690?697.
[10] 吳龍華, 李寧, 駱永明, 等. 利用修復植物海州香薷制作含銅有機肥料的方法: 中國, CN200610037757.3[P]. 2006?07?12.
WU Longhua, LI Nin, LUO Yongming, et al. Using the phytoremediation Elsholtzia haichowensis make a copper organic fertilizers: China, CN200610037757.3[P]. 2006?07?12.
[11] Ghosh M, Singh S P. A review on phytoremediation of heavy metals and utilization of it's by products[J]. Applied Ecology and Environmental Research, 2005, 3(1): 1?18.
[12] Koppolu L, Agblevor F A, Clements L D. Pyrolysis as a technique for separating heavy metals from hyperaccumulators. Part II: Lab-scale pyrolysis of synthetic hyperaccumulator biomass[J]. Biomass and Bioenergy, 2003, 25(6): 651?663.
[13] Garbisu C, Alkorta I. Phytoextraction: A cost-effective plant-based technology for the removal of metals from the environment[J]. Bioresource Technology, 2001, 77(3): 229?236.
[14] 彭紅云, 楊肖娥, 吳龍華, 等.從植于銅污染土壤的海州香薷中提取香料的方法: 中國, CN200610050052.5[P]. 2006?08?23.
PENG Hongyun, YANG Xiaoe, WU Longhua, et al. A method of extracting spices from the Elsholtzia haichowensis rooted in copper contaminated soil: China, CN200610050052.5[P]. 2006?08?23.
[15] YANG Jianguang. Heavy metals removal and crude bio-oil upgrading from Sedum plumbizincicola harvest using hydrothermal upgrading process[J]. Bioresource Technology, 2010, 101(19): 7653?7657.
[16] YANG Jianguang, TANG Chaobo, HE Jing, et al. Heavy metals removal and crude bio-oil upgrading from Sedum alfredii Hance harvest using hydrothermal upgrading[J]. Journal of Hazardous Materials, 2010, 179(1): 1037?1041.
[17] 陳同斌, 韋朝陽, 黃澤春, 等.[J]. 科學通報, 2002, 47(3): 207?210.
CHEN Tongbin, WEI Chaoyang, HUANG Zechun, et al. Arsenic Hyperaccumulator Pteris vittata L. and its Enrichment characteristics[J]. Chinese Science Bulletin, 2002, 47(3): 207?210.
[18] 安志裝, 陳同斌, 雷梅, 等. 蜈蚣草耐鉛, 銅, 鋅毒性和修復能力的研究[J]. 生態(tài)學報, 2003, 23(12): 2594?2598.
AN Zhizhuang, CHEN Tongbin, LEI Mei, et al. Tolerance of Pteris vittata L. to Pb, Cu and Zn[J]. Acta Ecologica Sinica, 2003, 23(12): 2594?2598.
Removal of heavy metals and upgrading crude bio-oil from Pteris vittata harvest using hydrothermal upgrading process
DENG Zixiang, YANG Jianguang, LI Junyuan, ZHANG Xuliang
(School of Metallurgy and Environment, Central South University, Changsha 410083, China)
Taking stems and leaves harvest of Pteris vittata as the research object, this experiment was carried out to separate heave metals and yield crude bio-oil from this heavy metals hyperaccumulator harvest through hydrothermal upgrading process. Parameters such as granularity, temperature, liquid-solid ratio, pressure, duration and catalysts were examined for their effect on the removal efficiency of heavy metals and upgrading efficiency of crude bio-oil. The maximum heavy metal removal efficiency of >99% and crude bio-oil upgrading efficiency of 83.76% were attained with 75 μm granularity, liquid-solid ratio 40:1 and pressure 23 MPa at 380 ℃ in the presence of 0.1 mol/L K2CO3for 30 min. GC-MS analysis results show that the resulting bio-oil mainly consists of benzene 11.81%, ketone 42.85%, alcohols 14.7%, alkene 15.28% and ester 11.8%, and the relative molecular mass distribution lies in 94?282, carbon number distribution lies in 6?18, and calorific value is 32.72 MJ/kg.
Pteris vittata; biomass; hydrothermal upgrading process; heavy metals; hyperaccumulator
X7
A
1672?7207(2015)01?0358?08
2014?02?09;
2014?04?23
國家自然科學基金資助項目(51174237);國家“十一五”科技支撐計劃項目(2010ZX07212-008);湖南有色?中南大學聯(lián)合基金資助(YSZN2013YJ03);湖南省科技重大專項(2012FJ1010) (Project(51174237) supported by the National Natural Science Foundation of China; Project(2010ZX07212-008) supported by the National Science and Technology Pillar Program during the 11th Five-Year Plan Period; Project(YSZN2013YJ03) supported by Non-ferrous Metals Science Foundation of HNG-CSU; Project(2012FJ1010) supported by Major Science and Technology Projects of Hunan Province)
楊建廣,博士,副教授,從事有色金屬二次資源回收和環(huán)境保護;E-mail: jianguang_yang@163.com
10.11817/j.issn.1672?7207.2015.01.048
(編輯 楊幼平)

