外用藥物制劑藥品生產質量管理規范實施現狀分析與研究
龐鳳華 鄧子杰 鄧小群 陳珊麗
1.廣州白云山制藥股份有限公司白云山何濟公制藥廠,廣東廣州 510410;2.廣州共禾醫藥科技有限公司,廣東廣州 510663
藥品生產質量管理規范(GMP)作為藥品生產全過程中必須遵循的質量監督的法定技術規范,已經在世界上大部分國家中被廣泛應用,能有效地保證藥品生產質量,并為安全有效用藥提供可靠保障[1-2]。
外用藥物制劑生產企業實施新版藥品GMP的時候應當重新審視其重要性,在面臨各種實施的挑戰中,不斷地提高自身的質量管理的水平,建立更高效的藥品生產和管理體系,提高外用藥物制劑的質量水平,從根本上保證藥品質量,有效地促進藥品生產的質量保障;在全球經濟一體化的背景下,更多參與國際范圍的競爭中,使藥品真正達到國際水平,走向現代化、國際化。
1 我國外用藥物制劑GMP的實施現狀分析
自我國GMP推出后,經歷十多年的實施,仍有許多制藥企業在開展實施的進程中受到工藝技術、培訓機制和投入產出等因素的約束[3],執行GMP不到位的現象普遍存在,特別是外用藥無菌制劑[4]制藥企業企依然存在一些迫切需要解決的問題:①當前國內的外用藥物制劑企業素質有高有低,掌握新版GMP認證標準的尺度各異。②當前國內的外用藥物制劑企業存在著注冊制備工藝、注冊標準與車間生產實際不相符,但申請注冊工藝內容變更的相關手續比較繁瑣,需要各級要政部門嚴格審批。③當前國內的外用藥物制劑企業的真正最大風險是藥品注冊研發所帶來的歷史遺留問題,而不是潔凈區級別的提升。④目前外用藥物制劑企業實施新版GMP遇到的最大困難是如何實現工藝設備控制污染以及交叉污染的方式和手段,企業必須配備必要的清洗消毒區域、清洗消毒專用設備,增設公用系統管路,擴充公用系統[5]。⑤本次新版GMP的修訂,針對軟件方面的要求明顯增強,需要不斷加大高水平的專業技術人才的投入。⑥嚴格執行新版GMP的認證標準尺度和執行力度的問題,能直接影響新版GMP執行的效果和影響制藥企業的主觀能動性。
在此建議設置一個公平、公正的新版GMP認證檢查管理體系,通過公平、科學的認證檢查做到真正的優勝劣汰,使優秀的外用藥物制劑企業能夠真正脫穎而出,激發外用藥物制劑企業的主觀能動性,從而進一步提升藥企的市場競爭力。
2 某制藥集團屬下25家藥企實施2010版GMP的現狀調查
某制藥集團是華南地區最大的醫藥生產和流通企業,現有員工2萬多名。擁有現代化的生產廠房,全部獲得GMP認證,可生產片劑、注射劑、膠囊劑、顆粒劑、軟膠囊、乳膏劑、貼膏劑和搽劑等20多種劑型的中西藥產品。作為中國華南地區最大的藥品生產基地,在我國華南地區制藥企業中具有一定的代表性。筆者于2012年10月~2014年1月,對某制藥集團屬下25家制藥企業對2010版GMP的實施情況進行了調查。
在本次調研的某制藥集團屬下25家制藥企業中,無菌制劑企業為10家(40%)(含生物制品生產企業2家),普通制劑企業為24家(96%),中藥飲片企業為8家(32%)。調查的主要方式為現場走訪和交流調研分析。
2.1 本次對25家企業的調研結果
在25家藥品生產企業中,生產企業含無菌制劑,其關鍵工序的潔凈級別為C級的有21家(占84%);企業灌封工序為C+B級以上的企業有12家(占48%)。25家企業中保證了對原輔料全檢工作的有16家(64%);能夠對成品進行全檢的有 20家(80%),2家(8%)由于沒有標準品而不能完成全檢工作。在對中間產品的質量監控方面,絕大多數的企業對中間產品進行了質量監控,但在控制的項目方面,缺少較全面的科學評估。25家藥品生產企業中,按照注冊處方要求未改變藥品生產的工藝及參數的有24家(96%);企業未變更過原輔料、包材供應商穩定性較好的有17家(68%),變更1次的有 6家(24%),變更 2次有1家(4%),變更2次以上的有1家(4%)。25家企業對關鍵制藥設備、清潔消毒程序、檢測方法等進行確認和驗證情況:在一些GMP實施的薄弱環節,該制藥集團下屬企業有18家(72%)的藥企落實開展了偏差管理、變更控制、風險評估;21家(84%)企業開展了在產品種的穩定性考察工作;19家(76%)企業詳細記錄了對標準品、對照品及標準溶液、對照品溶液、菌種傳代的使用和銷毀記錄;13家(52%)企業對生產全過程中的中間產品、待包裝產品的有效期進行了留樣考察;19家(76%)企業認真開展新版GMP的自檢工作,并認真完成相配套的自檢報告和自檢記錄工作,將工藝驗證、設備驗證、清潔驗證、年度質量回顧以及確認的數據運用于制藥生產過程控制中。
2.2 對該制藥集團下屬企業執行新版GMP認證檢查的缺陷分布及分析
對該制藥集團下屬企業執行新版GMP認證檢查的缺陷分布情況見表1。通過對本次現場檢查以及調研數據的綜合分析,企業實際執行情況與新版GMP的要求還存在一定的差距,主要表現在以下幾個方面:①質量管理體系的強效型有待增強;②相關崗位操作人員的培訓效果、持續性和針對性有待增強;③生產設備對清潔驗證沒有落實到位;④生產物料出入庫管理不規范;⑤確認和驗證的系統性與科學性有待完善;⑥文件管理方面的條理明晰性不強;⑦無菌條件下的灌封操作風險的預防控制措施不足。
企業應該根據各自的缺陷項,從以上幾個方面加強新版GMP的執行力度,不能僅限于新版GMP的認證檢查過程中,應該保證新版GMP執行的日常化和GMP管理的常態化,只有保證了日常的GMP實施,才能有效地保證藥品生產的高質量、低風險,有效地促進藥品生產的質量保障[6-7]。
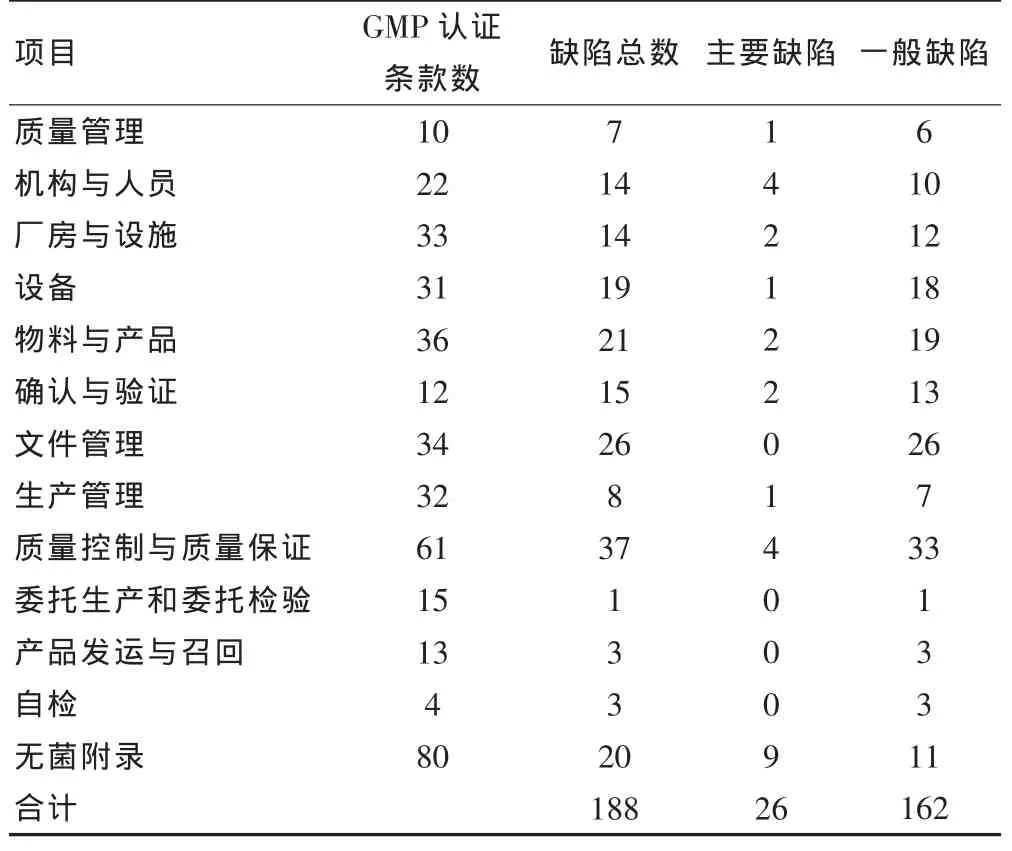
表1 本次2010版GMP認證調查檢查本各類缺陷分布情況(個)
3 我國外用藥物制劑生產企業實施GMP的現狀分析
3.1 外用藥物制劑生產企業概況
外用藥物制劑是我國醫藥市場中不可或缺的一部分,由于外用藥物制劑的本身的特點,使用方便,應用廣泛,通過局部給藥而達到全身治療作用等,其種類也較多,橫跨十幾種劑型。檢索國家食品藥品監督管理總局的官方網站進行外用藥物制劑的生產企業的數據,發現生產軟膏劑的企業有361家、乳膏劑306家、搽劑222家、凝膠劑206家、栓劑173家、貼膏劑中橡膠膏劑94家、洗劑180家,外用藥物制劑是一個廣闊的醫藥市場。據不完全統計,外用藥物制劑的銷售額占醫藥銷售收入份額的10%~15%,在未來的幾年,外用藥物制劑的份額有望進一步提升[8]。
皮膚病藥物市場最大的特點之一就是OTC終端市場占有比例較大,因此如何做好產品的宣傳,提高產品的知名度,創立品牌優勢,將直接影響到產品的銷售市場的擴大。
3.2 GMP在外用藥物制劑生產企業的實施現狀分析
由于外用藥物制劑本身的特點,以皮膚科用藥、外用貼膏、婦科用藥以及外用涂搽方式等藥用劑型,主要通過皮膚進行透皮吸收或者是通過腔道給藥等,其風險相對較小,這也使外用藥物制劑生產企業在實施GMP[9-10]的過程中相對較為松弛,同時也會導致外用藥物制劑藥品GMP實施效果較差,這與外用藥物制劑生產企業的質量意識較薄弱有關,同時,也與藥品監管部門對外用藥物制劑的監督相對偏弱等有關,外用制劑生產企業在實施GMP中遇到的問題,主要體現在以下6個方面:①外用藥物制劑企業的藥品生產質量管理意識不強;②外用藥物制劑的生產企業的職責分工不明確;③文件管理系統不夠完善,執行性不強;④對原輔料、包裝材料的供應商審核不到位;⑤驗證工作不到位,人員對驗證工作的不重視;⑥監管的力度不強,對外用藥物制劑監管忽視。
為使我國可以與先進的藥品生產質量管理體系接軌,更好地參與國際競爭,同時也是提高國內的藥品生產質量的要求,實現我國從醫藥大國到醫藥強國的轉變。雖然外用藥物制劑的藥品GMP認證周期會延續到2015年12月31日,很多生產企業還持觀望的認態度,但這些都是徒勞的。因此,外用藥物制劑生產企業都應該端正自己的態度,認識到自己的一些不足,抓緊有限的認證周期,全面加入新版藥品GMP的認證工作中去,爭取早日拿到GMP證書。
綜上所述,外用藥物制劑生產企業實施新版藥品GMP的時候應當重新審視其重要性,在面臨各種實施的挑戰中,不斷地提高GMP的水平[12-13]。在參與國際范圍的競爭中,外用藥物制劑生產企業可以積極準備藥品GMP的實施認證工作,建立更高效的藥品生產和管理體系,提高外用藥物制劑的質量水平,從根本上可以保證藥品質量,為實現我國從醫藥大國到醫藥強國的改變而不斷進步[14-15]。
[1]孫忠達.GMP管理中“機構與人員”工作的探討[J].上海醫藥,2002,23(1):32.
[2]申麗莎.藥品生產質量管理規范(GMP)在我國的實施與展望[J].重慶中草藥研究,2010,61(1):33-37.
[3]馮盛威,鄧喬華.談談認證后GMP的實施[J].廣東藥學,2005,15(1):68.
[4]劉樹林.無菌藥品生產企業實施2010版GMP的策略研究[D].天津:天津大學,2011:5-10.
[5]陳玉龍,李嬋.對陜西省藥品GMP認證實踐的思考[J].西北藥學雜志,2006,21(1):41.
[6]謝博生.關于推進實施GMP的思考[J].中國藥事,2008,22(10):847.
[7]陳廣龍.藥品生產實施GMP存在的問題及探討[J].中國藥事,2005,19(1):53-55.
[8]屈浩鵬,劉燕魯.對北京市藥品生產企業GMP認證工作的幾點建議[J].首都醫藥,2000,7(5):13.
[9]李榮.GMP與我國藥業現狀及對策[J].中國藥事,2003,17(7):447.
[10]林桂梅.談對實施 GMP的認識[J].海峽藥學,2005,17(5):193-194.
[11] 黃勝炎.國外新外用制劑[J].上海醫藥,2012,33(1):16-17.
[12]張星一.透皮吸收促進劑在經皮給藥系統中的質控和評價方法[J].中國新藥雜志,2010,19(4):273-276.
[13]龐鳳華,溫愷嘉,吳傳斌.藥品生產質量管理規范在外用藥制劑生產管理中的應用[J].今日藥學,2012,9(1):40-45.
[14]張睿智.河南省保健食品的現狀及對策[J].中國醫藥導報,2012,9(36):155-158.
[15]李紅艷,陳愛青.6σ管理在藥品生產質量管理過程中應用的可行性分析[J].醫學與社會,2008,12:31-32.

