淺析高考試題中的差異充氣電池
吳克勇+蔡子華
摘要:結(jié)合高考試題中出現(xiàn)的一些金屬腐蝕形式,介紹了差異充氣電池形成的根本原因,并就因供氧差異而產(chǎn)生的一些重要吸氧腐蝕形式如鹽水滴腐蝕、水線腐蝕的具體形成機(jī)理加以介紹,可為相關(guān)教學(xué)提供有益的參考,并期望能引起廣大教師對自身專業(yè)發(fā)展的認(rèn)識和重視。
關(guān)鍵詞:差異充氣電池;氧濃差電池;鹽水滴腐蝕;水線腐蝕;高考試題
文章編號:1005–6629(2015)9–0078–04 中圖分類號:G633.8 文獻(xiàn)標(biāo)識碼:B
金屬與含氧量不同的溶液相接觸而形成腐蝕電池,又稱差異充氣電池或供氧差異腐蝕電池。它是吸氧腐蝕的一種重要形式,也是普遍存在的、危害性很大的腐蝕形式,是造成金屬局部腐蝕的重要因素之一,是引起鹽水滴腐蝕、水線腐蝕、沉積物腐蝕和縫隙腐蝕的主要原因。在近幾年的各地高考試題中,以這類腐蝕為背景的試題頻繁出現(xiàn)。
1 差異充氣電池形成的根本原因
許多腐蝕發(fā)生的原因在于差異充氣,如鋼鐵材料在實際的應(yīng)用中,因為某種原因造成了金屬表面不同區(qū)域的溶解氧濃度不同,從而形成供氧差異腐蝕電池,在與缺氧溶液相接觸的金屬表面發(fā)生了強(qiáng)烈的腐蝕,而與富氧溶液相接觸的金屬表面相對來講腐蝕微弱,即形成缺氧溶液區(qū)域為腐蝕電池的陽極區(qū),腐蝕速率加快;而富氧溶液區(qū)域為腐蝕電池的陰極區(qū),腐蝕速率減慢。
在一些教材[1]中,把這種由于供氧差異而形成的電池稱為“氧濃差電池”,并用能斯特方程式來解釋這種腐蝕電池的成因,這種解釋是錯誤的。首先,金屬在腐蝕介質(zhì)中處于自腐蝕狀態(tài)下的電位稱為自腐蝕電位,常簡稱為腐蝕電位。通常,腐蝕介質(zhì)中起初并不含有腐蝕金屬的離子,腐蝕體系是不可逆體系,因此腐蝕電位是離開平衡電極電位相當(dāng)遠(yuǎn)的非平衡電極電位,與該金屬的標(biāo)準(zhǔn)平衡電位偏差很大。隨著腐蝕的進(jìn)行,電極表面附近該金屬的離子會逐漸增多,因而腐蝕電位隨時間推移發(fā)生變化。一定時間后,腐蝕電位趨于穩(wěn)定,這時的電位可稱為穩(wěn)定電位,但仍不是可逆平衡電位,其原因是金屬仍在不斷地溶解,而陰極去極化劑(腐蝕劑)仍在不斷地消耗,不存在物質(zhì)的可逆平衡。而只有可逆電極才能滿足能斯特方程式,因此用能斯特方程式來解釋供氧差異腐蝕電池的形成是不正確的。其次,如果兩個電極體系僅是由于溶解氧濃度的不同,而金屬的表面陽極溶解將遵循同一動力學(xué)規(guī)律,是不會導(dǎo)致缺氧區(qū)域強(qiáng)烈的局部腐蝕,而只會使兩個區(qū)域陽極溶解速率相等。
實際上,當(dāng)鋼鐵表面形成供氧差異腐蝕電池時,隨著腐蝕過程的進(jìn)行,因電極反應(yīng)產(chǎn)物和電場作用下的離子遷移的影響引起溶液的成分等因素發(fā)生變化,進(jìn)而引起金屬表面不同區(qū)域的陽極行為也隨之發(fā)生了方向不同的變化,與富氧溶液接觸的表面區(qū)域因為供氧充足和pH升高而使氧化膜加厚,變得致密,陽極過程變得比原來更難進(jìn)行,而與缺氧溶液接觸的表面區(qū)域因供氧不足、pH下降以及氯離子的富集而被減薄直至完全溶解,陽極過程變得比原來更容易進(jìn)行,盡管腐蝕電位不變,但富氧區(qū)域的腐蝕電流密度降低,缺氧區(qū)域的腐蝕電流密度增大。這種不同表面區(qū)域的陽極行為差異,會導(dǎo)致陽極區(qū)和陰極區(qū)之間有電流流過,也必然帶來各區(qū)域溶液的組成和金屬的表面狀態(tài)進(jìn)一步發(fā)生變化,腐蝕過程的進(jìn)行不但不會被消弱,反而會加強(qiáng),最終導(dǎo)致與缺氧區(qū)域溶液接觸的表面部分(陽極區(qū))發(fā)生了嚴(yán)重的局部腐蝕。
常見的局部腐蝕,如水線腐蝕、縫隙腐蝕、沉積物腐蝕、鹽水滴腐蝕等都是由差異充氣電池引起的。
2 各種形式的差異充氣電池
2.1 氧濃差電池
例1 (2011年海南化學(xué)卷第12題)根據(jù)圖1,下列判斷中正確的是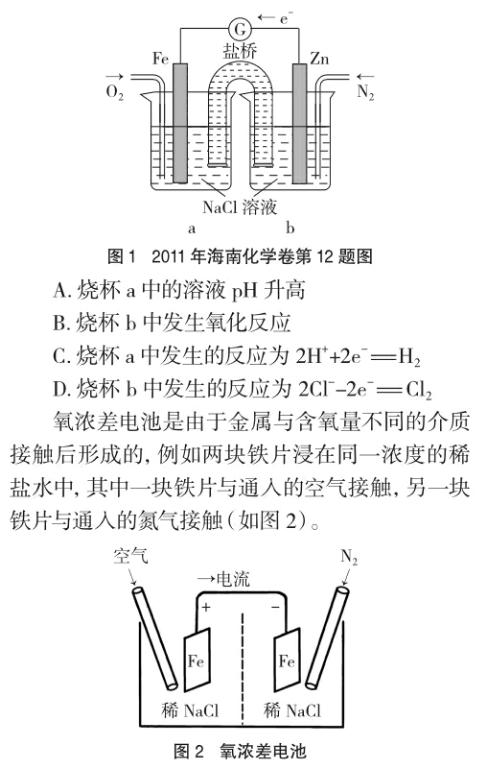
在這兩塊鐵片上負(fù)電荷密度本來應(yīng)該是相同的,但是由于溶液中含氧量不同,在發(fā)生下列反應(yīng)時所進(jìn)行的程度也不同:O2+2H2O+4e-=4OH-。在通入空氣的鐵電極上,氧氣的還原反應(yīng)較迅速,因而表面電子被中和,負(fù)電荷密度降低較多。在通入氮氣因而空氣較少的鐵電極上,氧氣的還原反應(yīng)難以進(jìn)行,因此負(fù)電荷密度幾乎沒有什么變化。這樣,由于溶液中氧氣濃度的不同造成了電位差,產(chǎn)生了腐蝕電流。在上述電池中可觀察到,與氮氣接觸的鐵片發(fā)生了溶解,而與空氣接觸的鐵片沒有腐蝕。
在例1中,可能是命題者出于降低試題難度的考慮,將兩個電極設(shè)置為活潑性不同的兩種金屬,但其實質(zhì)仍然是氧濃差電池,該題的正確答案應(yīng)該為A、B。
2.2 鹽水滴腐蝕
例2 (2011年浙江理綜卷第10題)將NaCl溶液滴在一塊光亮清潔的鐵板表面上,一段時間后發(fā)現(xiàn)液滴覆蓋的圓周中心區(qū)(a)已被腐蝕而變暗,在液滴外沿棕色鐵銹環(huán)(b),如圖3所示。導(dǎo)致該現(xiàn)象的主要原因是液滴之下氧氣含量比邊緣少。下列說法正確的是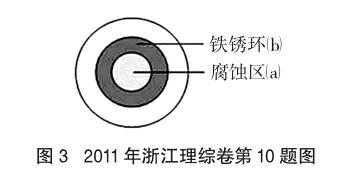
A.液滴中的Cl-由a區(qū)向b區(qū)遷移
B.液滴邊緣是正極區(qū),發(fā)生的電極反應(yīng)為:O2+2H2O+4e-=4OH
C.液滴下的Fe因發(fā)生還原反應(yīng)而被腐蝕,生成的Fe2+由a區(qū)向b區(qū)遷移,與b區(qū)的OH-形成Fe(OH)2,進(jìn)一步氧化、脫水形成鐵銹
D.若改用嵌有一銅螺絲釘?shù)蔫F板,在銅鐵接觸處滴加NaCl溶液,則負(fù)極發(fā)生的電極反應(yīng)為Cu-2e-=Cu2+
該題涉及的是一個早期進(jìn)行的、經(jīng)典的腐蝕實驗,稱為鹽水滴實驗[2],這也是一種局部腐蝕現(xiàn)象。鹽水滴實驗是在一塊拋光、干凈的鋼片上滴上一滴含有少量酚酞和鐵氰化鉀并為空氣所飽和的食鹽水。在液滴覆蓋的區(qū)域內(nèi)很快就出現(xiàn)粉紅色和藍(lán)色的小斑點(圖4-a)。再過幾分鐘,則液滴中心部分主要呈現(xiàn)藍(lán)色,液滴邊緣為一紅色圓環(huán),而在兩者之間有一棕褐色環(huán)(圖4-b)。
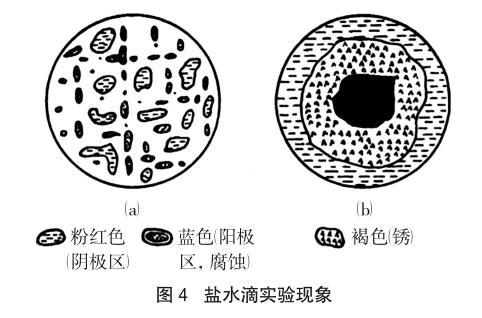
由于鋼鐵表面的劃痕或成分的不均勻,鹽水滴接觸鋼板表面后,出現(xiàn)的藍(lán)色斑點是微電池的負(fù)極區(qū),鐵溶解產(chǎn)生的Fe2+與鐵氰化鉀反應(yīng),生成滕氏藍(lán)沉淀Fe3[Fe(CN)6]2,故該區(qū)域呈現(xiàn)藍(lán)色。藍(lán)色以外的區(qū)域是正極區(qū),發(fā)生反應(yīng)O2+2H2O+4e-=4OH-,生成的OH-使酚酞變紅,所以該區(qū)域呈現(xiàn)粉紅色。圖4-a中的這種微電池分布情況稱為初生分布,這種分布情況不會持續(xù)很久。當(dāng)液滴中的氧氣逐漸被消耗,需要從空氣中補(bǔ)充氧氣時,作為腐蝕介質(zhì)的鹽水滴出現(xiàn)了含氧氣不均勻的情況:液滴中心部位,由于液層較厚,氧氣從空氣中通過擴(kuò)散到達(dá)中心部位的鋼板表面路程較長,故供氧較慢,成為貧氧區(qū)域,原有的正極反應(yīng)逐漸終止,在這里主要進(jìn)行鐵溶解的電極過程,故呈現(xiàn)藍(lán)色;而液滴邊緣部分液膜較薄,氧氣容易到達(dá),成為富氧區(qū)域,主要進(jìn)行氧分子的還原反應(yīng),形成大量的OH-離子,這里原有的負(fù)極區(qū)被新生成的較致密的Fe(OH)2所覆蓋,氧化反應(yīng)停止,藍(lán)色斑點消失,所以邊緣上呈現(xiàn)粉紅色。負(fù)極區(qū)產(chǎn)物Fe2+和正極區(qū)產(chǎn)物OH-,由于擴(kuò)散和電遷移,在中間區(qū)域相遇,首先生成Fe(OH)2,之后被大氣中的氧氣進(jìn)一步氧化生成棕褐色的鐵銹。故中心的藍(lán)色區(qū)域和邊緣的粉紅色區(qū)域之間,存在著一個棕褐色圓環(huán)。根據(jù)上述分析,隨著腐蝕過程的進(jìn)行腐蝕電池中將產(chǎn)生凈電流。在液滴內(nèi)電流從中心向邊緣呈輻射狀流動,然后進(jìn)入鋼板;在鋼板內(nèi)部,電流則是由邊緣流向中心。如果將形成次生分布后的試件,置于磁場中,則會觀察到液滴像電動機(jī)中的轉(zhuǎn)子似地轉(zhuǎn)動;如果改變磁場方向,則液滴又會反方向旋轉(zhuǎn)。這充分證明了液滴內(nèi)部確實有電流流動,因此這一實驗有力地證明了金屬腐蝕的電化學(xué)機(jī)理。
綜上分析,例2的答案為B。
2.3 水線腐蝕
例3 (2014年福建理綜卷第24題)鐵及其化合物與生產(chǎn)、生活關(guān)系密切。
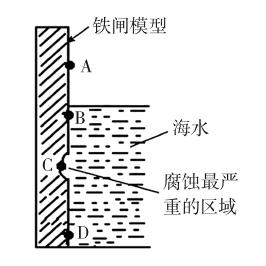
(1)圖5是實驗室研究海水對鐵閘不同部位腐蝕情況的剖面示意圖。
①該電化腐蝕稱為 。
②圖中A、B、C、D四個區(qū)域,生成鐵銹最多的是
(填字母)。
……
人們在生活中獲得這樣的經(jīng)驗,一個未裝滿水的金屬容器常比完全裝滿水的容器容易腐蝕。在腐蝕科學(xué)發(fā)展史上,艾文斯曾經(jīng)進(jìn)行過一個著名的實驗[3],他將金屬Zn試樣垂直插入含KCl的電解質(zhì)溶液中,試樣的一半浸入溶液中,另一半暴露于空氣中,結(jié)果發(fā)現(xiàn),金屬Zn試樣從底部開始腐蝕,逐漸向上蔓延,底部腐蝕很嚴(yán)重。我們在實際生產(chǎn)中也會發(fā)現(xiàn)許多類似的實例,例如,橋樁、船體、儲罐等在靜止的中性水溶液中受到嚴(yán)重腐蝕的部位常在靠近水線下面,受腐蝕部位形成明顯的溝或槽。這種腐蝕稱為水線腐蝕,如圖6所示,這是生產(chǎn)上最普遍的一種局部腐蝕。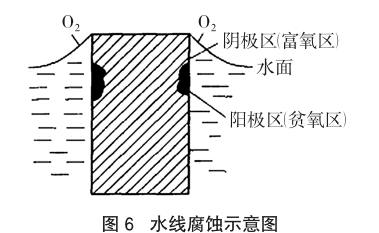
之所以會發(fā)生水線腐蝕,是由于液面下不同距離處水中的氧氣含量不同,水的表層含有較高濃度的氧氣,表層的氧氣如果被消耗,將可及時從大氣中得到補(bǔ)充,但氧氣的擴(kuò)散速度緩慢,水的下層氧氣濃度則較低,水下層的氧氣被消耗后由于氧氣不易到達(dá)而補(bǔ)充困難,因而產(chǎn)生了氧氣的濃度差。表層為富氧區(qū),水下為貧氧區(qū),富氧區(qū)的金屬表面主要進(jìn)行O2的還原反應(yīng):O2+2H2O+4e-= 4OH-,貧氧區(qū)的金屬表面主要發(fā)生金屬的氧化溶解。遠(yuǎn)離水線以下的區(qū)域雖然氧氣濃度低,但由于距離遠(yuǎn),水溶液的電阻大,腐蝕電流小,因而腐蝕并不嚴(yán)重,通常嚴(yán)重腐蝕的部位離開水線是不遠(yuǎn)的,故稱水線腐蝕。
鋼鐵的生銹和腐蝕是不同的兩個概念,鐵氧化轉(zhuǎn)化為亞鐵離子,變質(zhì)損壞,是腐蝕;鐵生成水合氧化鐵是生銹。鋼鐵閘門在海水中發(fā)生吸氧腐蝕的過程中,所生成的亞鐵離子擴(kuò)散到接近水面區(qū)域,和OH-相遇形成Fe(OH)2,并繼續(xù)演化形成鐵銹。(當(dāng)然,上部區(qū)域的OH-也會擴(kuò)散到下部,但是,下部氧氣少,形成鐵銹能力弱。)相反,下部的鐵閘氧化腐蝕的程度大于接近水面的區(qū)域。這在日常生活中是可以觀察到的,如釘入木頭很久的銹鐵釘,釘?shù)南虏勘壬喜扛g更嚴(yán)重,變得更細(xì),釘?shù)纳喜勘砻驿P得更厲害。
所以,上述例題中,②的答案為B。
此外,在工程部件中常用鉚、焊,螺釘?shù)确椒ㄟB接,在其連接處形成的縫隙深處因供氧困難導(dǎo)致嚴(yán)重的局部破壞,疏松的沉積物下面發(fā)生的垢下腐蝕,也是差異充氣電池造成的。
隨著科學(xué)的發(fā)展,人們對一些自然現(xiàn)象和問題的認(rèn)識會逐步深入,及時吸收一些新的發(fā)現(xiàn)、新的認(rèn)識,補(bǔ)充到我們的日常教學(xué)之中,這不僅僅是教材編寫者應(yīng)該考慮的問題,同時也是教師教學(xué)應(yīng)關(guān)注的。這種補(bǔ)充不但會豐富我們的教學(xué),也會激起學(xué)生強(qiáng)烈的探究欲望。不要讓高考試題倒逼我們,我們才想起做改變。化學(xué)的發(fā)展已經(jīng)滲透到自然科學(xué)的各個方面,成為人類進(jìn)步的關(guān)鍵,涉獵與化學(xué)密切相關(guān)的一些學(xué)科,將廣泛地拓展化學(xué)教師對化學(xué)本身的認(rèn)識,也將極大地改變我們的日常教學(xué)。
參考文獻(xiàn):
[1]楊文治.電化學(xué)基礎(chǔ)[M].北京:北京大學(xué)出版社,1982:246.
[2]朱日彰等編.金屬腐蝕學(xué)[M].北京:冶金工業(yè)出版社,1989:98.
[3]李松林編著.材料化學(xué)[M].北京:化學(xué)工業(yè)出版社,2008:224.
[4]曹楚南.腐蝕電化學(xué)原理[M].北京:化學(xué)工業(yè)出版社,2008:230.

