溫度對CT80連續油管鋼電化學腐蝕行為的影響
任國琪,申 毅,王 榮,韋 甲
(1. 西安石油大學 材料科學與工程學院,西安 710065; 2. 中國石油天然氣股份有限公司 西北銷售武漢分公司,武漢 430030)
?
溫度對CT80連續油管鋼電化學腐蝕行為的影響
任國琪1,申 毅1,王 榮1,韋 甲2
(1. 西安石油大學 材料科學與工程學院,西安 710065; 2. 中國石油天然氣股份有限公司 西北銷售武漢分公司,武漢 430030)
采用動電位極化和電化學阻抗方法,研究了CT80連續油管鋼在不同溫度(20,40,60,80 ℃)的3.5% NaCl溶液中的腐蝕行為。結果表明,隨著溫度的升高,CT80鋼的開路電位呈現先負移后正移的趨勢,在60 ℃時達到最小;CT80鋼的自腐蝕電流密度呈先升高后降低的趨勢,在60 ℃時具有最大的自腐蝕電流密度,腐蝕速率最大; CT80鋼的極化電阻隨溫度升高呈先減小后增大的趨勢,在60 ℃時極化電阻最小,相應的腐蝕速率最大。
CT80鋼;溫度;動力學參數;開路電位;電化學阻抗譜
連續油管適用于修井、測井、鉆井等多種油田作業,可用作陸上或海上油氣輸送管線,也可用作速率管柱在氣田上作業[1]。在采用連續油管作為速率管柱進行采氣或排水作業時,由于連續油管壁厚比較薄,環境介質引起的腐蝕不可避免,主要為地層水和淡化地層水,且井區井筒溫度為常溫至110 ℃之間,氣流速率大約在0.005 9 m/s,氣流速率對腐蝕影響比較小,因此,井區不同溫度環境所引起的腐蝕可能會成為連續油管作為速率管柱使用的較大問題[2-5]。
為了深入了解CT80連續油管在高溫服役環境下的腐蝕特性,本工作采用動電位極化和電化學阻抗譜研究了溫度對CT80鋼材料在3.5% NaCl溶液中的腐蝕行為的影響,為控制含Cl-溶液中不同溫度下CT80鋼級連續油管的腐蝕提供依據。
1 試驗
1.1 試驗材料
試驗材料取自CT80鋼管,其化學成分(質量分數/%)為:C 0.11,Si 0.45,Mn 0.92,S 0.008,P 0.019,Ni 0.08,Cr 0.62,Nb 0.16,V 0.20,Fe 97.433。從鋼管上切取10.5 mm×10.5 mm×2.5 mm片狀試樣,作為電化學測試試樣。試樣打磨后的工作面的尺寸為10 mm×10 mm,工作面的面積為1 cm2,其余非工作面部分用環氧樹脂密封與腐蝕介質絕緣。
腐蝕試驗的腐蝕溶液為3.5% NaCl中性溶液, 采用分析純和蒸餾水配制而成,其pH在6.8~7.1之間。
1.2 試驗方法
為了研究不同溫度下CT80鋼的腐蝕情況,將打磨好的試樣分別放入20 ℃,40 ℃,60 ℃,80 ℃的3.5% NaCl溶液中進行試驗。
電化學測量在PARSTAT 2273電化學測試系統上進行,電解池為1 L的玻璃電解池。電化學測量采用三電極體系,研究電極為工作試樣,輔助電極為鉑電極,參比電極為飽和甘汞電極(SCE)。試驗前將試樣用砂紙逐級打磨至800號。測試試樣在不同溫度3.5% NaCl溶液中的開路電位測試時間為4 h。電化學阻抗譜測試的頻率范圍為5 mHz ~100 Hz,阻抗測量信號幅值為10 mV正弦波[6]。將電化學阻抗試試驗后的試樣用砂紙逐級打磨至1 000號后,測量其動電位極化曲線。極化曲線掃描范圍為-900~-300 mV,掃描速率為1 mV/s。
浸泡用的試樣采用100~800號砂紙逐級打磨光滑,丙酮清洗,然后稱量并精確測量試樣的尺寸,計算試樣的暴露表面積。
浸泡試驗采用動態浸泡,分別在20 ℃,40 ℃,60 ℃和80 ℃下進行,試驗周期為7 d,試樣旋轉的圓周線速率為1 m/s。浸泡試驗結束后,將試樣取出,用自來水沖洗約5 min,以去掉試樣表面殘留的腐蝕介質,然后清除腐蝕產物(本試驗所采用的腐蝕產物清洗液為10%的鹽酸,并用空白試樣進行校正),再用無水乙醇對試樣進行脫水,吹干,用分析天平稱量,應用失重法計算其腐蝕速率。
2 結果與討論
2.1 開路電位
圖1為不同溫度下CT80鋼試樣在3.5% NaCl溶液中的開路電位Eop隨測試時間的變化關系圖。可以看出,在3.5% NaCl溶液中,不同溫度下CT80鋼試樣的電極電位變化趨勢基本相同,都是隨著時間的延長逐漸下降,最后趨于穩定,2 h后電極電位基本達到穩定,可得到一個穩定的電極電位,作為開路電位。CT80鋼試樣在20 ℃,40 ℃,60 ℃,80 ℃的Eop分別為-633 mV,-698 mV,-711 mV,-688 mV。隨著溫度的增加,CT80鋼的Eop先負移后正移,在60 ℃時達到最負,表明60 ℃時CT80鋼的腐蝕傾向性較其他溫度下顯著增大。
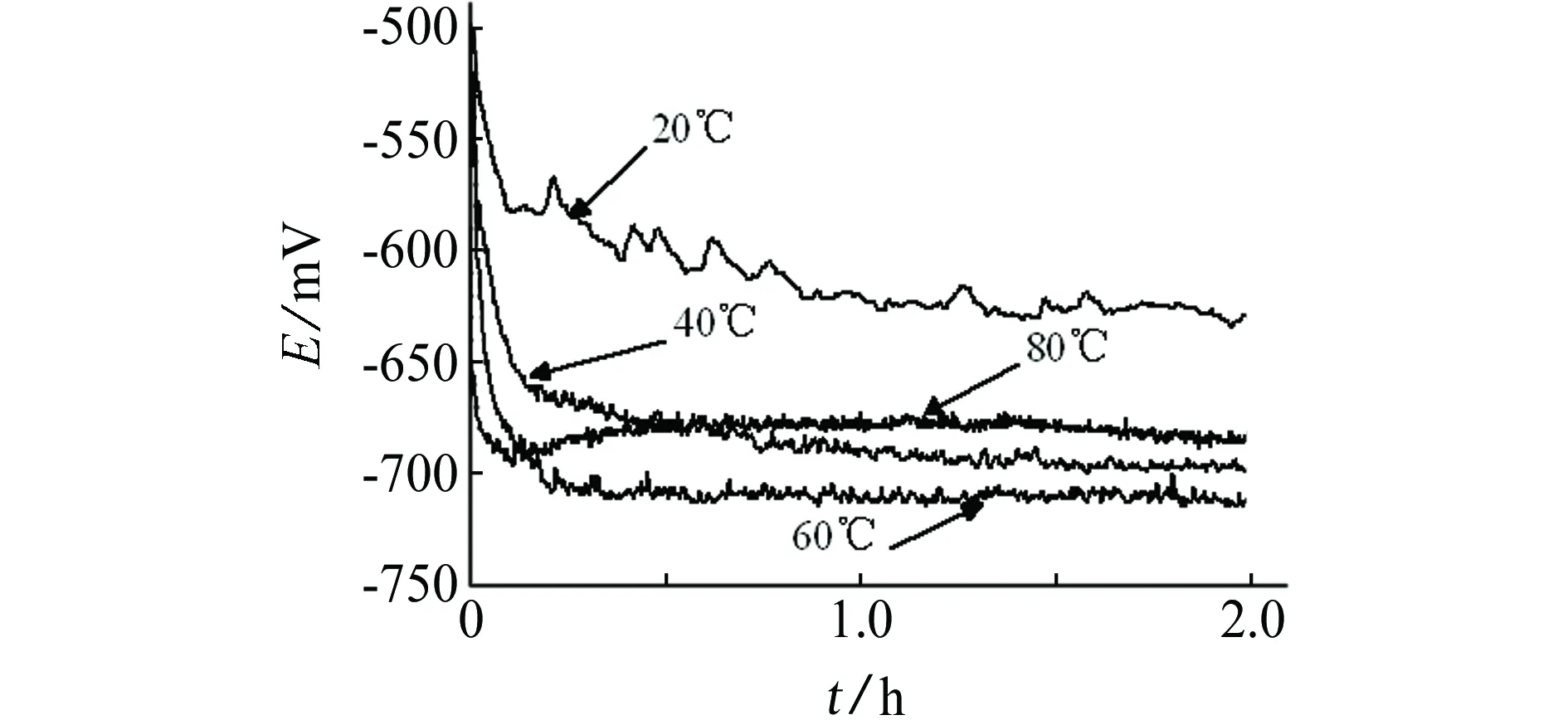
圖1 不同溫度下CT80鋼試樣在3.5% NaCl溶液中開路電位隨時間變化關系Fig. 1 Open circuit potential vs test time of CT80 steel samples in 3.5% NaCl solution at different temperatures
按照雙電層理論,穩定狀態的開路電位應該為穩態試樣表面陽極反應速率等于陰極氧還原速率時的電位。當試樣從大氣中移入到腐蝕溶液后,開路電位先朝負方向移動,然后在一定浸泡時間后基本達到一個穩定值,這是由于試樣在大氣中預腐蝕的氧化膜受溶液中腐蝕性陰離子的作用發生溶解[9],達到穩定開路電位的狀態對應金屬的自腐蝕狀態[10],同時溫度升高使得達到穩定狀態的時間縮短。
2.2 動電位極化曲線
圖2為CT80鋼在3.5% NaCl溶液中不同溫度下的動電位極化曲線。由圖2可見,相對于20 ℃時,40 ℃,60 ℃和80 ℃試樣的陰陽極極化曲線依次右移,在40~60 ℃區間內移動幅度最大,隨著溫度的增加,在80 ℃時試樣的陰極極化曲線小幅度的左移。四種溫度下的CT80鋼在強極化區即Tafel區的陽極極化曲線變化不大,均為活化控制,而陰極極化在60 ℃和80 ℃表現為明顯的擴散控制。在極化曲線上,溫度對腐蝕電位影響的趨勢與圖1中開路電位測量的結果一致,但具體數值具有一定的差別,因為電位的測量不是處于穩定狀態。
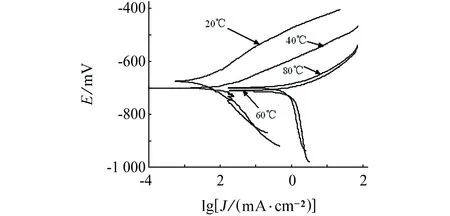
圖2 不同溫度下CT80鋼試樣在3.5% NaCl溶液中的極化曲線Fig. 2 Polarization curves of CT80 steel samples in 3.5% NaCl solution at different temperatures
表1為極化曲線的相關電化學參數擬合。由表1結果可見,CT80鋼在四種溫度下的陽極Tafel
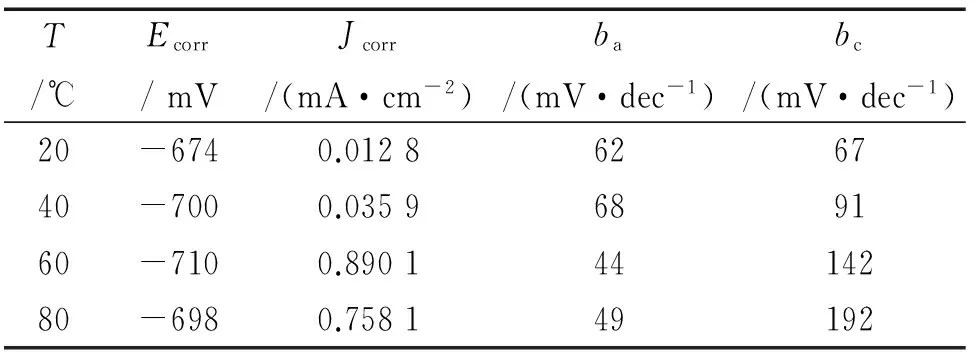
表1 不同溫度下CT80鋼試樣在3.5% NaCl溶液中的極化曲線參數
常數變化不大; 陰極Tafel常數的變化范圍在67~192 mV之間,變化較大。因此,溫度對陽極Tafel常數沒有明顯的影響,但溫度顯著提高陰極Tafel常數的值。對比腐蝕電流密度,可見溫度明顯增加腐蝕電流密度。
2.3 電化學阻抗譜
圖3是CT80鋼分別在不同溫度下3.5% NaCl溶液中的電化學阻抗譜。由圖3可見,四種溫度下的電化學阻抗譜都呈現出兩個時間常數,20 ℃時為高頻容抗弧和Warburg阻抗,40 ℃,60 ℃,80 ℃時為高頻容抗弧和低頻容抗弧。每個阻抗譜呈不完整的、變形的半圓,溫度顯著降低不完整半圓的直徑,說明升高溫度加速腐蝕過程。
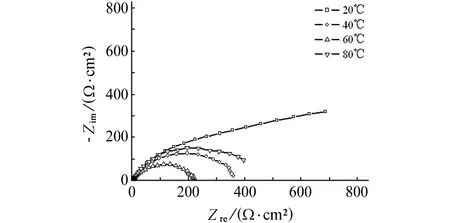
圖3 不同溫度下CT80鋼試樣在3.5% NaCl溶液中的電化學阻抗譜Fig. 3Nyquist figures of CT80 steel samples in 3.5% NaCl solution at different temperatures
如圖4所示為不同溫度下,CT80鋼在3.5% NaCl溶液中的電化學阻抗等效電路圖。圖中,Rs是溶液電阻,Qdl代表雙電層電容的常相位角元件,Rt是電荷傳遞電阻,Rp為極化電阻,W是Warburg阻抗,n為彌散指數。
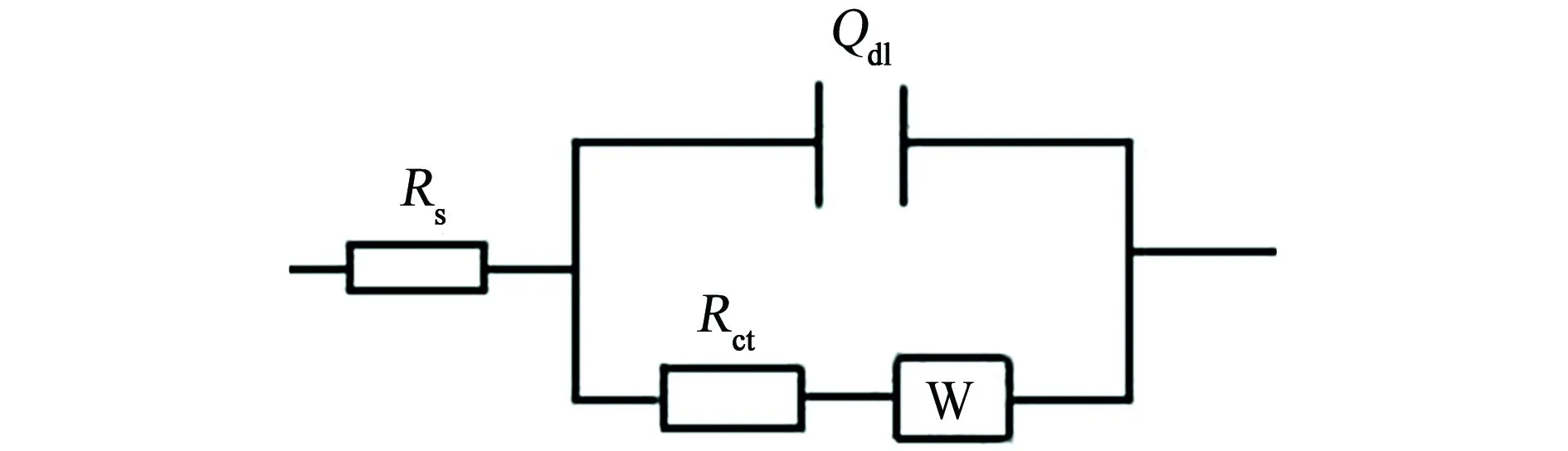
(a) 20 ℃
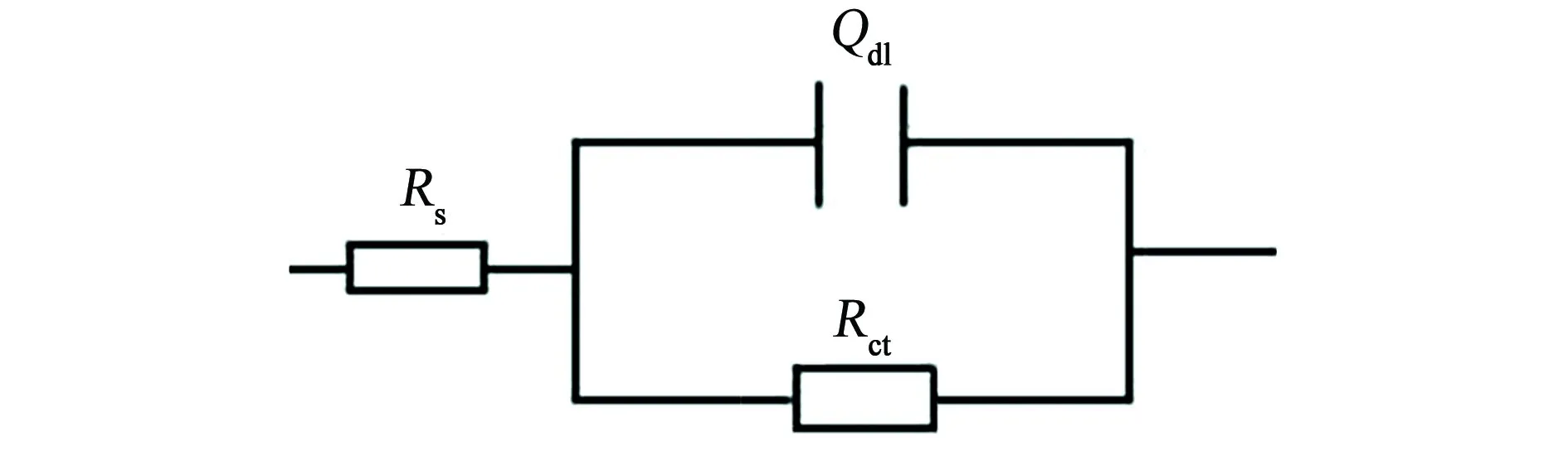
(b) 40 ℃,60 ℃,80 ℃圖4 不同溫度下CT80鋼試樣在3.5% NaCl溶液中的電化學阻抗譜等效電路Fig. 4 EIS equivalent circuit figure of CT80 steels samples in 3.5% NaCl solution at different temperatures
表2為采用軟件ZSIMP-WIN,在最佳擬合條件下得到CT80鋼在不同溫度下的等效電路參數。由表2可見,溫度主要增加了雙電層的電容值,而溫度變化使得電荷傳遞電阻Rct值呈現峰值變化,在60 ℃達到最小值。
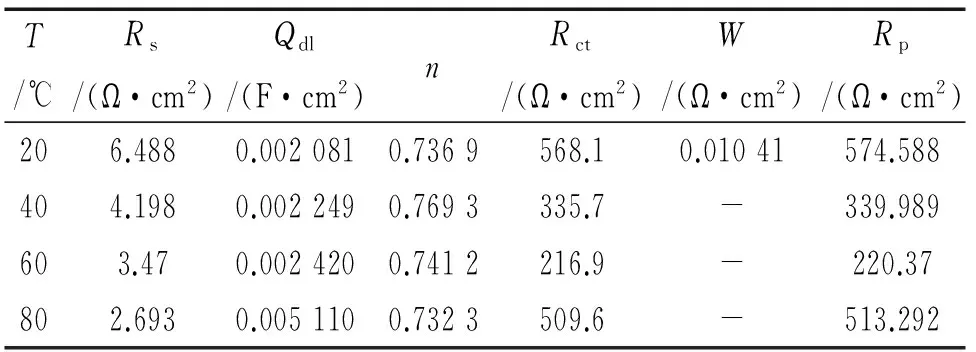
表2 不同溫度下CT80鋼試樣在3.5% NaCl溶液中的電化學阻抗譜擬合參數
從電化學阻抗譜可得到腐蝕過程的極化電阻值,它被廣泛用來研究電化學腐蝕過程的動力學[11-12]。極化電阻值越高,表示材料的腐蝕抗力越高。由表2可見,20 ℃時試樣的Rp最大,依次是80 ℃,40 ℃,60 ℃,在20 ℃時具有最小的腐蝕電流密度,腐蝕速率最小。在60 ℃的低頻容抗弧半徑明顯小于40 ℃和80 ℃,所對應的電荷傳遞電阻Rct和極化電阻Rp也最小,說明在60 ℃時腐蝕電流密度最大,腐蝕速率最大。即通過阻抗譜分析的結果和上述極化曲線擬合所得到的數據具有一致性。
2.4 電化學腐蝕機理
在整個腐蝕過程中,溫度的升高促進了腐蝕反應的陽極過程和陰極過程,加速了介質中反應物的反應速率。另一方面,由于溫度的增加,對腐蝕產物形成動力學起到促進作用。綜合作用,使腐蝕速率在60~80 ℃出現峰值[13]。
由于一般二電子反應在25 ℃時陽極Tafel斜率的理論值為59 mV/dec,由表1中陽極Tafel斜率的數值即實際測量的ba變化不大可知,溫度的升高并沒有改變腐蝕機理,CT80鋼在不同溫度下的陽極反應為:
(1)
由于試驗用3.5% NaCl溶液為中性鹽溶液,其陰極過程為氧的還原去極化,所以CT80鋼在不同溫度下3.5% NaCl溶液中的陰極反應為:
(2)
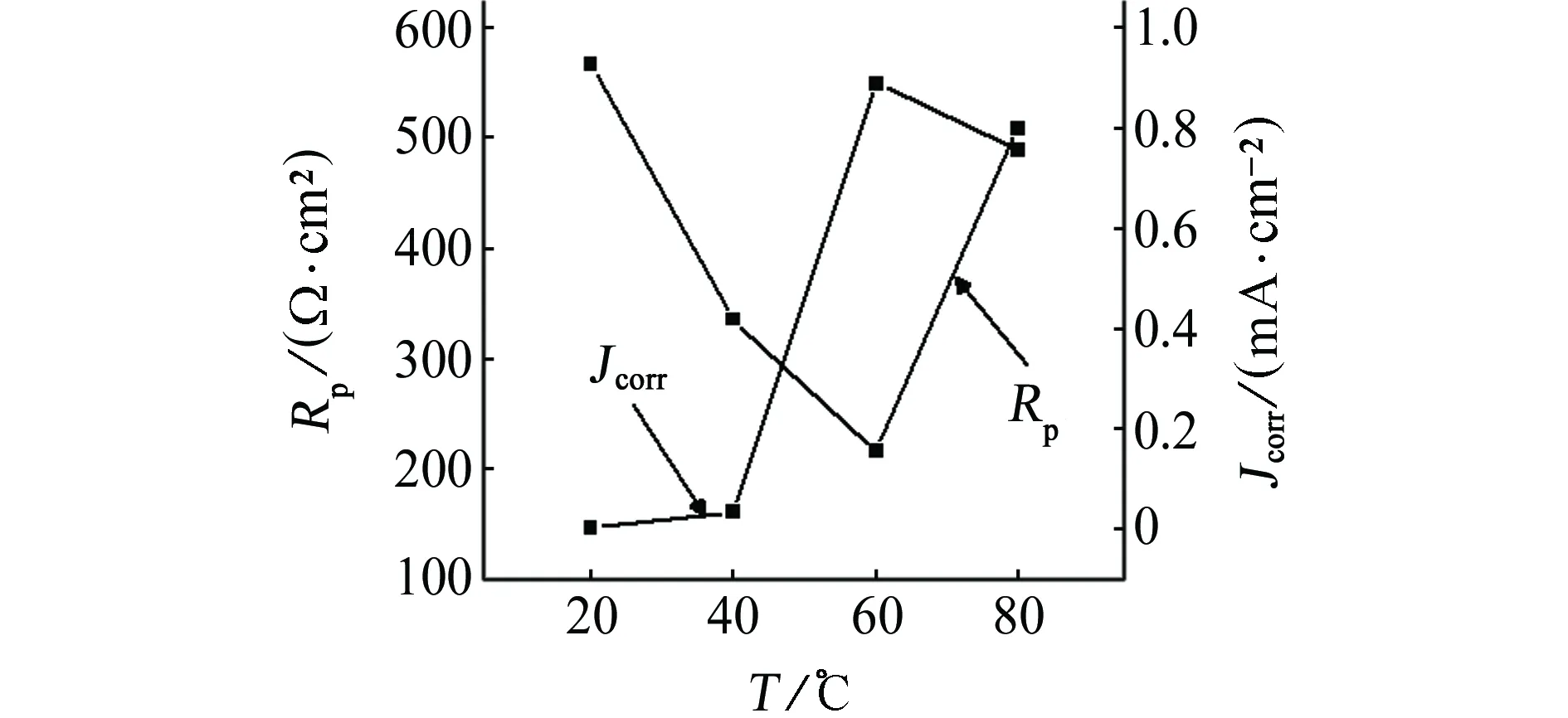
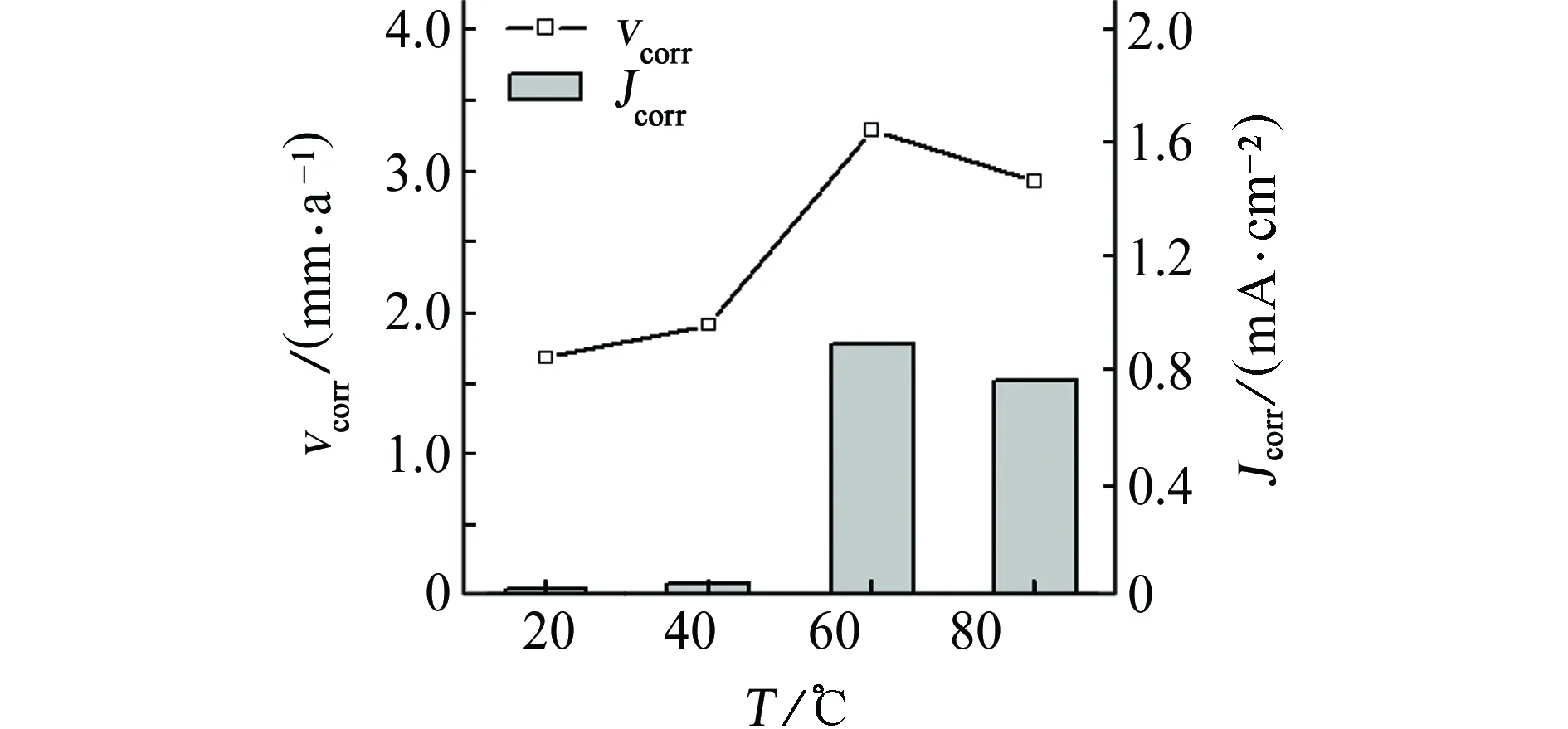
分析表1給出的擬合電化學參數可見,Tafel常數ba 由于Tafel常數可估算陽極和陰極反應的電荷傳遞系數[7]: 陽極反應的電荷傳遞系數: (3) 陰極反應的電荷傳遞系數: (4) 式中:R為氣體常數,F為法拉第常數。陽極電荷傳遞系數表示電化學極化時超電位在電極溶液界面產生的是氧化反應進行的極化能量的分量,陰極電荷傳遞系數表示電化學極化時超電位在電極溶液界面產生的是還原反應進行的極化能量分量,當β=α=0.5時,且β+α=1,陽極極化和陰極極化是對稱的。在這種情況下,腐蝕過程是電子傳遞電荷[14]。 將表1中的的ba、bc分別帶入式(3)、(4),可得到CT80鋼試樣在不同溫度下的電荷傳遞系數α、β值將計算結果列入表3中。由表3可見,各個溫度 表3 CT80鋼試樣在不同溫度下3.5% NaCl溶液中的電荷傳遞系數 下β+α的數值均接近于理論值1,腐蝕過程主要受電子傳遞電荷過程的控制[14]。 圖5為不同溫度下CT80鋼在3.5% NaCl溶液中的自腐蝕電流密度與阻抗譜擬合的極化電阻Rp的關系。由圖5可見,CT80鋼的自腐蝕電流密度在60 ℃時明顯升高,而極化電阻明顯減小,因而在60 ℃時具有較大的腐蝕速率。即通過阻抗譜分析的結果與上述極化曲線擬合所得數據所得到的電化學腐蝕速率的結果具有一致性。 圖5 不同溫度下CT80鋼的自腐蝕電流密度和極化電阻之間的關系Fig. 5 Relationship between corrosion current density and polarization resistance of CT80 steels at different temperatures 2.5 腐蝕速率 表4為試樣在3.5% NaCl溶液中不同溫度下腐蝕7 d的試驗結果。有表4可見,在20~80 ℃試驗溫度范圍,試片的平均腐蝕速率存在極值現象,在大約60 ℃時具有最高的腐蝕速率。 表4 CT80鋼試樣在在3.5% NaCl溶液中不同溫度下腐蝕7 d的平均腐蝕速率 圖6為浸泡試驗的平均腐蝕速率與極化曲線測量的自腐蝕電流密度之間的關系。由圖6可見,由浸泡試驗測得的失重腐蝕速率在不同溫度下的變化趨勢與電化學極化曲線測得的腐蝕電流密度的變化趨勢具有一致性。 圖6 不同溫度下腐蝕速率與腐蝕電流密度之間的關系Fig. 6 Corrosion rate vs. corrosion current density at different temperatures 溫度對CT80鋼腐蝕速率的影響與腐蝕過程的電極反應速率、去極化劑的擴散及溶液中的含氧量有關。溫度升高,使得電極反應的速率加快,同時增加溶液中氧的擴散,從而加速了腐蝕過程,使得腐蝕速率增大;但溫度升高時,氧在水溶液中的溶解度降低,陰極反應減緩,所以溫度對腐蝕速率的影響具有雙重性[7]。另外,溫度升高使得腐蝕膜的形成加快,腐蝕膜的形成對腐蝕過程起一定的抑制作用。正是溫度在這幾個方面所起的綜合作用,使得CT80鋼腐蝕的溫度效應呈現出先增加后降低的變化規律,并在一定溫度下(如60 ℃)達到最大值。 (1) 在3.5% NaCl溶液中,隨著溫度的增加,CT80鋼的開路電位先負移后正移,在60 ℃時最負。表明在60 ℃時CT80鋼的電化學腐蝕熱力學趨勢或電化學活性增強,熱力學穩定性降低。 (2) CT80鋼在20 ℃時出現Warburg阻抗,隨著溫度的升高,Warburg阻抗消失,使CT80鋼的EIS譜呈現出雙容抗的特征,極化電阻值隨溫度升高呈現先減小后增大的趨勢,在60 ℃時達到最小。 (3) 在3.5% NaCl溶液中,隨著溫度的升高,CT80鋼的腐蝕速率呈現出先增大后減小的趨勢,其腐蝕速率在60 ℃時達到最大值。 [1] CRABTREE A R,GAVIN W. Coiled tubing in sour environment theory and practice. SPE/ICoT A Coiled Tubing Conference and Exhibition[C]//NACE 2004,Houston Texas:[s.n],2004:1045-1052. [2] BI Z Y,WANG R,JING X T. Grooving corrosion of oil coiled tubes manufactured by electrical resistance welding[J]. Corr Sci,2012,57(4):67-73. [3] CHENG Y F,WILMOTT M,LUO J L. Analysis of the role of electrode capacitance on the initiation of pits for A516 carbon steel by electrochemical noise measurements[J]. Corr Sci,1999,41(7):1245-1256. [4] GRIGORIS E K,STEFANO M S. Pitting corrosion of artificially aged T6AA2024/SiCp composites in 3.5% NaCl aqueous solution[J]. Corr Sci,2007,49(6):2711-2725. [5] AZZERRI N,MANCIA F,TAMBA A. Electrochemical prediction of corrosion behavior of stainless steels in chloride-containing water[J]. Corr Sci,1982,22(7):675-687. [6] 孫建波,柳偉,楊麗穎,等. 高礦化度介質中J55鋼的CO2腐蝕電化學行為[J]. 金屬學報,2008,44(8):991-994. [7] ROCCHINI G. Evaluation of the electrochemical parameters by means of series expansion[J]. Corr Sci,1994,36(8):1347-1361. [8] 宋詩哲. 腐蝕電化學研究方法[M]. 北京:化學工業出版社,1988:120-135. [9] EVANS U R. The corrosion of metals[M]. London:Edward Arnold,1960:50-55. [10] SHAMS El Din A M,Mohammed R A,Haggag H H. Corrosion inhibition by molybdate/polymaliate mixtures[J]. Desalination,1997,114(1):85-95. [11] ZHANG X,PEHKONEN S O,KOCHERGINSKY N,et al. Copper corrosion in mildly alkaline water with the disinfectant monochloramine[J]. Corr Sci,2002,44:2507-2528. [12] SOBRAL A V C,RISTOW J R W,AZAMBUJIA D S,et al. Potentiodynamic tests and electrochemical impedance spectroscopy of injection molded 316L steel in NaCl solution[J]. Corr Sci,2001,43:1019-1030. [13] SRDJAN N. Key issues related to modelling of internal corrosion of oil and gas pipelines-areview[J]. Corr Sci,2007,49:4308-4338. [14] GILEADI E,KIROWA-EISNER E. Some observations concerning the tafel equation and its relevance to charge transfer in corrosion[J]. Corr Sci,2005,47(12):3068-3085. Effect of Temperature on Electrochemical Corrosion Behavior of CT80 Coiled Tubing Steel REN Guo-qi1, SHEN Yi1, WANG Rong1, WEI Jia2 (1. School of Materials Science and Engineering, Xi′an Shiyou University, Xi′an 710065, China; 2. Northwest Sales Company of China National Petroleum Corp, Wuhan Branch, Wuhan 430030, China) Potentiodynamic polarization measurement and electrochemical impendence spectroscopy were employed to investigate the corrosion behavior of CT80 coiled tubing steel in 3.5% NaCl solution at different temperature(20 ℃, 40 ℃, 60 ℃, 80 ℃). The results showed that with the rise of temperature, the open circuit potential of CT80 coiled tubing steel shifted to the negative direction and then to the positive direction, it reached the minimum at 60 ℃, the corrosion current density of high CT80 coiled tubing steel firstly increased then decreased, it reached the maximum at 60 ℃, and its corrosion rate came to the maximum at 60 ℃,and the polarization resistance of CT80 coiled tubing steel firstly decreased and then increased, it reached the minimum at 60 ℃ with the maximum corrosion rate. CT80 steel; temperature; dynamic parameter; open circuit potential; electrochemical impedance spectroscopy (EIS) 2014-04-14 任國琪(1988-),碩士研究生,從事材料腐蝕機理與應用技術,13279210116,renguoqi@sina.com TG172 A 1005-748X(2015)03-0245-05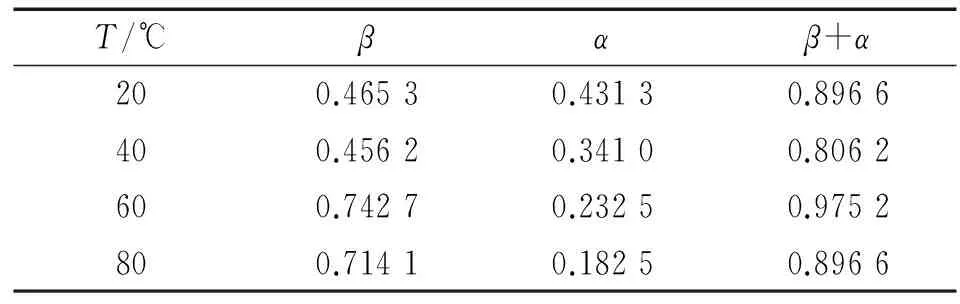

3 結論

