鐵的析氫腐蝕和吸氧腐蝕的實(shí)驗(yàn)原理探查
呂琳+袁夢(mèng)玥+張瑜+吳星
摘要:利用改進(jìn)的實(shí)驗(yàn)裝置和實(shí)驗(yàn)操作方法,探究了高中化學(xué)選修課程模塊《化學(xué)反應(yīng)原理》中“鐵的析氫腐蝕和吸氧腐蝕”實(shí)驗(yàn)的原理,結(jié)果表明:(1)在酸性環(huán)境中,鐵的析氫腐蝕和吸氧腐蝕是同時(shí)發(fā)生的,且發(fā)生析氫腐蝕后鐵的吸氧腐蝕強(qiáng)度更大;(2)利用改進(jìn)的實(shí)驗(yàn)裝置進(jìn)行鐵的析氫腐蝕和吸氧腐蝕實(shí)驗(yàn),可很好地幫助學(xué)生理解鐵的析氫腐蝕和吸氧腐蝕的原理。
關(guān)鍵詞:鐵粉;吸氧腐蝕;析氫腐蝕;腐蝕原理;實(shí)驗(yàn)探究
文章編號(hào):1005–6629(2015)10–0046–04 中圖分類(lèi)號(hào):G633.8 文獻(xiàn)標(biāo)識(shí)碼:B
1 問(wèn)題的提出
金屬的電化學(xué)腐蝕是高中化學(xué)新教材《化學(xué)反應(yīng)原理》中的一個(gè)重要內(nèi)容。為了幫助學(xué)生理解金屬的吸氧腐蝕和析氫腐蝕的原理,蘇教版教材《化學(xué)反應(yīng)原理》[1]中安排了鐵的吸氧腐蝕和析氫腐蝕實(shí)驗(yàn):將鐵粉和碳粉混合后分別撒入用氯化鈉和稀醋酸潤(rùn)濕的具支試管中,通過(guò)觀(guān)察與具支試管相連接導(dǎo)管中的水柱上升或下降情況,以體驗(yàn)鐵的電化學(xué)腐蝕。但有化學(xué)教師發(fā)現(xiàn),按照教材中的實(shí)驗(yàn)方法可能需要幾十分鐘的時(shí)間才能觀(guān)察到明顯現(xiàn)象[2]。很多教師就此實(shí)驗(yàn)進(jìn)行了改進(jìn)研究,如譚文生[3]通過(guò)用泡菜水浸濕的濾紙條沾附鐵粉和碳粉混合物進(jìn)行鐵的吸氧腐蝕實(shí)驗(yàn),和用稀醋酸浸濕的濾紙條沾附鐵粉和碳粉混合物進(jìn)行鐵的析氫腐蝕實(shí)驗(yàn);陶俞佳[4]對(duì)鐵粉和碳粉混合物的吸氧腐蝕實(shí)驗(yàn)裝置進(jìn)行了改進(jìn);唐敏[5]改用不同溶液浸濕鐵粉和碳粉混合物探究鐵的電化學(xué)腐蝕。總體看來(lái),多數(shù)對(duì)鐵的析氫、吸氧腐蝕實(shí)驗(yàn)的改進(jìn),旨在使實(shí)驗(yàn)現(xiàn)象更為明顯,而對(duì)于鐵析氫腐蝕的同時(shí)是否也發(fā)生吸氧腐蝕的探查較少。為了幫助學(xué)生更好地理解鐵的析氫腐蝕和吸氧腐蝕的原理,筆者改進(jìn)了實(shí)驗(yàn)裝置和實(shí)驗(yàn)操作方法,從定量的角度探究鐵的析氫腐蝕和吸氧腐蝕過(guò)程。
2 實(shí)驗(yàn)過(guò)程
2.1 實(shí)驗(yàn)原理
經(jīng)NaCl溶液濕潤(rùn)的碳粉、鐵粉混合物在空氣中發(fā)生吸氧腐蝕,其電極反應(yīng)及電池反應(yīng)的方程式為:
2.2 實(shí)驗(yàn)裝置
改進(jìn)后的實(shí)驗(yàn)裝置如圖1所示。裝置中具支試管壁上沾有NaCl溶液或稀酸溶液濕潤(rùn)的碳粉、鐵粉混合物,具支試管上的玻璃活塞用于腐蝕實(shí)驗(yàn)開(kāi)始時(shí)調(diào)節(jié)具支試管中的壓強(qiáng)與外界壓強(qiáng)一致;具支試管與盛有紅墨水的U型玻璃細(xì)導(dǎo)管相連,結(jié)合標(biāo)尺,可觀(guān)察記錄U型玻璃細(xì)導(dǎo)管中紅墨水的液面差(Δh)隨時(shí)間的變化。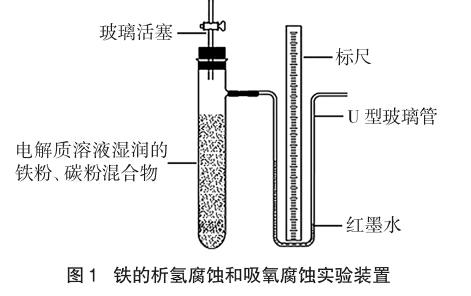
2.3 實(shí)驗(yàn)操作
實(shí)驗(yàn)1 HCl濃度變化對(duì)鐵析氫腐蝕影響的探究
在圖1所示裝置的具支試管中分別加入1.5mL 3% HCl、4% HCl、5% HCl溶液,使溶液充分潤(rùn)濕試管壁;稱(chēng)取3.0g還原性鐵粉和0.6g碳顆粒在研缽中充分研磨,將研磨好的碳粉、鐵粉混合物迅速倒入具支試管中,振蕩試管使碳粉、鐵粉混合物附著在試管壁上,迅速塞緊橡皮塞,打開(kāi)活塞,U型玻璃導(dǎo)管中紅墨水左右兩邊液面持平后關(guān)閉活塞。每隔一定時(shí)間記錄U型玻璃導(dǎo)管中紅墨水左右兩邊的液面高度差Δh。
實(shí)驗(yàn)2 飽和NaCl溶液、5% HAc溶液對(duì)鐵腐蝕影響的探究
分別以飽和NaCl溶液、5% HAc溶液代替實(shí)驗(yàn)1中的鹽酸溶液,在圖1所示裝置中進(jìn)行鐵的析氫腐蝕和吸氧腐蝕實(shí)驗(yàn)。
實(shí)驗(yàn)3 鐵析氫腐蝕和吸氧腐蝕組合實(shí)驗(yàn)探究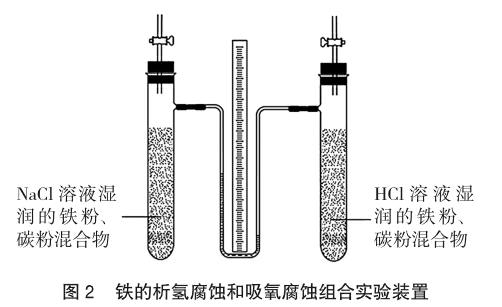
在圖2所示裝置的兩只具支試管中分別加入1.5mL飽和NaCl溶液和1.5mL 5% HCl溶液,使溶液充分潤(rùn)濕試管壁,分別稱(chēng)取兩份0.6g碳顆粒和3.0g還原性鐵粉,在研缽中充分研磨,將研磨好的碳粉、鐵粉混合物迅速倒入具支試管中,振蕩試管使碳粉、鐵粉混合物附著在試管壁上,迅速塞緊橡皮塞,打開(kāi)活塞,U型玻璃導(dǎo)管中紅墨水左右兩邊液面持平后關(guān)閉活塞。每隔一定時(shí)間記錄U型玻璃導(dǎo)管中紅墨水左右兩邊的液面高度差Δh。
3 實(shí)驗(yàn)結(jié)果與討論
3.1 不同酸度溶液對(duì)鐵析氫腐蝕的影響
在空氣中,鹽酸溶液濕潤(rùn)的碳粉、鐵粉混合物發(fā)生電化學(xué)腐蝕,導(dǎo)致實(shí)驗(yàn)裝置中U型玻璃導(dǎo)管內(nèi)紅墨水的液面發(fā)生變化。不同濃度的鹽酸溶液濕潤(rùn)的碳粉、鐵粉混合物發(fā)生電化學(xué)腐蝕時(shí)U型玻璃細(xì)導(dǎo)管中紅墨水的液面差(Δh)隨時(shí)間的變化曲線(xiàn)如圖3所示。圖中Δh<0表示具支試管內(nèi)壓強(qiáng)增大,具支試管內(nèi)有氣體生成;Δh>0表示具支試管內(nèi)壓強(qiáng)減小,具支試管內(nèi)有氣體被消耗。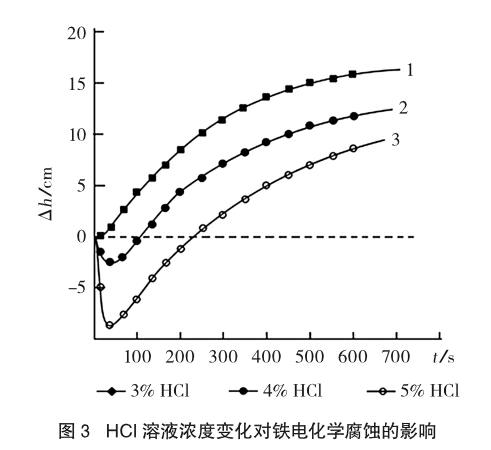
從圖3中可以看出:(1)用濃度為3%~5%的鹽酸溶液濕潤(rùn)的碳粉、鐵粉混合物,在空氣中經(jīng)過(guò)約10分鐘的電化學(xué)腐蝕,具支試管內(nèi)壓強(qiáng)均會(huì)減小,說(shuō)明即使在酸性環(huán)境中,鐵電化學(xué)腐蝕也會(huì)消耗氧氣。(2)用濃度為5%的鹽酸溶液濕潤(rùn)的碳粉、鐵粉混合物,在空氣中發(fā)生電化學(xué)腐蝕時(shí),可明顯觀(guān)察到析出氫氣和吸收氧氣的現(xiàn)象,在鐵開(kāi)始腐蝕約1分鐘內(nèi),由于腐蝕的酸度較大,析氫腐蝕導(dǎo)致的具支試管內(nèi)壓強(qiáng)增大強(qiáng)于吸收氧氣導(dǎo)致的具支試管內(nèi)壓強(qiáng)減小,可觀(guān)察到具支試管內(nèi)壓強(qiáng)增大(Δh<0);隨著腐蝕的繼續(xù)進(jìn)行,環(huán)境的酸度不斷下降,鐵析氫腐蝕的速率減小,吸收氧氣導(dǎo)致的具支試管內(nèi)壓強(qiáng)減小明顯地表現(xiàn)出來(lái),總體觀(guān)察到具支試管內(nèi)壓強(qiáng)減小(Δh增大)。(3)在空氣中用3%的鹽酸溶液濕潤(rùn)的碳粉、鐵粉混合物的腐蝕實(shí)驗(yàn),實(shí)驗(yàn)過(guò)程中很難觀(guān)察到發(fā)生析氫腐蝕產(chǎn)生的析出氫氣的現(xiàn)象,只能觀(guān)察到具支試管內(nèi)壓強(qiáng)減小。筆者認(rèn)為這并不能說(shuō)明該條件下不發(fā)生析氫腐蝕,只是在該條件下鐵電化學(xué)腐蝕吸收氧氣導(dǎo)致具支試管內(nèi)壓強(qiáng)減小比析氫腐蝕析出氫氣導(dǎo)致具支試管內(nèi)壓強(qiáng)增大要強(qiáng)得多,因而只能觀(guān)察到具支試管內(nèi)壓強(qiáng)減小的現(xiàn)象。
3.2 不同介質(zhì)對(duì)鐵電化學(xué)腐蝕的影響
圖4給出了分別用5%的鹽酸溶液、醋酸溶液和飽和氯化鈉溶液濕潤(rùn)的碳粉、鐵粉混合物在空氣中電化學(xué)腐蝕時(shí),U型玻璃導(dǎo)管中紅墨水左右兩邊的液面高度差Δh隨時(shí)間的變化曲線(xiàn)。為了說(shuō)明鐵析氫腐蝕時(shí)吸氧腐蝕的速率,圖4中同時(shí)給出了在圖2裝置中所做的鐵析氫腐蝕和吸氧腐蝕組合實(shí)驗(yàn)的結(jié)果。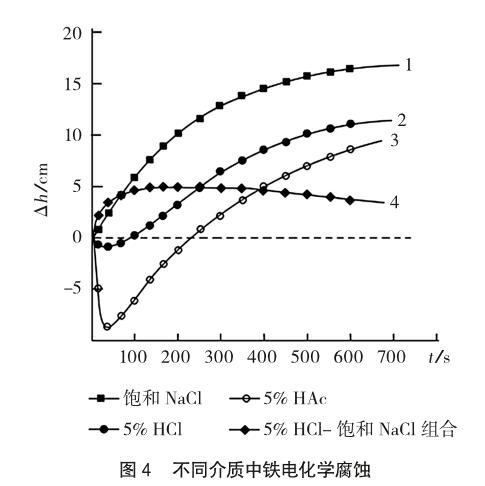
比較圖4中的曲線(xiàn)1、2、3發(fā)現(xiàn):(1)用5%的鹽酸溶液、醋酸溶液和飽和氯化鈉溶液濕潤(rùn)的碳粉、鐵粉混合物在空氣中電化學(xué)腐蝕時(shí),都能觀(guān)察到鐵的吸氧腐蝕。用飽和氯化鈉溶液濕潤(rùn)的碳粉、鐵粉混合物在空氣中腐蝕時(shí)僅能觀(guān)察到吸氧腐蝕;用5%的鹽酸溶液或醋酸溶液濕潤(rùn)的碳粉、鐵粉混合物在空氣中腐蝕時(shí),既能觀(guān)察到析氫腐蝕又能觀(guān)察到吸氧腐蝕。(2)碳粉、鐵粉混合物用5%的鹽酸溶液濕潤(rùn)比用5%的醋酸溶液濕潤(rùn),更利于觀(guān)察鐵在酸性氛圍中的析氫腐蝕。
利用裝置2進(jìn)行的鐵析氫腐蝕和吸氧腐蝕組合實(shí)驗(yàn)的結(jié)果為圖4中的曲線(xiàn)4。該裝置中U型玻璃導(dǎo)管一邊聯(lián)接著鐵吸氧腐蝕裝置,另一邊聯(lián)接著鐵析氫腐蝕裝置,記錄的Δh為與鐵吸氧腐蝕裝置相連的U型玻璃導(dǎo)管內(nèi)紅墨水上升和與鐵析氫腐蝕裝置相連的U型玻璃導(dǎo)管內(nèi)紅墨水下降的差值(Δh增大表示鐵吸氧腐蝕裝置內(nèi)壓強(qiáng)減小)。比較曲線(xiàn)1和曲線(xiàn)4發(fā)現(xiàn):(1)在時(shí)間約為90秒前曲線(xiàn)4的Δh上升的速率明顯大于曲線(xiàn)1的Δh上升的速率,說(shuō)明在該時(shí)間段內(nèi)裝置2中用5%的鹽酸溶液濕潤(rùn)的碳粉、鐵粉混合物發(fā)生的析氫腐蝕產(chǎn)生的氫氣速率大于其發(fā)生吸氧腐蝕消耗的氧氣速率,加上裝置2中用飽和氯化鈉溶液濕潤(rùn)的碳粉、鐵粉混合物發(fā)生著吸氧腐蝕消耗氧氣,整體表現(xiàn)為曲線(xiàn)4中的Δh上升的速率大于僅存在用飽和氯化鈉溶液濕潤(rùn)的碳粉、鐵粉混合物發(fā)生著吸氧腐蝕的Δh上升的速率。(2)在實(shí)驗(yàn)中鐵腐蝕發(fā)生約90秒后,曲線(xiàn)4的Δh上升的速率明顯減小,并出現(xiàn)下降。說(shuō)明在該時(shí)間段裝置2中用5%的鹽酸溶液濕潤(rùn)的碳粉、鐵粉混合物發(fā)生的析氫腐蝕析出氫氣的速率下降,而其吸氧腐蝕消耗氧氣的速率上升,且出現(xiàn)用5%的鹽酸溶液濕潤(rùn)的碳粉、鐵粉混合物吸氧腐蝕消耗的氧氣速率大于用飽和氯化鈉溶液濕潤(rùn)的碳粉、鐵粉混合物發(fā)生的吸氧腐蝕消耗氧氣的速率。其可能原因是,用酸性溶液濕潤(rùn)的碳粉、鐵粉混合物發(fā)生析氫腐蝕的同時(shí),還發(fā)生著兩個(gè)反應(yīng),一是析氫腐蝕生成的Fe2+和Fe(OH)2進(jìn)一步與氧氣反應(yīng)消耗氧氣,二是暴露在空氣中的鐵粉(特別是沒(méi)有完全被酸性溶液濕潤(rùn)的鐵粉)直接發(fā)生吸氧腐蝕消耗氧氣,這兩個(gè)反應(yīng)消耗氧氣的總速率比用飽和氯化鈉溶液濕潤(rùn)的碳粉、鐵粉混合物發(fā)生的吸氧腐蝕消耗氧氣的速率大。
3.3 結(jié)論
(1)鐵在酸性環(huán)境中發(fā)生腐蝕時(shí),析出氫氣和消耗氧氣的反應(yīng)同時(shí)發(fā)生著。通過(guò)觀(guān)察鐵腐蝕體系中的壓強(qiáng)差來(lái)說(shuō)明鐵發(fā)生析氫腐蝕的實(shí)驗(yàn),必須在鐵腐蝕析出氫氣的速率大于鐵腐蝕消耗氧氣的條件下進(jìn)行。即用類(lèi)似于裝置1進(jìn)行鐵析氫腐蝕實(shí)驗(yàn)時(shí),要求濕潤(rùn)碳粉、鐵粉混合物的酸性溶液具有一定的酸度,例如用4%~5%的鹽酸溶液濕潤(rùn)碳粉、鐵粉混合物。
(2)鐵在酸性環(huán)境中發(fā)生腐蝕時(shí),如果酸性介質(zhì)中H+的物質(zhì)的量不是較大(酸性介質(zhì)中H+的物質(zhì)的量較大時(shí),發(fā)生的是酸與鐵的反應(yīng)),用如圖1所示裝置,實(shí)驗(yàn)中能同時(shí)觀(guān)察到析出氫氣和吸收氧氣的現(xiàn)象。
(3)在其他條件相同時(shí),用裝置2進(jìn)行鐵析氫腐蝕和吸氧腐蝕組合實(shí)驗(yàn),可觀(guān)察到“鐵發(fā)生析氫腐蝕過(guò)程中消耗氧氣的速率大于鐵單純發(fā)生吸氧腐蝕消耗氧氣的速率”的現(xiàn)象。
參考文獻(xiàn):
[1]王祖浩主編.普通高中課程標(biāo)準(zhǔn)實(shí)驗(yàn)教科書(shū)·化學(xué)反應(yīng)原理(選修)[M].南京:江蘇教育出版社,2009:23~25.
[2]任志強(qiáng),徐素芳.蘇教版《化學(xué)反應(yīng)原理》中值得商榷的幾個(gè)問(wèn)題[J].中學(xué)化學(xué)教學(xué)參考,2008,(11):36.
[3]譚文生.鐵的吸氧腐蝕與析氫腐蝕對(duì)比實(shí)驗(yàn)設(shè)計(jì)[J].化學(xué)教學(xué),2011,(6):46~47.
[4]陶俞佳,李桂林.吸氧腐蝕實(shí)驗(yàn)的改進(jìn)[J].化學(xué)教學(xué),2009,(6):26~27.
[5]唐敏.實(shí)驗(yàn)探究鋼鐵的腐蝕[J].化學(xué)教育,2011,(6):58~59.

