Fenton氧化降解活性深藍B-2GLN的在線分光光度法研究
高愛舫,王衛平,李愛國
?
Fenton氧化降解活性深藍B-2GLN的在線分光光度法研究
高愛舫1, 2,王衛平1,李愛國1
(1. 石家莊經濟學院水資源與環境學院,河北石家莊,050031;2. 河北省水資源可持續利用與開發重點實驗室,河北石家莊,050031)
采用在線分光光度法研究水溶液中活性深藍染料B-2GLN的Fenton氧化降解過程。考查FeSO4和H2O2的初始劑量、pH以及活性深藍染料B-2GLN的初始質量濃度對染料降解過程的影響,并通過離子色譜法對Fenton氧化后的產物進行分析。研究結果表明:在Fenton氧化過程中,在線分光光度法是研究活性深藍染料色度去除率的一種快速、方便及可行的技術,含活性深藍染料廢水的Fenton氧化過程分為2個階段;Fenton氧化過程降解活性深藍染料B-2GLN的最佳條件,即H2O2最佳劑量為2.635 mmol/L,pH為2.7,催化劑 Fe2+的投加量為 0.069 6 mmol/L;水溶液中活性深藍染料B-2GLN的分子結構只是被Fenton氧化分解而未被完全礦化(300 s)。
在線分光光度法;Fenton氧化;活性深藍染料B-2GLN;廢水
活性染料是當今紡織工業應用最廣的一種染料,在給世界帶來亮麗色彩的同時也給人類的生存環境帶來了嚴重的污染[1]。每年有12%的合成染料在生產過程中流失,造成含染料廢水具有很高的色度和化學需氧量(COD)以及較低的生化需氧量、抗氧化以及難以生物降解等特點[2],因此,在染色行業中最關鍵的問題是如何處理染料廢水中所含的可見污染物[3]。目前,有許多方法來處理染料廢水,如活性炭吸附[4]、膜分離技術[5]、化學混凝、超聲波協同降解[6]、生物降解[7]、TiO2光催化氧化[8]、Fenton氧化[9]等方法。Fenton氧化法是一種處理有色廢水的常用方法。過氧化氫溶液和亞鐵離子催化劑可以有效地氧化有機污染物。在弱酸性條件下,Fe2+被H2O2氧化,生成Fe3+,羥基(·OH)和OH?[10],產生的高活性·OH破壞并分解有機染料的分子結構,達到染料廢水的脫色效果。分光光度計可以對染料的質量濃度進行分析[11?12]。NaOH和Na2SO4可以用來分解H2O2并在測量之前結束反應。Fe2+是一種常用的無機凝結離子,它可以在堿性介質中去除一部分染料。此外,在氧化過程中染料溶液樣品被取出的過程也會消耗時間。在線分光光度法可以用來監測Fenton氧化過程中染料的瞬時狀態。Coque等[13?14]使用在線分光光度法來研究紅雷馬素染料RR,錐蟲藍染料TB和活性亮藍X-BR 染料RBB X-BR的脫色過程,均證明了在線分光光度法對于研究快速脫色反應而言是一種簡單、有效的方法。本文作者為了監測染料的即時吸光度而建立在線分光光度系統,用此方法對Fenton氧化過程中活性深藍染料B-2GLN的降解進行可行性分析,研究FeSO4和H2O2的初始劑量,pH以及染料的初始質量濃度對活性深藍染料B-2GLN降解的影響。通過紫外?可見吸收光譜和離子色譜法對活性深藍染料B-2GLN降解的中間產物進行分析。
1 實驗
1.1 實驗材料
活性深藍染料B-2GLN購置于石家莊染料廠,其分子結構如圖1所示。模擬染料廢水由一定量的活性深藍染料溶于二次蒸餾水中進行配置。FeSO4·7H2O、H2O2(體積分數為30%)和硫酸,均為分析純,購置于石家莊現代化學試劑公司。
1.2 實驗裝置
圖2所示為在線分光光度系統。從圖2可見:在線分光光度系統由反應裝置、光學測量裝置和記錄裝置3部分組成。反應裝置包括磁力攪拌器和250 mL燒杯。測量裝置包括紫外?可見分光光度計、蠕動泵和比色皿。廢水在系統中的流動速度為22 mL/min。記錄裝置為計算機,在反應過程中其記錄頻率為 12次/min。
1.3 實驗方法
在250 mL燒杯中進行Fenton氧化過程,選擇一定質量濃度的染料溶液,配置一定濃度的FeSO4加入染料廢水中,調節染料溶液的pH,同時開啟攪拌器和蠕動泵,溶液通過蠕動泵被輸送到紫外?可見分光光度計的比色皿中。通過紫外?可見分光光度計測定染料的吸收峰,并選擇測定波長。計算物質濃度的H2O2并將其添加到廢水中,與此同時與分光光度計連接的計算機開始記錄實驗的吸光度。
1.4 離子色譜分析
使用瑞士萬通881型離子色譜儀通過電導檢測器、離子色譜柱和MagIC Net操作軟件來測量降解后的染料廢水中的無機離子(Cl?,NO3?和SO42?),淋洗液由Na2CO3和NaHCO3混合配制而成。淋洗液的流動速度為1.0 mL/min。
2 結果與討論
2.1 在線分光光度法的可行性分析
在線分光光度法用來分析Fenton氧化過程中的活性深藍染料B-2GLN。圖3所示為實驗材料的紫外?可見光譜。從圖3可見:活性深藍染料B-2GLN,H2SO4,Fe2+,Fe3+和H2O2的紫外?可見光光譜。只有活性深藍染料B-2GLN(RDB B-2GLN)在500~700 nm光譜范圍有1個最大吸收峰(波長為600 nm)。在此最大吸收峰處且pH為中性時,RDB B-2GLN的質量濃度()和吸光度()的標準方程和標準曲線如圖4所示(=47.945 03+2.247 49,2=0.999 9)。在實驗中通過計算機記錄樣品的即時吸光度,并根據標準方程將吸光度轉化為染料質量濃度。從圖4可見:當溶液中加入Fe2+,Fe3+和H2SO4時活性深藍染料B-2GLN溶液的紫外?可見光譜有很大的改變。但是加入Fe2+,Fe3+和H2SO4的染料溶液的光譜在500~700 nm沒有發生任何變化,這表明染料溶液的紫外?可見光譜在可見光范圍內未受Fe2+,Fe3+和H2SO4影響。所以,本實驗中,選擇測定波長為600 nm,對Fenton氧化過程中染料溶液的氧化降解進行在線測定研究。
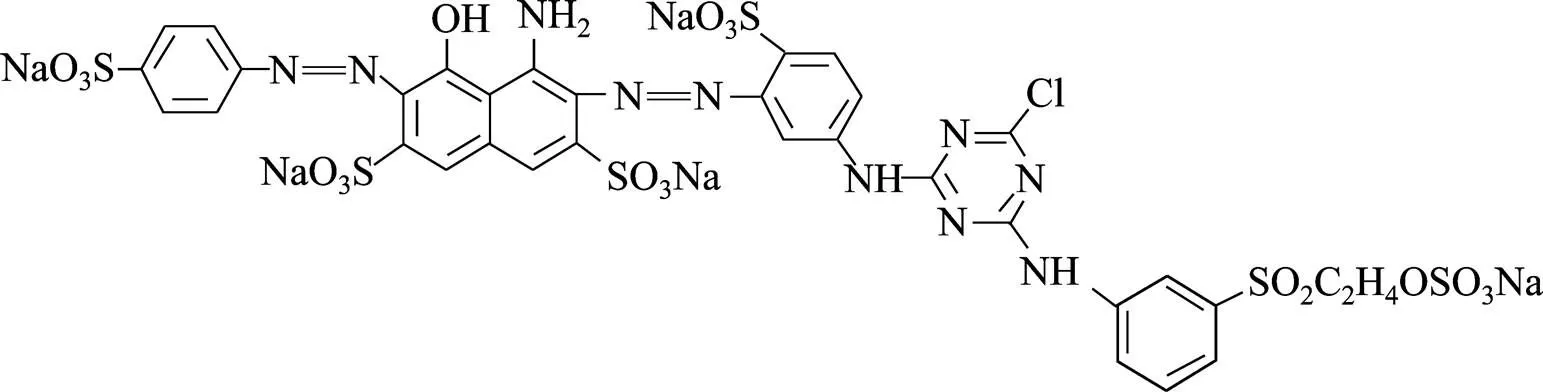
圖1 活性深藍染料B-2GLN分子結構
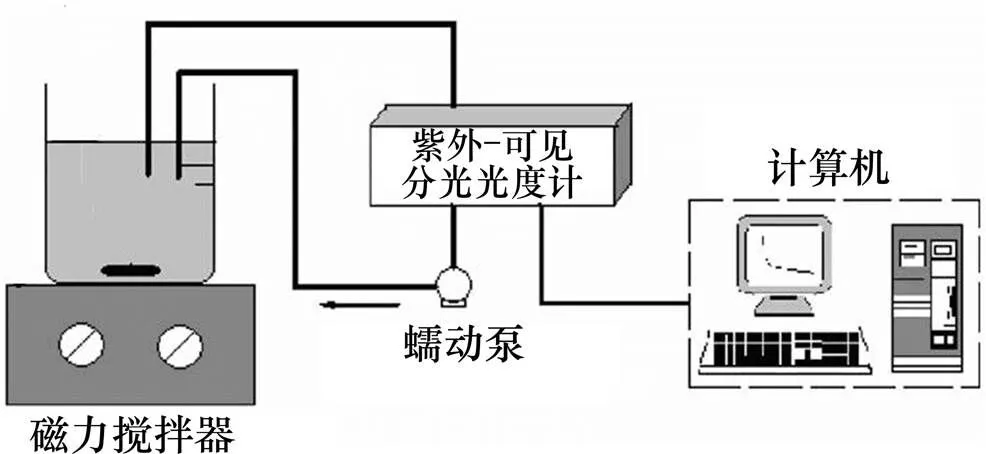
圖2 在線分光光度系統
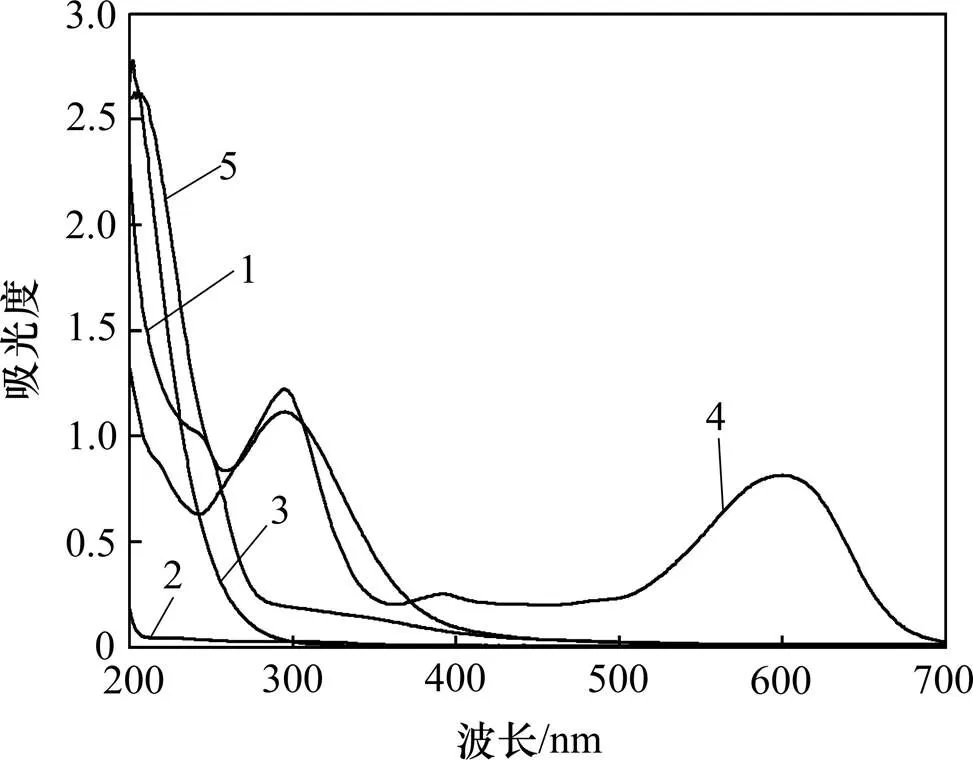
1—Fe2+; 2—H2SO4; 3—H2O2; 4—RDB B-2GLN; 5—Fe3+
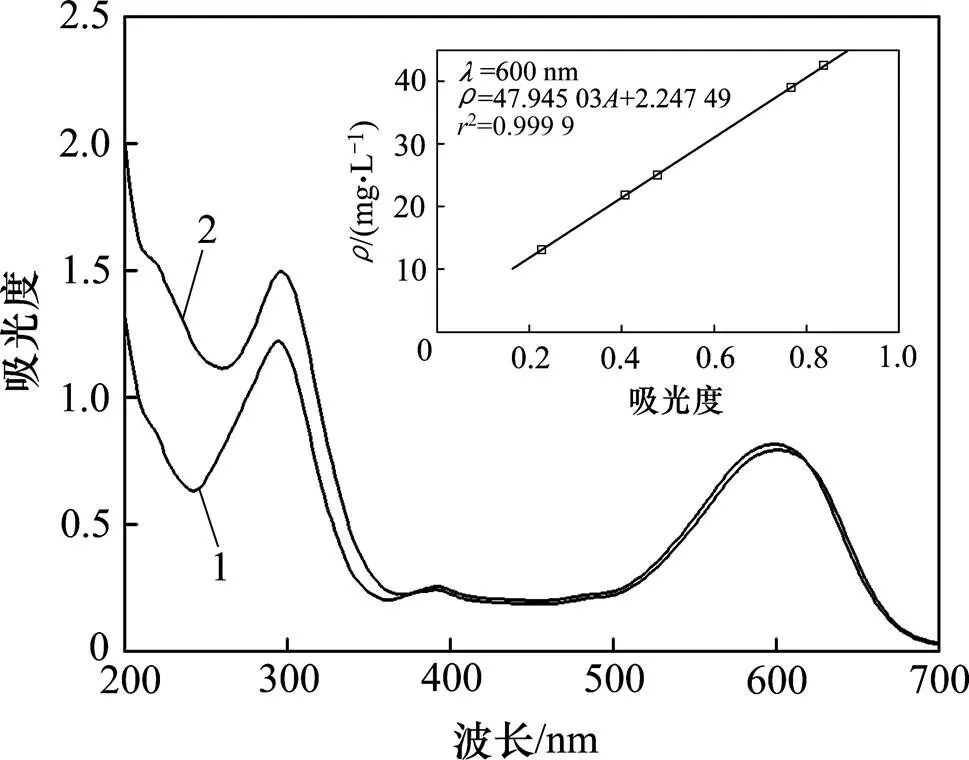
1—RDB B-2GLN; 2—RDB B-2GLN+H2SO4+Fe2++Fe3+
2.2 時間對活性深藍染料B-2GLN降解的影響
圖5所示為染料的/0值隨時間的變化規律((RDB B-2GLN)0=16 mg/L,(Fe2+)0=0.069 6 mmol/L,(H2O2)0=2.635 mmol/L,pH=2.7,=27℃)。為伴隨時間的即時染料質量濃度,0為染料的初始質量濃度。處理活性深藍染料B-2GLN廢水,可以得出Fenton氧化過程分2個階段進行:第1個階段,降解速率非常的快;第2個階段(≥25 s),隨著反應時間的延長脫色速率的增加明顯放緩。這些實驗現象可以從2個方面解釋。首先,溶液中Fe2+和H2O2的量隨著Fenton氧化過程的消耗而減少。其次,反應所產生的中間產物會降低染料降解的速率。Fenton氧化過程在第1階段明顯遵循一級動力學。ln(0/)=ap。通過數據點的最佳擬合曲線的斜率代表一級速率常數。從圖5可以看出:研究結果符合簡單的一級動力學定律。

圖5 活性深藍染料B-2GLN的降解與時間的關系
2.3 各種因素對活性深藍染料B-2GLN降解的影響
主要研究FeSO4和 H2O2的初始濃度,pH以及活性深藍染料B-2GLN的初始質量濃度對反應的影響。在不同實驗條件下,對脫色反應速率常數ap和300 s時的染料去除率(=(0?)/0)×100%)進行比較。
2.3.1 Fe2+初始濃度的影響
圖6所示為在一系列不同初始濃度Fe2+的條件下染料的色度去除率和反應速率常數ap((RDB B-2GLN)0=16 mg/L,(H2O2)0=2.635 mmol/L,pH=2.7,=27℃)。從圖6可見:Fe2+的初始濃度從0.016 7 mmol/L到0.069 6 mmol/L時RDB B-2GLN的脫色率從33.19%增加至85.04%。但是當Fe2+的初始濃度繼續增加時RDB B-2GLN的脫色率略有降低。這一實驗現象表明高初始濃度的Fe2+并沒有對Fenton氧化過程中RDB B-2GLN的脫色產生作用,這是由于Fe2+和染料分子對·OH的爭奪[15]。因此選擇0.069 6 mmol/L初始濃度的Fe2+作為反應的最佳劑量。當Fe2+的初始濃度從0.016 7 mmol/L到0.069 6 mmol/L時ap從0.014 43 s?1增至0.062 65 s?1。它表明Fe2+催化劑可以明顯的促進H2O2的分解和·OH的產生。

1—kap; 2—R
2.3.2 H2O2初始濃度的影響
過氧化氫是Fenton氧化過程中需要考慮的1個重要因素。圖7所示為Fe2+的初始濃度保持不變((RDB B-2GLN)0=16 mg/L,pH=2.7,=27℃),但H2O2的初始濃度不同時,RDB B-2GLN的色度去除率和反應速率常數ap。H2O2的初始濃度從0.907 mmol/L增加到2.635 mmol/L時, RDB B-2GLN的色度去除率從44.26%增加到85.04%。與此相反,當H2O2的初始濃度增加到4.508 mmol/L時RDB B-2GLN的色度去除率僅為76.3%。當H2O2的初始濃度從0.907 mmol/L增加到2.635 mmol/L時, 反應速率常數ap從 0.036 37 s?1增加到0.062 65 s?1。當H2O2的初始濃度從2.635 mmol/L增加到4.508 mmol/L時反應速率常數ap在0.062 65 s?1到0.052 77 s?1之間有較大波動。H2O2初始濃度的增加使·OH的產生加快。然而,由于H2O2和·OH之間會產生反應,高濃度的H2O2可以消耗·OH。因此,在Fenton氧化過程中處理RDB B- 2GLN染料廢水時,最佳的H2O2初始濃度可選擇為2.635 mmol/L。

1—kap; 2—R
2.3.3 初始pH的影響
在Fenton氧化降解染料的過程中,溶液的pH起到了重要的作用。圖8所示為pH對Fenton氧化降解染料的影響((RDB B-2GLN)0=16 mg/L,(Fe2+)0= 0.069 6 mmol/L,(H2O2)0=2.635 mmol/L,=27℃)。從圖8可見:當溶液的pH由2.0增加到2.7時,染料的色度去除率和ap分別由76.57%增至85.04%和由0.042 29 s?1增至0.062 65 s?1。但是隨著pH繼續增長至5.0時,染料的色度去除率和ap分別由85.04%降至64.32%和由0.062 65 s?1降至0.047 16 s?1。因此,選取pH=2.7為Fenton氧化處理活性深藍B-2GLN染料廢水的最佳pH。在pH<2.7時,色度去除率和反應速率是有限的,是因為過量的氫離子消耗羥基·OH,發生反應·OH+H++e?→H2O。當pH>2.7時,由于氫氧化鐵絡合物的形成,使得過氧化氫分解并使亞鐵離子催化劑失效,導致Fenton氧化能力降低。所以,在Fenton氧化處理RDB B-2GLN染料廢水時對溶液的pH敏感。
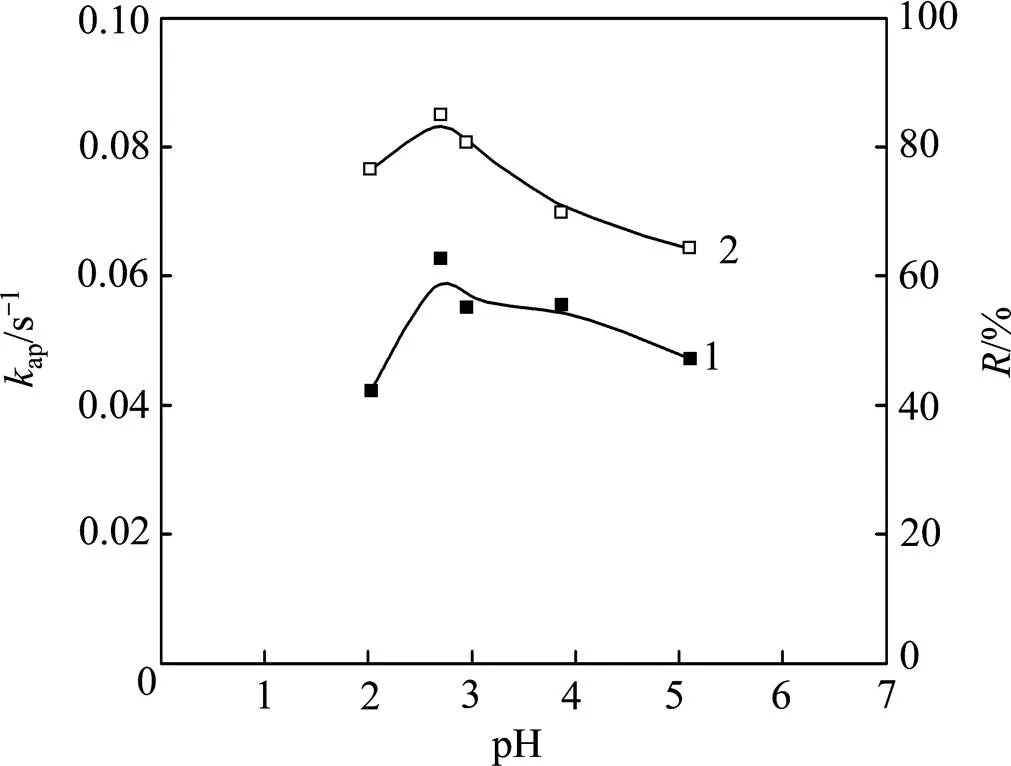
1—kap; 2—R
2.3.4 染料初始質量濃度的影響
染料初始質量濃度對色度去除率和反應速率常數的影響如圖9所示((Fe2+)0=0.069 6 mmol/L,(H2O2)0= 2.635 mmol/L,pH=2.7,=27℃)。從圖9可以看到:當染料的初始質量濃度從8.4 mg/L變化至29.8 mg/L時,RDB B-2GLN染料的色度去除率和反應速率常數(ap)相應略有降低;隨著染料溶液初始質量濃度的升高,水中的染料分子的數量相應增加,由于溶液中·OH的數量沒有變化,色度去除率和反應速率常數(ap) 降低。
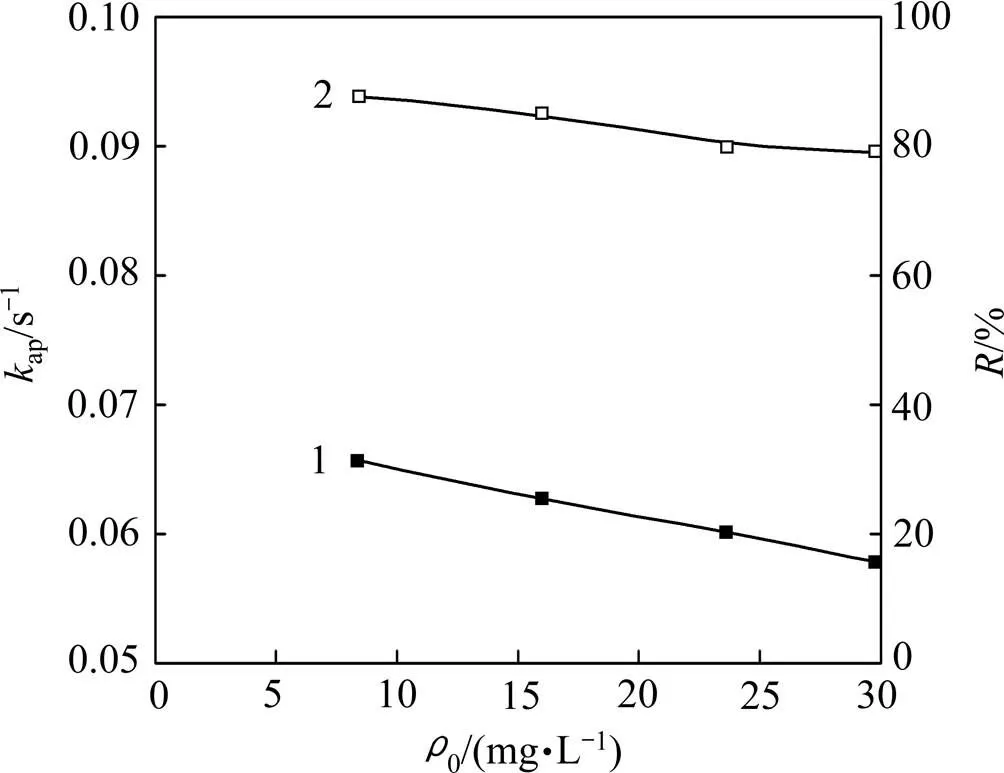
1—kap; 2—R
2.4 Fenton氧化后產物的分析
為了推測染料在Fenton氧化過程后的產物,運用紫外?可見分光光度法和離子色譜法分析降解后的中間產物。反應條件如下:RDB B-2GLN染料的初始質量濃度為16 mg/L,Fe2+的初始濃度為0.069 6 mmol/L,H2O2的初始濃度為2.635 mmol/L,pH為2.7,溫度為27 ℃,反應時間為300 s。
2.4.1 紫外?可見光譜
從Fenton法處理前后樣品的紫外?可見光譜[16]中可以看出:處理之前樣品溶液在可見光范圍有1個很大的吸收峰;經過300 s處理后,樣品在可見光范圍的吸光度大幅度減小,而其在紫外光區域的吸光度卻大幅增加。以上現象表明RDB B-2GLN染料可以通過Fenton氧化法來降解,該過程可以將染料的分子結構破壞。但是處理后樣品在紫外光范圍具有很大的吸光度,表明Fenton氧化法無法將RDB B-2GLN染料完全礦化,該過程有中間產物和副產物存在。
2.4.2 離子色譜(IC)分析
Fenton氧化后的產物經過IC分析,得出水溶液存在大量的SO42?離子,表明Fenton氧化破壞了RDB B-2GLN的化學結構。然而,在溶液中有少量的NO3?和Cl?存在,表明反應不徹底。在300 s內,染料被降解產生了中間產物或副產物,與經Fenton氧化后染料的紫外?可見光譜結果相一致。如果Fenton氧化反應徹底,那么溶液中會有大量的Cl?和NO3?存在。因此,在短時間內,Fenton氧化過程不能使RDB B-2GLN完全礦化。
3 結論
1) 在Fenton氧化去除活性深藍染料B-2GLN的色度過程中,在線分光光度法是一種方便、可行的監測技術。活性深藍染料B-2GLN廢水的Fenton氧化過程分為2個階段:第1個階段(≤25 s),降解速率非常快;第2個階段,隨著反應時間的延長,脫色速率的增加明顯降低。
2) 降解染料的最佳實驗條件如下:催化劑 Fe2+的劑量為0.069 6 mmol/L,H2O2的初始濃度為 2.635 mmol/L,初始pH為2.7。
3) Fenton氧化過程能夠快速降解活性深藍染料B-2GLN (300 s),破壞了其化學結構,通過離子色譜法分析了氧化后有機廢水中的中間體和副產物,表明Fenton氧化在300 s時間內不能完全礦化活性深藍染料B-2GLN。
[1] Ku?i? H, Bo?i? A L, Koprivanac N. Fenton type processes for minimization of organic content in colored wastewaters. Part Ⅰ: Processes optimization[J]. Dyes Pigments, 2007, 74(2): 380?387.
[2] Kritikos D E, Xekoukoulotakis N P, Psillakis E, et al. Photocatalytic degradation of reactive black 5 in aqueous solution: Effect of operating conditions and coupling with ultrasound irradiation[J]. Water Research, 2007, 41(10): 2236?2246.
[3] Karim M M, Das A K, Lee S H. Treatment of colored effluent of the textile industry in Bangladesh using zinc chloride treated indigenous activated carbons[J]. Analytica Chimica Acta, 2006, 576(1): 37?42.
[4] Lee J W, Choi S P, Thiruvenkatachari R, et al. Submerged microfiltration membrane coupled with alum coagulation/ powdered activated carbon adsorption for complete decolorization of reactive dyes[J]. Water Research, 2006, 40(3): 435?444.
[5] Kim T H, Park C, Kim S Y. Water recycling from desalination and purification process of reactive dye manufacturing industry by combined membrane filtration[J]. Journal of Cleaner Production, 2005, 13(8): 779?786.
[6] LI Jitai, LI Mei, LI Jihui, et al. Decolorization of azo dye direct scarlet 4BS solution using exfoliated graphite under ultrasonic irradiation[J]. Ultrasonics Sonochemistry, 2007, 14(2): 241?245.
[7] Park C, Lee M, Lee B, et al. Biodegradation and biosorption for decolorization of synthetic dyes by Funalia trogii[J]. Biochemical Engineering Journal, 2007, 36(1): 59?65.
[8] CHEN Shifu, LIU Yunzhang. Study on the photocatalytic degradation of glyphosate by TiO2photocatalyst[J]. Chemosphere, 2007, 67(5): 1010?1017.
[9] Gulkaya ?, Surucu G A, Dilek F B. Importance of H2O2/Fe2+ratio in Fenton’s treatment of a carpet dyeing wastewater[J]. Journal of Hazardous Materials, 2006, 136(3): 763?769.
[10] Ku?i? H, Koprivanac N, Bo?i? A L, et al. Photo-assisted Fenton type processes for the degradation of phenol: A kinetic study[J]. Journal of Hazardous Materials, 2006, 136(3): 632?644.
[11] CHEN Jianxin, ZHU Lizhong. Catalytic degradation of orange 2 by UV-Fenton with hydroxyl-Fe-pillared bentonite in water[J]. Chemosphere, 2006, 65(7): 1249?1255.
[12] Liou M J, Lu M C, Chen J N. Oxidation of explosives by Fenton and photo-Fenton processes[J]. Water Research, 2003, 37(13): 3172?3179.
[13] Coque Y, Touraud E, Thomas O. On line spectrophotometric method for the monitoring of color removal processes[J]. Dyes Pigments, 2002, 54(1): 17–23.
[14] XU Hang, ZHANG Dongxiang, XU Wenguo. Monitoring of decolorization kinetics of reactive brilliant blue X-BR by online spectrophotometric method in Fenton oxidation process[J]. Journal of Hazardous Materials, 2008, 158(2/3): 445?453.
[15] ZHENG Huaili, PAN Yunxia, XIANG Xinyi. Oxidation of acidic dye Eosin Y by the solar photo-Fenton processes[J]. Journal of Hazardous Materials, 2007, 141(3): 457?464.
[16] 高愛舫, 王衛平, 李愛國, 等. Fenton氧化活性深藍染料B-2GLN的動力學[J]. 環境工程學報, 2014, 8(6): 2407?2412. GAO Aifang, WANG Weiping, LI Aiguo, et al. Kinetics of reactive dark blue B-2GLN with fenton oxidation process[J]. Chinese Journal of Environmental Engineering, 2014, 8(6): 2407?2412.
(編輯 羅金花)
Online spectrophotometricstudy of thedegradation of reactive dark blue B-2GLN by Fenton oxidation process
GAO Aifang1, 2, WANG Weiping1, LI Aiguo1
(1. School of Water Resources and Environment, Shijiazhuang University of Economics, Shijiazhuang 050031, China;2. Hebei Province Key Laboratory of Sustained Utilization and Development of Water Resources, Shijiazhuang 050031, China)
Online spectrophotometric method was employed to monitor simulated reactive dark blue B-2GLN (RDB B-2GLN) in aqueous solution in Fenton oxidation process. The dye degradation effects of initial dosage of FeSO4and H2O2, pH, initial mass concentration of dye were studied, and the products of Fenton oxidation were analyzed by ion chromatography method. The results show that online spectrophotometric method is a quick, feasible and convenient technique to monitor color removal of RDB B-2GLN in Fenton process. Fenton oxidation process for the treatment of RDB B-2GLN consists of two stages. The optimal dosage of H2O2is 2.635 mmol/L and pH is 2.7. The optimal dosage of Fe2+for the dye degradation is 0.069 6 mmol/L; the molecular structure of RDB B-2GLN in aqueous solution is decomposed and not mineralized by Fenton’s reagent (300 s).
online spectrophotometric method; Fentonoxidation; reactive dark blue B-2GLN; wastewater
10.11817/j.issn.1672-7207.2015.09.053
X791
A
1672?7207(2015)09?3553?06
2014?11?22;
2015?01?25
河北省教育廳優秀青年基金資助項目(Y2011110);河北省首批青年拔尖人才計劃項目(2013) (Project(Y2011110) supported by the Excellent Youth Foundation of Department of Education of Hebei Province; Project(2013) supported by the First Batch of Young Talent Plan of Hebei Province)
高愛舫,博士,副教授,從事水污染控制理論與處理技術的研究;E-mail: llhx2006@126.com

