納米級二氧化錫的清潔制備
馬敬環,趙寶軍,吳紹斌,劉 瑩,康雪婧,胡道友
(1.天津工業大學環境與化學工程學院,天津300387;2.天津濱瀚環保科技發展有限公司,天津300451)
納米級二氧化錫的清潔制備
馬敬環1,2,趙寶軍1,吳紹斌1,劉 瑩1,2,康雪婧1,胡道友1
(1.天津工業大學環境與化學工程學院,天津300387;2.天津濱瀚環保科技發展有限公司,天津300451)
以結晶氯化錫為原料,采用水熱法制備納米級二氧化錫,過程中不添加沉降劑和分散劑,避免在晶體洗滌過程中產生酸液及有機廢液,實現了納米二氧化錫的清潔制備.采用X射線衍射儀(XRD)、熱重分析儀、傅里葉紅外光譜(FT-IR)、粒度分析儀、掃描電子顯微鏡(SEM)對制備的納米級二氧化錫進行晶體結構及性能表征.結果表明:所制備納米二氧化錫具有良好的結晶性、熱穩定性和較高的相純度;粒徑分布均勻,粒徑范圍在40~60 nm之間.
納米級二氧化錫;清潔制備;晶體結構
納米二氧化錫具有獨特的光學、電學性能、表面特性和吸附特性,其在化工催化、氣體傳感器、涂料、壓敏材料、電池電極材料以及有機廢水處理等眾多領域都具有廣泛的應用[1].但其性能對顆粒尺寸有較強的依賴性,要得到性能優異的二氧化錫納米材料,就必須制備出粒徑小、粒度分布均勻、分散性好的二氧化錫納米粉體[2].納米二氧化錫材料的研究非常活躍,在過去20年中,納米結構的二氧化錫成為最受關注的氧化物納米材料[3].
現階段制備二氧化錫的方法有很多,如水熱法[4]、機械化學法[5]、溶膠凝膠法[6]、化學沉淀法[7]、電沉積法[8]等.其中水熱法工藝和設備簡單,易于控制,無需高溫灼燒處理,且產物結晶和分散良好,已成為當今納米材料重要的制備方法.目前,在水熱法制備過程中大都通過添加強酸或堿液作為沉降劑以方便進一步沉降分離,這就使得在沉淀洗滌的過程中造成了大量廢酸液和有機廢液,不僅難以回收處理,而且不當的排放會造成水體污染.鑒于此,本文亦采用該法制備納米級二氧化錫,但不同以往的是在制備過程中不添加硝酸[9]等作為沉降劑,也不加入正丁醇[4]等有機試劑作為分散劑,僅以結晶四氯化錫為原料,采用適當的水熱處理條件制備粒徑適當、粒度分布均勻的二氧化錫納米粉體,并研究了不同的水熱溫度對二氧化錫粒子粒徑和晶型的影響及該法所制備的粉體的熱穩定性.
1 實驗部分
1.1 實驗藥品及儀器
所用藥品包括:五水結晶四氯化錫,分析純,350.6 g/mol,天津市科密歐化學試劑有限公司產品;硝酸銀,分析純,169.87 g/mol,天津市贏大稀貴化學試劑廠產品.
所用儀器包括:FA2004N型精密電子天平,上海箐海儀器有限公司產品;TD5A-WS型高速離心機,湘儀儀器有限公司產品;WO-5L型智能數顯恒溫油水浴鍋,天津科諾儀器設備有限公司產品;KSW-6-12型馬弗爐,北京市永光明醫療儀器廠產品;NICOLET 6700 FT-IR型傅里葉紅外光譜儀,TA Thermo-fisher公司產品;S-4800型場發射掃描電子顯微鏡,日本日立儀器有限公司產品;Zetasizer nano ZS90型納米粒徑電位分析儀,英國馬爾文儀器有限公司產品;Dmax2500型X射線衍射儀,日本理學公司產品;SDT Q600型熱重(TG)分析儀,美國TA公司產品.
1.2 納米級粒子的制備
(1)回流:稱取17.53 g五水結晶四氯化錫溶于1 000 mL去離子水中,室溫下磁力攪拌30 min使其充分溶解.然后將該水溶液在95℃條件下攪拌回流2 h,待溶液自然降溫至室溫后離心分離得到沉淀,采用去離子水洗滌沉淀直至洗滌液中不能檢測出氯離子(硝酸銀滴定法).最后通過冷凍干燥機冷凍干燥24 h獲得干燥粉末.
(2)水熱處理:將所得粉體分為3份,其中1份作為對比樣品即不進行水熱處理(HTT);另外2份分別取部分樣品置入各自反應釜中,然后加入適量去離子水,將2份樣品分別在100℃和150℃下水熱處理24 h.
(3)焙燒:將未經水熱處理和經100℃、150℃水熱處理的樣品分別置于馬弗爐中,分別進行400℃和600℃高溫焙燒,持續5 h,以驗證本文區別于傳統水熱法所制備的二氧化錫粉體的熱穩定性.
1.3 性能表征
采用X射線衍射儀(XRD)表征粉體的晶體結構;采用熱重分析儀(TG)對所制備粉體的熱穩定性進行測定;采用傅里葉紅外光譜儀(FT-IR)對其進行相純度表征;采用納米粒徑電位分析儀測定粉體的粒徑及其分布范圍;采用場發射掃描電子顯微鏡(SEM)確定其表面形貌.
2 結果與討論
2.1 粒子物象及晶型表征
圖1所示為制得粉體的X射線衍射(XRD)譜圖.
由圖1可以看出,在2θ分別為26.6°(110晶面)、33.9°(101晶面)、51.8°(211晶面)出現了衍射峰,在水熱處理溫度大于100℃時在38°(200晶面)附近出現了另一個峰,經400和600℃焙燒后在62°(310晶面)以及65°(112晶面、301晶面)附近出現衍射峰,這些峰的峰位與JCPDS標準衍射圖(卡片號:41-1445)吻合,說明本試驗所制備的粉體為四方晶系金紅石型二氧化錫.

圖1 二氧化錫粒子XRD譜圖Fig.1 XRD patterns of SnO2particles
由圖1(a)可以看出,隨著水熱溫度的增加衍射峰逐漸趨于尖窄,表明粒子逐漸長大,結晶性越來越好.隨著溫度的升高,粒子內部發生接觸重結晶,由無定型向結晶型的轉變更為充分[10].
由圖1(b)和(c)可以看出:在100℃或150℃水熱處理后,與未經高溫焙燒的粒子的譜圖相比,經400℃或600℃焙燒后粒子的衍射峰位置并沒有發生變化,而且衍射峰更加尖窄.表明通過100℃和150℃水熱處理所制得的二氧化錫粒子具有較好的熱穩定性,且隨著焙燒溫度的升高粒子的結晶性越好.這可以解釋為水熱處理使得納米二氧化錫微晶中不規則排布的原子或離子趨于規則化、均一化,從而使得所制備的粒子具有較好的熱穩定性.而經400℃或600℃焙燒后在60°至70°之間又出現了晶面310、112及301[11-12],這是由于高溫焙燒的情況下晶粒出現生長,其生長方式有表面擴散和晶界位移,而在600℃后出現衍射峰裂分亦是由于高溫焙燒使得晶胞發生收縮或膨脹,從而晶面間距發生變化所致[13].
2.2 粉體熱穩定性表征
圖2所示為在100℃和150℃情況下,水熱法所制備二氧化錫的熱重曲線圖.
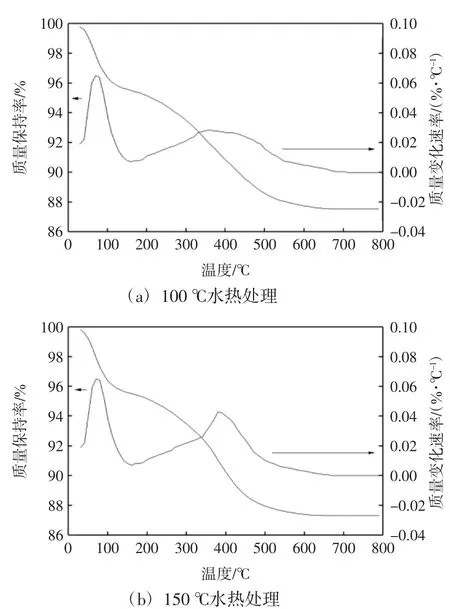
圖2 水熱法制備的二氧化錫納米粒子的熱重(TG)曲線Fig.2 TG plots of hydrothermally treated SnO2particles
由圖2可知,在100℃附近出現失重峰,這是由于樣品中物理吸附水的脫除引起的,對于100℃或者150℃水熱法所制得的二氧化錫納米粒子在這一點上基本一致.圖中失重過程一直持續到約450℃,這是由于樣品的結合水在這一過程中緩慢脫除,此后曲線趨于平滑[14].相較于圖2(a),圖2(b)中失重曲線稍早達到了恒重,這可能是由于采用150℃作為水熱溫度時粒子的結晶化程度較高,從而使得樣品中含有較少的結合水所致.
2.3 粉體相純度的表征
圖3所示為水熱法所制備的二氧化錫樣品以及在400℃和600℃焙燒時的傅里葉紅外光譜圖.
由圖3可知,位于3 430和1 630 cm-1處的吸收譜帶是由二氧化錫表面水所引起的;位于2 350 cm-1處的峰是空氣中少量CO2的吸收峰;而在850至1 350 cm-1之間出現的弱峰是二氧化錫表面不同類型的羥基造成的;在600 cm-1處的強峰則是Sn-O-Sn的對稱和非對稱振動引起的.
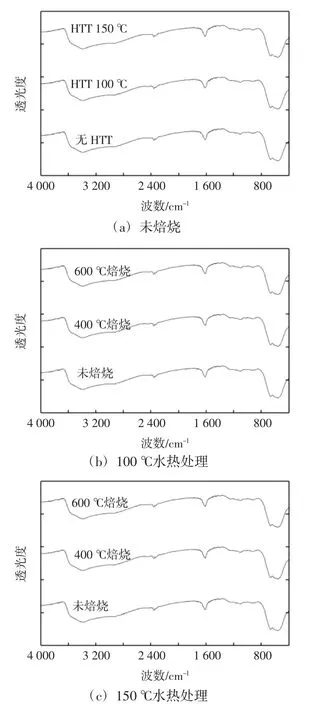
圖3 二氧化錫粒子紅外光譜譜圖Fig.3 FT-IR spectra of SnO2particles
圖3(a)為未進行水熱處理(HTT)、經100℃和150℃水熱處理(HTT)24 h樣品的傅里葉紅外光譜圖,可以看出,3份樣品各吸收峰位置高度一致,由此可知,回流及水熱處理過程中并未引入其他雜質,試驗制得的二氧化錫粉體相純度高.圖3(b)為經100℃水熱處理后未經焙燒和分別在400℃和600℃焙燒.圖3(c)為經150℃水熱處理后未經焙燒和分別在400℃和600℃焙燒,可以看出水熱法制備所得的二氧化錫粒子在400℃和600℃焙燒后依然保持較高的相純度.
2.4 納米級粒子的粒徑及其分布
圖4所示為100℃水熱法制得的二氧化錫粒子的粒徑分布圖.
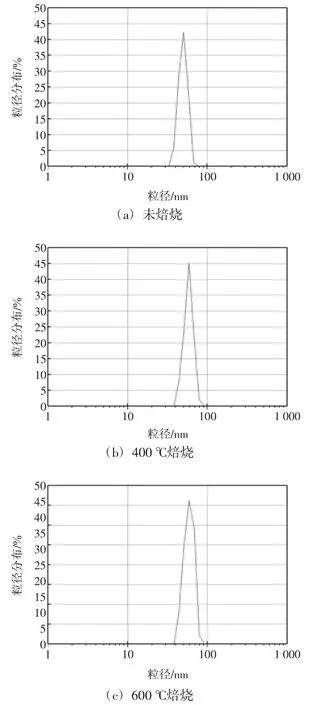
圖4 100℃水熱處理所制備二氧化錫粒子的粒徑分布圖Fig.4 Size distribution of SnO2particles hydrothermally treated at 100℃
由圖4可以看出,100℃水熱處理條件下所制得的二氧化錫粒子其粒徑基本處于40~60 nm之間,經過400℃和600℃焙燒后其粒徑范圍基本位于50~70 nm之間.這是由于高溫焙燒使得粒子出現了生長,這一結果正好與圖1所示XRD譜圖結果相吻合,但從圖中發現其粒徑增長幅度較小.
圖5所示為150℃水熱法制得的二氧化錫粒子的粒徑分布圖.
由圖5可以看出,在150℃水熱處理條件下所制得的二氧化錫粒子其粒徑也基本處于40~60 nm之間,經過400℃和600℃焙燒后其粒徑范圍基本位于50~70 nm之間,可以判斷采用100℃和150℃水熱處理所制備的納米級二氧化錫粒子其粒徑基本一致,而且高溫煅燒對其粒子粒徑的影響并不明顯.
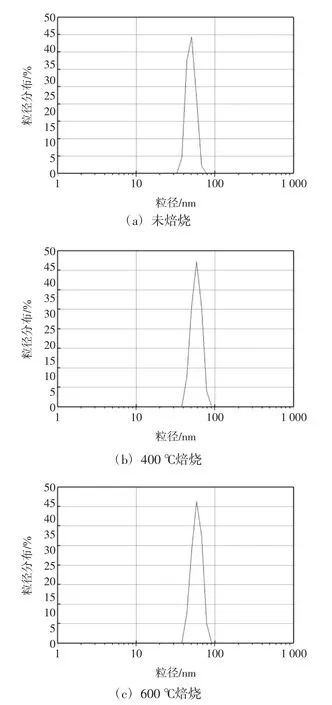
圖5 150℃水熱處理所制備二氧化錫粒子的粒徑分布圖Fig.5 Size distribution of SnO2particles hydrothermally treated at 150℃
2.5 粒子的微觀形貌表征
圖6所示為經100℃水熱處理后二氧化錫粒子的掃描電鏡圖.
由圖6可以看出,在水熱溫度為100℃時所制備的二氧化錫粒子粒徑均位于40~60 nm之間,且粒子粒徑分布較為均勻;隨著焙燒溫度的增加,粒子逐漸長大,結晶性越來越好,但是粒徑增長幅度并不大.
圖7所示為經150℃水熱處理后二氧化錫粒子的掃描電鏡圖.
綜合圖6與圖7可以看出,水熱法所制備的二氧化錫粒子粒徑均位于40~60 nm之間,且粒子粒徑分布較為均勻,但是仔細觀察還是能發現后者中粒子的表觀粒徑稍大于前者中粒子的粒徑,這一結果與圖1XRD譜圖相契合;隨著水熱處理溫度由100℃增至150℃衍射峰變尖窄,粒子在這一過程中出現生長,從而導致粒子粒徑有少許增加.而圖7(b)和圖7(c)亦再次驗證了圖5中所示粒徑分布圖的結果.

圖6 100℃水熱處理所制備二氧化錫粒子的掃描電鏡圖Fig.6 SEM images of SnO2particles hydrothermally treated at 100℃

圖7 150℃水熱處理所制備二氧化錫粒子的掃描電鏡圖Fig.7 SEM images of SnO2particles hydrothermally treated at 150℃
3 結論
區別于傳統水熱法,在制備過程中不加入任何沉降劑(硝酸或氨水等)和有機試劑,避免了在結晶洗滌過程中產生難以回收處理的酸液和有機廢液,實現了納米級二氧化錫的清潔制備.實驗結果表明:
(1)所制備的納米級二氧化錫粉體粒徑位于40~60 nm之間,粒度適中且分布均勻.
(2)在100℃或者150℃水熱處理溫度下,制得的納米級二氧化錫粉體具有較好的熱穩定性.在400℃和600℃條件下焙燒5 h,均對粒子的粒徑和形貌無較大影響,僅是粒子出現少許生長.
(3)水熱處理溫度從100℃增加至150℃,使得粒子具有更好的結晶性,粒子有少許生長,但均具有較好的熱穩定性.
[1]周存,鄭幗,程博聞.摻銻氧化錫納米粉體的表面改性[J].天津工業大學學報,2008,27(4):34-38.
[2]龐承新,張麗霞,譚健,等.溶膠-凝膠法制備納米二氧化錫的研究[J].廣西師范學院學報:自然科學版,2006,23(3):26-29,40.
[3]韓衛清,周剛,王連軍,等.陽極氧化制備二氧化錫納米孔[J].無機材料學報,2007,22(3):395-399.
[4]楊幼平,張平民,張永龍,等.水熱法制備超細均勻二氧化錫粉體[J].銅業工程,2004(4):23-25.
[5]敖偉琴,李均欽,楊華明.機械化學法合成二氧化錫納米晶[J].深圳大學學報:理工版,2007,24(1):24-28.
[6]王迪,田均慶,張書濤,等.溶膠凝膠法制備二氧化錫納米晶體[J].哈爾濱商業大學學報:自然科學版,2014,30(2):224-228.
[7]張曉順,邱竹賢,翟秀靜,等.超聲波-化學沉淀法制備納米二氧化錫[J].東北大學學報,2005,26(4):265-267.
[8]李超,魏偉,方少明,等.SnO2的電沉積法制備及電化學性能[J].鄭州輕工業學院學報:自然科學版,2008,23(5):1-4,20.
[9]劉冬,施哲,朱云.凝膠水熱法制備納米二氧化錫[J].云南冶金,2003,32(1):26-29.
[10]張義華,張景新,王學勤,等.二氧化錫納米粒子的制備及表征[J].大連理工大學學報,2000,40(1):64-66.
[11]于桂霞,祝洪良,姚奎鴻.二氧化錫(SnO2)納米顆粒的水熱合成及表征[J].浙江理工大學學報,2006,23(2):166-168.
[12]BILLIK P,CAPLOVICOVA M.Synthesis of nanocrystalline SnO2powder from SnCl4by mechanochemical processing[J]. Powder Technology,2009,191(3):235-239.
[13]CHETRI Pawan,CHOUDHURY Amarjyoti.Investigation of optical properties of SnO2nanoparticles[J].Physica E,2013(47):257-263.
[14]KRISHNAKUMAR T,JAYAPRAKASH R.Microwave-assisted synthesis and investigation of SnO2nanoparticles[J].Materials Letters,2009,63(11):896-898.
Pollution free preparation of SnO2nanoparticles
MA Jing-huan1,2,ZHAO Bao-jun1,WU Shao-bin1,LIU Ying1,2,KANG Xue-jing1,HU Dao-you1
(1.School of Environmental and Chemical Engineering,Tianjin Polytechnic University,Tianjin 300387,China;2.BIN HAN Eco-Technologies Co Ltd,Tianjin 300451,China)
Tin oxide nanoparticles were made from Stannic chloride pentahydrate by applying pollution free methods,in which precipitant and dispersant were not added firstly in comparing with the traditional routes for avoiding wastewater includes acid and organic substance which were hard to be reused during cleaning of the crystal.The crystal structure and characters of tin oxide nanoparticles were identified by X-ray diffraction(XRD)analysis,Thermal Gravity Analysis,Fourier transform infrared(FT-IR)spectroscopy,size instrument Zetasizer nano and scanning electronic microscope(SEM).The results show that the tin oxide nanoparticles have good crystallization,excellent thermal stability,high phase purity and uniform size distribution which is between 40-60 nm.
tin oxide nanoparticles;pollution free preparation;crystal structure
TQ134.3.2
A
1671-024X(2015)06-0041-05
10.3969/j.issn.1671-024x.2015.06.009
2015-09-25基金項目:天津市科技計劃項目(14ZCZDSF00013);國家自然科學基金資助項目(51308390)
馬敬環(1964—),女,博士,教授,博士生導師,主要研究方向為海水淡化與水資源綜合利用.E-mail:13920893096@163.com

