β-Bi2O3修飾Bi2WO6光催化降解苯酚及其可能機理
李曉金 盛珈怡 陳海航 許宜銘(浙江大學化學系,硅材料國家重點實驗室,杭州310027)
β-Bi2O3修飾Bi2WO6光催化降解苯酚及其可能機理
李曉金 盛珈怡 陳海航 許宜銘*
(浙江大學化學系,硅材料國家重點實驗室,杭州310027)
采用簡單混合法制備了一系列Bi2O3/Bi2WO6復合光催化劑.在紫外光降解水中苯酚的過程中,Bi2O3/ Bi2WO6的光催化活性隨Bi2O3含量的增加呈現先增大后減小的趨勢.當Bi2O3最佳負載量等于12.5%(質量分數,w)時,該復合光催化劑的活性大約是單一Bi2WO6的4倍.固體樣品表征表明,Bi2O3主要以β-Bi2O3存在,復合光催化劑是Bi2O3和Bi2WO6的簡單混合物.此外,在電催化氧化水的過程中,β-Bi2O3/Bi2WO6薄膜電極的光電流遠大于β-Bi2O3和Bi2WO6薄膜電極的光電流之和.Bi2O3對Bi2WO6光催化的促進作用是由于前者接受后者的光生空穴,提高Bi2WO6光生載流子的分離效率,從而加快了O2的還原和苯酚的降解.
氧化鉍;鎢酸鉍;光催化;電荷轉移;有機物降解
1 引言
半導體光催化降解有機物被認為是治理環境污染的重要方法之一.一直以來,TiO2因其高效、廉價和穩定等優點而被廣泛研究.1-3然而,TiO2的禁帶寬度較寬,只能吸收紫外光.為此,人們不斷尋求一種高效的可見光催化劑.例如,Bi2WO6是一種良好的可見光光催化活性,能吸收波長小于440 nm的太陽光,引發許多有機物的降解.4-7但是,Bi2WO6的光催化活性較低.這主要是由于光生載流子的分離效率低,并由于O2多電子還原較慢的緣故.6,8,9已有文獻報道,采用Bi2O3修飾Bi2WO6,能夠顯著提高光催化降解有機物的效率.10-16許多作者認為,這是因為Bi2O3向Bi2WO6導帶注入電子,Bi2WO6向Bi2O3價帶注入空穴,從而提高了光生載流子的分離效率.但是,這些報道沒有測定這二種半導體的電化學數據.再者,以有機染料為模擬分子,以β-Bi2O3/Bi2WO6與α-Bi2O3和Bi2WO6比較,也存在不當之處.眾所周知,有機染料既能通過半導體光催化降解,也能通過光敏化過程降解.17最近,Jiao等18報道,α-和β-Bi2O3都屬于n型半導體,它們在pH=0的水溶液中的平帶電位分別等于0.19和0.50 V(vs NHE(標準氫電極)).根據Bi2WO6的平帶電位(0.20 V(vs NHE)8),Bi2O3既可以向Bi2WO6導帶注入電子,也可以從Bi2WO6導帶得到電子.因此,Bi2O3對Bi2WO6光催化的影響及其機理還需要進一步佐證.
?Editorial office ofActa Physico-Chimica Sinica
本文采用簡單混合法,將商品Bi2O3與煅燒過的Bi2WO6混合,制備了一系列Bi2O3/Bi2WO6復合光催化劑.這種方法將不會改變Bi2O3和Bi2WO6的基本物理參數.再者,本文以無色的苯酚作為模擬分子避免了光敏化的影響.因此,實驗觀察到的Bi2O3影響一定歸結于它對Bi2WO6光催化過程的影響.催化劑采用X射線衍射(XRD)、N2吸附-脫附等溫線和紫外-可見(UV-Vis)漫反射等方法表征.此外,本文還通過電化學方法,研究了Bi2O3對Bi2WO6光電催化氧化H2O的影響,并提出了可能的反應機理.
2 實驗部分
2.1 試 劑
Na2WO4·2H2O購于國藥集團化學試劑有限公司,Bi(NO3)3·5H2O和Bi2O3購于阿拉丁試劑公司,苯酚購于上海化學試劑集團公司,HNO3購于浙江中星化學試劑有限公司,色譜純甲醇購于淮安市恒天工貿有限公司.除甲醇為外,其他試劑均為分析純.實驗用水為Mill-Q超純水.
Bi2WO6樣品通過水熱法進行合成.4,5將1.26 g Na2WO4·2H2O和3.64 g Bi(NO3)3·5H2O分別溶于40 mL H2O和0.4 mol·L-1HNO3.然后,將Na2WO4· 2H2O溶液逐滴加入到Bi(NO3)3·5H2O溶液中,生成白色的前驅體懸濁液.繼續攪拌30 min,超聲30 min.將該懸濁液轉移到150 mL聚氟乙烯管中,并加入H2O使反應液體積達到聚氟乙烯管容積的80%.在160°C下反應20 h以后,冷卻,過濾,水洗,烘干.最后,樣品在空氣氛圍和350°C下煅燒3 h.
Bi2O3/Bi2WO6樣品通過以下方法合成:適量Bi2WO6與40 mL H2O混合,分別攪拌和超聲30 min.然后,向該懸浮液加入所需比例的商品Bi2O3,再分別攪拌和超聲30 min.該混合液置于80°C烘箱中烘干,所得樣品再用瑪瑙研缽研磨.
2.2 主要儀器
X射線粉末衍射譜圖由D/max-2550/PC (Rigaku,日本)衍射儀測定,Cu Kα為X射線源,工作電壓為40 kV,工作電流為300 mA.根據最強衍射峰和Scherrer公式,計算晶粒尺寸.UV-Vis吸收光譜在Shimadzu UV-2550光度計上測定,以BaSO4為參比物,并采用文獻方法計算樣品的禁帶寬度.10氮氣吸附-脫附等溫線在ASAP2020(麥克,美國)分析儀上測定,溫度77 K.
2.3 光催化實驗和分析
光催化反應在Pyrex夾層反應器中進行,反應器內徑為2.9 cm,高為9.1 cm.實驗光源為300 W高壓汞燈(亞明,上海),其到達反應器的光強為3.2 mW·cm-2(光強計,北京師范大學制).通過循環水,維持反應器溫度為25°C.在50 mL反應液中,催化劑濃度為1.3 g·L-1,苯酚濃度為0.21 mmol·L-1.光照前,避光攪拌60 min.光照后,每隔一段時間,移取2.0 mL反應液,經0.22 μm濾膜過濾.通過Dionex P680高效液相色譜儀,定量分析濾液中有機物濃度.色譜柱為Apollo C18反相色譜柱,流動相為體積比為1:1的甲醇和水混合液,并含0.1%(體積分數)的乙酸.
2.4 電化學實驗
采用Doctor-Blade方法,制備以下三種薄膜電極:(1)將4.85 g Bi(NO3)3·5H2O溶于18 mL的2 mol· L-1硝酸溶液中,制備β-Bi2O3膠體.19加入1.92 g檸檬酸(CA)和1 g聚乙烯醇(PEG2000),攪拌6 h.然后,在導電玻璃上,制備β-Bi2O3薄膜.(2)將1 g Bi2WO6粉末與330 μL H2O混合,研磨均勻.加入1 mL含有0.5 g PEG20000的水溶液,繼續研磨.再在導電玻璃上制備Bi2WO6薄膜.最后,以上二種電極再經400°C煅燒3 h,去除有機物.(3)在β-Bi2O3膜上,滴加50 μL的1 g·L-1Bi2WO6懸浮液.80°C烘干,200°C煅燒20 min,最后制得β-Bi2O3/Bi2WO6薄膜電極.
電化學工作站為CHI660 E(上海辰華),Pt電極為對電極,飽和甘汞電極(SCE)為參比電極,0.5 mol· L-1NaClO4溶液為電解質溶液(pH=6.98),并以N2排除溶解O2.掃描速率為10 mV·s-1,光源為500 W高壓氙燈(暢拓,北京),波長大于320 nm,光強為10 mW·cm-2.通過E(vs NHE)=E(vs SCE)+0.24 V,本文電位數據均被換算成標準氫電極電位.
3 結果與討論
3.1 樣品表征
圖1(A)為固體樣品的XRD譜圖.本文合成得到的Bi2WO6在2θ=28.2°,32.8°,47.2°,55.9°,58.6°處出現衍射峰,這與正交晶型Bi2WO6的標準圖譜(PDF No.39-0256)一致.本文制得的Bi2O3薄膜在2θ= 28.0°,30.4°,31.7°,32.8°,46.3°,47.1°,54.2°,55.7°, 57.9°處出現衍射峰,這與β-Bi2O3的標準圖譜(PDF No.27-0050)一致(注:在2θ=35.2°處出現的衍射峰歸屬于ITO導電玻璃).商品Bi2O3主要在2θ=28.1°, 31.9°,32.8°,46.3°,47.0°,54.4°,55.6°,57.9°處出現衍射峰,對應于β-Bi2O3.此外,商品Bi2O3還在2θ= 27.0°,27.4°,33.4°處出現微弱的衍射峰,改組衍射峰與α-Bi2O3的標準圖譜(PDF No.65-2366)一致.根據XRD衍射峰的相對強度,可以判斷商品Bi2O3主要是β-Bi2O3.當商品Bi2O3與Bi2WO6混合以后,Bi2O3和Bi2WO6的特征峰衍射強度隨Bi2O3含量的增加而分別上升和下降.這是因為晶體的衍射峰強度一般與它在混合物中的含量呈正比.當Bi2O3含量為12.5% (w)時,在2θ=27.4°,30.4°處分別出現α-Bi2O3(120)和β-Bi2O3(211)晶面的特征峰.通過Scherrer公式計算, Bi2WO6晶粒的尺寸大約等于16 nm,且幾乎不受Bi2O3含量的影響(表1).此外,根據N2吸附-脫附等溫線,Bi2WO6的比表面積和孔體積都遠大于商品Bi2O3.但是,當Bi2O3含量較低時,Bi2O3/Bi2WO6的比表面積則明顯小于理論計算值.由于Bi2O3的比表面積只有0.32 m2·g-1,這可能說明Bi2WO6的表面或孔道被Bi2O3小顆粒占據,從而導致比表面下降.
圖1(B)為固體樣品的紫外-可見漫反射吸收光譜圖.在200到450 nm的范圍內,純Bi2WO6具有較強的吸收,其帶邊約為450 nm.該吸收帶歸結于O 2p和Bi 6s雜化軌道到W 5d軌道躍遷.7商品Bi2O3為深黃色粉末,比Bi2WO6具有更寬的吸收區域,能吸收波長小于580 nm的可見光.通過微分計算法, Bi2WO6和Bi2O3的禁帶寬度分別等于2.87和2.51 eV.前者與文獻10-14報道基本一致,后者則分別大于和接近α-Bi2O3(2.6-2.8 eV)和β-Bi2O3(2.48 eV)的禁帶寬度).12,13,18光譜分析進一步表明:商品Bi2O3主要是β-Bi2O3.當Bi2WO6與Bi2O3混合以后,吸收光譜隨Bi2O3含量的增加而逐漸紅移.顯然,這是由于混合物中Bi2O3的吸收特征造成的.以上固體分析表明, Bi2O3/Bi2WO6是Bi2O3和Bi2WO6的簡單混合物,本文所用溫和制備方法沒有顯著改變它們的晶粒大小、比表面積和光吸收等基本物理參數.

圖1 樣品的XRD(A)和UV-Vis漫反射光譜圖(B)Fig.1 X-ray diffraction(XRD)patterns(A)and UV-Vis diffuse reflection spectra(B)of the samples

表1 固體樣品的物理參數Table 1 Physical parameters of solid samples
3.2 苯酚的光催化降解
在可見光作用下(波長大于400 nm),Bi2WO6能夠引發水溶液中無色苯酚的氧化或降解,但反應較慢.8為了研究的方便,圖2(A)表示在波長大于320 nm的光作用下,苯酚在水溶液中的濃度隨反應時間的變化關系.可以看出,Bi2O3/Bi2WO6的活性明顯高于Bi2WO6.對照實驗表明,苯酚不僅難以吸附在催化劑表面(<5%),而且自身光解很慢.因此,觀察到的苯酚濃度下降一定是由于半導體光催化反應引起的.再者,苯酚的濃度與時間的變化曲線滿足一級動力學過程.由于光強和催化劑濃度保持恒定,這表明Bi2WO6和Bi2O3/Bi2WO6不僅能夠光催化還原O2,而且也具有較高的穩定性.11,14圖2(B)表示經一級動力學方程擬合后的苯酚氧化表觀速率常數.隨著Bi2O3含量的增加,Bi2O3/Bi2WO6的光催化活性呈現先增加后下降的趨勢.前者表明,Bi2O3對Bi2WO6光催化降解苯酚確實具有促進作用.后者可能歸結于Bi2WO6主體光催化劑的濃度下降.當Bi2O3的最佳混合比等于12.5%時,Bi2O3/Bi2WO6的光催化活性大約是Bi2WO6的4倍.由于這些混合光催化劑具有不同的比表面積(Asp,表1),我們又以Asp歸一化苯酚降解的表觀速率常數(kobs),結果列于圖2(B).可以看到,kobs/Asp隨Bi2O3濃度的變化趨勢與kobs幾乎一致.也就是說,Bi2O3/Bi2WO6光催化活性的提高并不是比表面積變化造成的.9,20,21
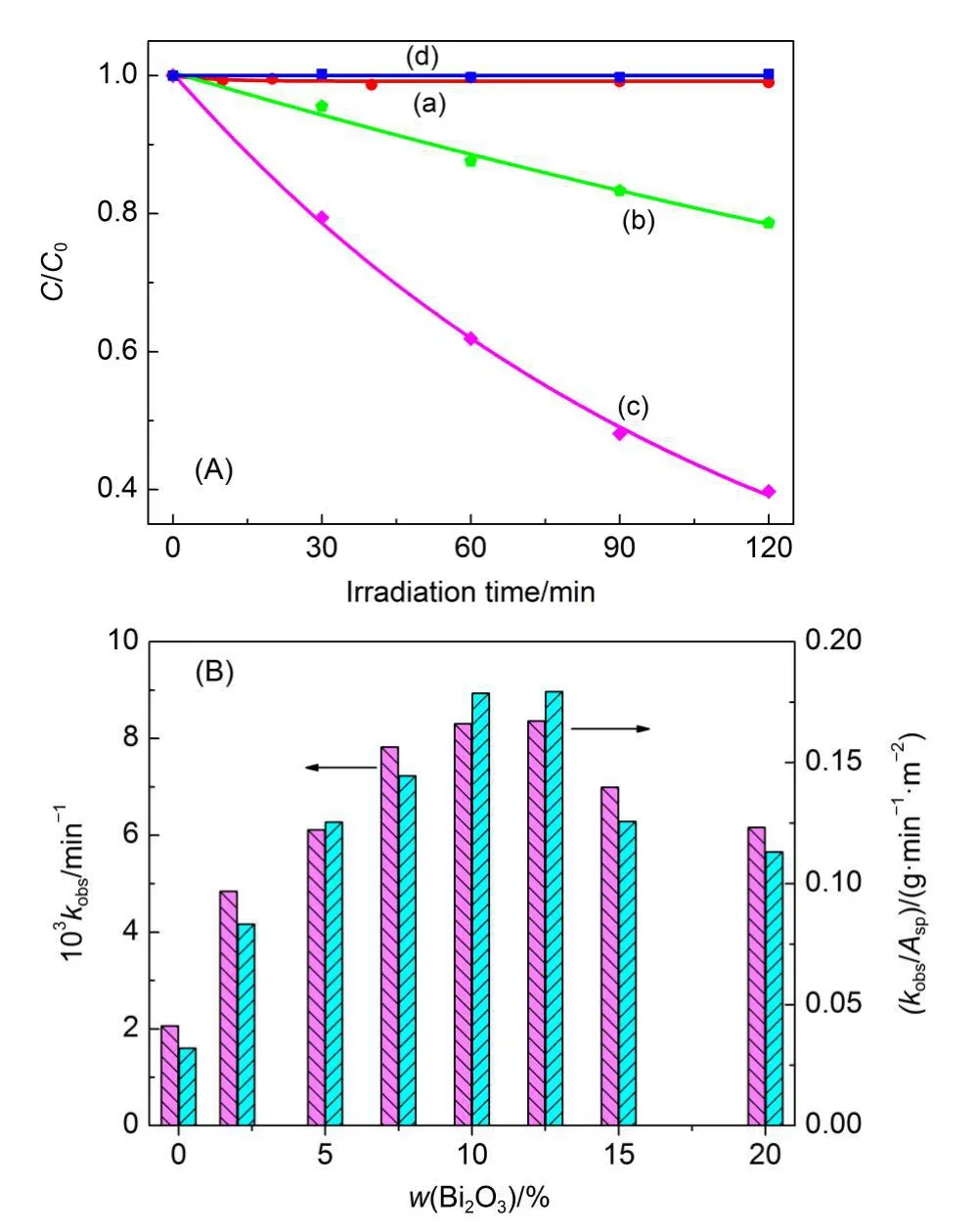
圖2 (A)紫外光光照下苯酚的降解曲線;(B)苯酚降解的表觀速率常數(kobs)和歸一化速率常數(kobs/Asp)Fig.2(A)Time profiles of phenol degradation under UV light;(B)apparent rate constant(kobs)and normalized rate constants(kobs/Asp)of phenol degradation

圖3 在N2下測定電極的暗態(虛線)和光照(實線)線性掃描伏安曲線Fig.3 Linear sweep voltammetry curves of electrodes obtained in the dark(dot line)and UV light (solid line)under N2atmosphere
3.3 光電化學實驗
為了排除有機物在催化劑表面的弱吸附可能帶來的影響,我們采用光電化學方法,直接測定光生空穴氧化H2O而產生的光電流.因商品Bi2O3主要是β-Bi2O3,我們單獨制備了β-Bi2O3薄膜電極,再表面沉積Bi2WO6而得到β-Bi2O3/Bi2WO6薄膜電極.圖3表示在除氧的NaClO4電解質溶液中,β-Bi2O3、Bi2WO6和β-Bi2O3/Bi2WO6薄膜電極的線性掃描伏安曲線.在暗態條件下,這些電極產生的電流很小,并且隨外加電壓(0.2-1.2 V(vs NHE))的變化不很明顯.這是因為外加電壓小于O2/H2O電對的標準電極電勢(1.23 V (vs NHE))與O2析出過電位之和.但是,在波長大于320 nm的紫外光照射下,三種薄膜電極均能產生光電電流.在相同的偏壓條件下,光電流的大小順序為β-Bi2O3/Bi2WO6>β-Bi2O3>>Bi2WO6.由于體系不含有機物,觀察到的光電流一定來源于水氧化.該實驗證實,β-Bi2O3與Bi2WO6之間確實存在相互作用.在pH 0的水溶液中,Bi2WO6和β-Bi2O3電極的平帶電位分別等于0.25和0.51 V(vs NHE).8,18對于n型半導體,導帶邊的電位與平帶電位數值相近.8,22-25根據禁帶寬度的數據,計算出Bi2WO6和β-Bi2O3的價帶電位分別等于3.12和3.02 V(vs NHE).從熱力學上來看,它們的價帶空穴都能氧化水,從而產生光電流.由于Bi2WO6的價帶電位比β-Bi2O3正0.10 V,它的價帶空穴可以轉移到β-Bi2O3,10,12-16從而提高光生載流子的分離效率,進一步加快O2的還原和H2O或苯酚的氧化.另一方面,Bi2WO6的導帶邊電位比β-Bi2O3負0.26 V,它的導帶電子也有可能轉移到β-Bi2O3.但是,Bi2WO6和β-Bi2O3的導帶邊電位差較大,不利于它們的前線軌道發生重疊.因此,相比于空穴轉移,這種電子轉移較慢或不易發生.再者,如果同時發生空穴和電子轉移,則相當于Bi2WO6受光激發而產生的一對空穴和電子又在β-Bi2O3表面重新復合,這應該導致Bi2WO6的光催化活性下降.顯然,這與事實不符.苯酚和水被氧化的實驗均表明,Bi2O3對Bi2WO6光催化反應確實具有促進作用.因此,我們認為,這種促進作用是由于Bi2O3接受Bi2WO6的光生空穴,從而降低了與光生電子之間的復合,同時提高了光生空穴和電子的利用率(示意圖1).

示意圖1 Bi2O3/Bi2WO6光催化活性提高的可能機理Scheme 1 Possible mechanism of the enhanced photocatalytic activity of Bi2O3/Bi2WO6
4 結論
利用苯酚作為降解底物,考查了Bi2O3修飾對Bi2WO6光催化活性的影響.Bi2WO6的光催化活性隨著Bi2O3修飾量的增加而呈現先上升后下降的趨勢, Bi2O3的最佳修飾量為12.5%(w).通過光電化學實驗,證明Bi2WO6的光生空穴可以轉移至Bi2O3,從而抑制了Bi2WO6光生載流子的復合.該復合光催化劑制備簡單,或許對于有機廢水的處理具有一定的應用價值.
(1)Hoffmann,M.R.;Martin,S.T.;Choi,W.Y.;Bahnemann,D.W. Chem.Rev.1995,95,69.doi:10.1021/cr00033a004
(2)Carp,O.;Huisman,C.L.;Reller,A.Prog.Solid State Chem.2004,32,33.doi:10.1016/j.progsolidstchem.2004.08.001
(3)Tachikawa,T.;Fujitsuka,M.;Majima,T.J.Phys.Chem.C2007,111,5259.
(4)Amano,F.;Nogami,K.;Abe,R.;Ohtani,B.J.Phys.Chem.C2008,112,9320.doi:10.1021/jp801861r
(5)Zhang,L.S.;Wang,W.Z.;Chen,Z.G.;Zhou,L.;Xu,H.L.; Zhu,W.J.Mater.Chem.2007,17,2526.doi:10.1039/b616460a
(6)Sun,S.M.;Wang,W.Z.;Zhang,L.J.Phys.Chem.C2012,116, 19413.doi:10.1021/jp306332x
(7)Fu,H.B.;Pan,C.S.;Yao,W.Q.;Zhu,Y.F.J.Phys.Chem.B2005,109,22432.doi:10.1021/jp052995j
(8)Sheng,J.Y.;Li,X.J.;Xu,Y.M.ACS Catal.2014,4,732.doi: 10.1021/cs400927w
(9)Sheng,J.Y.;Li,X.J.;Xu,Y.M.Acta Phys.-Chim.Sin.2014,30,508.[盛珈怡,李曉金,許宜銘.物理化學學報,2014,30, 508.]doi:10.3866/PKU.WHXB201312302
(10)Ge,M.;Li,Y.F.;Liu,L.;Zhou,Z.;Chen,W.J.Phys.Chem.C2011,115,5220.doi:10.1021/jp108414e
(11)Gui,M.S.;Zhang,W.D.J.Phys Chem.Solids2012,73, 1342.doi:10.1016/j.jpcs.2012.06.009
(12)Li,X.N.;Huang,R.K.;Hu,Y.H.;Chen,Y.J.;Liu,W.J.;Yuan, R.S.;Li,Z.H.Inorg.Chem.2012,51,6245.doi:10.1021/ ic300454q
(13)Wang,H.L.;Li,S.J.;Zhang,L.S.;Chen,Z.G.;Hu,J.Q.;Zou, R.J.;Xu,K.B.;Song,G.S.;Zhao,H.H.;Yang,J.M.;Liu,J.S. CrystEngComm2013,15,9011.doi:10.1039/c3ce41447g
(14)Li,Z.Q.;Chen,X.T.;Xue,Z.L.J.Colloid Interface Sci.2013,394,69.doi:10.1016/j.jcis.2012.12.002
(15)Gui,M.S.;Zhang,W.D.;Su,Q.X.;Chen,C.H.J.Solid State Chem.2011,184,1977.doi:10.1016/j.jssc.2011.05.057
(16)Gui,M.S.;Zhang,W.D.Nanotechnology2011,22,265601. doi:10.1088/0957-4484/22/26/265601
(17)Saison,T.;Chemin,N.;Chaneac,C.;Durupthy,O.;Ruaux,V.; Mariey,L.;Mauge,F.;Beaunier,P.;Jolivet,J.P.J.Phys.Chem. C2011,115,5657.doi:10.1021/jp109134z
(18)Hou,J.G.;Yang,C.;Wang,Z.;Zhou,W.;Jiao,S.Q.;Zhu,H. M.Appl.Catal.B2013,142-143,504.
(19)Timonah,N.S.;Yang,C.H.;Yu,Y.;Niu,Y.H.;Sun,L.Curr. Appl.Phys.2010,10,1372.doi:10.1016/j.cap.2010.04.006
(20)Sun,Q.;Xu,Y.M.J.Phys.Chem.C2010,114,18911.doi: 10.1021/jp104762h
(21)Cong,S.;Xu,Y.M.J.Phys.Chem.C2011,115,21161.doi: 10.1021/jp2055206
(22)Chen,H.H.;Leng,W.H.;Xu,Y.M.J.Phys.Chem.C2014,118,9982.doi:10.1021/jp502616h
(23)Leng,W.H.;Zhang,Z.;Zhang,J.Q.;Cao,C,N.J.Phys.Chem. B2005,109,15008.doi:10.1021/jp051821z
(24)Cheng,X.F.;Leng,W.H.;Liu,D.P.;Xu,Y.M.;Zhang,J.Q.; Cao,C.N.J.Phys.Chem.C2008,112,8725.doi:10.1021/ jp7097476
(25)Fei,H.;Leng,W.H.;Li,X.;Cheng,X.F.;Xu,Y.M.;Zhang,J. Q.;Cao,C.N.Environ.Sci.Technol.2011,45,4532.doi: 10.1021/es200574h
Improved Photocatalytic Degradation of Phenol over β-Bi2O3Modified Bi2WO6and Possible Mechanism
LI Xiao-Jin SHENG Jia-Yi CHEN Hai-Hang XU Yi-Ming*
(State Key Laboaratory of Silicon,Departement of Chemistry,Zhejiang University,Hangzhou 310027,P.R.China)
In this study,a series of Bi2O3-containing Bi2WO6catalysts were prepared by a simple mixing method.We used the oxidation of phenol in water under UV light as a model reaction,and found that as the amount of Bi2O3in the mixture increased,its photocatalytic activity increased,and then started to decrease.A maximum activity was observed with the catalyst containing 12.5%(mass fraction,w)of Bi2O3,about 4 times that of Bi2WO6.Solid characterization revealed that the composite was a mixture of β-Bi2O3and Bi2WO6.The water oxidation photocurrent over the β-Bi2O3/Bi2WO6thin film electrode was much larger than the sum of the photocurrents of the β-Bi2O3and Bi2WO6thin film electrodes.It is proposed that there is a valence hole transfer from Bi2WO6to β-Bi2O3,which improves the charge separation efficiency,and consequently increases the rate of phenol degradation.
Bismuth oxide;Bismuth tungstate;Photocatalysis;Charge transfer; Organic degradation
O643
10.3866/PKU.WHXB201501131www.whxb.pku.edu.cn
Received:October 30,2014;Revised:January 12,2015;Published on Web:January 13,2015.
?Corresponding author.Email:xuym@zju.edu.cn;Tel:+86-571-87952410.
The project was supported by the National Natural Science Foundation of China(21377110)and National Key Basic Research Program of China (973)(2011CB936003).
國家自然科學基金(21377110)和國家重點基礎研究發展規劃項目(973)(2011CB936003)資助

