化工熱力學在化工工藝課程設計中的應用
王菊 吳現力 杜春華

摘要:化工熱力學是化學工程的重要組成部分。如何使學生真正理解和掌握化工熱力學模型在解決化工過程實際問題中的應用一直是化工熱力學教學過程中的難題。將化工熱力學的教學與后續的化工工藝課程設計結合起來,通過課程設計的訓練強化熱力學模型的應用,使學生真正體會到化工熱力學對解決工程問題的指導意義。
關鍵詞:化工熱力學;化工工藝課程設計;模型應用
中圖分類號:G424.1 ? ? 文獻標志碼:A ? ? 文章編號:1674-9324(2016)08-0203-02
化工熱力學是化學工程學的一個重要分支,是化學工程與工藝專業必修的專業課程。化工熱力學上接物理化學中的熱力學部分,下連化工工藝學、分離工程、反應工程、化工設計等課程,是化工過程研究、開發與設計的理論基礎,是一門理論性與應用性均較強的課程,其重要性不言而喻。然而,化工熱力學理論概念嚴謹、抽象,涉及到的公式紛繁復雜,學生很容易“淹沒”在煩瑣的公式推導及計算過程中,不能真正理解化工熱力學對解決工程問題的重要性。
化工工藝課程設計是化學工程與工藝專業本科生在修完化工工藝學后進行的一次綜合設計訓練,是培養學生獨立完成某一化工產品設計的基本技能,分析和解決實際問題能力的重要教學環節[1]。
將化工熱力學的相關知識綜合應用到化工工藝課程設計中,不僅能讓學生真正理解和掌握熱力學研究和處理問題的基本方法,還能培養學生運用所學知識解決實際問題的能力,培養學生的工程意識,提高設計質量。筆者認為在化工工藝課程設計中可強化以下幾方面的應用。
一、流體的p-V-T關系
流體的p-V-T關系是化工熱力學的基石,利用流體的p-V-T數據和基本關系式可計算不能直接從實驗測得的其他性質,如焓、內能、熵、自由焓等。此外,流體的p-V-T關系可直接用于設計。
1.利用流體的p-V-T關系計算物料密度。在化工工藝課程設計中經常涉及到管道直徑的選取和間歇反應釜體積的估算,這些計算都需要所處理物料的密度。對于常規物質,如水、空氣、氨和氟利昂等的p-V-T數據可直接通過查手冊獲得。對于不常見的物質以及高溫高壓下的體系,數據的查找就比較困難了。而熱力學提供了多種計算流體的p-V-T關系的方法,如狀態方程和普遍化關系式。
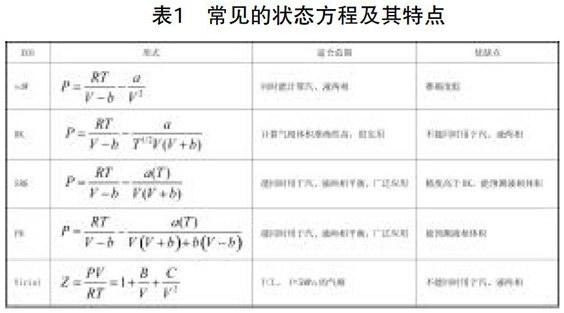
利用狀態方程可精確地代表相當廣范圍內的p-V-T數據。每一個狀態方程都有它的特點和應用范圍。在進行設計時,要根據處理物系的特點,如溫度、壓力、極性等以及所要求的計算精度選擇適合的方程進行計算。常見的狀態方程及其特點見表1。
若計算氣體體積,SRK和PR是大多數流體的首選。無論壓力、溫度、極性如何,它們能基本滿足精度要求,在工業上已廣泛使用。在沒有計算軟件又需要快速估算的情況下,可以使用普遍化方程。
若只是計算液體體積,直接用修正的Rackett方程既簡單精度又高,不需要用立方型狀態方程來計算。
在化工生產中,更常見的物系是多組分的混合物。在處理混合物時要根據采用的計算方法選用適當的混合規則。
2.利用流體的p-V-T關系計算焓、熵。熱量衡算是化工設計中極其重要的組成部分。通過熱量衡算可以確定過程中需要供給或移走的熱量,從而為換熱器的設計提供依據,同時也為反應器、結晶器、塔式設備、分離設備及各種控制儀表提供參數,并確定單位產品的能耗指標等[2]。焓是熱量衡算的關鍵數據,熵主要用于衡量過程的能量有效利用率。利用流體的p-V-T數據,結合理想氣體的熱容模型CPig,可通過熱力學基本關系式計算焓和熵。
焓的基本關系式:dH=C dT+V-T ?搖 dp
熵的基本關系式:dS=C ?- ?dP
理想氣體的熱容:C ?=a+bT+cT +dT
a、b、c、d為物性常數,可通過查手冊獲得。理想氣體的CPig-T關聯式,可用于低壓下的真實氣體,不能用于壓力較高的真實氣體。
計算真實氣體的焓變和熵變需要引入剩余性質HR和SR,如下圖所示。
ΔH=-H ?+ΔH +H ?=-H ?+ ? (T -T )+H
ΔS=-S ?+ΔS +S ?=-S ?+ ? ln -Rln +S
其中: = ?搖 ? =
剩余性質可用狀態方程進行計算,也可根據Tr、Pr和ω用普遍化關系式進行估算。學生在完成課程設計時,考慮到課程設計時間緊、任務重,可用普遍化關系式估算。
二、相平衡
在所有化工熱力學的研究內容中,相平衡占有無法比擬的重要地位。從某種意義上來說,在化工熱力學的研究內容中,對“能量”和“組成”的研究是最為重要的部分,而所謂對于“組成”的研究,實質上就是指相平衡和化學平衡,尤以相平衡占有更重要的地位[3]。
相平衡包括很多具體的類型,僅常見的兩相平衡就有汽液平衡、氣液平衡、液液平衡和固液平衡。這些相平衡理論是化工生產中廣泛采用的分離技術,如精餾、吸收、萃取、結晶等的理論和設計基礎[4]。由于相平衡計算量較大,學生不可能通過手算完成。在教學中僅僅要求學生能夠定性選擇適用的方法。因此在課程結束以后,學生對于相平衡計算模型的印象不深,而且不可能全部理解。化工工藝課程設計是一個很好的利用相平衡模型進行應用計算的機會。以下以汽液平衡為例,介紹其在化工工藝課程設計中的應用。
汽液平衡是精餾過程分析和設計計算的重要依據。在化工工藝課程設計中經常涉及到精餾塔的設計計算,如二甲醚生產工藝設計中甲醇回收塔的設計計算。
對常壓下操作的精餾塔,汽相可視為理想氣體。甲醇—水體系液相為非理想溶液。汽液平衡關系式為:py =γ x ?p
在設計中可引導學生利用Wilson方程計算液相的活度系數,再利用操作壓力和液相組成計算出相應的泡點溫度和汽相組成,從而得出常壓下甲醇—水體系的汽液平衡數據。根據汽液平衡數據繪出常壓下的x-y圖,為圖解法計算理論塔板數提供依據。計算中需試差求解,可利用MathCAD[5]或Matlab[6]進行計算。
上述計算屬于汽液平衡計算中已知體系的壓力p與液相組成xi,求泡點溫度T和汽相組成yi這一類型。在確定塔溫時,可對汽液平衡計算進行反復練習,如根據操作壓力和塔頂產品組成(塔頂采用全凝器)確定塔頂溫度,屬于已知體系的壓力p與汽相組成yi,求露點溫度T和液相組成xi這一類型。
又如二甲醚生產工藝設計中二甲醚精餾塔操作壓力的計算。二甲醚在常壓下的沸點是-24.9℃,如果想用普通冷卻水冷凝塔頂產品,需要加壓操作。先將塔頂溫度設為45℃,根據塔頂溫度和塔頂產品組成確定操作壓力,屬于已知體系的溫度T與汽相組成yi,求露點壓力p和液相組成xi這一類型。二甲醚精餾塔涉及二甲醚、水、甲醇三個組分,三組分為互溶體系,可用Wilson方程計算活度系數。由于是加壓操作,需要對汽相進行校正,可用SRK或PR方程計算逸度系數。
通過以上訓練,學生對汽液平衡計算的類型以及計算中涉及到的逸度和活度系數模型都有了深刻認識。
化工熱力學是化工專業重要的專業基礎課程之一。化工熱力學給出的原理和方法在化工從業人員的整個職業生涯中,發揮了重要的指導作用,是深入理解化工過程實質的關鍵。化工熱力學知識的教學是一個系統工程,僅通過一門課程的講解是難以取得良好效果的。將化工熱力學的相關知識應用于化工工藝課程設計中,為學生提供了一個很好的訓練機會,幫助他們掌握了熱力學重要模型的應用。
參考文獻:
[1]朱佳媚,周敏,孟獻梁,程相林,王月倫.提高《化工工藝學》課程設計教學質量的探討[J].化工時刊,2013,27(1):47-49.
[2]陳聲宗.化工設計[M].第1版.化學工業出版社,2001.
[3]陳明鳴,馬沛生,夏淑倩,常賀英,李永紅.相平衡——本科生化工熱力學課程的核心內容[J].化學工業與工程,2005,22(11):17-19.
[4]陳鐘秀,顧飛燕,胡望明.化工熱力學[M].第3版.化學工業出版社,2011.
[5]吳選軍.MathCAD在相平衡計算中的應用[J].化工高等教育,2009,(1):50-54.
[6]李克娥,蘇鐵軍.Matlab在處理化工熱力學數據中的應用[J].重慶科技學院學報(自然科學版),2005,7(3):100-102.

