鹽度驟降對云紋石斑魚肝臟代謝酶活力的影響
施兆鴻,廖雅麗,王孝杉,高權新,彭士明,張晨捷
(1.上海海洋大學水產與生命學院,上海 201306;2.中國水產科學研究院東海水產研究所,上海 200090)
鹽度驟降對云紋石斑魚肝臟代謝酶活力的影響
施兆鴻1,2,廖雅麗1,2,王孝杉2,高權新2,彭士明2,張晨捷2
(1.上海海洋大學水產與生命學院,上海 201306;2.中國水產科學研究院東海水產研究所,上海 200090)
為探討云紋石斑魚(Epinephelus moara)肝臟代謝酶活力對鹽度驟降的響應,設置27(對照組)、21、15、9共4個鹽度梯度對云紋石斑魚進行鹽度驟降脅迫實驗。分別在0、1、2、3、7 d時取樣,測定其肝臟中酸性磷酸酶(ACP)、堿性磷酸酶(AKP)、谷丙轉氨酶(GPT)、谷草轉氨酶(GOT)以及乳酸脫氫酶(LDH)活力。結果顯示,ACP活力鹽度21組先波動變化后恢復正常水平,鹽度15組先下降后升高,隨后第7天下降恢復正常水平;AKP活力鹽度21組和鹽度15組先呈下降趨勢,第3天大幅度升高;GPT與LDH活力鹽度21組和鹽度15組基本呈現先下降再上升并波動的變化趨勢;GOT活力變化趨勢鹽度21組先升后降,鹽度15組先降后波動。研究表明:在鹽度27驟降至21或15,均會使云紋石斑魚產生應激反應,磷酸酶、轉氨酶與乳酸脫氫酶活力初期均會受到抑制,隨時間延長可以得到恢復;而當鹽度從27驟降至9,3 d時實驗魚全部死亡。
云紋石斑魚;驟降低鹽脅迫;肝臟代謝酶
云紋石斑魚(Epinephelus moara)俗稱真油斑,屬鱸形目(Perciformes),鮨科(Serranidae),石斑魚屬。具有肉味鮮美、生長快、環境適應性強、經濟價值高等特點[1-2],是我國東南沿海地區重要養殖對象[3]。鹽度作為水產養殖中重要的環境因子,直接影響水生生物的生長與存活。目前國內外關于云紋石斑魚的研究主要有淋巴囊腫病、育苗技術、攝食生長、形態發育等[4-7],而鹽度脅迫方面的研究報道主要集中在形態學方面,如鹽度對其胚胎發育、仔魚活力、早期幼魚生長和存活的影響等[8-9]。
酸性磷酸酶(acid phosphatase,ACP)和堿性磷酸酶(akaline phosphatase,AKP)是衡量機體免疫機能和健康狀況的重要指標[10]。水生生物機體部分新陳代謝由物質的磷酸化和去磷酸化進行調節,這些過程主要依靠不同磷酸酶催化完成[11]。轉氨酶存在于血漿及多種身體組織中,但最常見與肝臟有關。轉氨酶的種類很多,以谷丙轉氨酶(alanine aminotransferase,GPT)和谷草轉氨酶(aspartate transaminase,GOT)最為重要,是氨基酸代謝過程中兩個重要的氨基轉移酶,可以作為評價攝食水平、生長發育和肝功能測試的指標[12]。乳酸脫氫酶(lactate dehydrogenase,LDH)是糖酵解途徑與檸檬酸循環之間的關鍵酶,能催化丙酮酸與乳酸之間的相互轉化,并提供能量[13],其活力大小在一定程度上反映了無氧代謝能力的高低。VIJAYAVEL等[14]對鋸緣青蟹(Scylla serrata)的研究認為,抑制乳酸脫氫酶活力能夠導致呼吸下降,并影響機體氧化磷酸化作用,進而影響生物體能量供給和生理活動的進行。因此,ACP、AKP、GPT、GOT及LDH 5種酶在研究魚類受鹽度脅迫下組織功能及生理變化具有重要的意義,酶活性變化趨勢可以間接的反映體內生理動態變化及組織損傷情況[15]。本實驗首次研究了從鹽度27驟降至9、15和21(7 d)對云紋石斑魚肝臟中代謝酶(ACP、AKP、GPT、GOT、LDH)的影響,旨在明確其對鹽度變化脅迫的響應,以期為養殖環境因子調控提供參考。
1 材料與方法
1 實驗用魚和條件
實驗于2014年9月在上海水產研究所啟東養殖基地進行。云紋石斑魚幼魚由黃海水產研究所提供,平均體長(10.43±1.08)cm,平均體質量(16.73±4.47)g。魚運抵養殖基地后先在水溫(27±1.0)℃、鹽度27的環境中暫養14 d。暫養密度20 ind·m-3,每天8∶00和17∶00各飽食投喂由日本林兼株式會社生產的“魚寶”牌6#(粒徑大小:1.1~1.3 mm)配合飼料,不間斷充氣,每天換同鹽同溫水25%,同時吸去底部污物及殘餌。實驗用水為沉淀過濾處理后的天然海水。
1.2 實驗設計
實驗在直徑1.0 m、深度0.8 m的圓形玻璃鋼桶中進行。鹽度梯度設為27、21、15、9,以暫養海水鹽度27為對照組,低鹽度海水(鹽度21、15、9)用曝氣后自來水兌天然海水配置,實驗用水配制穩定48 h后使用。每個鹽度梯度設3個平行,共12個桶。實驗開始時,用手操網隨機從暫養群體中撈取個體直接放入各鹽度組(含對照組)水體中,每個平行20 ind。實驗期間的投喂和管理與暫養期間相同,每天觀察魚的活動狀況,及時撈出死魚,統計死亡情況。從實驗魚放入各鹽度組水體作為起始0 h并開始計時,在1、2、3、7 d各鹽度梯度組中分別取樣,每平行每次取3 ind。
1.3 取樣和指標測定
取樣前停喂飼料1次,用MS222(200 mg· L-1)將魚麻醉后,將魚置于冰盤上解剖,取出肝臟,用預冷生理鹽水沖洗,并用吸水紙吸干,置于1.5 mL離心管中-20℃保存,在30 d內檢測ACP、AKP、GPT、GOT及LDH活力。測定前,先將肝臟在勻漿介質(pH 7.4,0.01 mol·L-1Tris-HCl,0.000 1 mol·L-1EDTA-2Na,0.01 mol· L-1蔗糖,0.8%NaCl)中剪碎,用勻漿機15 000 r·min-1研磨制成勻漿。用低溫離心機4℃下1 500 r·min-1離心5 min。根據需要,取上清液稀釋后進行酶活力及總蛋白測定。
總蛋白采用考馬斯亮蘭法(南京建成試劑盒)進行測定。酶活力均采用南京建成試劑盒檢測,按照說明書進行操作。其中,ACP活力和AKP活力測定采用磷酸苯二鈉法,活力單位定義為每克組織蛋白在37℃與基質作用30 min和15 min,產生1 mg酚者為1個活力單位。GOT和GPT兩種酶活力測定采用King氏法,活力單位定義為生成產物1 min內使NADH氧化成NAD+而引起吸光度每下降0.001為1個活力單位。LDH活力測定采用比色法測定,活力單位定義25℃條件下,每分鐘催化1μmol的丙酮酸轉化為乳酸的酶量為1個活力單位。
1.4 數據統計與分析
實驗數據用SPSS 19.0軟件進行統計與分析。運用單因素方差分析,先進行方差齊性檢驗,不滿足方差齊性時,對數據進行自然對數或平方根轉換,然后采用Duncan’s檢驗進行多重比較,P<0.05為有顯著性差異,數據以平均值±標準差(Mean±SD)表示。用Excel 2007繪制圖表。
2 結果與分析
2.1 不同鹽度下云紋石斑魚肝臟酸性磷酸酶(ACP)活性變化
隨著鹽度驟降的幅度增大和脅迫時間的延長,云紋石斑魚肝臟ACP活力的變化見圖1。鹽度21組的ACP活力呈波動的變化趨勢,在第1天和第3天出現兩個峰值,且峰值顯著高于其它時間的值(P<0.05);鹽度15組ACP活力呈先下降后升高的趨勢,第2天出現峰值且為各時間點中最高(P<0.05);鹽度21和15組在第7天時都恢復到實驗開始時水平,且均與鹽度27組之間無顯著性差異(P>0.05)。鹽度9組ACP活力呈不斷上升的趨勢(P<0.05)。此外,鹽度9組在實驗第2天出現個別死亡,至實驗第3天時全部死亡(死亡情況以下各部分不再重復描述)。同一時間的不同處理組,隨著鹽度的降低,第1、2、7天均呈波動變化趨勢,第3天呈不斷上升的變化趨勢。
2.2 不同鹽度下云紋石斑魚肝臟堿性磷酸酶(AKP)活性變化
不同鹽度下肝臟AKP活力的變化見圖2。鹽度21組與鹽度15組AKP活力呈先下降后上升最后恢復的趨勢,且均在第3天出現峰值;鹽度21組第3天AKP活力值為不同時間點各組中最高(P<0.05);鹽度9組AKP活力呈不斷下降趨勢(P<0.05)。對于同一時間的不同處理組:第1、3天AKP活力隨鹽度降低均呈波動變化趨勢,第2、7天隨鹽度降低AKP酶活力下降且均未低于對照組。
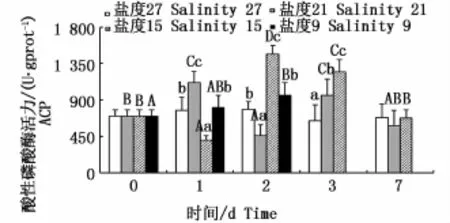
圖1 不同鹽度下云紋石斑魚肝臟酸性磷酸酶(ACP)活性Fig.1 Activity of ACP in the liver of Epinephelus moara reared at different salinities
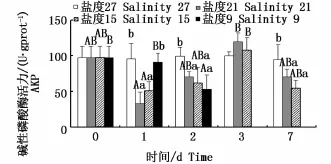
圖2 不同鹽度下云紋石斑魚肝臟堿性磷酸酶(AKP)活性Fig.2 Activity of AKP in the liver of Epinephelus moara reared at different salinities
2.3 不同鹽度下云紋石斑魚肝臟谷丙轉氨酶(GPT)活性
不同鹽度下肝臟GPT活力的變化見圖3。鹽度21組GPT活力呈波動的變化趨勢(P<0.05),且均未超過初始值;鹽度15組與鹽度9組GPT活力呈先下降后上升的趨勢,鹽度15組第3天出現峰值,且為不同時間點各組中最高(P<0.05);鹽度9組第2天AKP活力值顯著升高(P<0.05)。對于同一時間的不同處理組:隨鹽度降低各組GPT活力均呈波動變化趨勢。
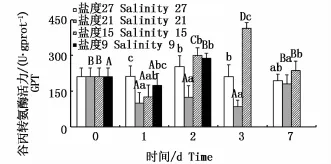
圖3 不同鹽度下云紋石斑魚肝臟谷丙轉氨酶(GPT)活性Fig.3 Activity of GPT in the liver of Epinephelus moara reared at different salinities
2.4 不同鹽度下云紋石斑魚肝臟谷草轉氨酶(GOT)活性
不同鹽度下肝臟GOT活力的變化見圖4。鹽度21組GOT活力呈先升高后降低的趨勢,第1天出現峰值(P<0.05);鹽度15組GOT活力呈先下降后上升再下降的趨勢,第2天出現峰值,且為不同時間點各組中最高(P<0.05);鹽度9組GOT活力呈不斷上升的變化趨勢(P<0.05)。對于同一時間的不同處理組,GOT活力隨鹽度降低均呈波動變化趨勢。
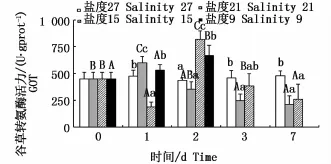
圖4 不同鹽度下云紋石斑魚肝臟谷草轉氨酶(GOT)活性Fig.4 Activity of GOT in the liver of Epinephelus moara reared at different salinities
2.5 不同鹽度下云紋石斑魚肝臟乳酸脫氫酶(LDH)活性
不同鹽度下肝臟LDH活力的變化見圖5。鹽度21組與15組LDH活力均呈先降低后升高再恢復的變化趨勢,且均在第3天出現峰值,鹽度21組第3天為不同時間點各組中最高(P<0.05);鹽度9組LDH活力呈先下降后上升的變化趨勢(P<0.05),但均未超過對照組。同一時間各處理組LDH活力隨鹽度降低均呈波動變化趨勢。
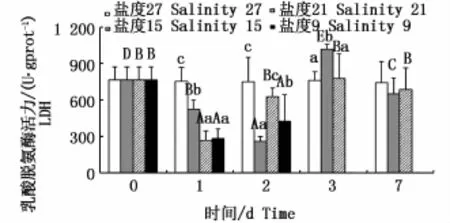
圖5 不同鹽度下云紋石斑魚肝臟乳酸脫氫酶(LDH)活性Fig.5 Activity of LDH in the liver of Epinephelus moara reared at different salinities
3 討論
3.1 不同鹽度對云紋石斑魚肝臟磷酸酶活力的影響
有研究顯示,海洋生物在應對鹽度變化的過程中,ACP與AKP活力會隨著鹽度的降低顯著升高或者先降低再升高。文昌魚(Branchiostoma lanceolatum)的培育鹽度低于28.0~32.0范圍時,磷酸酶活性顯著升高[16];仿刺參(Apostichopus japonicus)在鹽度脅迫下ACP和AKP活力先升高后降低[17];三疣梭子蟹(Portunus trituberculatus)在低鹽14脅迫下,ACP和AKP活力先降后升再降[18];鋸緣青蟹(Scylla serrata)在急性低鹽脅迫時AKP活力顯著被抑制,而高鹽度的和小幅度低鹽度的變化,會刺激機體使AKP活力增強[19]。本實驗結果與上述研究基本一致,ACP活力鹽度15組云紋石斑魚第1天降低,第2天顯著升高,鹽度21組呈波動趨勢,鹽度9組呈升高趨勢;AKP活力鹽度21組與15組實驗魚均先降低后升高再恢復,鹽度9組呈降低趨勢。即在本實驗初期鹽度脅迫基本上在短時間內會先顯著抑制磷酸酶活力,至實驗第2天或第3天磷酸酶活力恢復并大幅升高,也有部分鹽度脅迫會刺激魚體,磷酸酶活力直接升高。整體升高的趨勢說明鹽度驟降引起云紋石斑魚的應激反應,磷酸酶活力升高以增強魚體免疫防御能力。對于不同鹽度脅迫下,云紋石斑魚機體內磷酸酶活力并不隨鹽度降低而成比例的變化,說明云紋石斑魚在急性低鹽脅迫下,不同的鹽度范圍有不同的免疫調節反應。
3.2 不同鹽度對云紋石斑魚肝臟轉氨酶活力的影響
有研究表明,在鹽度脅迫下生物需要足夠的能量用于滲透調節,機體內大量營養物質被調動,多種氨基酸參與并被用于為滲透壓調節提供能量[20],體內游離氨基酸如谷氨酸、丙氨酸、甘氨酸、脯氨酸和牛磺酸[21]含量會隨鹽度脅迫而升高。凡納濱對蝦(Litopenaeus vannamei)在低鹽度脅迫下,其肝胰腺中蛋白質含量顯著升高,以保障機體分解蛋白質時有足夠的游離氨基酸來調節機體的滲透[22]。目前對于這種現象的解析主要有兩種觀點:GEOFFRIOR等[23]從能量學的角度認為機體在滲透脅迫下,體內游離氨基酸的動態變化與機體的能量消耗相關,高滲脅迫下,游離氨基酸的形成主要來自體內蛋白質的降解;而HOCHACHKA等[24]則認為機體為了獲得足夠的游離氨基酸用于滲透壓調節,在一定程度上降低了從頭合成途徑的效率,從而使機體組織中的某些游離氨基酸積累量升高。轉氨酶是組織中將一種氨基酸的氨基轉運到另一種氨基酸上的一類氨基轉移酶,參與氨基酸的分解和合成,其活性高低在一定程度可以反映氨基的轉移能力[25]。本研究測定了不同鹽度云紋石斑魚肝臟中谷草轉氨酶和谷丙轉氨酶的活力,結果發現,鹽度驟降脅迫下云紋石斑魚肝臟中轉氨酶活力呈先降低后升高的趨勢。由此可見,初期鹽度驟降對云紋石斑魚肝臟中轉氨酶活力產生一定的抑制作用,魚體適應后,轉氨酶活力恢復并顯著升高,使氨基轉運活力上升以抵抗環境脅迫。所以,根據轉氨酶的功能,筆者推測云紋石斑魚為了在低鹽度下進行滲透調節,動用機體儲存的蛋白質轉化成游離氨基酸為滲透調節供能,這種解釋與DEATON[26]的觀點相符,且因轉氨酶活力的升高推測魚體內游離氨基酸的升高主要來自于蛋白質的降解,這與凡納濱對蝦在低鹽度慢性脅迫下,其體內轉氨酶活力會升高以加快機體氨基轉運速度研究結果相似。
轉氨酶主要存在于肝臟中,正常情況下,肝細胞內的轉氨酶只有少量被釋放到血液中,血清中的轉氨酶活性較低。有研究通過測定血清中轉氨酶含量,來判斷環境變化對肝細胞的損傷程度。如大黃魚(Pseudosciaena crocea)在鹽度突降后血清中GPT和GOT顯著上升[27];紅耳龜(Trachemys scripta)在不同鹽度脅迫下血液中GPT和GOT活性均顯著升高[28]。肝臟中轉氨酶活性也會因滲透脅迫而發生變化,如虎斑烏賊(Sepia plaraonis)幼體在鹽度漸變情況下肝臟GOT活性和GPT呈先上升后下降的變化趨勢[29];大馬哈魚(Oncorhynchus keta)在低鹽度脅迫下,肝臟中GPT和GOT活性均降低[30]。
3.3 不同鹽度對云紋石斑魚肝臟乳酸脫氫酶活力的影響
脫氫酶類是生物體內氧化還原反應中重要的催化劑之一,在生物體內的氧化產能、解毒以及某些生理活動[31](如Cori循環)中起著很重要的作用。LDH是糖酵解途徑與TCA循環之間的關鍵酶[32-34],其活力可作為衡量無氧代謝水平的指標之一[35]。本實驗中,云紋石斑魚肝臟中LDH先降低后升高,說明鹽度驟降初期其機體內無氧代謝并不旺盛,甚至抑制了LDH的活力,直至第3天由LDH催化產生的NAD+保障了無氧條件下糖酵解作用的持續進行[34],從而為其抵御環境脅迫提供了能量。然而,鹽度驟降為9時,云紋石斑魚LDH活力逐漸下降并未恢復正常水平,說明鹽度驟降至9時云紋石斑魚無氧代謝會受到一定程度的阻礙,影響魚類生長存活。此外,SOMERO等[36]認為LDH活力水平與生物高速游動的能力密切相關,并且隨著規格的增大而增大。這可能是大規格生物游動對能量需求更大,使得LDH活力增大。由于魚的種類繁多,實驗所取的個體大小也各不相同,無法獲得一個標準的范圍值(如人類的LDH正常標準值為109~ 245、GPT和GOT標準值均為5~50),因此本實驗只能說明受脅迫后各測試指標的變化趨勢。
4 小結
本實驗通過檢測云紋石斑魚在鹽度驟降條件下肝臟中ACP、AKP、GPT、GOT及LDH活力隨時間變化的情況,探討了云紋石斑魚肝臟代謝酶對鹽度驟降的響應。研究結果表明云紋石斑魚在鹽度驟降脅迫下,部分鹽度下磷酸酶、轉氨酶與LDH酶活力初期會受到抑制,隨后恢復,部分直接升高以抵御脅迫傷害。本研究使用的魚規格較小,鹽度驟降對魚體生長影響大,因此在云紋石斑魚幼魚的養殖生產中應避免養殖水體鹽度大幅度急劇降低。
[1]宋振鑫,陳 超,翟介明,等.云紋石斑魚生物學特性及人工繁育技術研究進展[J].漁業信息與戰略,2012,27(1):47-53.
SONG Z X,CHEN C,ZHAI JM,et al.Biological characteristics and progress of artificial breeding technique for Kelp Bass,Epinephelus moara[J].Fisheries Information&Strategy,2012,27(1):47-53.
[2]區又君.石斑魚類的人工繁育技術[J].海洋與漁業,2009,12(3):14-15.
QU Y J.Artificial breeding technology ofEpinephalus[J].Ocean and Fishery,2009,12(3):14-15.
[3]王新安,馬愛軍,陳 超,等.七帶石斑魚(Epinephelus septemfasciatus)兩個野生群體形態差異分析[J].海洋與湖沼,2008,39(6):655-660.
WANG X A,MA A J,CHEN C,et al.Orphological varlation in two wild populations of sevenband grouper(Epinephelus septemfasciatus)[J].Oceanologia Et Limnologia Sinica,2008,39(6):655-660.
[4]孫 鵬,尹 飛,王建建,等.操作脅迫對云紋石斑魚肝臟抗氧化和鰓Na+-K+ATPase活力的影響[J].海洋漁業,2014,36(3):247-251.
SUN P,YIN F,WANG JJ,et al.Effects of handling stress on activities of antioxidant enzymes in liver and Na+-K+ATPase in gill ofEpinephelus moara[J].Marine Fisheries,2014,36(3):247-251.
[5]楊求華,黃種持,鄭樂云,等.云紋石斑魚(♀)×赤點石斑魚(♂)雜交子代胚胎發育及生長[J].海洋漁業,2014,36(3):224-231.
YANG Q H,HUANG Z C,ZHENG L Y,et al.Embryonic development and growth of hybrid from the hybridization ofEqinephelus moara(♀)×E.akaara(♂)[J].Marine Fisheries,2014,36(3):224-231.
[6]陸麗君,陳 超,馬愛軍,等.云紋石斑魚(Epinephelus moara)早期發育階段的攝食與生長特性[J].海洋與湖沼,2011,42(6):822-829.
LU L J,CHEN C,MA A J,et al.Studies on the feeding behavior and morphological developments ofEpinephelus moarain early development stages[J].Oceanologia Et Limnologia Sinica,2011,42(6):822-829.
[7]宋振鑫,陳 超,翟介明,等.云紋石斑魚胚胎發育及仔、稚、幼魚形態觀察[J].漁業科學進展,2012,33(3):26-34.
SONG Z X,CHEN C,ZHAI J M,et al.Embryonic development and morphological characteristics of larval,juvenile and young Kelp bass,Epinephelus moara[J].Progress in Fishery Sciences,2012,33(3):26-34.
[8]宋振鑫,陳 超,吳雷明,等.鹽度與pH對云紋石斑魚胚胎發育和仔魚活力的影響[J].漁業科學進展,2013,34(6):52-58.
SONG Z X,CHEN C,WU L M,et al.Effects of salinity and pH on the embryonic development and larval activity of kelp bassEpinephelus moara[J].Progress in Fishery Sciences,2013,34(6):52-58.
[9]劉銀華,鐘幼平,曾慶民,等.溫度和鹽度對云紋石斑魚早期幼魚生長和存活的影響[J].集美大學學報(自然科學版),2014,19(4):241-246.
LIU Y H,ZHONG Y P,ZENG QM,et al.Effects of temperature and salinity on the growth and survivability of youngEpinephelus moara[J].Journal of Jimei University(Natural Science),2014,19(4):241-246.
[10]劉樹青,江曉路,牟海津,等.免疫多糖對中國對蝦血清溶菌酶、磷酸酶和過氧化物酶的作用[J].海洋與湖沼,1999,30(3):278-283.
LIU SQ,JIANG X L,MOU H J,et al.effects of immunopoiysaccharide on LSZ,ALP,ACP and POD activities of penaeus chinensis serum[J].Oceanologia Et Limnologia Sinica,1999,30(3):278-283.
[11]PIPE R K.Hydrolytic enzymes associated with the granular haemocytes of the marine mussel mytilus edulis[J].The Histochemical Journal,1990,11(22):596-603.
[12]SAMSONOVA M V,MINKOVA N O,LAPTEVA T I,et al.Aspartate and alanine aminotransferases in early development of the keta[J].Russian Journal of Developmental Biology,2003,34(1):14-18.
[13]梁 淼.刺參(Apostichopus japonicas)個體生長差異的實驗研究[D].青島:中國海洋大學,2010:1-164.
LIANG M.Experimental studies on individual variation in growth and causes in sea cucumber,Apostichopus japonicus[D].Qingdao:Ocean University of China,2010:1-164.
[14]VIJAYAVEL K,BALASUBRAMANLANM P.Changes in oxygen consumption and respiratory enzymes as stress indicators in an estuarine edible crabScylla serrataexposed to naphthalene[J].Chemosphere,2006,63(9):1523-1531.
[15]賈 冬,趙 敏.膿毒癥大鼠血清乳酸、乳酸清除率及轉氨酶水平與肝臟損傷關系的探討[J].中國醫科大學,2013,15(10):1353-1357.
JIA D,ZHAO M.The serum lactate clearance rate and transaminase levels in septic rats and its relationship with liver damage[J].Chinese Medical Sciences University,2013,15(10):1353-1357.
[16]白秀娟,盧伙勝,劉曉彬,等.鹽度、pH脅迫對茂名海域文昌魚磷酸酶活性的影響[J].海洋通報,2009,28(4):42-46.
BAIX J,LU H S,LIU X B,et al.Effect of salinity and pH on the ACP and ALP ofBranchiostoma belcheriin Maoming Sea Area[J].Marine Science Bulletin,2009,28(4):42-46.
[17]王 沖,田 燚,常亞青,等.鹽度脅迫對刺參非特異性免疫酶的影響[J].中國農業科技導報,2013,15(3):163-168.
WANG C,TIAN Y,CHANG Y Q,et al.Effect of salinity stress on immune enzyme activity of sea cucumber(Apostichopus japonicus)[J].Journal of Agricultural Science and Technology,2013,15(3):163-168.
[18]鄭萍萍.鹽度脅迫對三疣梭子蟹血清非特異性免疫因子的影響[J].水產科學,2010,29(11):634-638.
ZHENG P P.Effect of salinity stress on serum nonspecific immune factors in swimming crab Portunus trituberculatus[J].Fisheries Science,2010,29(11):634-638.
[19]周素琴.環境脅迫對養殖鋸緣青蟹主要免疫因子的影響[D].青島:中國海洋大學,2006.
ZHOU S Q.Effects of environmental stress on the immune factors inScylla serrata[D].Qingdao:Ocean University of China,2006.
[20]CUZON G,LAWRENCEB A,GAXIOLACG,etal.Nutrition of Litopenaeus vannamei reared in tanks or in ponds[J].Aquaculture,2004,235(1-4):513-551.
[21]SOMERO G N,BOWLUS R D.3-Osmolytes and metabolic and products of molluscs:the design of compatible solute systems1[J].Mollusca,1983:77-100.
[22]李二超,陳立僑,曾 嶒,等.鹽度對凡納濱對蝦體組織蛋白質積累、氨基酸組成和轉氨酶活性的影響[J].水生生物學報,2009,33(3):532-538.
LI E C,CHEN L Q,ZENG C,et al.Protein accumulation,amino acid profile and amino transferase activities of the white shrimp,litopeneaus vannamei,at different salinities[J].Acta Hydrobiological Sinica,2009,33(3):532-538.
[23]GEOFFRION Y,GUDERLEY H,LAROCHELLE J.The effect of oxygen availability on the osmoregulatory contribution of free amino acids inAcanthamoeba castellanii[J].Canadin Journal of Zoology,1986,64(7):1430-1435.
[24]HOCHACHKA P W,SOMERO G N.Biochemical Adaptation[M].New Jersey:Princeton University Press.1984:27.
[25]PANA C H,CHIEN Y H,HUNTERC B.The resistance to ammonia stress ofPenaeus monodonFabricius juvenile fed diets supplemented with astaxanthin[J].Journal of Experimental Marine Biology&Ecology,2003,297(1):107-118.
[26]DEATON L E.Hyperosmotic volume regulation in the gills of the ribbed mussel,Geukensia demissa:rapid accumulation of betaine and alanine[J].Journal of ExperimentalMarine Biology and Ecology,2001,260(2):185-197.
[27]王 濤,苗 亮,李明云,等.突降鹽度脅迫對大黃魚(Pseudosciaena crocea)血清生理生化及鰓絲Na+/K+-ATP酶活性的影響[J].海洋與湖沼,2013,44(2):421-426.
WANG T,MIAO L,LIM Y,etal.Effects of abrupt salinity decrease on serum physiology,biochemistry and gill Na+/K+-ATP activity of the large yellow croaker pseudosciaena crocea[J].Oceanologia Et Limnologia Sinica,2013,44(2):421-426.
[28]舒超華,張 珂,洪美玲,等.鹽度脅迫對紅耳龜生長與血液生化指標的影響[J].四川動物,2012,36(6):912-916.
SHU C H,ZHANG K,HONG M L,et al.Effect of salinity stress on trachemys scripta elegans growth and blood biochemical ingredient[J].Sichuan Journal of Zoology,2012,36(6):912-916.
[29]樂可鑫,蔣霞敏,汪 元,等.鹽度對虎斑烏賊幼體生長與酶活的影響[J].熱帶海洋學報,2015,34(6):64-72.
LE K X,JIANG X M,WANG Y,et al.Salinity effects on growth and enzyme activity of juvenileSepia pharaonis[J].Journal of Tropical Oceanography,2015,34(6):64-72.
[30]劉 偉,支兵杰,戰培榮.鹽度對大麻哈魚幼魚血液生化指標及肝組織的影響[J].應用生態學報,2010,21(9):2411-2417.
LIUW,ZHIB J,ZHAN PR.Effects of salinity on haematological biochemistrical indices and liver tissue in juvenileOncorhynchus keta[J].Chinese Journal of Applied Ecology,2010,21(9):2411-2417.
[31]王棟樑,曾強貴,石 瑜.生物化學[M].鎮江:江蘇大學出版社,2015.
WANG D L,ZENG Q G,SHI Y.Biological chemistry[M].Zhenjiang:Jiangsu University Press,2015.
[32]ABDELMOHSEN H A.Assessment of respiratory and ion transport potential ofPenaeus japonicasgills in response to environmental pollution[J].Mediterranean Marine Science,2009,10(1):5-18.
[33]VALARMATHI S,AZARIAH J.Effects of copper chloride on the enzyme activities of the crabSesarma quadratum(Fabricius)[J].Turkish Journal of Zoology,2003,27(3):253-256.
[34]王鏡巖,朱圣庚,徐長法.生物化學(第三版)[M].北京:高等教育出版社,2005.
WANG J Y,ZHU S G,XU C F.Biological chemistry(3 edition)[M].Beijing:Higher Education Press,2005.
[35]BERGES J A,BALLANTYNE J S.Size scaling of whole-body maximal enzyme activities in aquatic crustaceans[J].Canadian Journal of Fisheries&Aquatic Sciences,1991,48(12):2385-2394.
[36]SOMERO G N,CHILDRESS J J.A violation of the metabolism-size scaling paradigm:activities of glycolytic enzymes in muscle increase in larger-size fish[J].Physiological Zoology,1980,53(3):322-337.
Impact of abrupt salinity decrease on metabolic enzymes in the liver of Epinehelus moara
SHI Zhao-hong1,2,LIAO Ya-li1,2,WANG Xiao-shan2,GAO Quan-xin2,PENG Shi-ming2,ZHANG Chen-jie2
(1.College of Fisheries and Life,Shanghai Ocean University,Shanghai201306,China;2.East China Sea Fisheries Research Institute,Chinese Academy of Fishery Sciences,Shanghai200090,China)
This experiment was conducted to investigate the response of metabolic enzymes in the liver ofEpinehelus moarato abrupt salinity decrease.Four salinity groups(27,21,15,9)were designed.The average body length ofEpinehelus moarawas(10.43±1.08)cm and the average body weight was(16.73± 4.47)g.The fish were reared temporarily in the water of(27±1.0)℃temperature and 27 salinity when reaching Shanghai Fisheries Research Institute of Qidong breeding base.The study was conducted in a circular glass cylinder barrelwith 1 m in diameter and 0.8 m in depth.The temporary rearing seawater at salinity 27 was the control group,and the seawater with lower salinities(salinity 21,salinity 15,salinity 9)used tap water after aerationmixed with natural seawater after purification treatment,and the experimentalwater could be used after stabling for 48 hours.Every salinity gradient had 3 parallels and 12 buckets.Fish livers in each group were sampled on day 0,1,2,3,and 7 tomeasure the activities of acid phosphatase(ACP),alkaline phosphatase(AKP),glutamic-pyruvic transaminase(GPT),glutamic-oxalacetic transaminase(GOT)and lactate dehydrogenase(LDH).Results showed that the activity of ACP in salinity 21 group first changed wavely,then recovered to the nomal level.ACP activity in salinity 15 group decreased first and then increased,finally decreased to the normal level on day 7;AKP activity in salinity 21 and 15 groups decreased on day 1 and 2,and then increased significantly on day 3;GPT and LDH activities in salinity 21 and 15 groups first decreased and then increased wavely;GOP activities in 21 salinity group increased first and then decreased,activities in salinity 15 group decreased first and then changed wavely.The results indicated that abrupt salinity decrease from 27 to 21 or 15 could cause stress response ofEpinehelus moara;the phosphatase,aminopherase and LDH activities were all inhibited first and recovered afterward;the abrupt salinity decrease from 27 to 9 caused the death of all fish on day 3.Research highlights:Epinehelus moaracan adapt themselves to a comparatively broad range of salinities and temperature.The impact of abrupt salinity decrease on the metabolic enzymes in the liver ofEpinehelus moarawas studied for the first time in this paper.Abrupt salinity decrease had a significant effect on metabolic enzymes in the liver ofEpinehelus moara,remaining steady salinity had an important ecophysiological significance on maintaining(or recovering)the normal metabolism and keeping the osmotic balance of organism during the culture period.
Epinehelus moara;abrupt salinity decrease;metabolic enzymes in liver
S 917
A
1004-2490(2016)02-0174-08
2015-07-15
中央級公益性科研院所基本科研業務費項目(東2015M04)
施兆鴻,研究員,主要研究方向為海水魚類繁育與養殖。E-mail:shizh@eastfishery.ac.cn

