沙蔥化學成分的分離與結構鑒定II*
董勇喆,史文中,楊圣財,李曉霞,張 祎,王 濤
(天津市中藥化學與分析重點實驗室,天津 300193)
沙蔥化學成分的分離與結構鑒定II*
董勇喆,史文中,楊圣財,李曉霞,張 祎,王 濤
(天津市中藥化學與分析重點實驗室,天津 300193)
[目的]對可食用植物沙蔥(Allium mongolicm Regel)的化學成分進行研究。[方法]采用大孔吸附樹脂、羥丙基葡聚糖凝膠等柱色譜及制備型高效液相色譜法對其所含化學成分進行分離、制備,并利用波譜學方法鑒定了結構。[結果]從沙蔥提取物中分離鑒定了異槲皮苷(1)、槲皮素-3-O-(6′′-O-乙酰基)-β-D-吡喃葡萄糖苷(2)、槲皮素-3,4′-二-O--D-吡喃葡萄糖苷(3)、quercetin-3-O-β-D-glucopyranosyl-(1→4)-β-D-glucopyranoside(4)、蘆丁(5)、quercetin 3-O-(6′′-O-α-L-rhamnopyranosyl)-β-D-glucopyranoside-7-O-β-D-glucopyranoside(6)等6個單體成分。[結論]化合物2、6為首次從蔥屬中分離得到,1、3~5為首次從該植物中分離得到。
沙蔥;化學成分;結構鑒定
沙蔥(Allium mongolicm Regel),為百合科蔥屬植物,又名蒙古韭,因具有揮發性的硫醚類化合物,使得與其他蔥屬植物同樣具有特殊刺激性氣味[1]。其富含粗蛋白質、粗脂肪、粗纖維和人體所需的常量、微量元素以及必需氨基酸。沙蔥以其地上部分入藥,可用于降血脂、降壓,治療胸悶胸痛以及禿瘡、青腿病等[2]。中醫理論認為食用沙蔥有利于增強胃腸蠕動,從而提高食欲,常用來治療消化不良,便秘、瘴氣、腹瀉、白痢、腸炎等疾病[3]。此外,長期食用還能強腎補陽,強志益目,更有通宣理表,防流感之效。在中國境內,主要分布于內蒙古自治區、甘肅、新疆、青海、寧夏、陜西等地,境外于俄羅斯、蒙古有少量分布,具有抗旱抗寒,適應性強的特點[4~6]。
沙蔥主要含有黃酮、生物堿、揮發油和多糖等化學成分。現代藥理學研究表明,沙蔥具有多種藥理學活性,如包美艷等[7]和藺婷娟等[8]在研究沙蔥多糖的過程中發現,其能夠促進羊外周血淋巴細胞的增殖和影響腸道免疫球蛋白數量和活性,從而發揮免疫調節作用。薩茹麗等[9]通過對沙蔥葉、花和稈的總提取物中總黃酮進行抗氧化能力和抗菌性的研究,發現三者均有一定作用,且葉提取物活性較高。此外,扈瑞平等[10]研究發現沙蔥多糖也有較強的體外抑菌作用,還有研究表明,在細胞分子水平上,沙蔥多糖在促進淋巴因子的表達中有顯著作用,進而發揮抗腫瘤作用[11]。
筆者在對沙蔥化學成分研究的過程中,利用與文獻[12~17]類似的方法,分離鑒定出6個單體化合物。其中,2、6為從蔥屬植物中首次分離得到,1、3~5為從該植物中首次分離得到,結構見圖1。
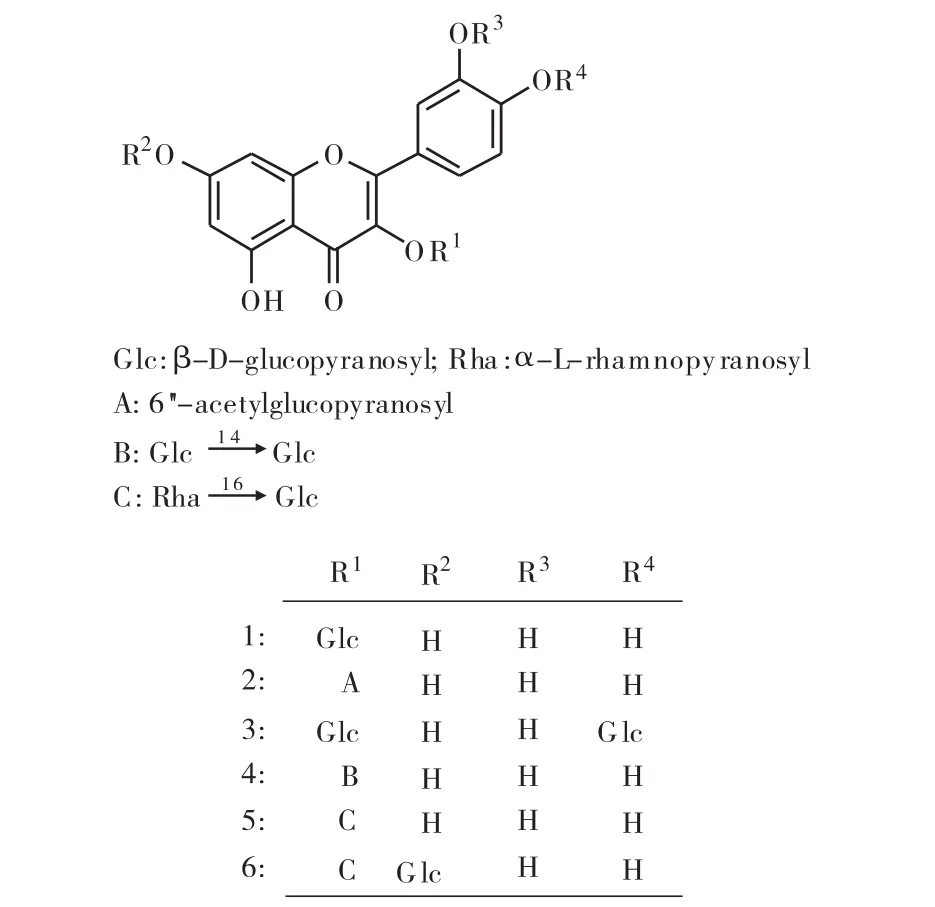
圖1 沙蔥中得到的黃酮類化合物(1~6)
1 儀器與材料
Bruker 500MR超導核磁共振波譜儀(瑞士Bruker公司,AvanceⅢ500MR),安捷倫6520 QTOF LC/MS,D101大孔吸附樹脂(天津海光化工有限公司),Sephadex LH-20(瑞典Ge Healthcare Bio-Sciences AB公司),Cosmosil 5C18-MS-II制備柱和分析柱(250 mm×4.6 mm和250 mm×20 mm,均為5 μm,Japan,Nacalai Tesque公司),TLC Silica gel 60 F254(Aluminium sheets 20 cm×20 cm,德國Merck公司)。
色譜/分析純氯仿、甲醇、乙腈、丙酮、冰醋酸等試劑購自天津康科德科技有限公司。
沙蔥采自內蒙古阿拉善盟,由天津中醫藥大學李天祥教授鑒定為百合科蔥屬植物沙蔥(Allium mongolicm Regel)。
2 提取與分離
取新鮮沙蔥17.8 kg,依次用2倍量95%乙醇溶液和2倍量50%乙醇加熱回流提取(2 h/1 h),減壓回收溶劑得乙醇提取物浸膏約515 g。取浸膏約470 g,加水溶解后,用乙酸乙酯-水(1∶1,V/V)萃取,得到乙酸乙酯層萃取物65 g和水層萃取物381 g。取萃取后水層342 g經D101大孔吸附樹脂柱層析,分別用水和95%乙醇依次洗脫,得到水洗脫物(289g)及95%乙醇洗脫物(30 g)。
上述95%乙醇洗脫物,經制備型高效液相色譜(PHPLC)分離制備[MeOH-H2O(20∶80→30∶70→55∶45→100∶0),得到22個組分(Fr.1~22)。
Fr.13(426.2 mg)經Sephadex LH-20柱層析[MeOH-H2O(1∶1,V/V)],得到6個組分(Fr.13-1~13-6)。Fr.13-2先后經 2次 PHPLC分離制備[CH3CN-H2O(9∶91,V/V)+1%HAc,CH3CN-H2O(11∶89,V/V)+1%HAc],得到化合物quercetin-3-O-(6′′-O-α-L-rhamnopyransoyl)-β-D-glucopyranoside-7-O-β-D-glucopyranoside(6,10.0 mg)。
Fr.16(3.2 g)經Sephadex LH-20柱層析[MeOHH2O(1∶1,V/V)],得到5個組分(Fr.16-1~16-5)。Fr.16-4經PHPLC分離制備[CH3CN-H2O(19∶81,V/V)+1%HAc],得到槲皮素-3,4′-二-O-β-D-吡喃葡萄糖苷(3,38.7 mg)。
Fr.18(1.4 g)經Sephadex LH-20柱層析[MeOHH2O(1∶1,V/V),得到4個組分(Fr.18-1~18-4)。Fr.18-4經PHPLC再次分離制備[CH3CN-H2O(20∶90,V/V)+1%HAc],得到異槲皮苷(1,131.0 mg)、quercetin-3-O-β-D-glucopyranosyl-(1→4)-β-D-glucopyranoside(4,61.3 mg)和蘆丁(5,340.3 mg),同時得到的組分Fr.18-4-6繼續經PHPLC分離制備[CH3CN-H2O(20∶90,V/V)+1%HAc],得到槲皮素-3-O-(6″-O-乙酰基)-β-D-吡喃葡萄糖苷(2,7.1mg)。
3 結構鑒定
化合物1:黃色結晶。高分辨Q-TOF-ESI-MS給出其準分子離子峰m/z 463.088 4[M-H]-,確定其分子式為C21H20O12(Calcd for C21H19O12,463.088 2)。1H-NMR(500 MHz,DMSO-δ6):δ 6.21(1H,br.s,H-6),6.41(1H,br.s,H-8),7.59(1H,d,J=2.0 Hz,H-2′),6.86(1H,d,J=8.0 Hz,H-5′),7.60(1H,dd,J=2.0、8.0 Hz,H-6′),12.65(1H,br.s,5-OH),5.48(1H,d,J=7.0 Hz,H-1″),3.11~3.62(6H,m,H-2″~6″)。其1H-、13CNMR(125 MHz,DMSO-d6,見表1)譜數據與文獻[18]相對照,鑒定該化合物為異槲皮苷(isoquercetin)。
化合物2:黃色粉末。高分辨Q-TOF-ESI-MS給出其準分子離子峰m/z 505.096 6[M-H]-,確定其分子式為C23H22O13(Calcd for C23H21O13,505.098 8)。1H-NMR(500 MHz,DMSO-d6):d 6.19(1H,br.s,H-6),6.39(1H,br.s,H-8),7.52(1H,br.s,H-2′),6.83(1H,d,J=8.0 Hz,H-5′),7.53(1H,br.d,ca.J=8 Hz,H-6′)、12.62(1H,br.s,5-OH),5.37(1H,d,J=7.0 Hz,H-1″),3.03~4.14(6H,m,H-2″~6″),1.73(3H,s,6″-COCH3)。其1H-、13C-NMR(125 MHz,DMSO-d6,見表1)譜數據與文獻[19]相對照,鑒定該化合物為槲皮素-3-O-(6″-O-乙酰基)-β-D-吡喃葡萄糖苷(quercetin-3-O-(6″-O-acetyl)-β-D-glucopyranoside)。
化合物3:黃色粉末。高分辨Q-TOF-ESI-MS給出其準分子離子峰m/z 661.115 0[M+Cl]-,確定其分子式為C27H30O17(Calcd for C27H30O17Cl,661.117 7)。1H-NMR(500 MHz,DMSO-d6):δ 6.19(1H,br.s,H-6),6.41(1H,br.s,H-8),7.65(1H,d,J=2.0 Hz,H-2′),7.22(1H,d,J=8.5 Hz,H-5′),7.62(1H,dd,J=2.0、8.5 Hz,H-6′),12.56(1H,s,5-OH),5.50(1H,d,J=7.0 Hz,H-1″),3.23(1H,dd,J=7.0、9.0 Hz,H-2″),3.24(1H,J=9.0、9.0 Hz,H-3″),3.12(2H,m,H-4″and 5″),[3.36(1H,dd,J=4.5、11.0 Hz),3.61(1H,br.d,ca.J= 11 Hz),H2-6″],4.88(1H,d,J=7.0 Hz,H-1″′),3.36(1H,dd,J=7.0、8.5 Hz,H-2″′),3.35(1H,dd,J=8.5、9.0 Hz,H-3″′),3.22(1H,dd,J=9.0、9.0 Hz,H-4″′),3.41(1H,m,H-5″′),[3.52(1H,dd,J=5.5、11.5 Hz),3.74(1H,br.d,ca.J=12 Hz),H2-6″′]。其1H-、13C-NMR(125 MHz,DMSO-d6,見表1)譜數據與文獻[20]相對照,鑒定該化合物為槲皮素-3,4′-二-O-β-D-吡喃葡萄糖苷(quercetin-3,4′-di-O-β-D-glucopyranoside)。
化合物4:黃色粉末。高分辨Q-TOF-ESI-MS給出其準分子離子峰m/z 625.142 1[M-H]-,確定其分子式為C27H30O17(Calcd for C27H29O17,625.141 0)。1H-NMR(500 MHz,DMSO-d6):δ 6.20(1H,br.s,H-6),6.41(1H,br.s,H-8),7.59(1H,d,J=2.0 Hz,H-2′),6.87(1H,d,J=7.5 Hz,H-5′)、7.57(1H,dd,J= 2.0,7.5 Hz,H-6′),12.63(1H,s,5-OH),5.52(1H,d,J=7.5 Hz,H-1″),3.37(1H,dd,J=7.5、8.0 Hz,H-2″),3.43(1H,J=7.5、8.0 Hz,H-3″),3.42(1H,J=8.0、8.0 Hz,H-4″),3.29(1H,m,H-5″),[3.52(1H,dd,J=4.5、11.5 Hz),3.66(1H,br.d,ca.J=12 Hz),H2-6″],4.29(1H,d,J=7.5 Hz,H-1″′),3.02(1H,dd,J=7.5、8.0 Hz,H-2″′),3.18(1H,dd,J=8.0、8.5 Hz,H-3″′),3.09(1H,J=8.5、8.5 Hz,H-4″′),3.23(1H,m,H-5″′),[3.44(1H,dd,J=5.5、12.0 Hz),3.73(1H,br.d,ca.J= 12 Hz),H2-6″′]。其1H-、13C-NMR(125 MHz,DMSO-d6,見表1)譜數據結合1H-1H COSY、HSQC、HMBC等2D-NMR譜的解析,鑒定該化合物為文獻[21]所報道的quercetin-3-O-β-D-glucopyranosyl-(1→4)-β-D-glucopyranoside。
化合物5:黃色粉末。高分辨Q-TOF-ESI-MS給出其準分子離子峰m/z 609.144 4[M-H]-,確定其分子式為C27H30O16(Calcd for C27H29O16,609.146 1)。1H-NMR(500 MHz,DMSO-d6):δ 6.17(1H,br.s,H-6),6.36(1H,br.s,H-8),7.53(1H,d,J=2.0 Hz,H-2′),6.84(1H,d,J=8.5 Hz,H-5′),7.55(1H,dd,J=2.0,8.5 Hz,H-6′),12.57(1H,s,5-OH),5.33(1H,d,J= 7.0 Hz,H-1″),3.22(2H,J=7.0、9.5 Hz,H-2″and 3″),3.07(1H,dd,J=9.5、9.5 Hz,H-4″),3.23(1H,m,H-5″),[3.28(1H,dd,J=6.0、12.0 Hz),3.71(1H,br.d,ca.J=12 Hz),H2-6″],4.39(1H,br.s,H-1″′),3.40(1H,br.d,ca.J=3 Hz,H-2″′),3.29(1H,dd,J=3.0,9.5 Hz,H-3″′),3.08(1H,dd,J=9.5、9.5 Hz,H-4″′),3.27(1H,m,H-5″′),1.00(3H,d,J=6.0 Hz,6″′-CH3)。其1H-、13C-NMR(125 MHz,DMSO-d6,見表1)譜數據與文獻[22]相對照,鑒定該化合物為蘆丁(rutin)。
化合物6:黃色粉末。高分辨Q-TOF-ESI-MS給出其準分子離子峰m/z 771.200 2[M-H]-,確定其分子式為C33H40O21(Calcd for C33H39O21,771.198 9)。1H-NMR(500 MHz,DMSO-d6):δ 6.45(1H,br.s,H-6),6.73(1H,br.s,H-8),7.57(1H,br.s,H-2′),6.86(1H,d,J=8.5 Hz,H-5′),7.55(1H,br.d,ca.J=9 Hz,H-6′),12.60(1H,s,5-OH),5.39(1H,d,J=7.0 Hz,H-1″),3.23(1H,J=7.0、9.5 Hz,H-2″),3.24(1H,J= 9.0、9.5 Hz,H-3″),3.06(1H,J=9.0、9.0 Hz,H-4″),3.25(1H,m,H-5″),[3.47(1H,dd,J=4.5,12.0 Hz),3.71(1H,br.d,ca.J=12 Hz),H2-6″],4.40(1H,br.s,H-1″′),3.38(1H,br.d,ca.J=3 Hz,H-2″′),3.27(1H,dd,J=3.0、9.5 Hz,H-3″′),3.08(1H,J=9.5、9.5 Hz,H-4″′),3.28(1H,m,H-5″′),1.00(3H,d,J=6.5 Hz,6″′-CH3),5.08(1H,d,J=7.5 Hz,H-1″″),3.26(1H,J=7.5、9.5 Hz,H-2″″),3.24(1H,J=9.5、9.5 Hz,H-3″″),3.18(1H,J=9.5、9.5 Hz,H-4″″),3.44(1H,m,H-5″″),[3.30(1H,m,overlapped),3.72(1H,br.d,ca.J=12 Hz),H2-6″″]。其1H-、13C-NMR(125 MHz,DMSO-d6,見表1)譜數據與文獻[23]相對照,鑒定該化合物為quercetin 3-O-(6″-O-α-L-rhamnopyranosyl)-β-D-glucopyranoside-7-O-β-D-glucopyranoside。
4 結果
為了進一步擴大對大漠植物沙蔥的開發與利用,筆者運用色譜和波譜學方法,對沙蔥的化學成分進行了研究,分離并鑒定了以下6個單體成分,分別是異槲皮苷(1)、槲皮素-3-O-(6″-O-乙酰基)-β-D-吡喃葡萄糖苷(2)、槲皮素-3,4′-二-O-β-D-吡喃葡萄糖苷(3)、quercetin-3-O-β-D-glucopyranosyl-(1→4)-β-D-glucopyranoside(4)、蘆丁(5)、quercetin 3-O-(6″-O-α-L-rhamnopyranosyl)-β-D-glucopyranoside-7-O-β-D-glucopyranoside(6)。其中,化合物2、6為首次從蔥屬中分離得到,1、3~5為首次從該植物中分離得到。
5 討論
沙蔥營養成分豐富[24],作為一種可食用綠色植物,已逐漸被人們所熟知。同時,作為一種優等飼料,綿羊飼用后,能夠明顯改善羊肉的口感和味道[25]。
目前,有關沙蔥藥理作用的研究多集中沙蔥多糖上,也有學者曾對沙蔥總提取物進行了研究[26~28],但仍需進一步深入。通常,黃酮類化合物因B環中含有C-2、C-3位雙鍵,C-4位羰基和C-3、C-5位的羥基取代,使得黃酮類化合物具有一定的抗氧化作用,且在防治心血管疾病[29]方面也有潛在的藥用價值,但對于沙蔥中所含的黃酮類化合物僅有少數藥理學方面的研究,對其藥效物質基礎和相應的構效關系以及其他的藥理活性,尚需進行更深層次的研究和探索。
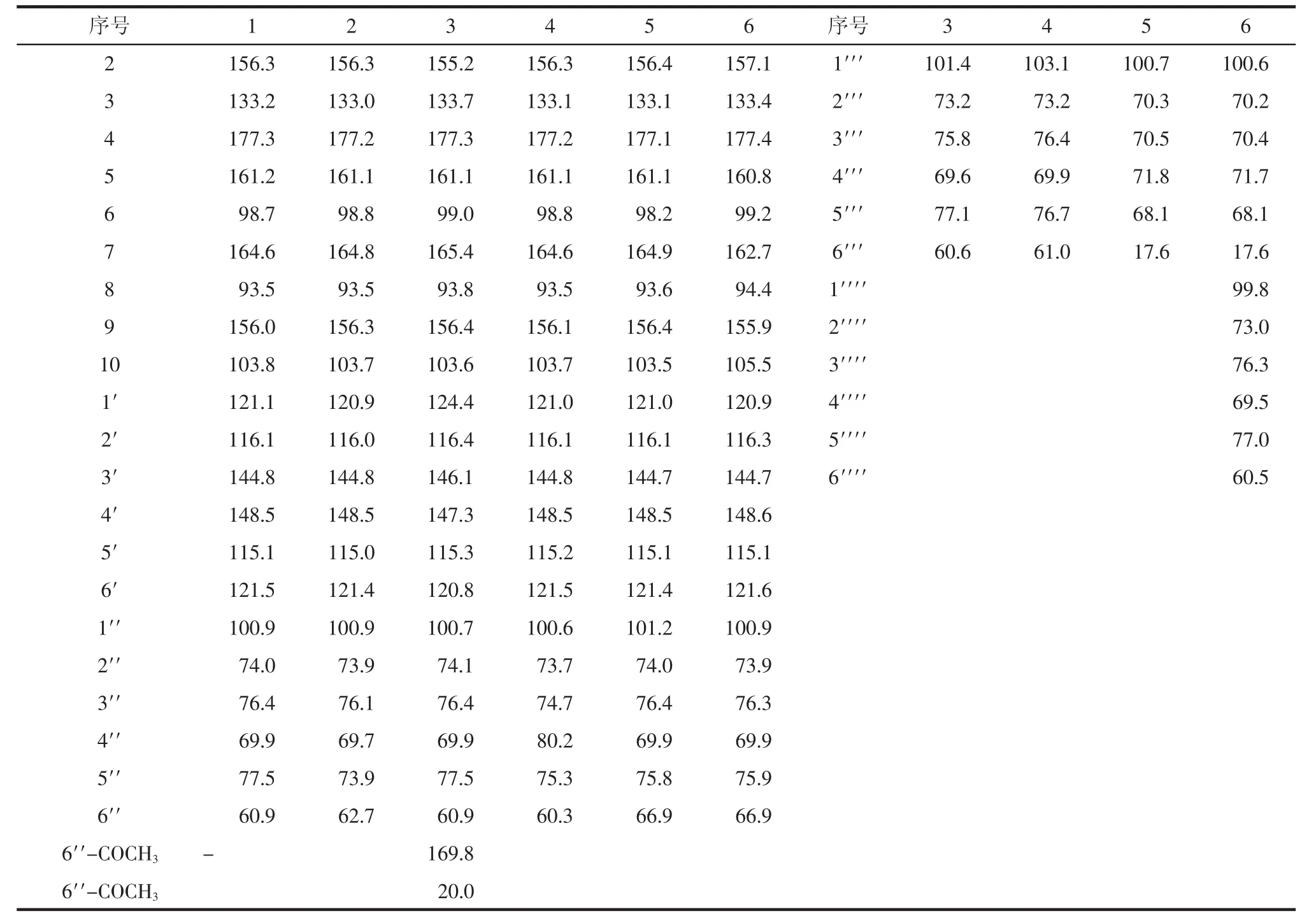
表1 化合物1~6的13C-NMR(125 MHz,DMSO-d6,δ)譜數據
[1]王俊魁.頂空固相微萃取結合氣質聯用分析沙蔥中揮發性成分[J].食品工業科技,2012,33(24):171-173.
[2]斯琴巴特爾,劉新民.蒙古韭的營養成分及民族植物學[J].中國草地,2002,24(3),52-54.
[3]王麗思,敖長金,張興夫.沙蔥多糖對小鼠腹腔巨噬細胞的激活作用[J].中國畜牧獸醫,2010,37(4):50-52.
[4]馬筑泉.內蒙古植物志(第5卷)[M].第2版.呼和浩特:內蒙古人民出版社,1994.
[5]劉英心,楊喜林,姚育英.中國沙漠植物志(第1卷)[M].北京:科學出版社,1987.
[6]陳 山.中國草地飼用植物資源[M].沈陽:遼寧民族出版社,1994.
[7]包美艷,敖長金,趙飛艷,等.沙蔥多糖對綿羊外周血淋巴細胞的調節作用研究[J].飼料工業,2013,34(12):9-12.
[8]藺婷娟.沙蔥多糖對肉羊血液生化指標和腸道粘膜免疫影響的研究[D].呼和浩特:內蒙古農業大學,2011.
[9]薩茹麗,木其爾,王翠芳,等.沙蔥不同部位提取物總黃酮含量及其體外抗氧化、抗菌活性研究[J].食品工業科技,2014,35(22):124-127.
[10]扈瑞平,敖長金,杜 玲,等.沙蔥多糖的體外抑菌試驗研究[J].內蒙古大學學報:自然版,2011,42(3):299-303.
[11]趙飛艷,敖長金,包美艷,等.沙蔥多糖對綿羊外周血淋巴細胞IFN-γ與STAT1 mRNA表達的影響[J].畜牧獸醫學報,2013,44(12):1932-1938.
[12]吳 帥,劉二偉,張 祎,等.川續斷中化學成分的研究[J].天津中醫藥大學學報,2010,29(3):147-150.
[13]劉麗麗,李曉霞,陳 玥,等.槐米中酚酸類化學成分的研究[J].天津中醫藥大學學報,2014,33(1):39-41.
[14]劉麗麗,李曉霞,陳 玥,等.槐米化學成分研究Ⅰ[J].天津中醫藥大學學報,2014,33(4):230-233.
[15]王 強,張 祎,韓立峰,等.中藥川續斷化學成分的研究Ⅲ[J].天津中醫藥大學學報,2014,33(2):108-111.
[16]鄧 屾,劉麗麗,陳 玥,等.益母草化學成分研究Ⅲ[J].天津中醫藥大學學報,2014,33(6):362-365.
[17]吳克磊,康利平,熊呈琦,等.蒺藜全草中甾體皂苷類化學成分研究[J].天津中醫藥大學學報,2012,31(4):225-228.
[18]陳江弢,馮 峰.四川寄生的化學成分研究[J].中藥材, 2007,30(11):1393-1395.
[19]許 芳,趙 軍,徐 芳,等.新疆圓柏枝葉化學成分研究[J].中藥材,2013,36(12):1957-1959.
[20]楊曉虹,劉銀燕,劉麗娟,等.分蘗蔥頭中新黃酮苷的結構鑒定[J].藥學學報,2000,35(10):752-755.
[21]Yamauchi K,Mitsunaga T,Batubara I,et al.Synthesis of quercetin glycosides and their melanogenesis stimulatory activity in B16 melanoma cells[J].Bioorganic&Medicinal Chemistry,2014,22(3):937-944.
[22]劉榮華,余伯陽.山里紅葉化學成分研究[J].中藥材, 2006,29(11):1169-1173.
[23]Lu Y,Sun Y,Foo LY,et al.Phenolic glycosides of forage legume Onobrychis viciifolia[J].Phytochemistry,2000,55(1): 67-75.
[24]張巧娥,敖長金.沙蔥提取物中營養成分分析[J].畜牧與獸醫,2008,40(5):53-54.
[25]盧 媛.沙蔥、地椒風味活性成分及其對綿羊瘤胃發酵和羊肉風味的影響[D].呼和浩特:內蒙古農業大學,2002.
[26]哈斯額爾敦,敖長金,張巧娥,等.沙蔥水溶性提取物對綿羊瘤胃發酵功能(體外)的影響[J].畜牧與獸醫,2008, 40(1),26-31.
[27]張巧娥,敖長金,繆亞娟.沙蔥提取物對綿羊消化道乳酸菌產共軛亞油酸(CLA)含量的影響[J].畜牧與獸醫,2008, 40(12):35-39.
[28]李亞蕾,羅瑞明.沙蔥提取物抗菌效果的研究[J].安徽農業科學,2008,36(33),14596-14597.
[29]Obdulio BG,Julian C,Francisco RM,et al.Uses and properties of citrus flavonoids[J].JAgricFoodChem,1997,45(12): 4505-4515.
Isolation and structural identification of constituents from Allium mongolicm Regel II
DONG Yong-zhe,SHI Wen-zhong,YANG Sheng-cai,LI Xiao-xia,ZHANG Yi,WANG Tao
(Key Laboratory of Traditional Chinese Medicinal Chemistry and Analytical Chemistry of Tianjin,Tianjin 300193,China)
[Objective]Study on chemical constituents of Allium mongolicum Regel.[Methods]The chemical constituents were obtained by Sephadex LH-20 and PHPLC chromatorgraphy isolation,and identified by chemical and spectral analysis.[Results]The structures of six flavonoids were elucidated to be isoquercetin(1),quercetin-3-O-(6″-O-acetyl)-β-D-glucopyranoside(2),quercetin-3,4′-di-O-β-D-glucopyranoside(3),quercetin-3-O-β-D-glucopyranosyl-(1→4)-β-D-glucopyranoside(4),rutin(5),quercetin 3-O-(6″-O-α-L-rhamnopyranosyl)-β-D-glucopyranoside-7-O-β-D-glucopyranoside(6).[Conclusion]Compounds 2,6 were obtained from Allium genus firstly,and 1,3-5 was isolated from the plant for the first time.
Allium mongolicum Regel;chemical constituents;structural identification
R284
A
1673-9043(2016)06-0404-05
2016-08-07)
10.11656/j.issn.1673-9043.2016.06.11
新世紀優秀人才支持計劃資助(NCET-12-1069);天津市高等學校創新團隊培養計劃資助項目(TD12-5033)。
董勇喆(1990-),男,碩士研究生,主要從事中藥化學研究。
王 濤,E-mail:wangt@263.net。

