關于實驗動物國家標準病毒檢測項目思考
佟 巍
( 中國醫學科學院 北京協和醫學院 醫學實驗動物研究所,北京 100021)
?
關于實驗動物國家標準病毒檢測項目思考
佟巍
( 中國醫學科學院 北京協和醫學院 醫學實驗動物研究所,北京100021)
【摘要】通過多年的檢測實踐,筆者建議:① 我國國家標準參照國外實驗動物質量標準設置我國特有的“核心檢測項目”及“備選檢測項目”質量標準。即:將現行國家標準檢測內容設置為“核心檢測項目”,“核心檢測項目”中保留原有的“必檢項目”(即“●”)及“必要時檢測項目”(即“○”);將國家標準中未涉及的病毒檢測內容設置為“備選檢測項”。②目前“核心檢測項目”中大鼠HV及小鼠Ect由“必檢項目”調整為“必要時檢測項目”;大鼠增加對LCMV的檢測要求,設置為“必要時檢測項目”;取消“核心檢測項目”中對TMEV病毒的檢測要求,將該病毒調整為“備選檢測項目”清單中。
【關鍵詞】實驗動物;病毒學檢測
在生命科學研究迅猛發展的今天,實驗動物作為最精密的實驗“儀器”,其標準化要求顯得更為重要,并被世界范圍的科研工作者們所重視。
1國內外實驗動物質量檢測概況
生命科學研究深入發展同時對實驗動物質量提出更高要求。一些發達國家及地區實驗動物機構建議實驗動物生產和使用單位在制定健康監測方案時不僅要考慮實驗動物等級標準,而且還應根據自身實際情況,制定個性化的健康監測方案。
歐洲實驗動物科學協會聯合會(FELASA)每隔幾年更新一版最新的嚙齒類、家兔繁殖和實驗單元的健康監測指導意見[1]。指導意見在全球范圍內得到廣泛的使用,成為實驗動物生產和使用單位健康監測的行動指南。該指導意見2014版涵蓋的病毒檢測項目小鼠19個、大鼠12個,具體見表1、表2[1]。FELASA強調其指導意見是健康監測的最低要求。
美國Charles River是全球最有實力的實驗動物產品和技術服務提供商,其健康監測理念具有很高的參考價值。目前該實驗室健康監測方案涉及病毒檢測項目小鼠18項,大鼠13項,具體見表1、表2。強調指出要根據實際情況制定適合的健康監測方案[2]。
日本實驗動物中央研究所(ICLAS)亦對實驗動物健康檢測方案進行了調整,將實驗小鼠病毒檢測項目20種及大鼠病毒檢測項目12種,分為核心檢測項目(小鼠5種,包括:SV、Ect、LCMV、MHV、HV;大鼠3種,包括:SV、HV、SDAV。)和備選的檢測項目(小鼠13種,包括:Mad(FL)、Mad(K87)、GD7/TMEV、MVM、PVM、Reo-3、EDIM、KV、mouse cytomegalovirus、MPV、MTLV、MNV、POLY;大鼠9種,包括:Mad(FL)、Mad(K87)、GD7、MVM、PVM、Reo-3、H-1、KRV、RPV)。他們還將感染性病原分為A、B、C、D、E五類,涉及病毒的有三類:A人獸共患病,2種(LCMV、HV);B實驗動物烈性傳染病,3種(Ect、MHV、SV);C隱性感染性疾病,15種(EDIM/Rota、LDHV、MAd、MCMV、GD7/TMEV、MNV、POLY、PVM、Reo-3、MVM、KRV、H-1、MPV、RPV、SDAV)。檢測內容基本涵蓋了Charles River Laboratories的病毒檢測內容。還有其他國家及地區檢測清單中沒有的檢測項目(鼠星狀病毒murine astrovirus)。(http://www.iclasmonic.jp/microbiology/inspection/mouse.html)
我國實驗動物國家標準(GB14922.2-2011)規定實驗小鼠病毒檢測項目11種,其中必檢項目6種(Ect、MHV、SV、PVM、Reo-3、MVM),必要時檢測項目5種(LCMV、HV、GD7/TMEV、MAd、POLY);大鼠病毒檢測項目8種(HV、SV、PVM、Reo-3、H-1/KRV、RCV/SDAV),全部為必檢項目[3]。

表1 國內外實驗小鼠病毒檢測項目
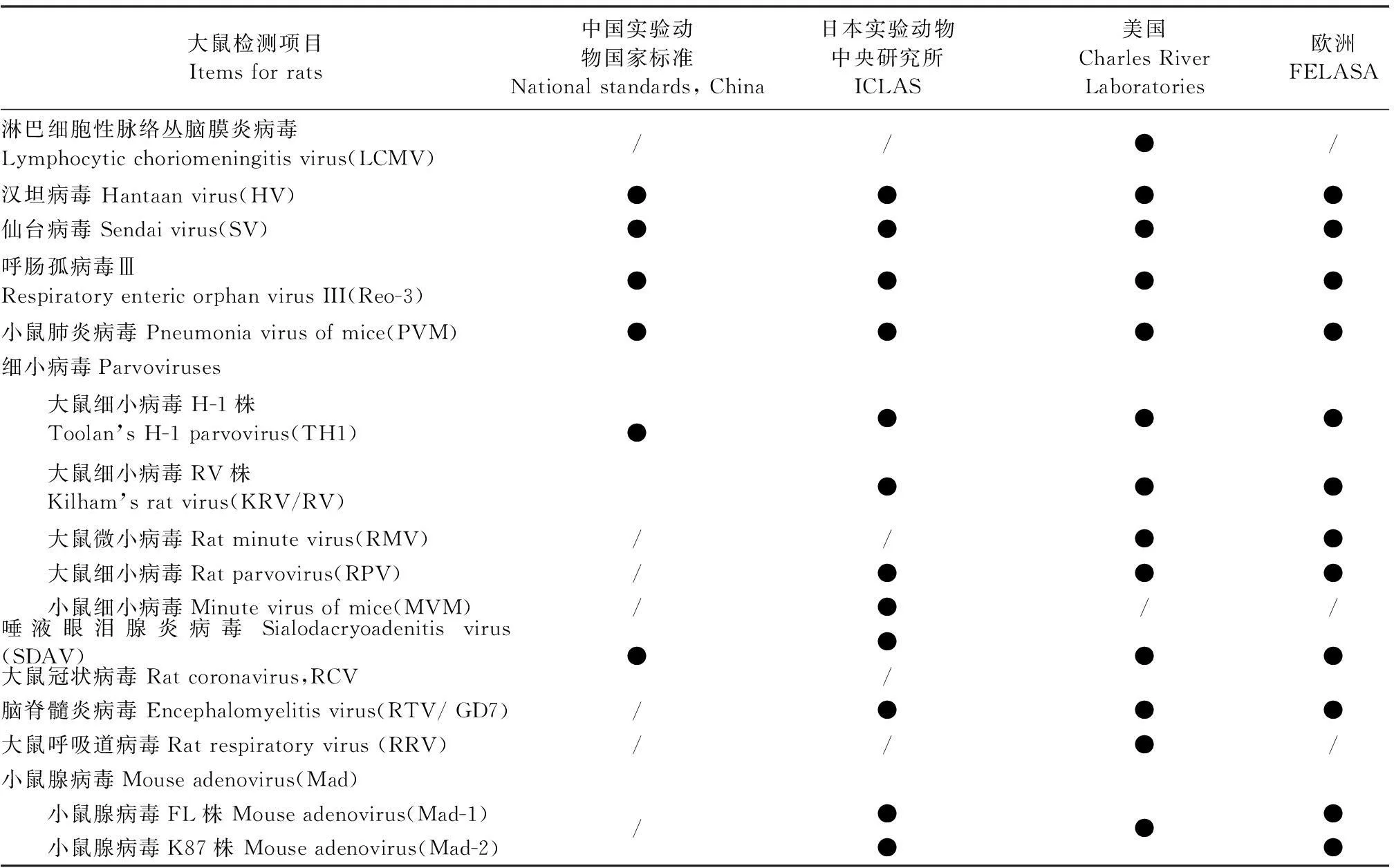
表2 國內外實驗大鼠病毒檢測項目
2病毒病原對動物健康及實驗研究的影響
早在1991年美國《Biology and Life Sciences - Lab Animal Research》就不同感染性疾病對實驗研究帶來的影響進行了闡述。1998年美國《Clinical Microbiology Reviews》亦對同樣問題進行了論述。他們均就不同病原對動物機體功能系統帶來的危害進行了詳盡說明[4-6]。見表3。
2.1呼吸系統疾病是小鼠、大鼠最常見健康問題
實驗小鼠、大鼠呼吸道病毒病原為SV、PVM、RCV、KV。常為隱性感染導致亞臨床癥狀,實驗條件下也可導致疾病的發生。通常與其它病原微生物合并感染后導致嚴重呼吸道疾病。SV感染易感小鼠或免疫缺陷鼠可導致疾病甚至死亡,是重要的實驗鼠群的病毒性傳染病之一,干擾生理、病理、免疫學及腫瘤學方面的研究;PVM是重要的呼吸道病毒,自然條件下可感染實驗鼠,對免疫缺陷鼠具有致病性,主要干擾生理、病理及腫瘤學方面的研究;RCV是感染率最高以及嚴重干擾實驗,胸腺缺如大鼠更為易感;KV實驗小鼠中較為少見,實驗感染裸鼠可致病。
2.2消化系統疾病在小鼠和大鼠中極為常見
乳鼠或幼鼠感染病原體會對消化系統帶來最嚴重的影響,產生明顯的臨床癥狀。當它們離乳或剛剛成年后臨床癥狀可能已不存在,也可能出現更加明顯消化道疾病臨床癥狀(例如腹瀉和生長阻滯)而未被發現。這些病毒病原包括:MCMV、RCMV、MPV、MTV、SDAV、MHV、MRV/ EDIM、RRV、Reo-3、Adenoviruses等。SDAV、MHV成年鼠常為隱性感染,新生鼠感染死亡率極高,是感染率最高以及嚴重干擾實驗的病原體,干擾腫瘤學、免疫學、生理學及生殖技術方面的實驗研究;MRV/ EDIM只對新生小鼠致病;大鼠感染Reo-3非常少見,一旦感染可能會干擾腫瘤移植和利用這些動物細胞進行的體外試驗;曾有RRV感染導致消化系統疾病的報道;RCMV感染在實驗鼠中極為罕見,野生鼠中較為常見,可以通過潛伏感染大鼠器官移植轉移到受體大鼠器官;MTV可通過亞臨床感染小鼠組織感染幼鼠對實驗造成復雜的影響;MCMV未見自然感染報道,實驗接種該病毒可引起嚴重干擾免疫反應;MPV是感染實驗小鼠非常重要的病原體之一,病毒感染免疫活性的小鼠后病毒可在胰腺、小腸淋巴器官,肝臟中復制,并可能持續幾個星期,病毒感染免疫缺陷小鼠后病毒可在機體內廣泛存在;腺病毒(adenoviruses)包括K87及FL株(也稱為MAd-1及MAd-2),MAd-1感染可對成年小鼠造成廣泛持久的病變。
2.3皮膚和關節異常在實驗鼠群中較為常見
可造成實驗鼠皮膚和關節異常的病毒病原有:Ect、RPV、mouse papule virus和MMTV。Ect感染常為亞臨床活動性,易感動物感染幾乎全部死亡,是重要的小鼠烈性傳染病,污染的動物組織及生物制品是實驗室間傳播的主要方式;RPV實驗鼠群中較少見,可隱性感染,易感動物感染死亡率幾乎50%,大鼠感染可造成肺、皮膚、肺及皮膚三種類型的損害;Mouse papule virus患病小鼠在腳和尾巴出現中央縮進或類似酒窩的丘疹,患處水腫和充血,皮膚損傷類似的鼠痘;MMTV高度致癌,是導致小鼠乳腺瘤的病毒。
2.4某些病原將機體的造血系統作為它們的主要目標組織
它們包括:LCMV、LDHV、MuLVs。LCMV是非常重要的人畜共患傳染病病原,盡管傳統被認為是中樞神經系統的主要病原體,實際上該病原主要損害的是機體的造血系統,主要影響免疫學、生理學和生理機能方面的研究;LDHV是小鼠腫瘤組織的常見污染物,感染鼠血清乳酸酶可增加5~10倍;MuLVs是一群基因相關的病毒被統稱為小鼠白血病病毒,許多近交系小鼠敏感,與腫瘤發生相關。
2.5影響中樞神經系統的病毒是TMEV/GD7
少有自然感染,實驗鼠感染該病毒出現類似人類感染脊髓灰質炎病毒的表現。
2.6對機體多系統造成損害的病毒病原有:KRV、H-1、MVM、MHV、POLY、HV、SDAV、MNV
KRV及H-1是細胞及生物制品的常見污染物,很少有自然感染,感染可能會干擾胎兒發育導致畸形發生;MVM在小鼠中流行較為廣泛,是移植腫瘤及敏感動物細胞系的常見污染物,感染對于大多數的研究幾乎沒有意義,但對小鼠移植腫瘤、白血病和體外免疫測定等研究非常重要。常會干擾病理學、免疫學、生理學、細胞生物學、發育學及腫瘤學等方面的研究;POLY也是移植腫瘤及細胞系的常見污染物,自然感染免疫正常鼠對實驗影響可能較小,沒有POLY污染的鼠群一旦感染新生鼠可引起腫瘤廣泛分布造成免疫力低下從而影響實驗;HV是最重要的人畜共患病之一,可造成實驗大鼠持久的亞臨床感染,導致嚴重疾病;MNV在實驗鼠群中感染率較高,免疫健全小鼠感染不引起臨床癥狀,一些品系的免疫缺陷鼠可引起感言、間質性肺炎、腦炎等,從而影響實驗。
3關于健康檢測計劃的制定
似乎制定更為全面的健康監測方案,采用更嚴格的微生物控制水平,才是實驗動物健康以及動物實驗可重復性的重要保證。然而在實際工作中,經濟成本、可操作性以及對實驗動物自然狀態模擬等因素是必須考慮的問題。因此,采用最嚴格的微生物控制水平排除所有病原,使用最高級別的實驗動物并不一定是最適合的[7、8]。
對于動物飼養機構來說,采用最嚴格的控制措施的確會浪費很多資源。實際上,有些病原體是相當難以清除的,一些動物設施實驗動物鼠群中存在一種或幾種病原感染的現象,所以徹底消除這些病原體是不現實的,應優先消除人獸共患病、動物烈性傳染病以及對研究數據影響較大的病原體。并且,在有可能根除某病原時對其監測才有意義[7、8]。
對于實驗動物使用者來說,實驗動物健康監測方案應根據研究目的來制定,不同類型的科研項目不應使用同一種健康監測方案。實驗人員應首先該考慮研究項目需要選擇何種級別的實驗動物,還要考慮需排除哪些可能干擾實驗的其它病原以及實驗設施或本地區的病原流行情況,才能制定更為科學的健康檢測及監測方案[7、8]。
4對現行國標檢測項目的建議
目前,我國實驗動物國家標準(GB14922.2-2011)病毒檢測與歐美日等國家和地區相比,涉及的檢測項目相對較少,一些新興的影響實驗動物及動物實驗的傳染性病原未能涉及。
筆者建議,設置我國特有的核心檢測項目(包括人獸共患病及實驗動物烈性傳染病,為最低檢測要求)及“備選檢測項目”(主要是隱性感染性病原,根據需要進行選擇)。借鑒這樣的分類方法既便于實驗動物工作者識別病原危害程度及可能存在潛在影響的因素,設計出符合實際需要的健康監測計劃,又可為實驗動物商品化、國際化以及科研信息的交流提供必要的保障。“備選檢測項目”可根據需要從中選擇,不做強制要求。“備選檢測項目”應包含盡可能多的檢測內容,提供更為廣泛的健康監測范圍,最大程度地滿足不同實驗需要。

表3 影響實驗動物小鼠、大鼠質量的病毒病原
備注:*存在感染的可能;**敏感;
另外,通過回顧十余年來我實驗動物質量檢測中心對二十余家實驗動物飼養及使用單位的大鼠、小鼠活體及血清樣本的檢測結果,通過查閱十余年來我國部分檢測實驗室的大鼠、小鼠病毒檢測報告,發現大鼠HV病毒、小鼠Ect病毒、GD7/TMEV病毒抗體檢出率呈極低水平或未曾檢出,在普通實驗大鼠血清樣品抽查過程中發現有人獸共患病LCMV病毒的檢出[9]。
綜上所述,作者建議實驗動物國家標準的等級標準中,調整大鼠HV及小鼠Ect由“必檢項目”(即“●”)調整為“必要時檢測的項目”(即“○”);在大鼠“核心檢測項目”清單中增加對LCMV的檢測要求,設置為“必要時檢測項目”(即,“○”);取消對TMEV病毒的檢測要求,將該病毒列至“備選檢測項目”清單中。見表4、表5。

表4 實驗動物大鼠、小鼠病毒檢測項目之——核心檢測項目
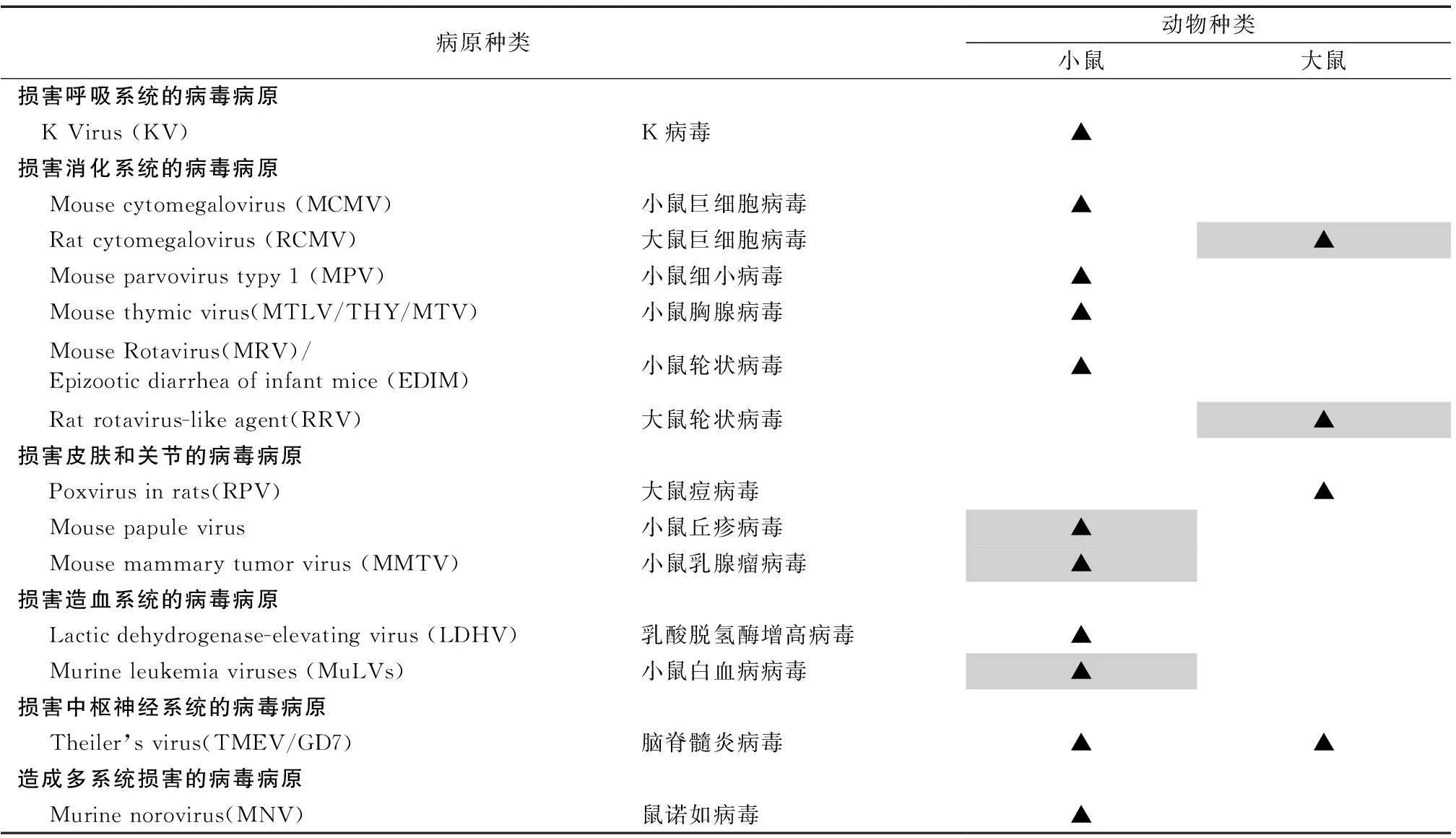
表5 實驗動物大鼠、小鼠病毒檢測項目之——備選檢測項目
注:根據實驗需要,選擇需要排除的病毒病原。備注:表格中“▲”的檢測項目為日本ICLAS、美國Charles River Laboratories、歐洲FELASA沒有列出的檢測項目。
參考文獻:
[1]M?hler (Convenor) M, Berard M, Feinstein R, et al. FELASA recommendations for the health monitoring of mouse, rat, hamster, guinea pig and rabbit colonies in breeding and experimental units [J]. Lab Anim Poblished Online, February 4, 2014,48(3):178-192.
[2]Clifford CB. Routine Health Monitoring of Charles River Rodent Barrier Production Colonie in Europe and North America [S]. Charles River Research Models. Technical Sheet. Charles River 2014, Laboratory International, Inc. http://www.criver.com/files/pdfs/rms/hmsummary.aspx
[3]GB/T14922.2-2001. 實驗動物微生物學等級及監測[S]. 中國人民共和國國家質量監督檢疫檢疫總局, 2011:1-6.
[4]Baker DG. Natural pathogens of laboratory mice, rats, and rabbits and their effects on research [J]. Clin Microbiol Rev, 1998; 11(2): 231-266.
[5]Infectious Diseases of Mice and Rats Committee on Infectious Diseases of Mice and Rats, Institute of Laboratory Animal Resources, Commission on Life Sciences, National Research Council. Infectious Diseases of Mice and Rats [M]. National Academy Press, Washington, D.C. 1991. ISBN: 0-309-55692-9. http://www.nap.edu/catalog/1429.html.
[6]Microbial and Phenotypic Definition of Rats and Mice: Proceedings of the 1998 US/Japan Conference [C]. International Committee of the Institute for Laboratory Animal Research, National Research Council. ISBN: 0-309-52018-5, (1999). http://www.nap.edu/catalog/9617.html.
[7]龐萬勇,賀爭鳴. 實驗用生物樣品的嚙齒類微生物污染的檢測管理中國比較醫學雜志 [J].中國比較醫學雜志, 2011, 21(10): 94-98.
[8]范文平, 賀爭鳴. 西方國家實驗動物健康監測的理念 [J]. 實驗動物科學, 2011, 23(43): 62-67.
[9]佟巍, 喬紅偉, 魏強, 等. 淋巴細胞脈絡叢腦膜炎病毒在實驗大鼠中的感染狀況 [J]. 醫學動物防治, 2010, 27(4): 46-48.
〔修回日期〕2015-12-27
Consideration of the virological items in the National Standard of Laboratory Animals
TONG Wei
(Institute of Laboratory Animals, Chinese Academy of Medical Sciences & Peking Union Medical College, Beijing 100021,China)
【Abstract】Based on the practice in laboratory animal monitoring, the following issues are suggested: (1) The core items and candidate items should be separated in the National Standard; (2) Hantaan virus and Ect virus should be omitted in the core list for mice; LCMV should be monitored as a candidate item for rats; TMEV should be listed as candidate item.
【Key words】Laboratory animals, Virological monitoring
doi:10.3969.j.issn.1671-7856. 2016.02.009
【中圖分類號】R-33
【文獻標識碼】A
【文章編號】1671-7856(2016) 02-0042-06
[通訊作者]佟巍(1972-),女,主管技師,實驗動物病毒學免疫學。E-mail: twtongwei@sina.com。
“實驗動物國家標準論壇”專題

