高三化學電源電極反應式書寫的思維建模教學策略
吳利敏 熊建飛
摘要:針對高考試題對化學電源電極反應式考查的特點,提出了回歸教材,以堿性鋅錳電池為例,對化學電源電極反應式書寫進行思維建模,構建電極反應式書寫模型:先寫出電池構成,再運用兩個意識。
關鍵詞:電極反應式; 思維建模;電池構成;兩個意識
文章編號:1008-0546(2016)06-0034-02 中圖分類號:G633.8 文獻標識碼:B
doi:10.3969/j.issn.1008-0546.2016.06.010
思維建模的方法適用于自我建構知識,是教師創設建構主義課堂的一把鑰匙。思維建模能夠幫助學生豐富和拓展知識結構,使學生用已有的知識構建起自己的思維模型,在建模的過程中積極地調整與修改原有知識結構,做到對知識和方法的內化。在高三化學復習課中,運用思維建模能夠有效的幫助學生建構知識體系,提高對知識遷移應用的能力。
化學電源電極反應式的書寫是高考的熱點,大多數題的特點是新,讓學生感覺很陌生,有點無從下手。其實只要掌握好原電池基本原理,運用兩個意識,此類題型就迎刃而解。本文擬回歸教材、挖掘教材,尋找高考試題與教材的聯系,進行思維建模,構建電極反應式書寫模型:先寫出電池構成,再運用兩個意識。
一、真題分析
真題一(2015課標Ⅱ) 酸性鋅錳干電池是一種一次性電池,外殼為金屬鋅,中間是碳棒,其周圍是由碳粉、MnO2、ZnCl2 和 NH4Cl等組成的糊狀填充物。 該電池放電過程產生MnOOH。 回收處理該廢電池可得到多種化工原料。
(1)該電池的正極反應式為 ,電池反應的離子方程式為 。
[試題分析] 此題與人教版《化學反應原理》中堿性鋅錳電池原理一樣,只不過這個電池是酸性鋅錳電池。在書寫電極反應式時,若不注意電池的環境(酸性環境),則很容易寫錯。
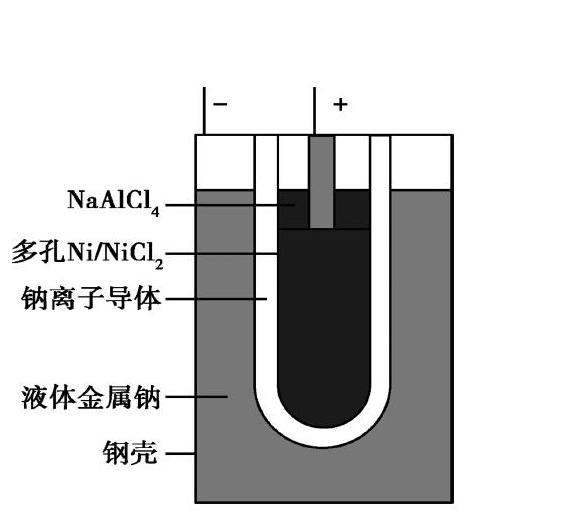
真題二(2013課標Ⅱ)“ZEBRA”蓄電池的結構如圖所示,電極材料多孔Ni/NiCl2和金屬鈉之間由鈉離子導體制作的陶瓷管相隔。下列關于該電池的敘述錯誤的是
A.電池反應中有 NaCl 生成
B.電池的總反應是金屬鈉還原三價鋁離子
C.正極反應為:NiCl2+2e- Ni+2Cl-
D.鈉離子通過鈉離子導體在兩電極間移動
[試題分析] 此題所給電池是一種新型化學電源,其特點是新,讓學生感覺陌生,不知怎樣下手。
真題三(2013課標Ⅰ) 銀質器皿日久表面會逐漸變黑,這是生成了Ag2S的緣故。根據電化學原理可進行如下處理:在鋁質容器中加入食鹽溶液,再將變黑的銀器浸入該溶液中,一段時間后發現黑色會褪去。下列說法正確的是
A.處理過程中銀器一直保持恒重
B.銀器為正極,Ag2S被還原生成單質銀
C.該過程中總反應為 2Al+3Ag2S 6Ag+Al2S3
D.黑色褪去的原因是黑色Ag2S轉化為白色AgCl
[試題分析] 此題對學生來說感覺很陌生,不知道怎樣入手,其實這是一道基于原電池原理的電化學試題,只不過比較隱含,需要學生用原電池基本原理去挖掘。
二、思維建模
以人教版《化學反應原理》中堿性鋅錳電池為例,對基于原電池原理的電化學試題進行思維建模。
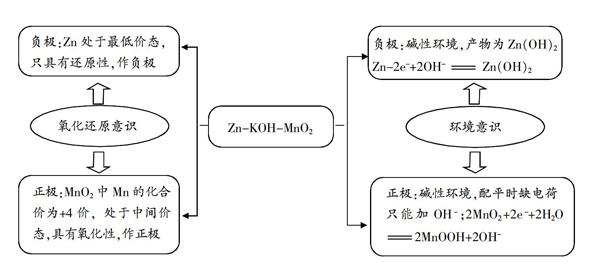
化學電源必備的兩個條件:兩個電極、電解質溶液。堿性鋅錳電池的兩個電極分別是Zn和MnO2,電解質溶液為KOH溶液,可以簡單地表示為:Zn—KOH—MnO2(電池構成)。根據氧化還原反應的規律,因為Zn只具有還原性,可以判斷出Zn作負極; MnO2中Mn的化合價為+4價,處于中間價態(Mn的化合價一般有0、+2、+3、+4、+6、+7價),具有氧化性,由于Zn只能做負極,因此MnO2做正極。在書寫電極反應式時,要考慮環境意識,即電極反應產物所處的環境,如在書寫負極反應時,Zn失電子變為Zn2+后還要和OH-生成Zn(OH)2沉淀。在書寫正極反應式時,2MnO2+2e-+2MnOOH +配平電荷守恒只能在右邊加OH-離子,而不能在左邊加H+,因為這是堿性環境。
由此得出化學電源電極反應式書寫思維模型:先寫出電池構成,再運用兩個意識。
三、遷移應用
真題一 (2015課標Ⅱ)
電池構成:Zn—ZnCl2、NH4Cl(酸性)—MnO2,根據氧化還原意識,Zn作負極,MnO2作正極。根據環境意識,書寫電極反應式,負極:Zn-2e-■Zn2+,正極:2MnO2+2e-+2H+2MnOOH,總反應為:2MnO2+Zn+2H+2MnOOH+Zn2+。
真題二(2013課標Ⅱ)
運用化學電源思維模型,首先寫出電池構成:Na—鈉離子導體—Ni/NiCl2。根據氧化還原意識,Na只具有還原性,作負極;NiCl2中鎳的化合價為+2價,具有氧化性,作正極。根據環境意識,書寫電極反應式,負極:2Na-2e-2Na+,正極:NiCl2+2e-Ni+2Cl-,總反應為:2Na+NiCl22Na++Ni+2Cl-。由此判斷出B選項錯誤
真題三(2013課標Ⅰ)
此題信息較為隱含,從題干中能看出考查的是電化學方面的知識。從題給信息來看是對原電池基本原理的考查,雖然不是化學電源,但原理卻是一樣的。應用思維模型,寫出電池的構成:Al—NaCl—Ag2S,根據氧化還原意識,Al作負極,Ag2S作正極。根據環境意識書寫電極反應式,負極:2Al-6e-2Al3+,正極:3Ag2S +6e-6Ag+3S2-,在寫總反應時,要注意Al3+與S2-在水溶液中要發生徹底雙水解,總反應為:2Al+3Ag2S+6H2O2Al(OH)3↓+6Ag+3H2S↑。由此分析可得正確答案為B。
四、教學反思
在思維建模時,要回歸教材,在教材中尋找原點并進行深入挖掘,所建的模型要具有代表性和一定的適用性。有效的思維建模會給學生留下深刻的印象,并具有本模型的典型特征,如化學電源電極反應式的書寫模型的典型特征:先寫出電池構成,再運用兩個意識。
參考文獻
[1] 趙 蘋.生物教學中實施思維建模的策略[J].新課程學習:社會綜合,2010,(7):125
[2] 仇雪梅.基于控制論建構主義的思維建模的應用研究[D].南寧:廣西師范學院,2010:4-6

