藥物性肝損傷臨床特點及致病藥物回顧性分析
李 俊,黃紹萍,陸基華,殷科珊,樊貞瑜,唐 榮,徐 烈,程計林
上海市(復旦大學附屬)公共衛生臨床中心消化科,上海 201508
藥物性肝損傷臨床特點及致病藥物回顧性分析
李 俊,黃紹萍,陸基華,殷科珊,樊貞瑜,唐 榮,徐 烈,程計林
上海市(復旦大學附屬)公共衛生臨床中心消化科,上海 201508
目的 探討藥物性肝炎患者的致病藥物和臨床特征,評價可疑藥物與疾病的相關性,提高臨床醫師對藥物性肝炎的認識。方法 回顧性總結2013年2月-2015年4月收治的198例藥物性肝炎患者的臨床資料,根據其用藥種類、臨床表現、實驗室檢查、發生藥物性肝炎的時間及停藥后的治療效果進行綜合分析。結果 藥物性肝炎發生在用藥后4周內最多見(116/198,占58.59%)。誘發藥物性肝炎的藥物中,以中藥(99/198,占50.00%)、抗結核藥(48/198,占24.24%)、抗感染藥(15/198,占7.58%)多見,其他導致肝損傷的藥物還有解熱鎮痛藥、抗腫瘤藥、抗精神病藥、降血脂藥、降血壓藥、降血糖藥、抗風濕藥、抗真菌藥、抗痛風藥、胃藥等(36/198,占18.18%)。臨床表現以肝細胞損傷型最多(144/198,占72.73%),重度肝損傷占64.14%(127/198)。結論藥物性肝損傷呈重度化趨勢,尤其以中藥比例居高,須警惕。
藥物性肝炎;致病藥物;臨床特點
肝損傷在臨床上很常見,近年來,隨著制藥技術的進步、新藥的不斷問世及人們對健康狀況的重視,藥物性肝炎的發病率呈逐年升高趨勢。據文獻[1]報道藥物性肝損傷(drug-induced liver injury,DILI)占所有藥物反應病例的10%~15%,嚴重者甚至出現急性肝功能衰竭等危及生命的并發癥。藥物性肝炎日益成為一個世界性的大問題。據報道[2],西方國家藥物引起肝衰竭占全部肝衰竭患者的10%~52%,病死率約為11.9%[3]。而藥物性肝炎的臨床表現多種多樣,診斷缺乏特異性指標,常易導致誤診、漏診[4],嚴重者可導致肝功能衰竭死亡。本文對198例藥物性肝炎患者的臨床資料進行綜合分析,旨在探究近年藥物性肝炎的臨床特點。
1 資料與方法
1.1 一般資料 收集2013年2月-2015年4月住院的藥物性肝炎患者198例,治療前均有明確的服藥史,均符合藥物性肝炎診斷標準[5]。男96例,女102例,男女比例1∶1.1。年齡3~81歲,平均年齡(49±15)歲,其中≤20歲5例(2.53%),21~40歲50例(25.25%),41~60歲103例(52.02%),≥61歲40例(20.20%)。
1.2 診斷標準 根據2004年DDW會議上日本肝病學會提出藥物性肝損傷診斷標準[5],對用藥與臨床癥狀出現的時間關系、病程中生化指標、嗜酸性粒細胞、有無飲酒或妊娠、除外其他原因、有意或無意再用藥、所用藥物既往有無肝損傷報告等方面進行量化評分。最后判斷:≤2分,藥物性肝炎可能性低;3~4分,藥物性肝炎有可能;≥ 5分,藥物性肝炎可能性大。本組198例患者,其中≤4分12例(6.06%),≥ 5分186例(93.94%)。
1.3 排除標準 (1)不符合藥物性肝炎的常見潛伏期;(2)停藥后肝臟異常升高指標不能迅速恢復;(3)有導致肝損傷的其他病因或疾病的臨床證據。如果具備第(3)項,且具備第(1)、(2)項中的任何一項,則認為藥物與肝損傷無相關性,可臨床排除藥物性肝炎。
1.4 臨床分型 參照CIOMS(國際醫學科學組織委員會)藥物性肝炎分型標準[6],分為:(1)肝細胞損傷型:定義為血清谷丙轉氨酶>2倍正常值上限或血清谷丙轉氨酶/血清堿性磷酸酶升高倍數比值≥5;(2)膽汁淤積型:定義為血清堿性磷酸酶升高程度>2倍正常值上限或血清谷丙轉氨酶/血清堿性磷酸酶升高倍數比值≤2;(3)混合型肝損傷:定義為血清谷丙轉氨酶與血清堿性磷酸酶升高倍數比值介于2~5。
1.5 肝損害程度 (1)輕度:臨床癥狀、體征輕微或缺如,肝功能指標僅1或2項輕度異常,ALT≤2倍正常值上限,或TBIL≤2倍正常值上限;(2)中度:癥狀、體征、實驗室檢查居于輕度和重度之間,2
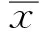
2 結果
2.1 出現藥物性肝炎的時間分布 導致藥物性肝炎的藥物種類較多,不同類型的藥物服藥后發生藥物性肝炎的時間略有差異。大多數藥物性肝炎出現在服藥后8周以內,其中發生在用藥后4周內占58.59(116/198)(見表1)。

表1 不同類型的藥物發生藥物性肝炎的時間分布[例數(%)]Tab 1 Time distribution of different types of medicines in drug-induced hepatitis[n(%)]
2.2 臨床表現 乏力82例(41.41%),納差74例(37.37%),惡心46例(23.23%),其中16例出現嘔吐,上腹部飽脹不適42例(21.21%),厭油10例(5.05%),發熱21例(10.61%),皮膚瘙癢10例(5.05%),皮膚黏膜及鞏膜黃染81例(40.91%),尿黃34例(17.17%),皮疹2例(1.01%),少數患者還表現為肝區不適、腹痛、腹瀉等,有33例(16.67%)無明顯臨床癥狀,主要是體檢發現。
2.3 引起藥物性肝炎的藥物種類 中藥導致的藥物性肝炎99例(50.00%),包括中藥湯劑和中成藥 (中藥湯劑中多包含雷公藤、何首烏、青黛、苦參、麝香、肉豆蔻、烏頭、斑蝥、三七等,中成藥有風濕骨痛膠囊、復方青黛膠囊、濕毒清膠囊、殼脂膠囊等),高于其他各類藥;其次為抗結核藥48例(24.24%),患者均聯合使用抗結核藥物[主要有異煙肼(isoniazid,INH)、利福平(rifampin,RFP)和吡嗪酰胺(pyrazinamide,PZA)等];抗感染藥15例(7.58%),主要是左氧氟沙星和克拉霉素等;解熱鎮痛藥12例(6.06%),抗腫瘤藥3例(1.52%),其他藥物(包括降血脂藥、降血壓藥、降血糖藥、抗風濕藥、抗真菌藥、抗痛風藥、胃藥等)21例(10.61%)。
2.4 肝損傷分型 本組資料顯示,藥物性肝炎發病以肝細胞損傷型為主,占72.73%(144/198),其次為膽汁淤積型(24.24%,48/198)和混合型肝損傷(3.03%,6/198)。
2.5 肝損傷程度 從肝臟損傷的程度分析,總體損傷重,其中重度占64.14%(127/198),重型占2.02%(4/198),中度占33.33%(66/198),輕度只占0.51%(1/198)。
2.6 實驗室檢查 三組患者實驗室檢查通過統計學分析顯示,TB、DB、CHE、TBA差異均無統計學意義(P>0.05);膽汁淤積型的ALT、AST與其他兩組比較,差異均有統計學意義(P<0.05);三組中AKP兩兩比較,差異均有統計學意義(P<0.05);而GGT只有肝細胞損傷型與混合型之間差異有統計學意義(P<0.05,見表2)。
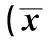
表2 各臨床類型中相關實驗室指標檢測結果±s)Tab 2 Related laboratory indexes in all clinical types of drug-induced ±s)
注:與膽汁淤積型相比,*P<0.05;與混合型肝損傷相比,※P<0.05。
2.7 治療及轉歸 198例患者入院后均立即予以停用提示可能導致肝損傷的藥物,予以保肝、降酶、退黃等治療。平均住院天數為(20.8±14.8)d。195例(98.48%)患者好轉或治愈,2例(1.01%)自動出院,1例(0.51%)死于肝衰竭。
3 討論
本研究結果表明,藥物性肝炎女性患者稍多見,考慮多與女性的性激素水平有關,雌激素和孕激素的水平可以使肝酶活性增加,從而增加藥物的積累或減少藥物的清除[8]。從發病年齡方面看,中老年發病率較高,考慮與中老年罹患疾病概率較大、用藥機會較多有關,同時隨年齡增長,體內藥物代謝的酶系總活性降低,肝臟血流量減少也是藥物代謝功能減退的重要原因[9]。
藥物性肝病的發生時間因藥物類型不同而有所不同[10]。從本組資料看,藥物性肝炎最快可以發生在服藥后1~2 d,抗感染藥用藥時間短,藥物性肝炎多發生在1周之內,其他需要長期治療的藥物導致藥物性肝炎,大多數在用藥后8周內產生,占73.74%(146/198)。由此可見,藥物性肝炎多發生在服藥的前2個月,提示我們用藥注意監測肝功能,尤其是用藥前2個月,注意護肝治療。
據報道[11],可引起肝損傷的藥物至少有1 000余種,國外報道[12]以抗生素為主,國內報道[13]以抗結核藥為主。本組資料中引起肝損傷的藥物幾乎包括臨床各科用藥,中藥所占比例最高,其次為抗結核藥物和抗生素。長期以來,人們一直認為中藥安全性高,但近年來隨著中藥的廣泛應用,中藥引起藥物性肝炎所占的比例在不斷增加。本組研究中,中草藥及中成藥所致肝損傷比例最大,與文獻報道一致[4]。中藥治療引起肝損傷,機制尚未完全明確。究其原因主要為中藥及中成藥成分復雜,往往為多種藥物混在一起煎制而成,缺乏臨床試驗對照研究及藥物毒理試驗;而肝臟作為人體主要的藥物代謝器官,中藥及其制品代謝產生的活性中間產物,可以和蛋白質、脂類及核酸等細胞大分子反應,導致蛋白質功能失調、脂質過氧化、DNA的損傷及氧化應激;同時這些活性中間產物可以引起細胞內離子梯度和儲存鈣的變化,導致線粒體損傷和能量產生障礙,從而引起肝細胞死亡甚至肝臟衰竭[14]。另外可能與品種、污染(包括農藥殘留)炮制和制劑工藝等諸多因素有關,此外劑量(單次劑量與總量)、療程與配伍、個體差異等影響因素有關[15]。因此我們必須對中草(成)藥可能出現的危害引起足夠的重視,在臨床藥物應用期間,肝功能的監測必不可少。
DILI的臨床表現無特異性,主要表現乏力、納差、惡心、嘔吐、上腹部飽脹不適等癥狀,部分以皮膚黏膜及鞏膜黃染、尿黃而就診,而部分患者無明顯臨床癥狀,主要是體檢發現肝功能異常。這些患者中不乏因消化道癥狀發病診斷為“胃病”,治療無效而導致病情延誤者。實驗室檢查中主要表現為肝功能異常,無特異性,嗜酸性粒細胞比例>6%的患者僅占12.63%(25/198)。這些與病毒性肝炎、梗阻性黃疸,特別是慢性乙型肝炎發作時的常見癥狀無明顯差異,原有基礎肝病或其他基礎性疾病的患者更容易誤診、漏診,且無特異性的實驗室檢查,更加給我們診斷帶來困難。因此診斷藥物性肝炎應詳細詢問病史,全面根據臨床表現及實驗室檢查分析,注意鑒別,盡可能做到不漏診、不誤診。
從肝臟損傷的程度分析,總體損傷重,導致重度藥物性肝炎考慮與下列原因有關:(1)許多藥物性肝炎起病隱匿,早期無特征性表現,如果對此缺乏認識,服藥期間未能定期檢查肝功能,以致發展為重度肝損傷。本組中33例患者無臨床癥狀,12例進展致重度。(2)因藥物性肝炎缺乏特異性臨床表現,臨床上以消化道癥狀就診患者較多,易誤診為“胃病”,導致患者出現肝功能異常后仍繼續用藥,使病情在用藥中不斷加重。(3)聯合用藥導致DILI加重,可能與藥物之間存在相互作用有關,48例聯合抗結核治療患者,有25例重度,2例重型。(4)中藥成分復雜,制備工藝參差不齊,服用周期長,且個體差異性較大,使藥物性肝炎發病重。本組99例中藥導致肝損傷患者中有66例重度(66.67%),1例重型。(5)考慮我院系傳染病專科醫院,肝損傷輕的患者基本于門診治療,故重度偏多。雖然藥物性肝炎肝損傷程度重,但預后良好,98.48%的患者均好轉或治愈出院。
綜上所述,藥物性肝炎在臨床上比較常見,因此必須嚴格按照說明書用藥,治療時要定期復查相關生化指標,要盡可能避免長期、大量、重復給藥,對兒童、老年人及肝、腎疾病患者,用藥時必須慎重選擇。應注意觀察乏力、惡心、嘔吐、皮膚黏膜黃染及尿黃等癥狀,以便早期發現藥物性肝炎,防止重度、重型肝炎的發生。對既往無肝炎病史的患者出現肝功能異常,應詳細詢問病史,仔細詢問其工作或生活中是否接觸過化學物質,是否服用過處方藥或非處方藥,是否服用過保健藥或中藥,在應用新藥期間如出現谷丙轉化酶異常增高,應重點考慮藥物引起的反應[16],對于發生過藥物性肝病的患者,要避免再次使用同一類藥物或化學結構相似的藥物,以減少藥物性肝病的發生。但由于藥物性肝炎的臨床表現與實驗室檢查無特異性,容易造成漏診、誤治,臨床上應高度重視藥物性肝炎的診斷與治療,特別應警惕中藥導致的不良反應,做到早發現、早治療,以提高治愈率。
[1]Cui ZM,Zhao JJ,Ren LN,et al. The clinical features and diagonsis realization of 213 patients with drug-induced liver injury [J]. Modern Digestion & Intervention,2014,19(2): 104-107.
崔忠敏,趙佳鈞,任麗楠,等.藥物性肝損害213例臨床特點及診治體會[J]. 現代消化及介入治療,2014,19(2):104-107.
[2]Larrey D,Pageaux GP. Drug-induced acute liver failure [J]. Eur J Gastroenterol Hepatol,2005,17(2): 141-143.
[3]Ibanez L,Perez E,Vidal X,et al. Prospective surveillance of acute serious liver disease unrelated to infectious,obstructive,or metabolic diseases: epidemiological and clinical features,and exposure to drugs [J]. J Hepatol,2002,37(5): 592-600.
[4]Teng GJ,Sun Y,Chang BX,et al. The clinical features and prognosis analysis of 418 patients with drug-induced liver injury [J]. Chinese Hepatology,2013,18(1): 11-14.
滕光菊,孫穎,常彬霞,等. 418例藥物性肝損害臨床特征及預后分析[J]. 肝臟,2013,18(1): 11-14.
[5]Chen CW. The evolution and evaluation of diagnostic standard for drug-induced liver injury [J]. Chinese Journal for Clinicians,2011,39(1): 68-71.
陳成偉. 藥物性肝損害診斷標準的演變和評價[J]. 中國臨床醫生,2011,39 (1): 68-71.
[6]Benichou C. Criteria of drug-induced liver disorders. Report of an international consensus meeting [J]. J Hepatol,1990,11(2): 272-276.
[7]Tan KP,Zhu SL,Tan GQ. Clinical features of patients with severe and gravis drug-induced hepatitis [J]. Medical Journal of National Defending Forces in Southwest China,2012,55(7): 726-728.
譚可平,朱勝利,覃國琦. 重度及重型藥物性肝炎患者臨床特征分析[J]. 西南國防醫藥,2012,55(7): 726-728.
[8]Soldin OP,Chung SH,Mattison DR. Sex differences in drug disposition [J]. J Biomed Biotechnol,2011,2011: 187103.
[9]Wang YE,Yao GB. Drug induced liver injury associated with Chinese herbal medicine and herbal related food supplements [J]. Chin J Dig,2007,27(7): 435-438.
汪月娥,姚光弼. 中草藥和相關保健食品引起藥物性肝病的研究[J]. 中華消化雜志,2007,27(7): 435-438.
[10]Li M,Lang MC,Wu JY. Clinical analysis of 219 cases of drug-induced hepatitis [J]. Journal of Nanchang University (Medical Science),2010,50(6): 67-68.
黎明,郎梅春,吳錦瑜. 219例藥物性肝炎臨床分析[J]. 南昌大學學報(醫學版),2010,50(6): 67-68.
[11]Weiler-Normann C,Schramm C. Drug induced liver injury and its relationship to autoimmune hepatitis [J]. J Hepatol,2011,55(4): 747-749.
[12]Zyoud SH,Awang R,Sulaiman SA. Reliability of the reported ingested dose of acetaminophen for predicting the risk of toxicity in acetaminophen overdose patients [J]. Pharmacoepidemiol Drug Saf,2012,21(2): 207-213.
[13]Liang B,Yu GM,Mao J. The Advances in drug-induced liver injury and its treatment [J]. Pharm J Chin PLA,2011,27(2): 175-177,188.
梁斌,余國梅,毛靜. 藥物性肝炎及其治療的研究進展[J].解放軍藥學學報,2011,27(2): 175-177,188.
[14]Holt MP,Ju C. Mechanisms of drug-induced liver injury [J]. AAPS J,2006,8(1): E48-E54.
[15]Gong XH,Chen LL. The reasons and measures of liver injury induced by Chinese herb [J]. Hubei Journal of Traditional Chinese Medicine,2011,33(5): 70-72.
龔小慧,陳良良. 中草藥所致藥物性肝損害的原因及對策[J]. 湖北中醫雜志,2011,33(5): 70-72.
[16]Liu XY,Li TH,Yang JX,et al. Change feature of blood serum zymogram and prognostic analysis of 256 cases of drug-induced liver injury [J]. China Modern Doctor,2009,47(17): 14-15.
劉序友,李庭華,楊繼雄,等. 256例藥物性肝病血清酶譜學變化特點及預后分析[J]. 中國現代醫生,2009,47(17): 14-15.
(責任編輯:李 健)
Retrospective analysis of clinical characteristics of liver injury induced by drugs and its causative agents
LI Jun,HUANG Shaoping,LU Jihua,YIN Keshan,FAN Zhenyu,TANG Rong,XU Lie,CHENG Jilin
Department of Gastroenterology and Hepatology,Shanghai Public Health Clinical Center of Fudan University,Shanghai 201508,China
Objective To analyze the drug-induced hepatitis and the clinical features of drug-induced hepatitis,and to explore the correlation between the suspected drugs and diseases. Methods One hundred and ninety-eight patients with drug-induced hepatitis were enrolled from Feb.2013 to Apr.2015. The clinical data were analyzed according to the kinds of the drugs,the clinical manifestation,the laboratory examination,the occurrence time of drug-induced hepatitis and the effect of drug discontinuance.Results Most drug-induced hepatitis occurred within 4 weeks after medication (116/198,58.59%). Among the inducements of liver damage,traditional Chinese medicine (99/198,50.00%),anti-tuberculosis drugs (48/198,24.24%),and anti-infective drugs (15/198,7.58%) were more commonly. Others were antipyretic analgesics,antitumor drugs,antipsychotics,lipid-lowering agents,antihypertensive drugs,hypoglycemic drugs,anti-rheumatism medicine,antifungal drugs,anti-gout drugs,the stomach medicine,etc. (36/198,18.18%). Most clinical manifestations were the liver cell damage type (144/198,72.73%). Severe liver injury accounted for 64.14% (127/198). Conclusion Drug-induced liver injury presents a severe tendency. Traditional Chinese medicine is an important reason for it. The clinicians should increasingly attach more importance to it.
Drug-induced hepatitis; The causative drugs; Clinical features
10.3969/j.issn.1006-5709.2016.02.012
李俊,住院醫師,研究方向:肝臟相關疾病的診斷及治療。E-mail:lijun@shaphc.org
程計林,博士生導師,主任醫師,研究方向:干細胞在肝臟疾病的分化及調控機制。E-mail:chengjilin@shaphc.org;徐烈,主治醫師,研究方向:肝臟疾病的隨訪及管理。E-mail:xulie@shaphc.org
R575
A
1006-5709(2016)02-0164-04
2015-08-28

