變異鏈球菌磷酸轉移酶系統ptxA、ptxB基因對細菌生長能力的影響
吳昕彧 陳曉丹 趙望泓 侯晉 陳璇南方醫科大學南方醫院·南方醫科大學口腔醫學院,廣州 510515
?
變異鏈球菌磷酸轉移酶系統ptxA、ptxB基因對細菌生長能力的影響
吳昕彧陳曉丹趙望泓侯晉陳璇
南方醫科大學南方醫院·南方醫科大學口腔醫學院,廣州 510515
[摘要]目的研究變異鏈球菌(S.mutans)磷酸轉移酶系統(PTS)中抗壞血酸家族ptxA、ptxB基因對細菌生長能力的影響。方法構建ptxA、ptxB和ptxAB雙重基因缺陷菌株以及ptxAB功能補償菌株。在僅以抗壞血酸作為唯一碳源時,使用實時熒光定量聚合酶鏈反應檢測野生株中ptxA、ptxB基因的表達情況。連續監測野生株、缺陷株和補償株的菌液OD600值,比較其生長能力。結果經過聚合酶鏈反應和測序鑒定,結果證明缺陷株和補償株構建成功。在以抗壞血酸作為唯一碳源的培養基中,野生株ptxA、ptxB基因的表達量均明顯增高(P<0.01)。缺陷株的生長能力較野生株有所下降,但是在補償株中可以得到補償。結論ptxA、ptxB基因與S.mutans對抗壞血酸的吸收利用密切相關,缺陷株和補償株的構建為進一步研究目的基因在S.mutans抗壞血酸代謝中的作用機制提供了理論基礎。
[關鍵詞]變異鏈球菌;磷酸轉移酶系統;ptxA基因;ptxB基因;抗壞血酸
Supported by:The National Natural Science Foundation of China(81050035);Project of Talent Introduction in Universities of Guangdong Province (C1030636);President Foundation of Nanfang Hospital, Southern Medical University(2013B003).Correspondence: Zhao Wanghong, E-mail: zhaowh@smu.edu.com.
齲病是人類發病率最高的口腔疾病。目前較為公認的致齲菌之一是變異鏈球菌(Streptococcus mutans,S.mutans)。S.mutans可代謝碳水化合物,從而發揮產酸、黏附、生物膜形成等與致齲相關的生物學特性。2002年,S.mutans血清c型UA159菌株的全基因組測序工作全部完成。通過對基因組的分析表明,S.mutans與碳水化合物代謝相關的基因占了15%,與現有其他已測序的革蘭陽性菌基因組相比,其呈現出更強的碳水化合物代謝能力[1]。而S.mutans對碳水化合物的轉運,主要是通過磷酸轉移酶系統(phosphotransferase system,PTS)完成的[2]。鑒于PTS對S.mutans代謝碳水化合物的重要作用,研究PTS相關基因對理解S.mutans的致齲作用有重要意義。
ptxA基因(NCBI GeneID:1027857)與ptxB基因(NCBI GeneID:1027854)分別編碼S.mutans UA159 PTS中抗壞血酸家族酶Ⅱ復合體中的酶ⅡA和酶ⅡB。有學者[3]曾對這兩個蛋白的三維晶體結構進行解析,并通過體外酶活性實驗證明它們對抗壞血酸的磷酸化具有特異性。抗壞血酸在自然界中分布廣泛,尤其在水果及蔬菜中含量豐富。目前已知大腸桿菌(Escherichia coli,E.coli)[4]、乳酸桿菌[5]等可在無氧條件下發酵抗壞血酸,以獲得維持生命活動的碳源,但未見關于S.mutans通過PTS吸收利用抗壞血酸以獲得碳源的報道。本研究擬構建ptxA、ptxB和ptxAB雙重基因缺陷菌株,以及ptxAB功能補償菌株,研究其在抗壞血酸特異性培養基中的生長情況,以揭示ptxA、ptxB基因在S.mutans利用代謝抗壞血酸中發揮的作用,并為進一步研究其作用機制提供基礎。
1 材料和方法
1.1菌株及培養條件
本實驗所用菌株S.mutans UA159(北京大學口腔醫學院中心實驗室惠贈)采用腦心浸液(brain heart infusion,BHI)培養基(青島海博生物技術有限公司)培養,或采用添加不同濃度葡萄糖(Sigma公司,美國)或抗壞血酸(Sigma公司,美國)的TV培養基(含3.5%胰蛋白胨、0.04 μg·mL-1對氨基苯甲酸、0.2 μg·mL-1鹽酸硫胺酸、1 μg·mL-1煙酰胺和0.2 μg·mL-1核黃素)(上海阿拉丁生化科技股份有限公司)進行培養。選擇性BHI培養基采用壯觀霉素(spectinomycin,spe)(Sigma公司,美國)抗性,spe的濃度為1 mg·mL-1。S.mutans的培養條件為37 ℃,厭氧培養(10%CO2、10%H2、80%N2)。E.coli DH5α[天根生化科技(北京)有限公司]采用Luria-Bertani(LB)培養基(青島海博生物技術有限公司)培養,選擇性LB培養基采用spe抗性,spe的濃度為0.1 mg·mL-1。E.coli的培養條件為37 ℃,200 r·min-1振蕩培養。
1.2ptxA、ptxB、ptxAB缺陷菌株及ptxAB功能補償菌株的構建
根據NCBI提供的S.mutans UA159全基因組序列,利用Primer Premier 5.0軟件針對ptxA、ptxB及ptxAB設計引物,具體見表1。

表1 引物序列Tab 1 Sequences of primers
聚合酶鏈反應(polymerase chain reaction,PCR)擴增各基因相應的上、下游片段,經雙酶切后與pFW5質粒(第四軍醫大學口腔醫學院余擎教授惠贈)進行連接,使用E.coli DH5α感受態細胞進行轉化。利用選擇性LB培養基篩選陽性克隆,提取陽性克隆的質粒進行測序鑒定。將構建成功的ptxA、ptxB 及ptxAB雙基因缺陷重組質粒轉化入S.mutans。使用1 μg·mL-1的感受態刺激肽(competence stimulating peptide,CSP)對野生型S.mutans UA159進行刺激,兩者混合后進行自然轉化[6]。利用選擇性BHI培養基篩選陽性克隆,提取陽性克隆的基因組DNA進行PCR及測序鑒定。利用類似方法,將啟動子序列及ptxAB片段克隆至pDL278質粒(美國路易斯安那州立大學牙學院Zezhang T.Wen教授惠贈),轉化入ptxAB雙重基因缺陷菌株,構建ptxAB功能補償菌株。
1.3抗壞血酸作為S.mutans生長唯一碳源時的最適濃度探究
分別檢測含有5、10、15、20、30 mmol·L-1抗壞血酸的TV培養基的pH值。將培養24 h后的野生型S.mutans UA159使用無菌PBS溶液洗滌2次,TV培養基重懸,調節菌液OD600≈0.8,按1︰100分別加入到含有上述濃度抗壞血酸的TV培養基中,37 ℃厭氧培養48 h,每隔2 h測量各組菌液OD600值,重復3次,繪制細菌在含不同濃度抗壞血酸的培養基中的生長曲線。
1.4檢測ptxA、ptxB基因在兩種不同碳源特異性培養基中的表達情況
將培養24 h后的野生型S.mutans UA159用無菌PBS溶液洗滌2次,TV培養基重懸,調節菌液OD600≈ 0.8,按1︰100分別加入到含有15 mmol·L-1抗壞血酸或葡萄糖的TV培養基中,37 ℃厭氧培養至對數生長后期。使用RNAiso試劑盒(Takara公司,日本)提取細菌總RNA,使用逆轉錄試劑盒(Takara公司,日本)進行逆轉錄。利用Primer Premier 5.0軟件設計ptxA、ptxB基因的引物,16S rRNA作為內參(表1),進行qPCR,檢測ptxA、ptxB基因的表達情況,重復3次。使用SPSS 13.0軟件進行兩獨立樣本t檢驗,檢驗水準為α=0.05。
1.5各菌株在以抗壞血酸為唯一碳源時的生長能力比較
將培養24 h后的野生型S.mutans UA159、ptxA基因缺陷菌株、ptxB基因缺陷菌株、ptxAB雙重基因缺陷菌株及ptxAB功能補償菌株使用無菌PBS溶液洗滌菌體2次,TV培養基重懸,調節菌液OD600≈0.6,按1︰100比例分別加入至含有15 mmol·L-1抗壞血酸的TV培養基中,37 ℃厭氧培養72 h,每隔2 h測量各菌液OD600值,重復3次,繪制各基因缺陷菌株和補償菌株在以抗壞血酸作為唯一碳源時的生長曲線。
2 結果
2.1ptxA、ptxB及ptxAB雙重基因缺陷菌株的鑒定
ptxA、ptxB及ptxAB雙重基因缺陷菌株的PCR鑒定結果見圖1。由圖1可見,各缺陷菌株PCR擴增的片段大小與使用相應重組質粒作為模版所擴增的片段大小一致,大小與預計相符。將片段測序結果在NCBI上進行BLAST對比,結果顯示99%相符。

圖1 ptxA、ptxB及ptxAB雙重基因缺陷菌株的PCR鑒定Fig 1 Identification of ptxA-, ptxB- and ptxAB-deficient mutant by PCR
2.2抗壞血酸作為S.mutans生長唯一碳源時的最適濃度
含5、10、15、20、30 mmol·L-1抗壞血酸的TV培養基的pH值分別為6.26、5.90、5.53、5.17、4.79。隨著抗壞血酸濃度的上升,培養基的pH值隨之下降。野生型S.mutans UA159在以不同濃度的抗壞血酸作為唯一碳源時,其生長情況有所不同(圖2)。隨著抗壞血酸濃度的增加,遲緩期逐漸延長。5 mmol·L-1組與10 mmol·L-1組的遲緩期較短,約為6 h,其達到穩定期所需的時間亦較短,約為16 h,但5 mmol·L-1組與10 mmol·L-1組的終末菌密度均較低。15 mmol·L-1組的遲緩期約為12 h,其達到穩定期所需的時間約為34 h,菌液終末OD600值約為0.6。20 mmol·L-1組的遲緩期約為24 h,但在監測的48 h內,未進入穩定期。而30 mmol·L-1組在監測的48 h內,細菌未見明顯增長。綜合考慮含不同濃度抗壞血酸的培養基的pH值、細菌生長的遲緩期、達到穩定期所需的時間及終末菌密度,選擇15 mmol·L-1作為S.mutans生長的最適抗壞血酸濃度,用于后續實驗。
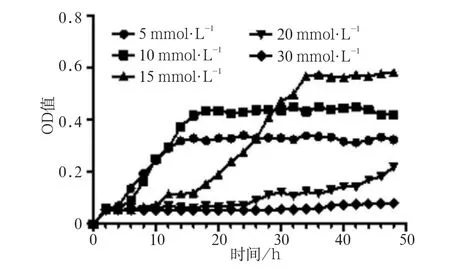
圖2 野生型S.mutans UA159在以不同濃度抗壞血酸作為唯一碳源時的生長情況Fig 2 Growth study of wild-type S.mutans UA159 using L-ascor-bate as the only carbon source at various concentrations
2.3ptxA、ptxB基因在兩種不同碳源特異性培養基中的表達情況
在以15 mmol·L-1抗壞血酸作為唯一碳源的TV培養基中,ptxA、ptxB基因的mRNA相對表達量顯著高于15 mmol·L-1葡萄糖組(圖3)。抗壞血酸組ptxA基因的表達量約為葡萄糖組的2倍,ptxB基因的表達量約為葡萄糖組的5倍,差異均具有統計學意義(P<0.01)。
2.4野生株與缺陷株在抗壞血酸特異性培養基中的生長能力
在以15 mmol·L-1抗壞血酸作為唯一碳源的TV培養基中,缺陷株的生長能力與野生株相比,受到明顯影響(圖4)。ptxA缺陷菌株的遲緩期延長,終末菌密度降低。而ptxB缺陷菌株與ptxAB缺陷菌株在監測的72 h內,未見明顯增長。ptxAB功能補償菌株能在一定程度上補償缺陷菌株的生長能力,但仍未達到野生型的水平。
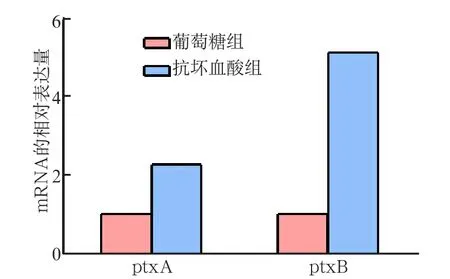
圖3 ptxA、ptxB基因在含15 mmol·L-1抗壞血酸或葡萄糖特異性培養基中mRNA的表達情況Fig 3 The mRNA expression of ptxA and ptxB gene in the medium with 15 mmol·L-1L-ascorbate or glucose
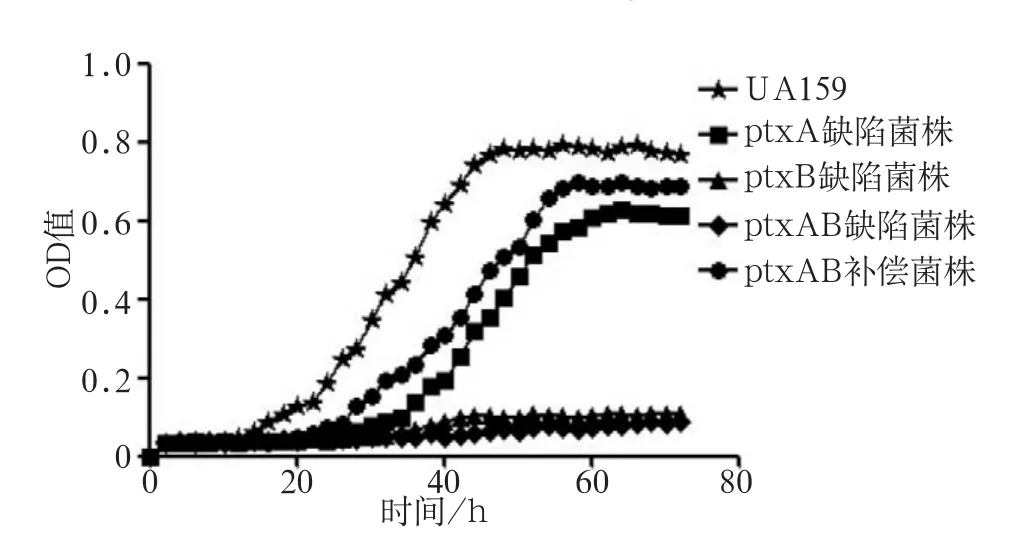
圖4 野生型S.mutans UA159與ptxA、ptxB、ptxAB基因缺陷菌株及ptxAB功能補償菌株在含15 mmol·L-1抗壞血酸特異性培養基中的生長能力Fig 4 Growth of wild-type S.mutans UA159, ptxA-, ptxB-, ptxAB-deficient mutant and ptxAB-complemented strain in the me-dium with 15 mmol·L-1L-ascorbate
3 討論
目前在S.mutans UA159中已發現超過14種PTS,包括葡萄糖、果糖、蔗糖、半乳糖、甘露糖等[7-10]。PTS一般由酶Ⅰ、含組氨酸的磷酸載體蛋白(histidinecontaining phosphocarrier protein,HPr)和酶Ⅱ復合體3部分組成。其中酶Ⅱ復合體具有糖特異性,負責對特定底物的跨膜轉運及磷酸化,一般由3個蛋白組成:ⅡA、ⅡB 和ⅡC[11]。關于PTS磷酸轉移的過程目前已較為清楚:首先酶Ⅰ通過自身磷酸化,從磷酸烯醇式丙酮酸中獲得磷酸,然后把磷酸依次傳遞給HPr、ⅡA、ⅡB,最后ⅡB把磷酸傳遞給通過ⅡC轉運進來的糖類[12]。ptxA、ptxB基因編碼S.mutans UA159 PTS中抗壞血酸家族酶Ⅱ復合體中的酶ⅡA和酶ⅡB。有學者[3]曾對ptxA、ptxB基因編碼的蛋白的作用底物進行體外實驗研究,發現在抗壞血酸、甘露醇、蔗糖、木糖、木糖醇和果糖6種底物中,這兩種蛋白僅對抗壞血酸有活性。
本研究通過“雙次交換”同源重組的方法,將目的基因的上、下游片段插入至pFW5載體的兩個多克隆位點中,使目的基因被壯觀霉素抗性基因aad9替換,從而構建ptxA、ptxB及ptxAB雙重基因缺陷菌株。“雙次交換”同源重組能使所得的轉化株傳代穩定,有效避免了極性效應[13]。關于抗壞血酸作為S.mutans生長唯一碳源時的最適濃度的研究表明,隨著抗壞血酸濃度的升高,野生株的遲緩期隨之延長,這可能與抗壞血酸濃度越高時,培養基的pH值越低,細菌需要更長的時間來適應這種酸性環境有關,亦可能是在高濃度時細菌胞內氧化還原反應改變的結果[4],也可能是高濃度提高了氧化應激水平,對細菌胞體造成了損傷所致[14]。qPCR檢測ptxA、ptxB基因在兩種不同碳源特異性培養基中mRNA的表達差異,結果顯示野生株目的基因在抗壞血酸特異性培養基中的表達水平明顯增高,表明抗壞血酸對ptxA、ptxB基因的表達有誘導作用。當培養基中僅存在抗壞血酸作為唯一碳源時,細菌為維持自身生長,上調ptxA、ptxB基因的表達量,以保證對抗壞血酸的充分利用。該實驗結果進一步證實了ptxA、ptxB基因與S.mutans抗壞血酸代謝相關。ptxA基因缺陷菌株在抗壞血酸特異性培養基中的生長能力明顯低于野生株,ptxB及ptxAB雙重基因缺陷菌株甚至無法生長,原因為細菌體內抗壞血酸特異性PTS過程的完整性和連續性受到破壞,細菌對抗壞血酸的吸收利用受到影響,從而影響生長,而功能補償菌株則能在一定程度上減少這種影響。但ptxA、ptxB基因在S.mutans抗壞血酸代謝中的具體調控機制及在細菌內是否存在其他代償機制仍有待進一步研究。
[參考文獻]
[1] Ajdi? D, McShan WM, McLaughlin RE, et al.Genome sequence of Streptococcus mutans UA159, a cariogenic dental pathogen[J].Proc Natl Acad Sci USA, 2002, 99(22): 14434-14439.
[2]Ajdic D, Chen Z.A novel phosphotransferase system of Streptococcus mutans is responsible for transport of carbohydrates with α-1,3 linkage[J].Mol Oral Microbiol, 2013,28(2):114-128.
[3]Lei J, Li LF, Su XD.Crystal structures of phosphotransferase system enzymes PtxB (ⅡB(Asc)) and PtxA (ⅡA(Asc))from Streptococcus mutans[J].J Mol Biol, 2009, 386(2): 465-475.
[4]Zhang Z, Aboulwafa M, Smith MH, et al.The ascorbate transporter of Escherichia coli[J].J Bacteriol, 2003, 185(7): 2243-2250.
[5]Linares D, Michaud P, Delort AM, et al.Catabolism of L-ascorbate by Lactobacillus rhamnosus GG[J].J Agric Food Chem, 2011, 59(8):4140-4147.
[6]Li YH, Lau PC, Lee JH, et al.Natural genetic transformation of Streptococcus mutans growing in biofilms[J].J Bacteriol, 2001, 183(3):897-908.
[7] Ajdi? D, Pham VT.Global transcriptional analysis of Streptococcus mutans sugar transporters using microarrays[J].J Bacteriol, 2007, 189(14):5049-5059.
[8]Zeng L, Burne RA.Comprehensive mutational analysis of sucrose-metabolizing pathways in Streptococcus mutans reveals novel roles for the sucrose phosphotransferase system permease[J].J Bacteriol, 2013, 195(4):833-843.
[9]Sato Y, Okamoto-Shibayama K, Azuma T.Glucose-PTS involvement in maltose metabolism by Streptococcus mutans[J].Bull Tokyo Dent Coll, 2015, 56(2):93-103.
[10]Zeng L, Xue P, Stanhope MJ, et al.A galactose-specific sugar: phosphotransferase permease is prevalent in the noncore genome of Streptococcus mutans[J].Mol Oral Microbiol, 2013, 28(4):292-301.
[11]Saier MH Jr, Reizer J.Proposed uniform nomenclature for the proteins and protein domains of the bacterial phosphoenolpyruvate: sugar phosphotransferase system[J].J Bacteriol, 1992, 174(5):1433-1438.
[12]van Montfort RL, Pijning T, Kalk KH, et al.The structure of an energy-coupling protein from bacteria, ⅡBcellobiose, reveals similarity to eukaryotic protein tyrosine phosphatases [J].Structure, 1997, 5(2):217-225.
[13]段勁, 劉筱娣, 郭麗宏.變形鏈球菌UA159磷酸蔗糖變位酶基因功能喪失菌株的構建[J].實用口腔醫學雜志, 2008, 24(1):69-73.Duan J, Liu XD, Guo LH.Construction of psm-negative mutans of S.mutans UA159[J].J Pract Stomatol, 2008, 24 (1):69-73.
[14]Campos E, Montella C, Garces F, et al.Aerobic L-ascorbate metabolism and associated oxidative stress in Escherichia coli[J].Microbiology, 2007, 153(Pt 10):3399-3408.
(本文編輯杜冰)
Effect of ptxA and ptxB genes of phosphotransferase system on growth of Streptococcus mutans
Wu Xinyu, Chen Xiaodan, Zhao Wanghong, Hou Jin, Chen Xuan.(Nanfang Hospital, School of Stomatology, Southern Medical University, Guangzhou 510515, China)
[Key words]Streptococcus mutans;phosphotransferase system;ptxA gene;ptxB gene;L-ascorbate
[Abstract]Objective This study aims to evaluate the effect of ptxA and ptxB genes, which are important genes in the L-ascorbate phosphotransferase system (PTS) of Streptococcus mutans (S.mutans).MethodsThe ptxA-, ptxB-, and ptxAB-double deficient mutant as well as ptxAB-complemented strain were constructed.Quantitative real-time polymerase chain reaction analysis was performed to evaluate the expression of the target genes of wild-type S.mutans when L-ascorbate was used as the sole carbohydrate source.The OD600values of the wild type, deficient, and complemented strains were continuously monitored, and their growth curves were constructed to compare growth capacity.ResultsPolymerase chain reaction and sequencing analyses suggested that deficient and complemented strains were successfully constructed.The expression levels of ptxA and ptxB significantly increased (P<0.01) when L-ascorbate was used as the sole carbohydrate source.The growth capacity of the deficient mutants decreased compared with that of the wild-type strain.However, the wild-type phenotype could be restored in the complemented strain.ConclusionptxA and ptxB genes are associated with L-ascorbate metabolism of S.mutans.The construction of deficient strains and complemented strain lay a foundation for further mechanism study on L-ascorbate metabolism in S.mutans.
[中圖分類號]Q 786
[文獻標志碼]A [doi]10.7518/hxkq.2016.03.017
[收稿日期]2015-08-11; [修回日期]2016-03-05
[基金項目]國家自然科學基金項目(81050035);廣東省高校人才引進項目(C1030636);南方醫科大學南方醫院院長基金項目(20-13B003)
[作者簡介]吳昕彧,碩士,E-mail:michely-wxywxy@163.com
[通信作者]趙望泓,教授,博士,E-mail:zhaowh@smu.edu.com

