多肽HM-3對人非小細胞肺癌裸鼠移植瘤抑制作用研究
程昊冉,王佳藝,吳小東,郝靜超,羅燕平,劉 晨,胡加亮,徐寒梅
(中國藥科大學,多肽藥物創制工程研究中心,江蘇 南京 210009)
?
多肽HM-3對人非小細胞肺癌裸鼠移植瘤抑制作用研究
程昊冉,王佳藝,吳小東,郝靜超,羅燕平,劉晨,胡加亮,徐寒梅
(中國藥科大學,多肽藥物創制工程研究中心,江蘇 南京210009)
摘要:目的>檢測HM-3類不同血管生成抑制劑治療人非小細胞肺癌裸鼠移植瘤的藥效學,考察血管生成抑制劑與腫瘤微環境的相互作用,為臨床確定治療方案提供參考和依據。方法建立人非小細胞肺癌A549的裸鼠移植瘤模型,以多西他賽(10 mg·kg-1)為陽性對照藥物,評價了在腫瘤體積≥300 mm3給予有效、過高劑量HM-3和貝伐單抗對腫瘤生長的抑制作用。結果動物實驗表明,腫瘤的體積≥300 mm3給藥,陽性對照組多西他賽具有很好的抗腫瘤活性。G2多西他賽(10 mg·kg-1)組的瘤重抑瘤率為60.80%。G3 HM-3(3 mg·kg-1)組、G4 HM-3(48 mg·kg-1)組、G5 Avastin(5 mg·kg-1)組抑瘤效果不佳,瘤重抑瘤率分別為43.60%、-34.80%、44.40%。結論由于受腫瘤生長階段、腫瘤微環境、作用靶點等影響,血管生成抑制劑HM-3有一定抑制腫瘤生長的效果,但效果不佳。HM-3抑瘤效果在(0~6 mg·kg-1)范圍內存在劑量依賴關系。而HM-3(48 mg·kg-1)過高劑量對人非小細胞肺癌A549裸鼠移植瘤無抑制作用,表現促進作用。特殊量效關系提示臨床使用血管抑制劑時應注意使用劑量。
關鍵詞:多肽HM-3;非小細胞性肺癌;貝伐單抗;血管生成抑制劑;裸鼠移植瘤模型;腫瘤微環境;多西他賽
肺癌是世界范圍內最常見的惡性腫瘤之一,且發病率和死亡率逐年增高。目前中國肺癌發病率也已躍居各種惡性腫瘤的首位[1]。非小細胞肺癌(non-small cell lung cancer,NSCLC)是肺癌最常見的組織類型,占全部肺癌的75%~80%,且5年生存率僅為15%[2-3]。雖然化療能顯著延長患者生存時間,減輕患者癥狀,改善患者生存質量,但化療藥物能夠引起嚴重的毒副反應,且有效率僅為14%~40%。因此尋找一種新型的治療手段是目前研究NSCLC的熱點。
HM-3是我們課題組自主設計合成的由18個氨基酸組成的新型高效血管生成抑制多肽,具有國家發明專利授權( 發明人: 徐寒梅,專利號:CN1699408)。HM-3能夠阻斷整合素αvβ3的信號通路,抑制VEGF表達,抑制內皮細胞遷移和新生血管生成,從而達到抑制腫瘤生長的效果。以整合素為靶點的抗腫瘤藥物的研發已成為當前腫瘤研究的熱點[4]。貝伐單抗(商品名Avastin)是美國Genentech開發的VEGF-A的人源化鼠單克隆抗體,通過抑制血管內皮生長因子(VEGF)的生物學功能發揮作用[5]。2006年,貝伐單抗被FDA批準與化藥聯合作為治療非鱗狀非小細胞肺癌的一線治療藥物[6]。多西他賽為半合成的紫杉醇類抗腫瘤藥物,具有周期特異性。多西他賽是FDA批準的治療非小細胞肺癌的一線和二線標準治療藥物。前期研究證明,HM-3對新生血管生成的抑制作用在一定范圍內存在劑量依賴關系。隨著藥物濃度的增大,藥效明顯增加,超過范圍量效關系不顯著[7]。本文研究了影響HM-3類血管抑制劑類藥物藥效的因素,為血管抑制劑應用于臨床提供指導。
1材料與儀器
1.1實驗動物和細胞株
SPF級BALB/c裸小鼠,由常州卡文斯實驗動物有限公司提供。實驗動物質量合格證許可證號:SCXK(蘇)2011-0003,合格證號:201400728。28~42 d日齡,體質量18~20 g;♂,每組動物數:每組6只,陰性對照組加倍。人非小細胞肺癌A549細胞由實驗室保存,已在體外傳代3~15代。所有動物實驗均符合動物倫理委員會標準。
1.2主要藥物與試劑
DMEM培養基(Life technologies公司);胰蛋白酶(Biosharp公司);胎牛血清(浙江天杭生物科技有限公司);青霉素、鏈霉素(Generay Biotech公司);HM-3(本課題組,批號:P140522);多西他賽(江蘇恒瑞制藥有限公司,批號:13062812);生理鹽水(山東魯抗辰欣藥業有限公司,批號:1207117102 ); 蘋果酸蘇尼替尼(大連美侖生物技術有限公司,批號:50511);貝伐單抗注射液(Roche Pharma,批號:H0129B07)。
2方法
2.1A549人非小細胞肺癌細胞的培養
復蘇A549細胞,用含10% FBS的DMEM培養基, 置于37 ℃,5% CO2培養箱內,飽和濕度培養。2 d傳代1次。用倒置顯微鏡觀察細胞呈貼壁生長,剛復蘇的細胞生長略受影響,傳代1~2次細胞狀態逐漸恢復正常。
2.2A549人非小細胞肺癌細胞裸鼠皮下移植瘤模型的建立
將非小細胞肺癌A549細胞株進行傳代培養,取對數生長期細胞,0.25%胰酶消化,含血清的培養基終止消化,機械吹打成單細胞懸液,離心,棄上清。用無血清培養基重懸細胞,細胞計數,將細胞懸液接種于右側腋窩皮下。接種量為每只裸鼠5×106個細胞,每只接種 0.1 mL。密切觀察裸鼠狀態,5~7 d左右裸鼠皮下可觸及出現白色結節,用游標卡尺測量裸鼠移植瘤直徑,14~21 d后待移植瘤體積生長至300 mm3左右時,挑選生長狀態良好且腫瘤大小均一性較好的荷瘤裸鼠47只,隨機分成5組,實驗組每組6只,陰性對照組11只。具體給藥方案如Tab 1。給藥期間,觀察并記錄裸鼠狀態,測量裸鼠體重,用游標卡尺測量瘤體積大小,體重和瘤體積每隔1天測量1次。d 22時,用頸椎脫臼法處死裸鼠,剝離瘤塊,稱重并計算抑瘤率,并將瘤組織進行免疫組化染色。
2.3給藥方案
隨機分為G1陰性對照(生理鹽水)、G2多西他賽(10 mg·kg-1)、G3 HM-3有效劑量(3 mg·kg-1)組、G4 HM-3過高劑量(48 mg·kg-1)組、G5 Avastin(5 mg·kg-1)組。給藥方案如表所示(Tab 1)。

Tab 1 Dosage regimen
劑量設置:多西他賽(10 mg·kg-1)、貝伐單抗(5 mg·kg-1)劑量由臨床上藥物有效劑量通過人與小鼠劑量換算公式計算得來;HM-3為國家1.1類新藥,現已進入一期臨床。前期本課題組已探索HM-3的敏感瘤株和藥物體內實驗的安全有效范圍,并探索了對超安全范圍的促生長和促轉移劑量。因此確定HM-3有效劑量(3 mg·kg-1)及 HM-3過高劑量(48 mg·kg-1)為給藥組劑量[8]。
2.4腫瘤測量及療效評價方法
2.4.1腫瘤體積及體積相對抑制率腫瘤體積(tumor volume,TV)的計算公式為:TV=1/2×a×b2,其中a、b分別表示腫瘤的長徑和短徑,即長和寬。根據測量的結果計算出相對腫瘤體積(relative tumor volume,RTV),計算公式為:RTV=Vt/V0。其中V0為分籠給藥時(即d0)測量所得腫瘤體積,Vt為每1次測量時的腫瘤體積。抗腫瘤活性的評價指標為相對腫瘤增殖率T/C/%,計算公式如下:T/C/%=TRTV/CRTV×100%,TRTV:治療組RTV;CRTV:陰性對照組RTV。根據《細胞毒類抗腫瘤藥物非臨床評價的技術指導原則》,評價標準為T/C>40%為無效;T/C≤40%,并經統計學處理與陰性對照組相比P<0.05為有效。
腫瘤體積抑制率/%=(陰性對照組平均體積-給藥組平均體積)/陰性對照組平均體積×100%。每2 d測一次腫瘤體積,根據體積抑制率可動態觀察各給藥組的抑瘤效果。
2.4.2腫瘤瘤重及抑瘤率瘤重抑瘤率/%=(陰性對照組平均瘤重-給藥組平均瘤重) /陰性對照組平均瘤重×100%。給藥21 d后,治療完成后,裸鼠手術剖瘤,腫瘤稱重。計算瘤重抑瘤率。
2.4.3裸鼠體重和存活情況每2 d測1次裸鼠體重,詳細觀察并記錄裸鼠體重變化情況和生長狀態,旨在檢測藥物的毒副作用。
2.5免疫組化檢測
給藥完成后,脫椎處死裸鼠,剖瘤。每組取2~3個樣本,所有瘤組織均經中性甲醛固定、脫水、常規石蠟包埋組織、切片、pH 6.0檸檬酸抗原修復緩沖液高溫抗原修復、BSA封閉,一抗(CD31)4 ℃過夜,二抗37 ℃孵育、DAB顯色、蘇木精復染細胞核、常規梯度乙醇脫水,最后中性樹膠脫水封片。顯微鏡鏡檢觀察腫瘤組織中微血管密度(MVD)。微血管密度的計數:腫瘤組織中的微血管定位在血管內皮細胞的細胞膜和細胞質,呈棕黃色,陽性定位在血管內皮細胞的細胞膜和細胞質,根據Weidner法[9]進行MVD計數,首先在低倍鏡(×100)下觀察整張切片,選3個微血管數最多的區域即“熱點”,腫瘤內硬化區及腫瘤交界處軟組織內的微血管不計數對象,在每個區域中計數一個高倍鏡(×40)下的微血管數,取其平均值作為此樣本的MVD值。任何一個被染為棕黃色的陽性內皮細胞或內皮細胞簇與相鄰的血管、腫瘤細胞或其他結締組織界限分開清楚,都被認為是一個能夠計數的微血管,管腔大于8個細胞或帶有較厚肌層的血管不計數[10]。
2.6統計學處理

3結果
3.1腫瘤體積及體積相對抑制率
根據腫瘤體積變化情況看(Fig 1),治療后7 d各組腫瘤體積開始不同程度的增長。腫瘤體積變化及體積抑制率見Fig 1A、1B,22 d剖瘤時所測的體積中,G1陰性組腫瘤體積為(2858.4±294.3) mm3; G2(多西他賽10 mg·kg-1)、G3(HM-3 3 mg·kg-1)、G4(HM-3 48 mg·kg-1)、G5(Avastin 5 mg·kg-1)的腫瘤體積分別為(1123.5 ±109.7)mm3、(1595.1±200.8)mm3、(3774.1±283.9)mm3、(1907.6±317.7)mm3。與陰性組相比,G2、G4組腫瘤體積差異有顯著性(P<0.01);根據Fig 1B中的腫瘤體積動態抑制率變化看,G2組在7~21 d期間的抑瘤率比較明顯,在給藥后期尤其明顯。
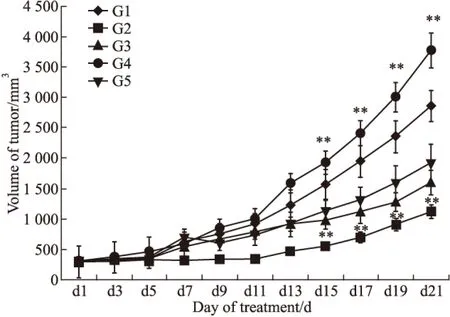
Fig 1A Tumor volume
G1:normal saline;G2:Docetaxel(10 mg·kg-1);G3:HM-3(3 mg·kg-1);G4:HM-3(48 mg·kg-1);G5:Avastin(5 mg·kg-1);**P<0.01vscontrol
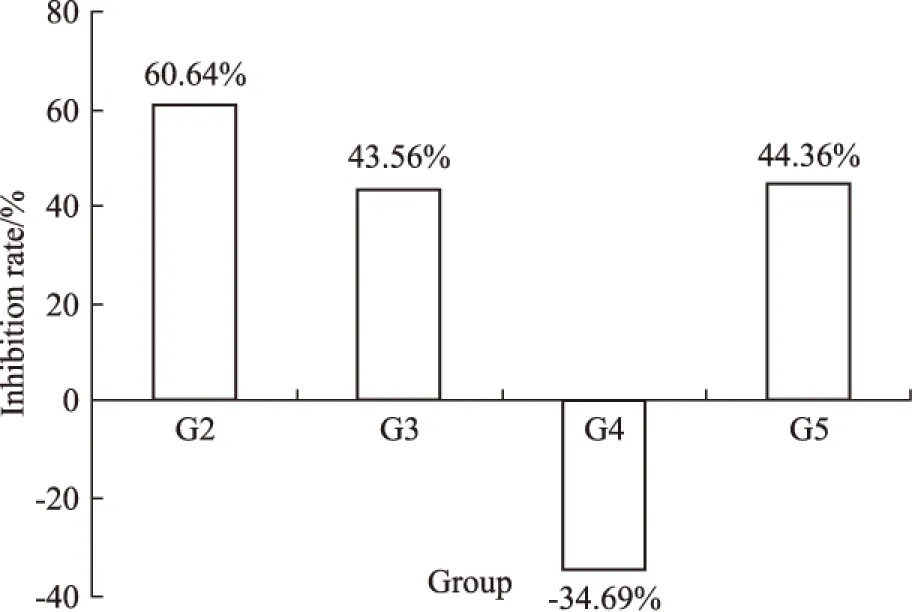
Fig 1B Inhibition rate on d 21 according to tumor volume
G1:Normal saline;G2:Docetaxel(10 mg·kg-1);G3:HM-3(3 mg·kg-1;G4:HM-3(48 mg·kg-1;G5:Avastin(5 mg·kg-1)
根據(Fig 2)的腫瘤體積相對增殖率變化看,G2(多西他賽10 mg·kg-1)組在7~21 d期間的T/C(%)值下降明顯,在給藥后期尤其明顯。T/C(%)值為37.24%。T/C(%)≤40%,并經統計學處理與陰性對照組相比P<0.05。
3.2腫瘤瘤重及抑瘤率
G1陰性組瘤重為(2.50±0.12) g,多西他賽(10 mg·kg-1)組瘤重為(0.98±0.14)g,明顯小于陰性組(P<0.01)。據瘤重計算出的抑瘤率見Tab 2,其中G2多西他賽(10 mg·kg-1)組的抑瘤率是60.80%,G3 HM-3(有效劑量)3 mg·kg-1和G4 HM-3(過高劑量)48 mg·kg-1抑瘤率分別是43.60%和-34.80%。 貝伐單抗(5 mg·kg-1)組的抑瘤率是44.40%。
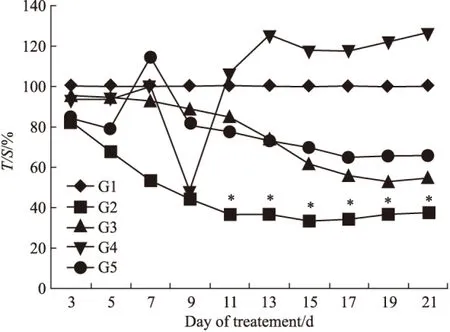
Fig 2 Relative cell proliferation rate T/C(%)
G1: Normal saline;G2: Docetaxel (10 mg·kg-1);G3:HM-3(3 mg·kg-1;G4:HM-3(48 mg·kg-1)*P<0.05vscontrol

Fig 3 Therapeutic effects of antiangiogenic agents on mice
G1: Normal saline;G2:Docetaxel(10 mg·kg-1);G3:HM-3(3 mg·kg-1);G4:HM-3(48 mg·kg-1;G5:Avastin(5 mg·kg-1)
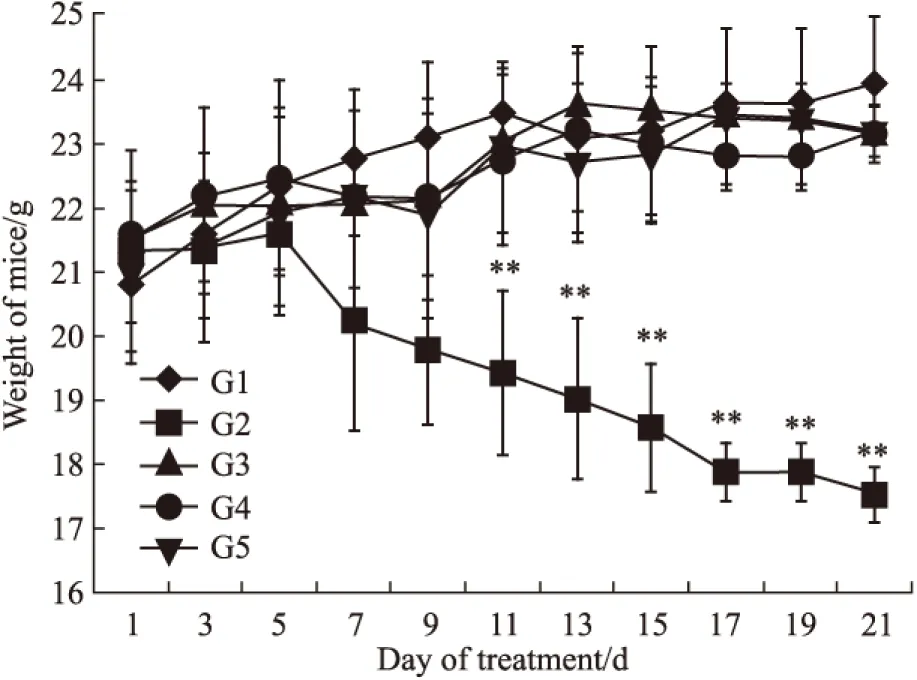
Fig 4 Weight of mice
G1: Normal saline;G2:Docetaxel(10 mg·kg-1);G3:HM-3(3 mg·kg-1);G4:HM-3(48 mg·kg-1;G5:Avastin(5 mg·kg-1);**P<0.01vscontrol
3.3裸鼠體重變化及存活情況
體重情況(Fig 4),陽性組多西他賽組給藥后,裸鼠體重有大幅度下降,與陰性組比較差異有統計學意義(P<0.01)。表明化藥多西他賽毒副作用明顯;多肽HM-3(有效劑量)組、HM-3(過高劑量)組、Avastin組的裸鼠體重與陰性組的相比,無明顯影響。說明多肽HM-3和Avastin的毒性較低。從動物存活情況看,各組動物全部存活。
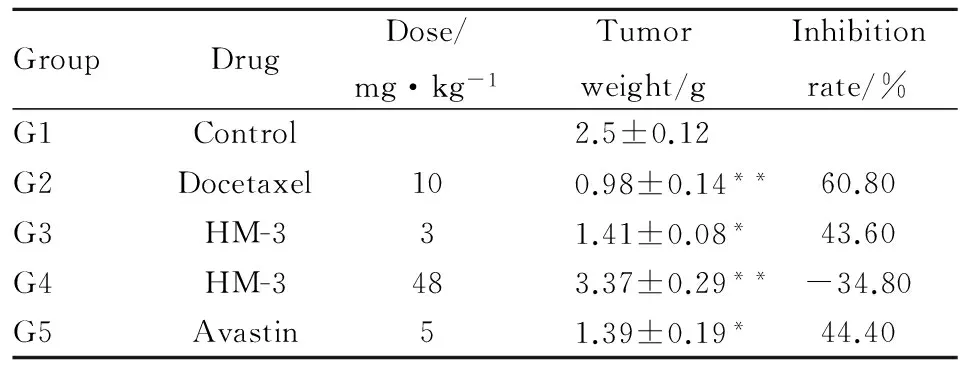
Tab 2 Tumor weight and inhibition rate
*P<0.05,**P<0.01vsControl group
3.4免疫組化染色
如Tab 3、Fig 5所示,陰性組MVD為(29.43±5.42),HM-3(3 mg·kg-1)和HM-3(48 mg·kg-1)MVD分別為(25.16±3.22)和(34.26±2.46),與陰性組對比,差異具有顯著性,證明HM-3在有效劑量下對腫瘤新生血管有抑制作用。過高劑量HM-3組微血管密度高于陰性組,證明過高劑量HM-3無抑制血管作用。多西他賽(10 mg·kg-1)組MVD為(20.33±3.13)。
4討論
1971年,Folkman等首先提出腫瘤生長與血管新生密切相關的概念。近年來研究發現,腫瘤血管新生對其生長、浸潤和轉移有重要意義,并且大部分腫瘤預后與血管新生有關[11]。血管生成抑制劑類藥物與傳統化療藥物相比,具有毒副作用低、高效、抗腫瘤譜廣、靶向性強和不易產生耐藥性等優點。通過抑制腫瘤血管新生的形成,并且切斷腫瘤血供而使腫瘤組織因缺氧而被破壞,抑制腫瘤細胞的增殖和轉移,血管生成抑制劑類藥物在多學科治療NSCLC領域具有廣闊的前景。HM-3是具有整合素親和性的一種新型高效血管生成抑制多肽,本課題組探索了其與傳統化藥聯用的抗腫瘤藥效活性,試驗建立多種癌癥的裸鼠移植瘤模型,根據臨床前抗腫瘤藥效學方法評價聯合用藥的抑瘤作用。實驗結果顯示,與單獨用藥相比,聯合用藥組的抑瘤效果更好。實驗證明,HM-3與化藥聯合用藥后,不但能增加療效,同時也能減少化藥的使用劑量,從而減少毒副作用[12]。
本課題組前期進行了人非小細胞肺癌A549裸鼠移植瘤體積<100 mm3時,給予HM-3類型不同血管生成抑制劑類藥物的藥效學研究。藥效學結果顯示,陽性對照多西他賽組對人非小細胞肺癌A549裸鼠移植瘤生長的抑制率為83.63%,多肽HM-3有效劑量組 (3 mg·kg-1)的抑制率為71.62%,Avastin組的抑制率為76.05%。HM-3過高劑量組(48 mg·kg-1) 時,對人非小細胞肺癌A549裸鼠移植瘤的生長無抑制作用,甚至出現促進作用。說明腫瘤初期階段給予HM-3類血管生成抑制劑類藥物抑瘤效果良好[13]。本試驗探討了人非小細胞肺癌A549裸鼠移植瘤體積≥300 mm3時,HM-3類血管生成抑制劑類藥物的藥效學研究。結果顯示,陽性對照多西他賽組有很好的抗腫瘤活性,與陰性組比較,差異具有顯著性(P<0.01)。整合素阻斷劑HM-3有效劑量(3 mg·kg-1)組和單抗Avastin(5 mg·kg-1)組,由于給藥時腫瘤體積較大,血管生成抑制劑類藥物抑瘤效果不明顯,HM-3過高劑量(48 mg·kg-1)甚至促進腫瘤生長。說明在給予HM-3類血管生成抑制劑類藥物治療時,最佳的介入治療時期和合理給藥劑量很重要。

Tab 3 Microvessel density(CD31)
Microvessel density(CD31),G1:Normal saline;G2:Docetaxel(10 mg·kg-1);G3:HM-3(3 mg·kg-1);G4:HM-3(48 mg·kg-1);G5:Avastin(5 mg·kg-1).*P<0.05,**P<0.01vsG1
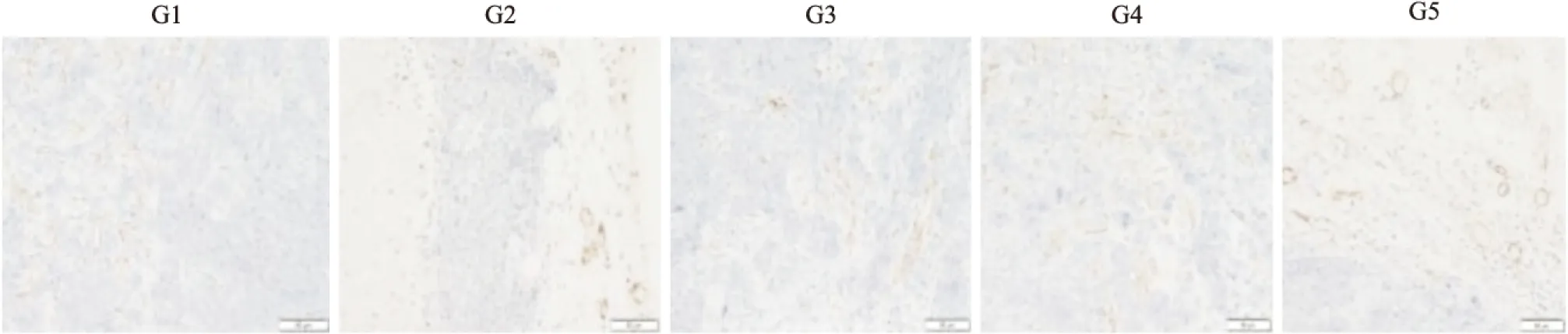
Fig 5 Microvasculature of each histological grade by CD 31 immunostaining(×200)
G1:Normal saline;G2:Docetaxel(10 mg·kg-1);G3:HM-3(3 mg·kg-1);G4:HM-3(48 mg·kg-1);G5:Avastin(5 mg·kg-1)
綜合分析實驗結果,Avastin體現出了一定的抑瘤效果,這與藥物介入的階段有關。前期實驗表明,在腫瘤體積小于100 mm3時給藥,Avastin的抑瘤效果較好。Avastin在腫瘤體積大于300 mm3時給藥,此時腫瘤內部生長緩慢,只有腫瘤外部血管豐富,還繼續生長,所以Avastin只能有效抑制腫瘤外部的生長,不能體現出較高的抑瘤效果。多肽HM-3作為整合素阻斷劑類抗腫瘤多肽,前期研究結果顯示,HM-3抑瘤效果在(0~6 mg·kg-1)范圍內存在劑量依賴關系。而HM-3(48 mg·kg-1)過高劑量對人非小細胞肺癌A549裸鼠移植瘤無抑制作用,甚至出現促進作用,這也與免疫組化結果相吻合(Fig 5)。HM-3特殊的量效關系與其作用機制是相關的,HM-3是多靶點的分子,可作用于整合素的信號通路,對VEGF信號通路也有影響。動物體內的各種信號通路是處于一個平衡狀態下的,當有效劑量藥物介入動物體內時,可改變動物體內的平衡狀態;當藥物濃度過高時,動物體內會出現調節機制,“補償”藥物的作用結果,甚至會出現相反的作用,因此HM-3的抑瘤效果不呈現劑量依賴性。本研究的結果表明,HM-3類血管抑制劑與化藥比較作用機制不相同,單獨使用或與化藥聯合使用都可減少化藥的毒副作用。另外使用血管生成抑制劑類藥物抗腫瘤時,還要受到動物品系、瘤株、腫瘤體積和介入時間等多種因素影響,尤其是劑量與藥效的關系有時不呈線性關系,因此臨床上使用這些藥物時,必須確定上述影響因素,才能保證安全用藥。
(致謝:本實驗在中國藥科大學多肽藥物創制工程研究中心完成。感謝導師徐寒梅教授為本實驗提供充足的資金支持和整體的思路指導;感謝胡加亮老師的精心指導;感謝趙長宏、何俊勁、郝靜超、王佳藝、吳曉東同學的盡心協助。)
參考文獻:
[1]沈紅兵, 俞順章. 我國肺癌流行現狀及其預防對策[J]. 中國腫瘤, 2004,13(5):283-5.
[1]Shen H B, Yu S Z. Epidemiological status of lung cancer in China and atrategies for prevention[J].ChinaCanc, 2004, 13(5):283-5.
[2]Walkers, Updates in non-small cell lung cancer[J].ChinJOncolNurs, 2008, 22(4):587-96.
[3]石遠凱, 牛奕. 美國國家綜合癌癥網非小細胞肺癌治療指南2007年第一版介紹[J]. 中華腫瘤雜志, 2007, 29(10): 799-800.
[3]Shi Y K, Niu Y. National comprehensive cancer network treatment guidelines for non-small cell lung cancer in 2007 introduced the first edition[J].ChinJOncol, 2007, 29(10): 799-800.
[4]Han J Y, Kim H S, Lee S H, et al. Immunohistochemical expression of integrins and extracellular matrix proteins in non-small cell lung cancer: correlation with lymph node metastasis[J].LungCancer, 2003, 41(1): 65-70.
[5]Cox D, Brennan M, Moran N. Integrins as therapeutic targets: lessons and opportunities[J].NatRevDrugDiscov, 2010, 9(10):804-20.
[6]Gerber H P, Ferrara N. Pharmacology of bevacizumab as monotherapy or in combination with cytotoxic therapy in preclinical studies[J].CancerRes, 2005, 65(3):671-80.
[7]Xu H M, Pan L, Ren Y L, et al. RGD-Modified angiogenesis inhibitor HM-3 dose : Dual function during cancer treatment[J].BioconjugateChem, 2011, 22(7): 1386-93.
[8]張曉娟,任印玲,徐寒梅. 整合素阻斷多肽HM-3體外抑制新生血管的研究[J]. 藥物生物技術,2012,19(02):129-33.
[8]Zhang X J,Ren Y L,Xu H M. HM-3 inhibiting angiogenesisinvitro[J].PharmBiotechnol,2012, 19(02):129-33.
[9]Weidner N, Semple J P, Welch W R, et al. Tumor angiogenesis and metastas is correlation in invasive breast carcinoma[J].NEnglJMed, 1991,324(1):1-8.
[10]白麗淼,黃曉峰,徐寒梅.人結腸癌HT-29移植瘤不同生長階段微血管密度及相關因子的表達研究[J]. 中國藥理學通報, 2014, 30(6):796-800.
[10]Bai L M, Huang X F, Xu H M. Investigation of microvessel density and related factors expression for xenografts tumor of HT29 cells in nude mice at different growth stage[J].ChinPharmacolBull, 2014, 30(6):796-800.
[11]Folkman J. Anti-angiogenesis: new concept for therapy of solid tumors[J].AnnSurg, 1972, 175: 409-16.
[12]王佳藝,何俊勁,郝靜超,等.多肽AP25與多西他賽聯合用藥對人乳腺癌裸鼠移植瘤的抑制活性研究[J]. 中國藥理學通報, 2015, 31(9):1233-8.
[12]Wang J Y, He J J, Hao J C, et al. Antitumor effects of combined use of peptide AP25 and docetaxel against breast cancer[J].ChinPharmacolBull, 2015, 31(9): 1233-8.
[13]何俊勁,王佳藝,郝靜超,等. 多肽mPEG-SC-(20k)-HM-3聯合奧沙利鉑對人肝癌細胞SMMC-7721裸鼠移植瘤的抑制作用[J]. 中國藥科大學學報, 2015, 46(4): 476-80.
[13]He J J, Wang J Y, Hao J C, et al. Antitumor effect of peptide mPEG-SC20k-HM-3 and oxaliplatin combination against human hepatocellular carcinoma SMMC7721 in nude mice[J]JChinPharmUniv, 2015, 46(4): 476-80.
Antitumor effects of peptide HM-3 against non-small cell lung cancer xenografts in nude mice
CHENG Hao-Ran, WANG Jia-Yi, WU Xiao-Dong,HAO Jing-Chao, LUO Yan-Ping, LIU Chen, HU Jia-Liang, XU Han-mei
(TheEngineeringResearchCenterofPeptideDrugDiscoveryandDevelopment,ChinaPharmaceuticalUniversity,Nanjing210009,China)
Abstract:AimsTo evaluate the pharmacodynamic efficacy of different types of antiangiogenic agents as HM-3 on a non-small cell lung cancer xenografts tumor model . To explore the interaction between the antiangiogenic agents and the tumor microenvironment, and to offer suggestions for clinical therapy. MethodsThe non-small cell lung carcinoma xenograft model was established in Balb/c nude mice. The model mice were treated with Docetaxel(10 mg·kg-1) as the positive control. The mice were parallelly treated with, HM-3 at the doses of 3 mg·kg-1and 48 mg·kg-1and, Avastin(5 mg·kg-1). The parameters include tumor volume, tumor weight and immunohistochemical analysis.ResultAnimal experiments showed that docetaxel had good anti-tumor activity. Tumor growth inhibition by tumor weight of G2 docetaxel(10 mg·kg-1) group was 60.80%. Tumor growth inhibition by tumor weight of G3 HM-3(3 mg·kg-1) group, G4 HM-3(48 mg·kg-1) group , G4 Avastin(5 mg·kg-1) group, were 43.60%, -34.80%, 44.40%, respectively.ConclusionThe antigiogenic effect is affected by tumor growth stage, tumor microenvironment and their working mechanisms. Angiogenesis inhibitors HM-3 has a certain effect of inhibiting tumor growth, but to little avail. HM-3 shows on inhibitory effect in a dose-dependent manner at the doses of 0~6 mg·kg-1. HM-3 at a high dose of 48 mg·kg-1has no inhibitory but promoting effects on human non-small cell lung carcinoma A549 xenografts in nude mice . Special dose-effect relationship indicates that dosage should be paid attention to in the clinical use of blood vessel inhibitors.
Key words:peptide HM-3; non-small cell lung cancer; Avastin; angiogenesis inhibitor; xenografts in nude mice; tumor microenvironment; docetaxel
收稿日期:2016-02-23,修回日期:2016-03-10
基金項目:國家高技術研究發展計劃(863計劃)資助項目(No.SQ2011SF11B02030)
作者簡介:程昊冉(1990-),女,碩士生,研究方向:腫瘤藥理學,E-mail:hrcheng1887@163.com;
doi:10.3969/j.issn.1001-1978.2016.06.014
文獻標志碼:A
文章編號:1001-1978(2016)06-0806-06
中國圖書分類號:R-332;R364.3;R734.205.3;R977.6; R979.1
網絡出版時間:2016-5-25 15:39網絡出版地址:http://www.cnki.net/kcms/detail/34.1086.R.20160525.1539.028.html
徐寒梅(1966-),女,博士,教授,博士生導師,研究方向:抗腫瘤新藥研究開發,通訊作者,E-mail:13913925346@126.com

