腫瘤靶向治療抗體藥物的研究進(jìn)展
曹睿,邵榮光,李亮
(中國(guó)醫(yī)學(xué)科學(xué)院&北京協(xié)和醫(yī)學(xué)院醫(yī)藥生物技術(shù)研究所 腫瘤室,北京 100050)
腫瘤靶向治療抗體藥物的研究進(jìn)展
曹睿,邵榮光,李亮Δ
(中國(guó)醫(yī)學(xué)科學(xué)院&北京協(xié)和醫(yī)學(xué)院醫(yī)藥生物技術(shù)研究所 腫瘤室,北京 100050)
近年來(lái),隨著人類對(duì)癌癥的細(xì)胞生物學(xué)和遺傳學(xué)方面的認(rèn)識(shí)達(dá)到分子生物學(xué)水平,新的治療理念和方法被不斷的提出,其中關(guān)于腫瘤的分子靶向性治療藥物的研發(fā)與應(yīng)用受到了廣泛的關(guān)注。抗體藥物以其靶向性強(qiáng),副作用小,療效顯著等優(yōu)點(diǎn),迅速成為了腫瘤靶向治療領(lǐng)域中的熱點(diǎn)藥物。目前已有20多種抗腫瘤抗體藥物經(jīng)過(guò)批準(zhǔn)應(yīng)用于臨床,并取得了顯著的療效。本文總結(jié)了靶向腫瘤的單克隆抗體藥物的發(fā)展歷程和現(xiàn)狀,及其抗腫瘤作用的機(jī)制。同時(shí)總結(jié)了單抗藥物在腫瘤研究領(lǐng)域中取得的新進(jìn)展,并對(duì)其應(yīng)用前景以及存在的不足做了概述。
腫瘤;單克隆抗體;分子靶向治療;抗體藥物
以抗體為基礎(chǔ)研發(fā)的藥物統(tǒng)稱為抗體藥物。近年來(lái),抗腫瘤抗體藥物的研發(fā)與應(yīng)用受到了廣泛的關(guān)注。最初,抗腫瘤抗體主要是通過(guò)抗原免疫動(dòng)物而獲得抗血清。通過(guò)此途徑獲得的抗體,稱之為多克隆抗體。由于抗血清中含有眾多針對(duì)不同抗原的抗體分子,這些抗原不僅存在于病變的腫瘤細(xì)胞上,同時(shí)存在于正常細(xì)胞的表面。因而多克隆抗體存在著嚴(yán)重的交叉反應(yīng),在臨床應(yīng)用中不僅未獲得確切的療效,反而會(huì)引發(fā)一系列不良反應(yīng)。而單克隆抗體的出現(xiàn),大大減少了機(jī)體與正常組織之間的交叉反應(yīng),降低了抗體治療的不良反應(yīng),為腫瘤治療帶來(lái)了新的希望。目前,用于制備抗體藥物(抗體治療劑)的抗體均屬于單克隆抗體[1]。
1 單克隆抗體藥物的發(fā)展歷程
利用抗體治療疾病已經(jīng)有近百年的歷史。1960年諾貝爾獎(jiǎng)得主Burnet提出克隆選擇學(xué)說(shuō),認(rèn)為每個(gè)B淋巴細(xì)胞表面的抗原受體只識(shí)別一種抗原決定簇(抗原表位),并產(chǎn)生針對(duì)該抗原決定簇的抗體,這一學(xué)說(shuō)為治療級(jí)單克隆抗體的研發(fā)奠定了理論基礎(chǔ)[2]。1975年諾貝爾獎(jiǎng)得主Milstein和Kohler發(fā)明了雜交瘤細(xì)胞技術(shù),通過(guò)特定抗原篩選出表達(dá)特定抗體的B淋巴細(xì)胞系,使得該細(xì)胞與骨髓瘤細(xì)胞雜交,實(shí)現(xiàn)了雜交瘤細(xì)胞的體外存活,并篩選和培養(yǎng)出了陽(yáng)性的克隆細(xì)胞。雜交瘤技術(shù)的成熟為單克隆抗體的體外短時(shí)間大規(guī)模培養(yǎng)提供了可能。
1986年全球第一個(gè)單抗治療腎移植排斥反應(yīng)的鼠源化抗體OTK-3宣告上市,雖然治療效果并不樂(lè)觀,且容易觸發(fā)人抗鼠免疫反應(yīng),但該藥獲得批準(zhǔn)用于臨床標(biāo)志著單抗藥物時(shí)代的開始[3]。1997年第一個(gè)治療腫瘤的嵌合抗體利妥昔單抗(Rituximab),被用于非霍奇金氏淋巴瘤的治療,獲得了臨床上的一致認(rèn)可。單抗藥物的發(fā)展由此得到了極大的改善。1998年全球第一個(gè)人源化單抗帕利珠(Palivizumab)用于防治呼吸道合胞病毒(RSV)引起的下呼吸道疾病[4]。同時(shí)FDA批準(zhǔn)了用于腫瘤治療的多個(gè)單抗,如人源化單抗曲妥珠(Trastuzumab)上市,用于Her2陽(yáng)性的乳腺癌治療,自此單抗產(chǎn)業(yè)進(jìn)入高速發(fā)展期。雖然人源化抗體能夠大大降低抗體藥物的免疫原性,但仍會(huì)出現(xiàn)人抗人源抗體的反應(yīng)。2002年全球第一個(gè)全人源單抗,即用于治療類風(fēng)濕性關(guān)節(jié)炎的阿達(dá)木單抗(Adalimumab),是目前全球最暢銷的藥物之一。2013年T-DM1(Trastuzumabemtansine)被用于治療HER-2陽(yáng)性的乳腺癌,并獲準(zhǔn)上市[5]。它是由赫賽汀(Herceptin)與一種化療藥物emtansine偶聯(lián)在一起制備的首個(gè)抗體藥物偶聯(lián)物(antibody drug conjugates,ADC)。自此單抗藥物隨之向著更低的免疫原性以及更高的特異性方向發(fā)展。
2 單克隆抗體藥物的發(fā)展現(xiàn)狀
目前研制與應(yīng)用的單克隆抗體藥物基本上是以由細(xì)胞工程技術(shù)和基因工程技術(shù)為主體的抗體工程技術(shù)制備的藥物。臨床研究表明,單獨(dú)應(yīng)用單抗在腫瘤治療中是有效的,且在多數(shù)情況下,單抗藥物與常規(guī)的放射療法、化療藥物和免疫調(diào)節(jié)藥物等聯(lián)合應(yīng)用時(shí)也能表現(xiàn)出協(xié)同作用,這使得單抗藥物的研發(fā)一直處于熱潮中。自1997年以來(lái),抗體藥物在腫瘤治療領(lǐng)域取得了突破性進(jìn)展。近年來(lái),由于DNA重組技術(shù)的飛速發(fā)展,其被應(yīng)用于抗體的結(jié)構(gòu)改造中,各種形式的重組抗體相繼出現(xiàn)。如人源化抗體,單價(jià)小分子抗體,多價(jià)小分子抗體以及抗體融合蛋白等大批抗體藥物涌入市場(chǎng),截至2014年12月,用于癌癥治療的抗體藥物總計(jì)20多種[6]。迄今為止,美國(guó)FDA批準(zhǔn)上市的靶向腫瘤的抗體藥物已有26種,見表1。除此之外,尚有160多種抗腫瘤抗體藥物處于臨床研究階段[7]。
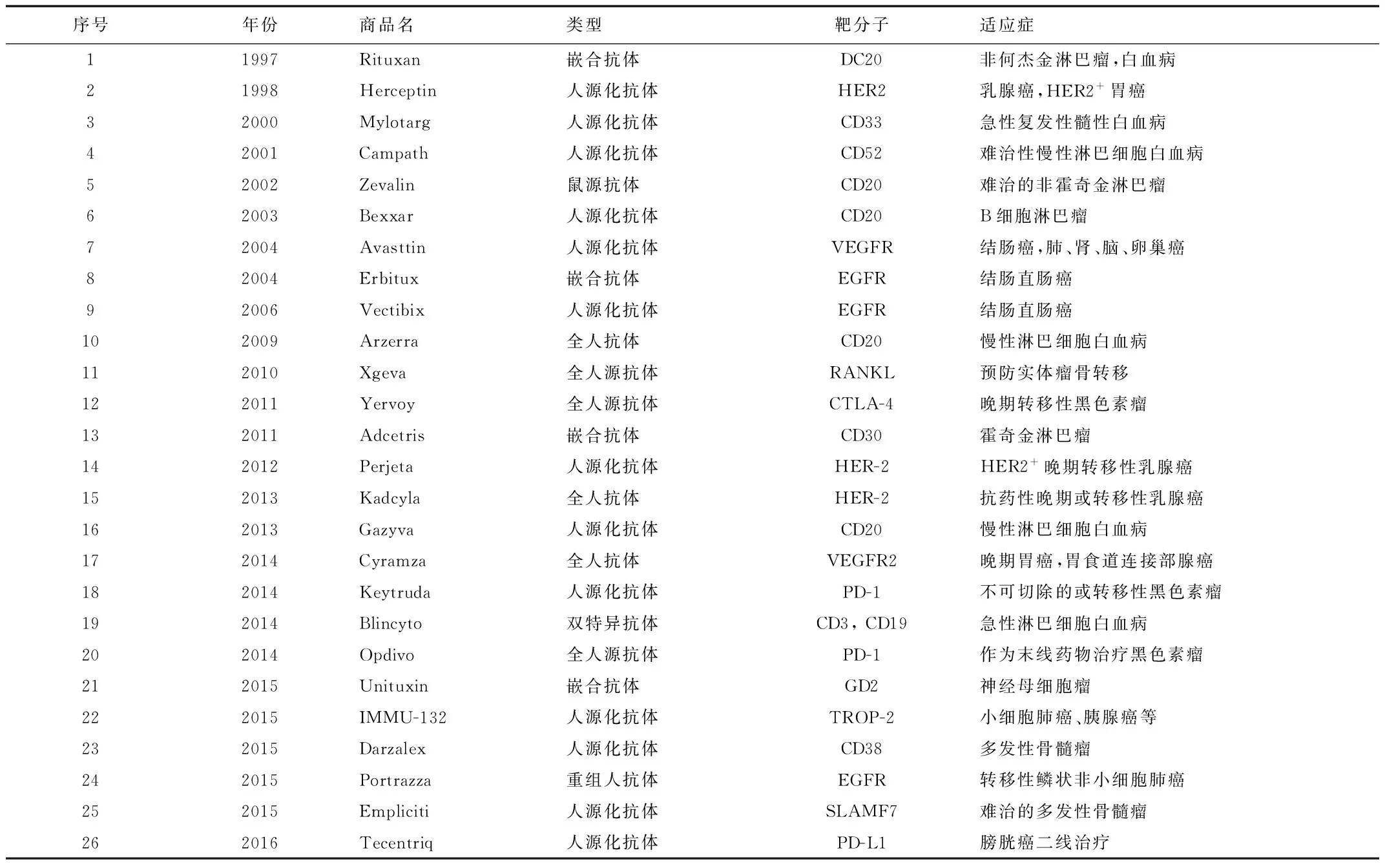
表1 美國(guó)FDA批準(zhǔn)上市的抗腫瘤抗體藥物
基于抗體的療法其關(guān)鍵在于尋找合適的靶向抗原。一個(gè)理想的單抗,其靶點(diǎn)應(yīng)該是在腫瘤細(xì)胞表面特異性表達(dá)或高表達(dá),而在正常組織中不表達(dá)或低表達(dá)的抗原。近些年來(lái),科研界對(duì)于腫瘤靶點(diǎn)的研究也取得了突破性的進(jìn)展,隨著分子生物學(xué)的發(fā)展和許多腫瘤新靶點(diǎn)的出現(xiàn),為抗體藥物的研發(fā)提供了新的方向。目前上市的單抗藥物的靶點(diǎn)涵蓋了血液分化抗原(CD20,CD30,CD33和CD52等),細(xì)胞生長(zhǎng)因子(CEA,EGFR,HER-2,HER-3,MET和IGFR1等),腫瘤壞死因子配基(TRAIL-R1,TRAIL-R2和TANKL等)和血管內(nèi)皮生長(zhǎng)因子(VEGF)等[8]。
3 新型抗腫瘤抗體的發(fā)展
隨著抗體工程技術(shù)的發(fā)展以及免疫檢查點(diǎn)藥物靶點(diǎn)的發(fā)現(xiàn),新型抗腫瘤抗體藥物的作用機(jī)制與療效都顯著區(qū)別于傳統(tǒng)抗體藥物,不再局限于通過(guò)結(jié)合腫瘤特異性蛋白或生長(zhǎng)因子而發(fā)揮其靶向作用。
3.1 基于抗體的腫瘤免疫療法 腫瘤細(xì)胞可以通過(guò)多種機(jī)制逃避免疫系統(tǒng)的監(jiān)控,免疫療法旨在增強(qiáng)機(jī)體正常的免疫系統(tǒng)對(duì)抗腫瘤的能力。機(jī)體的T細(xì)胞表面的共刺激因子可以通過(guò)與相應(yīng)配基結(jié)合而提供激活細(xì)胞免疫的“第二信號(hào)”,而這種激活效應(yīng)細(xì)胞所需的共刺激因子,稱之為免疫檢查點(diǎn)蛋白,可以作為抗體藥物的新型靶點(diǎn)。其中包括免疫球蛋白超家族(如CTLA-4、PD-1等)和腫瘤壞死因子超家族(如4-1BB、OX40、GITR等)。通過(guò)設(shè)計(jì)“共抑制因子”的拮抗劑或“共刺激因子”的激動(dòng)劑,可以啟動(dòng)機(jī)體的細(xì)胞免疫治療惡性腫瘤[9]。2014年靶向PD-1的Nivolumab[10]和Pembrolizumab[11]先后在日本和美國(guó)上市,而靶向PD-L1的抗體MPDL3820A成為30年來(lái)對(duì)轉(zhuǎn)移性膀胱癌唯一有效的抗體藥物[12]。
3.2 抗體藥物偶聯(lián)物(ADCs) 抗體藥物偶聯(lián)物是將抗體與細(xì)胞毒藥物進(jìn)行偶聯(lián),通過(guò)抗體的靶向作用將藥物直接傳送至腫瘤細(xì)胞,而減少其對(duì)正常組織器官的藥物分布,從而提高療效,降低不良反應(yīng)的一種新型抗體藥物。通過(guò)這種設(shè)計(jì)方法可以提高抗體藥物的殺傷能力,同時(shí)擴(kuò)大了小分子化療藥物的治療窗。目前有3種抗體藥物偶聯(lián)物獲得批準(zhǔn)上市,尚有超過(guò)30種ADC藥物處于臨床研究階段[13]。例如2001年由FDA獲準(zhǔn)上市的Gemtuzumabozogamicine,是由抗CD33的單抗與加里奇霉素偶聯(lián)而得,用于治療復(fù)發(fā)性急性髓系淋巴瘤,但該藥在2010年由于其安全性和有效性受到質(zhì)疑而自動(dòng)退市[14]。2013年抗體藥物偶聯(lián)物T-DM1被成功應(yīng)用于HER-2陽(yáng)性的轉(zhuǎn)移性乳腺癌治療中,它是由曲妥珠單抗與美登素衍生物偶聯(lián)而成,具有良好的療效與藥動(dòng)學(xué)特征,且患者的耐受良好。T-DM1的成功應(yīng)用,促進(jìn)了針對(duì)各種實(shí)體瘤和血液癌癥的ADC藥物的快速發(fā)展。并且隨著腫瘤新靶點(diǎn)的發(fā)現(xiàn),高效化療藥物分子的發(fā)展以及新型連接子(linker)的不斷開發(fā),相信ADC藥物的療效和安全性會(huì)得到進(jìn)一步的提高。
4 抗體藥物的作用機(jī)制
4.1 抗體藥物治療腫瘤的作用機(jī)制 臨床上應(yīng)用的抗腫瘤抗體藥物(未偶聯(lián)的裸抗體),其抗腫瘤作用機(jī)制主要是通過(guò)抗體的2種功能。其一是親和性,即與腫瘤表面靶抗原特異性結(jié)合,而后發(fā)揮其效應(yīng)功能,殺傷腫瘤細(xì)胞。抗體分子通過(guò)與靶抗原結(jié)合,能夠阻斷腫瘤生長(zhǎng)因子信號(hào)通路,誘導(dǎo)細(xì)胞凋亡或是抑制腫瘤微環(huán)境中新生血管的形成。其二,對(duì)腫瘤細(xì)胞的殺傷作用也可依靠免疫系統(tǒng)來(lái)介導(dǎo)細(xì)胞死亡,如抗體恒定區(qū)介導(dǎo)的抗體依賴性細(xì)胞介導(dǎo)的細(xì)胞毒作用ADCC(antibody-dependent cellular cytotoxicity),補(bǔ)體依賴的細(xì)胞毒作用CDC(complement-dependent cytotoxicity)以及抗體依賴的細(xì)胞吞噬作用ADPC(antibody-dependent cellular phagocytosis)等機(jī)制實(shí)現(xiàn)對(duì)腫瘤細(xì)胞的殺傷作用[15]。抗體藥物偶聯(lián)物的作用機(jī)制一般是通過(guò)偶聯(lián)抗體與靶向抗原的特異性親和,將高效的小分子化藥或放射性分子攜帶至靶位點(diǎn),從而抑制或者殺死腫瘤細(xì)胞[16]。
針對(duì)同一個(gè)靶點(diǎn)的不同單抗藥物,其作用機(jī)制并不一定完全相同,臨床的療效與不良反應(yīng)也有所差異[17]。例如,Trastuzumab和Pertuzumab均可以靶向表皮生長(zhǎng)因子受體家族中的HER-2受體,但是2者的抗原識(shí)別表位不同,前者可抑制HER-2受體的同源二聚化和異源二聚化,而后者只抑制HER-2與EGFR或者HER-3的異源二聚化,因而2者在臨床上的聯(lián)合用藥也能表現(xiàn)出一定的“協(xié)同效應(yīng)”[18]。Cetuximab、Panitumumab和Nimotumab都是靶向EGFR的單克隆抗體,而且它們所識(shí)別的抗原結(jié)合表位雖然相同,但是由于親和力和lgG亞型的差異,在臨床上引起的皮膚毒性也有所差異[19]。
4.2 抗體藥物治療腫瘤的作用特點(diǎn)
4.2.1 與腫瘤細(xì)胞的特異性結(jié)合:抗體藥物能夠與腫瘤細(xì)胞表面的靶抗原進(jìn)行特異性親和,從而使得到達(dá)腫瘤部位的抗體藥物多而進(jìn)入正常組織細(xì)胞的抗體藥物少,這是單抗藥物可以用于靶向治療的基礎(chǔ)。
4.2.2 抗體藥物的多樣性:主要表現(xiàn)為靶向抗原的多樣性、抗體結(jié)構(gòu)的多樣性、作用機(jī)制的多樣性以及在抗體藥物偶聯(lián)物中“彈頭”藥物的多樣性[1,20]。
4.2.3 在體內(nèi)能夠?qū)崿F(xiàn)特異性分布:抗腫瘤抗體藥物能夠在腫瘤局部聚集,顯示特異性的定位,而在非腫瘤區(qū)域分布較少。
4.2.4 制備抗腫瘤抗體藥物的定靶性:可以針對(duì)特定的靶向分子而定向制備相應(yīng)的抗體藥物,或者是可以根據(jù)特定的效應(yīng)分子來(lái)制備相應(yīng)的偶聯(lián)物或融合蛋白等[20]。
4.3 抗體藥物應(yīng)用注意事項(xiàng)及缺點(diǎn)
4.3.1 篩選適用病患:抗體作為靶向治療藥物,靶標(biāo)敏感性篩選已經(jīng)成為抗體治療是否可行的常規(guī)步驟。如乳腺癌,只有HER-2高表達(dá)的患者(約20%)才可能對(duì)trastuzumab治療有效;又如針對(duì)EGFR的靶向治療,KRAS基因突變的腸癌患者用cetuximab或panitumumab治療均無(wú)效。
4.3.2 注意抗體的免疫原性:作為一種大分子生物制劑,抗體同時(shí)也是一種免疫原,可能誘發(fā)排斥反應(yīng),使機(jī)體生成與抗體藥物相對(duì)應(yīng)的抗體,導(dǎo)致藥物療效下降或失效。臨床醫(yī)生需要在用藥過(guò)程中隨時(shí)檢測(cè)患者體內(nèi)的免疫排斥反應(yīng)。
4.3.3 昂貴的治療費(fèi)用:抗體生產(chǎn)工藝復(fù)雜,涉及許多環(huán)節(jié),包括高表達(dá)細(xì)胞株篩選、培養(yǎng)基研發(fā)、純化技術(shù)研發(fā)等諸多方面。通常而言,抗體藥物的研發(fā)周期長(zhǎng)達(dá)數(shù)十年,成本高達(dá)數(shù)十億美元,因而其價(jià)格昂貴,如何縮短研發(fā)周期,降低生產(chǎn)成本是抗體藥研發(fā)的重要因素。
5 抗體藥物的設(shè)計(jì)策略和趨勢(shì)
5.1 靶點(diǎn)的選擇
5.1.1 特異性:靶分子在腫瘤細(xì)胞中高表達(dá),而在正常組織細(xì)胞尤其是重要器官內(nèi)無(wú)顯著性表達(dá)。
5.1.2 對(duì)于腫瘤生長(zhǎng)的重要性:該分子靶點(diǎn)對(duì)于腫瘤的惡性表型具有關(guān)鍵性的作用,一旦受到阻斷,能夠干擾腫瘤的生長(zhǎng)和轉(zhuǎn)移等。
5.1.3 由單一靶點(diǎn)向多靶點(diǎn)方向發(fā)展:早期,針對(duì)單靶點(diǎn)的抗體藥物在應(yīng)用一段時(shí)間之后,腫瘤細(xì)胞會(huì)通過(guò)產(chǎn)生突變等途徑來(lái)實(shí)現(xiàn)對(duì)此類藥物的耐藥。為此開發(fā)出多靶點(diǎn)類的抗體藥物來(lái)克服上述耐藥情況。2009與2011年,Genentech公司基于“two-in-one”策略,相繼研發(fā)了同時(shí)可以靶向VEGR與HER-2,以及同時(shí)靶向EGFR與HER-3的雙特異性抗體,療效明顯優(yōu)于針對(duì)單個(gè)靶標(biāo)的單抗藥物[21-23]。
5.2 抗體的人源化 由于鼠源化抗體在人體內(nèi)可以誘發(fā)人抗鼠抗體反應(yīng),不僅影響其療效,同時(shí)也引發(fā)一系列的不良反應(yīng)。故對(duì)鼠源化抗體的人源化改造一直是抗體發(fā)展領(lǐng)域的研究熱點(diǎn)。人們通過(guò)制備嵌合抗體和人源化抗體等,逐步的降低了抗體藥物在人體內(nèi)的免疫原性,并在臨床上取得了良好的效果。隨著PCR技術(shù)的發(fā)展,利用基因工程技術(shù)可以將全套的人抗體重鏈和輕鏈V區(qū)基因克隆出來(lái),并在噬菌體表面表達(dá)分泌,經(jīng)過(guò)篩選獲得特異性抗體,即噬菌體抗體庫(kù)技術(shù)[24],該技術(shù)的出現(xiàn)使得人工合成全抗體成為可能。近幾年又發(fā)展了核糖體展示抗體庫(kù)技術(shù)[25],可構(gòu)建高容量、高質(zhì)量的抗體庫(kù),從而篩選具有更高親和力的抗體。此外,Lonberg[26]的研究表明除了利用單細(xì)胞生物構(gòu)建的人源化抗體篩選庫(kù)獲得全人源抗體外,轉(zhuǎn)基因動(dòng)物也是此類抗體的重要來(lái)源。值得注意的是,有報(bào)告指出,完全的人抗體在臨床使用中尚未確定優(yōu)于人源化抗體,這表明了人源化程度不一定是越高越好。
5.3 抗體藥物的小型化 抗體及其偶聯(lián)物均為大分子物質(zhì),這使得其難以通過(guò)毛細(xì)血管內(nèi)皮層和細(xì)胞外間隙而到達(dá)腫瘤的實(shí)體部位。通過(guò)酶切方法獲得的Fab片段,其分子量相當(dāng)于完整抗體的1/3,通過(guò)基因工程技術(shù)制備的單鏈抗體scFv或單域抗體(VH,VL)的分子量更小,約分別相當(dāng)于完整抗體的1/6或1/12。通過(guò)制備Fab片段、單鏈抗體、雙特異性抗體、三價(jià)抗體和微型抗體等手段可以實(shí)現(xiàn)抗體的小型化,從而提高其對(duì)實(shí)體瘤的穿透性。但需要注意的是設(shè)計(jì)過(guò)程中需根據(jù)其藥代動(dòng)力學(xué)特點(diǎn)而進(jìn)行適度的小型化,以防止抗體藥物與靶抗原親和力的減弱和半衰期的下降,從而研發(fā)出更適用于臨床的小型化抗體藥物。
5.4 抗體藥物的高效化 提高抗體藥物對(duì)于靶向細(xì)胞的殺傷作用,可以降低藥物的用量,從而節(jié)省治療費(fèi)用。通過(guò)在抗體分子上連接具有高效殺傷力的“彈頭”藥物,制成抗體藥物偶聯(lián)物或是基因工程融合蛋白,可以實(shí)現(xiàn)抗體藥物的高效化。中國(guó)醫(yī)學(xué)科學(xué)院北京協(xié)和醫(yī)學(xué)院醫(yī)藥生物技術(shù)研究所自主研發(fā)的抗腫瘤抗生素力達(dá)霉素,對(duì)腫瘤細(xì)胞具有強(qiáng)烈的殺傷作用,體外研究中對(duì)大部分腫瘤細(xì)胞的IC50值在pmol/L的水平,通過(guò)將其與靶向抗體偶聯(lián)制成抗體藥物偶聯(lián)物或是通過(guò)基因工程的手段,將其與抗體制備成相應(yīng)的融合蛋白,目前已取得一些成果,同時(shí)部分研究正在進(jìn)行中。
6 結(jié)語(yǔ)
腫瘤的發(fā)生是多因素、多階段、多基因和相互作用的結(jié)果。功能基因組學(xué)和蛋白質(zhì)組學(xué)的發(fā)展將為腫瘤的治療提供新的分子靶點(diǎn),而針對(duì)這些新靶點(diǎn),有可能研發(fā)出新的抗體藥物。同時(shí),對(duì)已有靶點(diǎn)新功能的發(fā)現(xiàn)和多靶點(diǎn)之間相互作用關(guān)系的闡明,也為抗體藥物的研發(fā)提供了新的方向,如雙(多)特異性抗體藥物等。基于單克隆抗體的腫瘤免疫療法也在近幾年中得到迅速發(fā)展,相信在不久的將來(lái),抗體藥物將會(huì)為人們的健康帶來(lái)更多的福音。
[1] ZhenY.Antibody-durg and tumor targeted therapy[J].J Med Res,2007,36(2):1-2.
[2] Wolchok JD,Kluger H,Callahan MK,et al.Nivolumab plus ipilimumab in advanced melanoma[J].N Engl J Med,2013,369(2):122-133.
[3] Sis B,Mengel M,Haas M,et al.Banff 09 meeting report: antibody mediated graft deterioration and implementation of Banff working groups[J].Am J Transplant,2011,10(3):464-471.
[4] Sliwkowski MX,Mellman I.Antibody therapeutics in cancer[J].Science,2013,341(6151):1192-1198.
[5] Verma S,Miles D,Gianni L,et al.Trastuzumabentansine for HER-2 positive advanced breast cancer[J].N Engl Med,2012,367:1783-1791.
[6] Guo YJ.Progress in momoclonal antibody-based immunotherapy for cancer treatment[J].Chin J Biotech,2015,31(6):857-870.
[7] Kovaleva M,Ferguson L,Steven J,et al.Shark variable new antigen receptor biologics-a novel technology platform for therapeutic drug development[J].Expert Opin Biol ther,2014,14(10):1527-1539.
[8] Reichert JM,Dhimolea E.The future of antibodies as cancer drugs[J].Drug Discov Today,2012,17(17/18):954-963.
[9] Pardoll DM.The blockade of immune checkpoints in cancer immunotherapy[J].Nat Rev Cancer,2012,12(4):252-264.
[10] Topalian SL,Hodi FS,Brahmer JR,et al.Safety,activity,and immune correlates of anti-PD-1 antibody in cancer[J].N Engl J Med,2012,366(26):2443-2454.
[11] Hamid O,Robert C,Daud A,et al.Safety and tumor responses with lambrolizumab (anti-PD-1) in melanoma[J].N Engl J Med,2013,369(2): 134-144.
[12] Powles T,Eder JP,Fine GD,et al.MPDL3280A (anti-PD-1) treatment leads to clinical activity in metastatic bladder cancer[J].Nature,2014,515(7528):558-562.
[13] Sassoon I,Blanc V.Antibody-drug conjugate (ADC) clinical pipeline: a review//DucuyL,Ed.Antibody-Drug Conjugates.Methods in Molecular Biology Volume 1045[M].Humana: Humana Press,2013: 1-27.
[14] Castaigne S,Pautas C,Terre C,et al.Effect of gemtuzumaboaogamicin on survival of adult patients with de-novo acute myeloid leukaemia(ALFA-0701): a randomized,open-label,phase 3 study[J].Lancet,2012,379(9825): 1508-1516.
[15] Hagenbeek A,Gadeberg O,Johnson P,et al.Frist clinical use of ofatumumab,a novel fully human anti-CD20 monoclonal antibody in relapsed or refractory follicular lymphoma: results of a phase 1/2 trial[J].Blood,2008,111(12):5486-5495.
[16] Casi G,Neri D.Antibody-durg conjugates: Basic concepts,examples and future perspectives[J].J Control Release,2012,161(2):422-428.
[17] Shim H.Onetarget,different effects: a comparison of distinct therapeutic antibodies agsinst the same targets[J].Exp Mol Med,2011,43(10):539-549.
[18] Sakai K,Yokote H,Murakami-Murofushi K,et al.Pertuzumab,a novel HER dimerization inhibitor,inhibits the growth of human lung cancer cells mediated by the HER-3 signaling pathway[J].Cancer Sci,2007,98(9):1498-1503.
[19] Ramakrishnan MS,Eswaraiah A,Crombet T,et al.Nimotuzumab,a promising therapeutic monoclonal for treatment of tumors of epithelial origin[J].mAbs,2009,1(1):41-48.
[20] Douthwaite J,Jerutus L.Exploiting directed evolution for the discovery of biological[J].Nat Biotechnol,2005,23(9):1073-1078.
[21] Parrent PW,Buton DR.Immunology.Two-in-one designer antibodies[J].Science,2009,323(5921):1567-1568.
[22] Bostrom J,Yu SF,Kan D,et al.Variants of the antibody Herceptin that interact with HER2 and VEGF at the antigen binding site[J].Science,2009,323(5921):1610-1614.
[23] Zuo MH,Jin HJ,Li J,et al.Construction of Fc fusion protein EVP1 targeting members of VEGF-EGFR and its binding affinity[J].Chinese Journal of Cancer Biotherapy,2012,19(3):239-246.
[24] Osbourn J,Jermutus L,Duncan A.Current methods for the generation of human antibodies for treatment of autoimmune diseases[J].Drug Discov Today,2003,8(18):845-851.
[25] Lonberg N.Human monoclonal antibodies from transgenic mice[J].HandbExpPharmacol,2008(181):69-97.
[26] Lonberg N.Human antibodies from transgenic animals[J].Nat Biothchnol,2005,23(9):1117-1125.
(編校:吳茜)
Advances in antibody drug for cancer targeted therapy
CAO Rui, SHAO Rong-guang, LI LiangΔ
(Department of Oncology, Institute of Medicinal Biotechnology of Chinese Academy of Medical Sciences & Peking Union Medical College, Beijing 100050, China)
With the recent understanding of cancer biology, physiopathology, and cancer genetics & genomics, new treatments and methodologies are constantly developed, including on the development and application of molecular targeted drugs for cancer therapy have been widespread concerned.Antibody-based drugs targeting over-expressed oncogenes or other functional proteins in cancer with its high specificity, less side-effects and significant clinical efficacy became rapidly the hot-spot of anti-tumor drug research.Currently, there are already more than 20 of anti-tumor antibody-based drugs approved for clinical application, and achieved remarkable results.This article summarizes the development and current situation of monoclonal antibody-based drug research for cancer therapy, as well as their anti-tumor mechanism of action.At the same time summarizes the new advances in cancer research in the field of monoclonal antibody drugs made,and its prospects as well as shortcomings were outlined.
anti-tumor; monoclonal antibody; molecular targeted therapy; antibody-based drugs
10.3969/j.issn.1005-1678.2016.06.04
國(guó)家“重大新藥創(chuàng)制”科技重大專項(xiàng)(2014ZX09201042)
曹睿,男,博士在讀,研究方向:腫瘤藥理與藥物基因組學(xué),E-mail: songwp920@163.com;李亮,通信作者,女,博士,研究員,研究方向:腫瘤藥理與藥物基因組學(xué),E-mail:liliang@imb.pumc.edu.cn。
R730.5
A

