高效液相色譜法同時測定發(fā)酵液中木糖醇和L-木酮糖的含量
葛馳宇,蔣潔,翁旭,張君麗
(1.江蘇食品藥品職業(yè)技術(shù)學(xué)院 藥學(xué)院,江蘇 淮安 223003; 2.江蘇省蛋白質(zhì)類藥物工程實驗室,江蘇 淮安 223003)
高效液相色譜法同時測定發(fā)酵液中木糖醇和L-木酮糖的含量
葛馳宇1,蔣潔1,翁旭1,張君麗2Δ
(1.江蘇食品藥品職業(yè)技術(shù)學(xué)院 藥學(xué)院,江蘇 淮安 223003; 2.江蘇省蛋白質(zhì)類藥物工程實驗室,江蘇 淮安 223003)
目的 建立高效液相色譜(HPLC)同時測定發(fā)酵液中底物木糖醇和產(chǎn)物L(fēng)-木酮糖含量的方法。方法 采用C18色譜柱 (250 mm×4.6 mm),柱溫35 ℃,以乙腈-水(體積比為85:15)為流動相,流速0.8 mL/min。用示差折光檢測器檢測木糖醇,檢測器溫度為33 ℃。用紫外檢測器在室溫下檢測L-木酮糖,檢測波長為210 nm。結(jié)果 所得木糖醇的線性范圍為0.50~30.00 g/L,相關(guān)系數(shù)為0.9995,最低檢出限為0.18 g/L,最低定量限為0.58 g/L;所得L-木酮糖的線性范圍為0.30~30.00 g/L,相關(guān)系數(shù)為0.9986,最低檢出限0.15 g/L,最低定量限為0.40 g/L;木糖醇的日內(nèi)和日間相對標(biāo)準(zhǔn)偏差(RSD)均分別小于0.64%和 0.80%,L-木酮糖的日內(nèi)和日間RSD均分別小于0.31%和0.59%;回收率均在99.00%~101.00%之間。結(jié)論 建立的HPLC法不受發(fā)酵液中其他組分的干擾,可同時測定底物木糖醇和產(chǎn)物L(fēng)-木酮糖的含量,并實時監(jiān)控發(fā)酵的全過程。
高效液相色譜;同時測定;木糖醇;L-木酮糖;發(fā)酵液
L-木酮糖是一種在多種原核和真核生物代謝途徑發(fā)現(xiàn)的代謝物,是一種稀有糖[1]。口服L-木酮糖可以通過抑制α-葡萄糖苷酶來有效控制餐后血糖升高,此外L-木酮糖用于腫瘤治療時能顯著抑制惡性腫瘤細(xì)胞的生長[2-4]。目前生產(chǎn)L-木酮糖的傳統(tǒng)方法是以D-山梨糖醇為原料的化學(xué)合成法,但該方法合成路線繁瑣,產(chǎn)量很低,且有異構(gòu)體污染[5]。微生物轉(zhuǎn)化法是通過利用菌體靜息細(xì)胞氧化木糖醇生產(chǎn)L-木酮糖,該法反應(yīng)條件溫和,環(huán)境友好,成本較低且產(chǎn)品純度高[6-7]。目前,以廉價的木糖醇為底物,通過生物轉(zhuǎn)化法生產(chǎn)L-木酮糖,已成為獲取昂貴的稀有糖的重要方法。
發(fā)酵過程中需要建立底物和產(chǎn)物的含量檢測方法來監(jiān)測發(fā)酵的全過程,以便確定發(fā)酵終點。木糖醇屬于多元醇,其檢測方法主要是碘量法[8-9]。在發(fā)酵后期,由于產(chǎn)物L(fēng)-木酮糖的干擾,需要將木糖醇單獨從發(fā)酵液中純化出來進行檢測,分離過程復(fù)雜會導(dǎo)致結(jié)果誤差較大;L-木酮糖主要是半胱氨酸咔唑法和斐林試劑法[7-12],半胱氨酸咔唑法試劑配制繁瑣,且存在一定的危險性;斐林試劑法屬于滴定分析法,操作繁瑣,容易出現(xiàn)誤差,準(zhǔn)確度不高。此外,劉宇鵬等[13-14]對L-木酮糖的同系物L(fēng)-赤蘚酮糖的含量測定使用了紫外分光光度法,但是該法只有吸光值在 0.3~0.7之間數(shù)據(jù)才準(zhǔn)確可靠,往往發(fā)酵液需要經(jīng)過多次稀釋才能達到該范圍,因此測定過程會產(chǎn)生較大的誤差;對于HPLC法,目前僅有只針對木糖醇或L-木酮糖的含量進行測定的HPLC方法的報道[15-16]。為此,本實驗旨在建立可以同時測定發(fā)酵液中底物木糖醇和產(chǎn)物L(fēng)-木酮糖的HPLC法。
1 材料與方法
1.1 材料 木醋桿菌(中國工業(yè)微生物菌種保藏管理中心)。
L-木酮糖對照品(HPLC純度為95%)和木糖醇對照品(含量≥99%)均購自美國Sigma公司;乙腈(色譜純,南京化學(xué)試劑有限公司);葡萄糖、蛋白胨、酵母粉均為分析純(英國Oxoid公司)。
分析天平,發(fā)酵罐,Agilent 1260高效液相色譜儀,紫外檢測器和示差折光檢測器(美國Agilent有限公司)。
1.2 方法
1.2.1 色譜條件
色譜柱:Aglient C18(250 mm×4.6 mm);柱溫:35 ℃;流動相:乙腈-水(85:15,v/v);流速:0.8 mL/min。用示差折光檢測器檢測木糖醇,檢測器溫度為33 ℃。用紫外檢測器在室溫下檢測L-木酮糖,檢測波長為210 nm。
1.2.2 供試品溶液的制備:將木醋桿菌接種至30 mL種子液(10 g/L酵母粉,80 g/L葡萄糖)中培養(yǎng)24 h,再按3%的比例接種至100 mL發(fā)酵培養(yǎng)基(30 g/L木糖醇、5 g/L酵母粉、5 g/L蛋白胨、5 g/L NaCl,pH調(diào)至7.0)中。取發(fā)酵18 h的發(fā)酵液樣品1 mL,4000 r/min離心10 min,收集上清液,用孔徑0.22 μm濾膜過濾,收集濾液用流動相稀釋至1 mL,即為供試品溶液。
1.2.3 標(biāo)準(zhǔn)溶液的配制及標(biāo)準(zhǔn)曲線的繪制:精密量取木糖醇和L-木酮糖的對照品溶液適量,分別定容于10 mL容量瓶中,用流動相制成濃度為30.00 g/L 的儲備液,再將其分別稀釋成0.00、3.00、6.00、12.00、18.00、24.00、30.00 g/L的標(biāo)準(zhǔn)溶液,每一濃度分別進樣20 μL,測定3次,取峰面積平均值。以峰面積平均值為縱坐標(biāo)(y),以標(biāo)準(zhǔn)溶液濃度為橫坐標(biāo)(x),得到線性方程、相關(guān)系數(shù)和線性范圍。以信噪比(S:N)為3時對照品的濃度為最低檢測限(LOD),S:N為10時對照品的濃度確定最低定量限(LOQ)。
1.2.4 專屬性考察:在發(fā)酵過程中,由于發(fā)酵液中成分比較復(fù)雜,需要考察這些成分是否會對木糖醇和 L-木酮糖的含量測定產(chǎn)生干擾。為此,分別對空白發(fā)酵培養(yǎng)基(不含木糖醇和L-木酮糖)、木糖醇對照品、L-木酮糖對照品和供試品溶液進行專屬性考察。
1.2.5 精密度實驗:在木糖醇和L-木酮糖的標(biāo)準(zhǔn)曲線的線性范圍里選擇低、中、高3個質(zhì)量濃度,配制各濃度的對照品溶液樣品。每個濃度樣品分別在同一天內(nèi)和不同天內(nèi)連續(xù)測定6 次,分別考察每一濃度樣品同一天內(nèi)測定結(jié)果的相對標(biāo)準(zhǔn)偏差(RSD),獲得日內(nèi)精密度;分別考察每一濃度樣品不同天之間測定結(jié)果的RSD,獲得日間精密度。
1.2.6 回收率實驗:在木糖醇和L-木酮糖標(biāo)準(zhǔn)曲線的線性范圍里選擇低、中、高3個質(zhì)量濃度,配制各質(zhì)量濃度的對照品溶液樣品,每個濃度樣品配制6份,分別加入空白發(fā)酵培養(yǎng)基,計算每一濃度的加樣平均回收率。
1.2.7 發(fā)酵終點的確認(rèn):取發(fā)酵0、6、12、18、24、30 h 6個時間點的供試品溶液分別進樣,根據(jù)木糖醇和L-木酮糖的標(biāo)準(zhǔn)曲線計算木糖醇和L-木酮糖的含量,并根據(jù)各個時間段木糖醇與L-木酮糖的含量變化趨勢確定發(fā)酵終點。
2 結(jié)果
2.1 專屬性考察結(jié)果 由圖1可見,空白培養(yǎng)基無雜質(zhì)峰出現(xiàn)(a),示差檢測器均可以檢測到木糖醇對照品(b)與L-木酮糖對照品(c),供試品溶液在木糖醇與L-木酮糖的保留時間位置處無明顯雜質(zhì)出現(xiàn)(d);由圖2可見,空白培養(yǎng)基無雜質(zhì)峰出現(xiàn)(a),紫外檢測器無法檢測到木糖醇對照品(b),只能檢測到 L-木酮糖對照品(c),供試品溶液在L-木酮糖保留時間處也無明顯雜質(zhì)峰出現(xiàn)(d)。表明本文建立的HPLC法木糖醇與L-木酮糖分離度高,且不受發(fā)酵液中其它組分干擾,可用于木糖醇與L-木酮糖的含量測定。
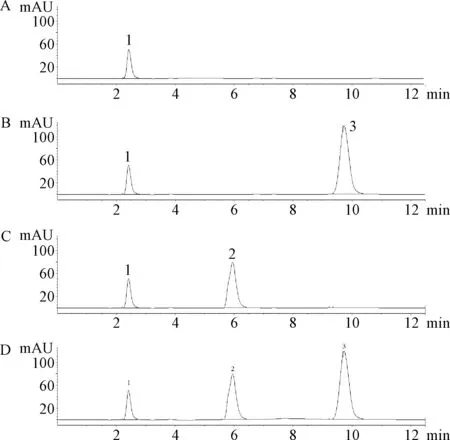
圖1 示差折光檢測器色譜圖a:空白培養(yǎng)基;b:木糖醇對照品溶液;c:L-木酮糖對照品溶液;d:樣品溶液1:溶劑峰;2:L-木酮糖;3:木糖醇Fig.1 Chromatograms detected by refractive index (RI) detector a:blank fermentation broth sample;b:xylitol standard;c:L-xylulose standard;d:fermentation broth sample 1:solvent peak;2:L-xylulose;3:xylitol

圖2 紫外檢測器檢測色譜圖a:空白培養(yǎng)基;b:木糖醇對照品溶液;c:L-木酮糖對照品溶液;d:樣品溶液1:溶劑峰;2:L-木酮糖Fig.2 Chromatograms detected by ultraviolet(UV) detector a:blank fermentation broth sample;b:xylitol standard;c:L-xylulose standard;d:fermentation broth sample 1:solvent peak;2:L-xylulose
2.2 標(biāo)準(zhǔn)曲線結(jié)果 木糖醇和L-木酮糖標(biāo)準(zhǔn)曲線測定結(jié)果見表1。

表1 木糖醇和L-木酮糖的回歸方程、相關(guān)系數(shù)、線性范圍、
2.3 精密度試驗 取同一份木糖醇對照品溶液,準(zhǔn)確稀釋至5.00、15.00、25.00 g/L 3 個質(zhì)量濃度,按1.2.1色譜條件進行檢測,測得日內(nèi)RSD分別為 0.27%、0.41%、0.64%。測得日間RSD分別為0.32%、0.80%、0.35%。
取同一份L-木酮糖的對照品溶液,準(zhǔn)確稀釋至5.00、15.00、25.00 g/L 3個質(zhì)量濃度,按1.2節(jié)色譜條件進行檢測,測得日內(nèi)RSD分別為0.16%、0.08%、0.31%,測得日間RSD分別為0.28%、0.20%、0.59%。
木糖醇與L-木酮糖的RSD均小于2.00%,符合檢測要求。
2.4 回收率試驗結(jié)果 分別配制5.00、15.00和25.00 g/L的木糖醇和L-木酮糖對照品溶液,加入空白發(fā)酵培養(yǎng)基,回收率結(jié)果見表2。可見高、低、中3個濃度的木糖醇和L-木酮糖的加樣回收率都在99.00%~101.00%之間,符合檢測要求。
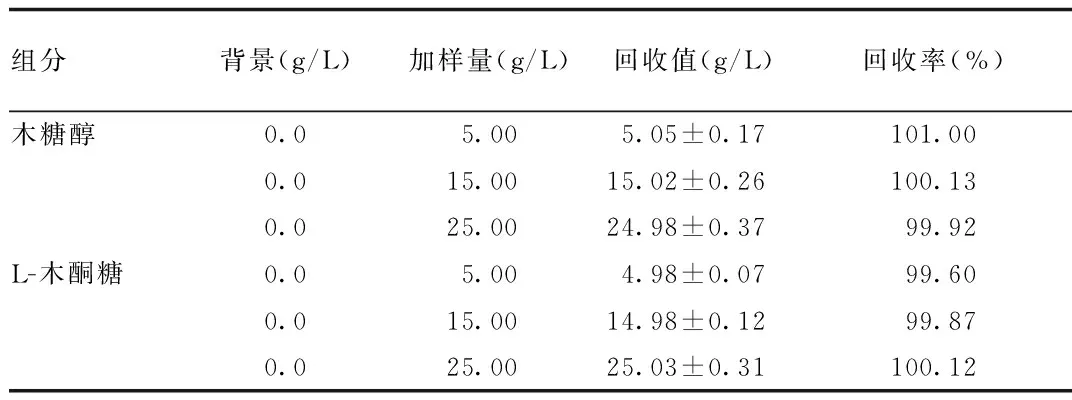
表2 發(fā)酵培養(yǎng)基中木糖醇與L-木酮糖的回收率

圖3 發(fā)酵過程中木糖醇和L-木酮糖含量的變化情況Fig.3 The content changes between xylitol and L-xylulose in the fermentation broth during the fermentation process
2.5 發(fā)酵終點的確認(rèn) 由圖3可知,隨著發(fā)酵時間的增加,底物的含量逐漸減小,產(chǎn)物的含量逐漸增多。當(dāng)發(fā)酵進行到24 h時,約86%的底物木糖醇轉(zhuǎn)化成為產(chǎn)物L(fēng)-木酮糖,約10%左右的木糖醇在發(fā)酵過程中作為木醋桿菌生長的碳源,發(fā)酵24 h與發(fā)酵30 h的產(chǎn)物含量幾乎沒有變化,但與發(fā)酵18 h相比,卻存在顯著性差異,因此判定發(fā)酵24 h為木糖醇轉(zhuǎn)化生產(chǎn)L-木酮糖的發(fā)酵終點。
3 討論
木糖醇和L-木酮糖的折光率不同,可以使用示差折光檢測器來進行測定,但木醋桿菌在發(fā)酵過程中會產(chǎn)生較多的代謝產(chǎn)物,且發(fā)酵培養(yǎng)基中除了蛋白胨和酵母粉外,還含有部分雜質(zhì),這些代謝產(chǎn)物和雜質(zhì)中如果存在結(jié)構(gòu)或保留時間與木糖醇或 L-木酮糖相似的物質(zhì),單用示差折光檢測器難以發(fā)現(xiàn)。此外,木糖醇屬于糖醇類物質(zhì),幾乎沒有紫外吸收,因此引入紫外檢測器來提高實驗結(jié)果的可靠性。對L-木酮糖進行全波長掃描發(fā)現(xiàn),其結(jié)構(gòu)中的酮基的最大紫外吸收峰在210 nm左右,因此以210 nm作為L-木酮糖的測定波長。
使用HPLC對糖類物質(zhì)進行測定常用的色譜柱是C18柱,流動相是乙腈-水或甲醇-水系統(tǒng),乙腈和甲醇的紫外吸收峰的截止波長分別在190 nm和205 nm附近,如果使用甲醇作為流動相,其背景吸收較大,會對L-木酮糖測定產(chǎn)生干擾。為此選擇乙腈-水作為流動相。
柱溫太低,會導(dǎo)致色譜柱內(nèi)壓力升高,樣品分離度會變差;柱溫過高,會降低色譜柱的使用壽命。C18色譜柱規(guī)定的最高溫度為50 ℃左右,經(jīng)反復(fù)驗證,本實驗的色譜柱最佳柱溫在35 ℃,可以使流動相黏度變小,提高樣品的溶解度,較好地保證了峰形與分離度。
流速低于0.8 mL/min時,樣品的峰形變寬,保留時間延長,甚至有色譜峰拖尾現(xiàn)象產(chǎn)生,降低測定效率;高于0.8 mL/min時,峰形變窄,保留時間過短,影響對樣品的定量與定性分析。經(jīng)反復(fù)調(diào)整后選擇流速為0.8 mL/min。
本文建立的方法可以同時測定發(fā)酵液中的L-木酮糖與殘余木糖醇的含量,分辨率高、線性范圍廣,且發(fā)酵液中的其它組分對這2種物質(zhì)的測定均不產(chǎn)生影響,可以實時反映木糖醇發(fā)酵生產(chǎn)L-木酮糖的全過程,結(jié)果準(zhǔn)確可靠。
[1] Meng Q,Zhang T,Jiang B,et al.Advances in applications,metabolism,and biotechnological production of L-xylulose[J].Appl Microbiol Biotechnol,2016,100(2):535-540.
[2] Usvalampi A,Turunen O,Valjakka J,et al.Production of L-xylose from L-xylulose using Escherichia coli L-fucose isomerase[J].Enzyme Microb Technol,2012,50(1):71-76.
[3] Usvalampi A,Kiviharju K,Leisola M,et al.Factors affecting the production of L-xylulose by resting cells of recombinant Escherichia coli[J].J Ind Microbiol Biotechnol,2009,36 (10):1323-1330.
[4] Tamburini E,Costa S,Marchetti MG,et al.Optimized production of xylitol from xylose using a Hyper-acidophilic Candida tropicalis[J].Biomolecules,2015,5(3):1979-1989.
[5] 李良智,胡學(xué)東,胡翠英.L-核酮糖的合成研究進展[J].食品工業(yè),2014,35(10):217-222.
[6] 沐萬孟,江波,程麗芳.戊糖類物質(zhì)生物轉(zhuǎn)化生產(chǎn)的研究進展[J].食品與發(fā)酵工業(yè),2007,33(11):93-97.
[7] 張玉寶,趙祥穎,楊麗萍,等.一株產(chǎn)L-木酮糖菌株的分離篩選及鑒定[J].食品科學(xué),2014,35(1):199-203.
[8] 張松青,游鵬程.木糖醇在醫(yī)藥領(lǐng)域的應(yīng)用[J].中國醫(yī)院藥學(xué)雜志,2007,27(11):1582-1584.
[9] 汪邯鄲,熊陽,何維維,等.木糖醇注射液中木糖醇的含量測定[J].現(xiàn)代醫(yī)藥衛(wèi)生,2005,21(16) :2115-2116.
[10] 張惟杰 主編.糖復(fù)合物生化研究技術(shù)[M].2版.杭州:浙江大學(xué)出版社,1999:12-20.
[11] 章銀良.食品檢驗教程[M].北京:化學(xué)工業(yè)出版社,2006:250.
[12] 張永勤,王哲平,宋雨梅,等.還原糖測定方法的比較研究[J].食品工業(yè)科技,2010,31(6):321-323,326.
[13] 劉宇鵬,潘龍,鄭小娟,等.發(fā)酵液中L-赤蘚酮糖的紫外法測定[J].江蘇農(nóng)業(yè)科學(xué),2014,42(8):281-283.
[14] 潘龍,靳魁奇,劉宇鵬.靜息細(xì)胞轉(zhuǎn)化赤蘚糖醇生產(chǎn)L-赤蘚酮糖條件優(yōu)化[J].食品與發(fā)酵工業(yè),2014,40(12):72-76.
[15] 張玉寶.轉(zhuǎn)化木糖醇生產(chǎn)L-木酮糖菌株的篩選[D].泰安:山東農(nóng)業(yè)大學(xué),2013:20.
[16] 趙光輝,王成福,李俊萍.采用高效液相色譜法測定木糖醇產(chǎn)品中各組分含量[J].食品與發(fā)酵工業(yè) 2004,30 (7):117-119.
(編校:吳茜)
Simultaneous determination of xylitol and L-xylulose in fermentation broth with high performance liquid chromatography
GE Chi-yu1, JIANG Jie1, WENG Xu1, ZHANG Jun-li2Δ
(1.School of Pharmacy, Jiangsu Food and Pharmaceutical Science College, Huai’an 223003, China;2.Jiangsu Protein Drug Engineering Laboratory, Huai’an 223003, China)
ObjectiveA high performance liquid chromatographic (HPLC) method was established for the simultaneous determination of xylitol and L-xylulose in fermentation broth.MethodsThe chromatographic conditions were as follows:C18 column (250 mm×4.6 mm) with the temperature 35 ℃, acetonitrile-water (85:15,v/v)as mobile phase with the flow rate of 0.8 mL/min.Xylitol was detected by refractive index (RI) detector at 33 ℃ and L-xylulose was determined by ultraviolet (UV) detector at 210 nm at room temperature.ResultsThis method showed good linearity over the range from 0.50~30.00 g/L with a correlation coefficient of 0.9995 for xylitol and 0.30~30.00 g/L with a correlation coefficient of 0.9986 for L-xylulose. Moreover, the limit of quantification (LOQ) for xylitol and L-xylulose were 0.58 and 0.40,respectively.The limit of determination (LOD) for xylitol and L-xylulose were 0.18 and 0.15,respectively.The relative standard deviations (RSDs) of intraday and interday for xylitol were less than 0.64%and 0.80%,respectively.The intraday and interday RSDs for L-xylulose were less than 0.31%and 0.59%.The recoveries of xylitol and L-xylulose in fermentation broth were between 99.00%-101.00%.ConclusionThere was no interference from other constitutes in the fermentation broth by this method.The methods were suitable for the simultaneous determination of the substrate xylitol and the product L-xylulose in fermentation process.
high performance liquid chromatographic (HPLC); simultaneous determination; xylitol; L-xylulose; fermentation broth
10.3969/j.issn.1005-1678.2016.06.58
江蘇省高等學(xué)校大學(xué)生創(chuàng)新創(chuàng)業(yè)訓(xùn)練計劃項目(201513104018X)
葛馳宇,男,博士,工程師,研究方向:微生物與生化藥學(xué),E-mail:gechiyu2002@163.com;通信作者,張君麗,女,工程師,研究方向:微生物與生化藥學(xué),E-mail:junli0009@163.com。
O658
A

