超聲造影肝實質灌注峰值強度反映肝硬化肝實質血流灌注變化的準確性
吳乃安 周亮
?
超聲造影肝實質灌注峰值強度反映肝硬化肝實質血流灌注變化的準確性
吳乃安周亮
830002烏魯木齊新疆自治區人民醫院
【摘要】目的探究超聲造影峰值強度反映肝硬化肝實質血流灌注的準確性,評價超聲造影在診斷肝硬化方面的價值。方法將2013年3月—2015年5月于我院就診并確診的43例肝硬化患者作為病例組,同時以同期來我院體檢健康者36名作為對照組,對以上79例(名)研究對象行超聲造影檢查,采用QLAB時間-強度曲線對造影過程進行定量分析,對兩組間定量參數(開始顯影時間、達峰時間、峰值強)差異性比較。選擇肝實質灌注峰值強度繪制時間-強度曲線,并采用受試者工作特征曲線(ROC)進行分析。結果病例組相比對照組,肝靜脈開始顯影時間及肝實質達峰時間明顯延遲(P<0.05);而肝動脈、門靜脈開始顯影時間,肝動脈、門靜脈、肝靜脈達峰時間及峰值強度在兩組間差異無統計學意義(P>0.05)。在肝實質灌注峰值強度界值為29.26 dB時,超聲造影診斷肝硬化的靈敏度及特異度最高,分別為88.6%和79.3%。結論肝臟造影的某些參數可以準確地反映肝硬化患者血流灌注的變化,肝實質灌注峰值強度大于或等于29.26 dB時,超聲對肝硬化的診斷具有較高的特異度。
【關鍵詞】超聲造影;肝實質血流灌注;肝硬化;峰值強度
肝硬化是各種慢性肝病發展的晚期階段,發病率較高,目前診斷肝硬化需依據患者病史、臨床表現、實驗室檢查及影像學檢查綜合結果,上述輔助檢查的特異性低。因此,肝硬化早期患者未出現臨床癥狀體征時,很難診斷肝硬化,確診需做有創的肝穿刺活檢,常常難以被患者接受,早期肝硬化診斷問題便成了臨床醫師很棘手的難題[1]。近年來,隨著超聲造影技術的不斷發展,應用造影劑在超聲下顯示出肝血管及肝實質的血流灌注時間及強度已成為可能。由于肝硬化患者,肝內小血管閉塞、扭曲或受到擠壓,血液循環紊亂,可引起肝內血流灌注的變化,因此推測早期肝硬化患者,即使尚未出現臨床癥狀,但往往病理改變已經形成,超聲造影后的參數很有可能與健康者有區別[2]。本次研究通過對比肝硬化患者與健康者之間超聲造影的各項定量參數差異和特點,進一步探索超聲造影在肝硬化的診斷和治療過程中的重要價值。
資料和方法
一、一般資料
選擇2014年3月—2015年5月就診于我院并經臨床外科(活檢)及病理學鑒定為肝硬化的患者43例作為病例組,其中男/女,29/14,年齡在28~67歲之間,平均年齡(52.5+10.3)歲,按肝硬化病因類型分為肝炎導致33例、酒精性5例、藥物性3例、自身免疫性2例。排除標準:(1)脾切除術后,門-體靜脈分流或斷流術后;(2)門靜脈血栓形成;(3)合并嚴重的心腎功能不全;(4)合并其他血液疾病或甲狀腺功能異常;(5)合并糖尿病;(6)對造影劑過敏者[3-4]。36名對照組為來自體檢中心的同期健康志愿者,均無肝病病史,且體檢時肝功能正常,男性/女性:22/14,年齡在25~66歲之間,平均年齡(50.7+11.6)歲。
二、儀器與方法
(一)儀器
采用荷蘭飛利浦公司生產的iU22型彩色多普勒超聲診斷儀,C5-2探頭,頻率2~5 MHz,應用反向脈沖諧波顯像技術原理。造影劑為英國阿莫仙醫藥公司生產的超聲造影劑,造影劑預處理為5 mL生理鹽水稀釋震蕩備用[5]。
(二)方法
所有研究對象取左側臥位,先行彩色多普勒對門靜脈、肝動脈、肝靜脈的血液流速情況進行初步分析,調整儀器使肝靜脈、門靜脈、肝動脈在同一斷面時,切換至造影模式,抽取造影劑2.4 mL注入患者肘靜脈,立即推入5 mL生理鹽水,待造影劑于肝臟顯影時,囑患者屏氣30 s后平穩呼吸,由兩名專業超聲醫師負責記錄并分析各定量參數[6]。根據影響因素資料對肝實質灌注峰值強度進行時間-強度曲線的繪制,并采用ROC曲線進行分析。
三、統計學方法
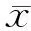
結果
一、病例組和對照組肝血管開始顯影時間記錄結果
肝動脈、門靜脈開始顯影時間在兩組間差異無統計學意義(P均>0.05),病例組與對照組相比,肝硬化患者肝靜脈開始顯影時間明顯延遲,差異具有統計學意義(P<0.05),見表1。
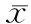
表1 病例組與對照組肝血管開始顯影時間情況(±s)
注:與對照組相比,*P<0.05
二、病例組和對照組造影劑達峰時間記錄結果
肝動脈、門靜脈及肝靜脈造影劑達峰時間在兩組間的差異無統計學意義(P均>0.05);肝實質達峰時間,病例組明顯延長,差異有統計學意義(P<0.05),見表2。
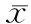
表2 病例組與對照組造影劑達峰時間情況(±s)
注:與對照組相比,*P<0.05
三、病例組與對照組峰值強度記錄結果
肝動脈、門靜脈、肝靜脈的峰值強度在兩組間的差異無統計學意義(P>0.05),病例組肝實質的灌注峰值強度病例數明顯低于對照組,差異有統計學意義(P< 0.05),見表3。
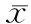
表3 病例組與對照組灌注峰值強度情況(±s)
注:與對照組相比,*P<0.05
四、肝實質的時間-強度曲線及ROC分析結果
以肝硬化1-特異度作為橫坐標,縱坐標為敏感度,進行ROC分析曲線標繪。兩組曲線下面積分別為病例組(0.91+0.03)、對照組(0.89+0.018),差異有統計學意義(P<0.05)。選擇靈敏度和特異度最優值作為是否診斷肝硬化的最佳閾值即29.26 dB,此時超聲造影診斷肝硬化的靈敏度為88.6%(影像學懷疑病例數:38/總病例數:43),特異度為79.3%(影像學確診病例:34/總病例數:43)。

圖1 對照組正常超聲造影時間-強度曲線

圖1 病例組肝硬化患者超聲造影后時間-強度曲線
討論
肝硬化的病理改變包括以下5個方面(1)各種致病因素導致大量肝細胞變性壞死,肝小葉結構破壞;(2)再生的肝細胞已失去正常組織排列結構,形成大小及功能都發生了變化,以不規則的肝細胞團形式存在;(3)各種致病因素導致纖維結締組織沿肝小葉中央靜脈-匯管區或匯管區-匯管區之間增生,纖維組織的增生會傾向包圍再生的肝細胞形成肝硬化病變典型的“假小葉”,同時假小葉內肝細胞排列紊亂進一步加劇,出現變性壞死或再生的肝細胞同時存在;(4)肝內小膽管增生;(5)肝內小血管閉塞、扭曲、受壓,小血管之間新的吻合支形成,引起肝內血液循化紊亂,是形成門靜脈高壓的病理基礎[7-8]。
在肝臟血流發生灌注變化時,相應的造影劑微泡的回聲效應也會隨著變化,超聲造影技術就是基于這一原理對肝臟的血流動態變化進行觀察。由于肝硬化患者受到異常增生肝細胞的影響對小血管的壓力增大,必然導致了肝內小血管收縮、肝內動靜脈分流、血管流出道梗阻現象的出現,相應的導致門靜脈系統血管阻力增加,血流量進行性減少,即便內臟高動力循環狀態可能會部分增加經門靜脈系統入肝的血流[9-10]。但由于肝硬化患者門-體靜脈側支循環開放,增加的血流大部分經側支循環流入體循環,分支血流明顯。因此綜合來看,肝硬化患者隨著病情的變化通過門靜脈途徑進入肝臟的血流量減少,甚至有些患者出現逆向出肝血流[11]。而經肝動脈系統入肝的血流量可出現不同程度的增加以代償經門靜脈系統減少的入肝血流,正常人可全部代償,肝硬化患者由于肝內血管床受壓、閉塞以及肝內動靜脈吻合支形成等原因,導致肝動脈系統阻力亦可出現不同程度的升高,因此代償能力有限[12-13]。本次超聲造影結果顯示,肝硬化患者的肝臟血流的達峰時間明顯延遲,與肝硬化的病理血流分析結果相符。
超聲造影為無創檢查,容易被患者接受。在無創檢查中,超聲在反映臟器血流灌注方面優于CT或MRI;且超聲造影技術在反映肝硬化患者肝臟血流灌注上,無論是理論方面或是實踐方面的價值都得到了證實。本次研究結果發現,經過ROC曲線繪制,并選擇診斷肝硬化的靈敏度及特異度結合的最優點位置,其靈敏度和特異度分別為88.6%、 79.3%。此時的肝實質血流灌注閾值(強度)為29.26 dB時,與相關研究比較發現特異度較低,原因主要是因為本研究沒有排除部分肝內分流的中晚期肝硬化患者,因為肝內分流是肝硬化患者中晚期門靜脈高壓的并發癥,分流的產生會造成肝實質在灌注峰值強度增加,靈敏度的增加必然會導致特異度的降低[14]。同時相關研究表明,CT診斷肝硬化的靈敏度及特異度分別為66.4%和58.5%,遠遠低于超聲造影[15]。且超聲造影檢查對人體無放射性損害等優勢,體內有金屬植入物的患者亦可接受此檢查,價格合理等,在診斷肝硬化方面臨床應用價值較高,前景可觀。
綜上所述,肝硬化患者肝實質血流灌注明顯低于正常人,超聲造影對于肝硬化的診斷價值較高,造影的峰值強度為29.26 dB是診斷肝硬化的最優界值。
參考文獻
[ 1 ]張金輝.超聲造影肝實質灌注峰值強度評價肝硬化的可行性研究.臨床和實驗醫學雜志,2014,13:932-934.
[ 2 ]吳迪,姚克純,李利,等.實時心肌超聲造影在評價冠狀動脈再通前后心肌血流灌注及隨訪中的價值.臨床和實驗醫學雜志,2013,12:747-749.
[ 3 ]劉冬,王金銳,錢林學,等.超聲造影評價肝硬化門脈高壓的可行性研究.中華醫學超聲雜志(電子版) ,2010,7:28-30.
[ 4 ]陳敏.實時超聲造影技術與病理對照評價肝纖維化分期的實驗研究. 山西:山西醫科大學,2013.
[ 5 ]韓萍,張健,李永綱,等.瞬時彈性掃描診斷肝纖維化準確性研究. 傳染病信息, 2010, 23: 139-140,143.
[ 6 ]Ishibashi H, Maruyama H, Takahashi M, et al. Assessment of hepatic fibrosis by analysis of the dynamic behaviour of microbubbles during contrast ultrasonography. Liver Int, 2010, 30: 1355-1363.
[ 7 ]Li N, Ding H, Fan P, et al. Intrahepatic transit time predicts liver fibrosis in patients with chronic hepatitis B: quantitative assessment with contrast-enhanced ultrasonography. Ultrasound Med Biol, 2010, 36: 1066-1075.
[ 8 ]葛永祥,王麗輝,馬健.肝纖維化診斷新進展. 醫學綜述, 2011,17:2952-2955.
[ 9 ]包中濤,葉真,古立娟,等.肝動靜脈渡越時間及剪切波速評估肝纖維化程度的對比研究.臨床超聲醫學雜志,2014,16:10-13.
[10]楊立新,魏強,馬芝倩,等.超聲造影在肝癌殘存病灶微波消融治療中的應用.現代醫學,2014,42:395-397.
[11]裴書芳,叢淑珍,馮占武,等.實時組織彈性成像診斷肝纖維化.中國醫學影像技術,2010,26:893-895.
[12]王彥冬,經翔. 術中超聲在肝癌手術中的應用進展. 武警后勤學院學報(醫學版),2014,23:177-186.
[13]經翔, 丁建民, 王彥冬, 等. 術中超聲在肝癌切除術中的應用研究. 中華醫學超聲雜志(電子版), 2010, 7:1674-1679.
[14]Wagnetz U, Atri M, Massey C, et al. Intraoperative ultrasound of the liver in primary and secondary hepatic malignancies: comparison with preoperative 1.5-T MRI and 64-MDCT. Am J Roentgenol, 2011, 196: 562-568.
[15]董家鴻, 唐茂盛, 張文智, 等. 精準肝臟外科理念和技術對大范圍肝切除圍手術期安全性的影響. 中華消化外科雜志, 2013, 12: 344-351.
(本文編輯:易玲)
(收稿日期:2015-12-30)

