牛初乳中免疫球蛋白G雙抗夾心ELISA檢測方法的建立
劉 金,王麗威,2,岳喜慶,*(.沈陽農業大學食品學院,遼寧 沈陽 0866;2.遼寧工程技術大學理學院,遼寧 阜新 23000)
?
牛初乳中免疫球蛋白G雙抗夾心ELISA檢測方法的建立
劉 金1,王麗威1,2,岳喜慶1,*
(1.沈陽農業大學食品學院,遼寧 沈陽 110866;2.遼寧工程技術大學理學院,遼寧 阜新 123000)
將牛免疫球蛋白G(immunoglobulin G,IgG)作為免疫原免疫BALB/c小鼠,通過細胞融合、篩選獲得分泌抗牛IgG單克隆抗體的細胞株。制備小鼠腹水抗體,進一步純化獲得抗牛IgG單克隆抗體。建立雙抗夾心酶聯免疫吸附法檢測牛初乳中IgG質量濃度,該方法在7.8~1 000 ng/mL范圍內有良好的線性關系,最低檢出限為7.06 ng/mL,批內變異系數為4.52%,批間變異系數為4.94%,回收率為91.85%~102.45%。此法操作簡便、準確度高、穩定性好,可用于實際牛初乳樣品的快速檢測。
牛初乳;免疫球蛋白G;單克隆抗體;雙抗夾心酶聯免疫吸附法
牛初乳一般是指奶牛分娩7 d內的乳汁。牛初乳不但含有常乳中的營養物質(蛋白質、脂肪、乳糖、脂肪酸、氨基酸和礦物質),還富含多種生理活性因子,包括免疫球蛋白、乳鐵蛋白、生長因子、乳過氧化氫酶和溶菌酶等[1]。其中,免疫球蛋白是最重要的一類免疫因子,牛初乳中的免疫球蛋白主要是IgG、IgM和IgA,其中IgG的含量最高,約占80%~90%[2-3]。因此,IgG含量成為衡量牛初乳及其制品質量的重要指標。目前,牛初乳中IgG檢測方法主要包括免疫擴散法[1,3-6]、免疫比濁法[1,6-8]、高效液相色譜法[1,9-10]、酶聯免疫吸附(enzyme linked immunosorbent assay,ELISA)法[1,11-16]和表面等離子體共振法[16]等。這些方法中免疫擴散法應用最為廣泛。但此法檢測時間長、精確度不高。高效液相色譜法操作繁瑣,不適合大批量檢測。ELISA法是近年來迅速發展的一類檢測方法,其操作簡便、特異性好、準確度高,適合大量樣品檢測,在多個領域都得到了廣泛應用。在牛初乳IgG含量檢測中,國外已成功開發了試劑盒,反應模式多數是競爭模式,也有夾心模式。我國在這方面起步較晚,目前主要依賴進口檢測試劑盒。本研究采用單克隆抗體和多克隆抗體,建立雙抗夾心ELISA法檢測牛初乳中IgG含量,為牛初乳的生產加工和質量監控提供可靠的檢測方法。
1 材料與方法
1.1 材料與試劑
牛初乳樣品為奶牛分娩3 d內所分泌的乳汁,采自遼寧輝山乳業,-20 ℃貯存。
BALB/c小鼠 白求恩醫科大學動物試驗中心;標準牛IgG、弗氏完全佐劑、弗氏不完全佐劑、聚乙二醇、雞卵清白蛋白、冷水魚明膠、辣根過氧化物酶標記羊抗鼠IgG抗體 美國Sigma公司;辣根過氧化物酶標記兔抗牛IgG多克隆抗體 博奧森公司;3,3′,5,5′-四甲基聯苯胺(3,3′,5,5′-tetramethylbenzidine,TMB)、96 孔酶標板、小鼠單隆抗體亞類鑒定試劑盒 鼎國昌盛生物技術公司;其他試劑純度均為分析純。
1.2 儀器與設備
Epoch微孔板分光光度計 美國Bio-Tex公司;移液器 美國Thermo公司;Milli-Q超純水系統 美國Millipore公司。
1.3 方法
1.3.1 溶液的配制
包被液:0.05 mol/L碳酸鹽緩沖液(pH 9.6);緩沖液:0.01 mol/L 磷酸鹽緩沖液(phosphatebuffered saline,PBS)(pH 7.4)、0.05 mol/L Tris-HCl緩沖液(pH 8.0);稀釋液:0.01%、0.05%磷酸鹽吐溫緩沖液(phosphate-buffered saline with Tween-20,PBST)(0.01 mol/L PBS溶液中分別加入0.01%、0.05% Tween-20)、0.05% Tris-HCl吐溫緩沖液(Tris-HCl with Tween-20,TBST)(0.05 mol/L Tris-HCl溶液加入0.05% Tween-20);底物:TMB底物;終止液:2 mol/L H2SO4。
1.3.2 抗體的制備
選擇6~8 周齡的雌性BALB/c小鼠,首次免疫時用標準牛IgG與等量弗氏完全佐劑充分乳化,腹腔注射,100 μg/只;2 周后進行二次免疫,與等量弗氏不完全佐劑充分乳化,腹腔注射,100 μg/只;二次免疫1周后尾尖采血,間接ELISA測定血清效價,血清效價達到6 000用于細胞融合。在融合前不加佐劑加強免疫,3 d后取鼠脾細胞,與sp20骨髓瘤細胞用聚乙二醇誘導融合后培養。采用間接ELISA法篩選陽性孔,克隆化培養[17]。選取效價最高的雜交瘤細胞注射于小鼠腹腔中,1 周后采集腹水,采用辛酸-硫酸銨法粗提純后,使用Protein G親和層析柱純化并進行十二烷基磺酸鈉-聚丙烯酰胺凝膠電泳(sodium dodecyl sulfate-polyacrymide gelelectrophoresis,SDS-PAGE)電泳分析[18]。測定單抗亞類、蛋白質質量濃度及純度,間接ELISA法測定純化前后效價、抗體親和力[18]。
1.3.3 雙抗夾心法的建立
包被:用包被液將1.3.2節制備的小鼠抗牛IgG單抗稀釋至一定質量濃度,每孔100 μL包被酶標板,4 ℃過夜;洗滌:棄去孔內溶液并拍打,每孔加入洗滌液200 μL后,洗板60 s,重復3 次,在每兩步驟之間均需洗滌,以下同;封閉:每孔200 μL封閉劑,37 ℃孵育;加樣:每孔加100 μL標準牛IgG或,37 ℃孵育;加酶標抗體:每孔加100 μL辣根過氧化物酶標兔抗牛IgG多克隆抗體(以下簡稱酶標抗體),37 ℃孵育,洗滌4 次;加底物顯色:各反應孔中加入剛剛配制的TMB底物溶液100 μL,37 ℃暗處反應10 min;終止反應:每孔加2 mol/L硫酸50 μL,酶標儀450 nm波長條件下讀取OD值。以不加牛IgG的空白孔作為陰性對照。
1.3.4 包被抗體及酶標抗體工作質量濃度的確定
采用方陣法確定單抗包被質量濃度和酶標抗體質量濃度,將純化后單抗按500、1 000、2 000、4 000 倍稀釋,包被酶標板;將酶標抗體分別稀釋至2 000、4 000、8 000、10 000 倍,選取陽性值(P值)1.0~1.5之間左右為最佳質量濃度條件。
1.3.5 樣品稀釋液的確定
按照最優條件進行操作,將稀釋液為分為3 組:a.0.01% PBST;b.0.05% PBST;c.0.05% TBST,測定OD450 nm值并計算陽性值/陰性值(P/N值),選擇P/N最大值對應的稀釋液作為最佳稀釋液。
1.3.6 封閉劑及封閉時間的確定
分別用0.1 mol/L氯化銨溶液、1%脫脂奶粉、1% OVA、1%冷水魚明膠作為封閉劑,計算P/N值。選擇最優封閉劑;封閉時間分別在設置37℃ 30、60、90、120 min,其余步驟按照夾心ELISA法,計算P/N值。
1.3.7 抗原及酶標抗體作用時間的確定
根據已確定的條件進行操作,分別設置抗原與抗體作用時間:37 ℃ 30、45、60、90 min;酶標抗體作用時間:37 ℃ 15、30、45、60 min,計算P/N值。
1.3.8 標準曲線的建立及靈敏度
將標準牛IgG連續稀釋至7.8、15.625、31.25、62.5、125、250、500、1 000 ng/mL質量濃度,按優化后的雙抗夾心ELISA方法,測定OD450 nm值。每個質量濃度設3 個平行。以標準品質量濃度值的對數為橫坐標,OD值為縱坐標,采用Excel計算回歸方程,繪制標準曲線,并根據結果計算最低檢出限,即靈敏度。
1.3.9 精密度實驗
采用優化后的雙抗夾心ELISA方法,檢測0.2 μg/mL標準牛IgG樣品,同一批次選取不同孔重復10 次,計算標準差和變異系數,表示批內差異;逐批重復10 次,計算標準差和變異系數,表示批間差異。
1.3.10 加標回收率實驗
取3 份同樣的牛初乳樣品,稀釋106倍后,取1 mL,分別加入0.2 mg/mL標準牛IgG 0.5、1、2.5 μL,使終質量濃度分別為100、200、500 ng/mL,按優化后的方法測定,每個質量濃度做3 次重復,計算加標回收率。
1.3.11 實際樣品檢測
按優化的ELISA方法測定10 份牛初乳樣品中IgG的含量。將樣品稀釋106倍后按優化后的方法測定后進行計算,每個樣品重復3 次,結果以平均值表示。
2 結果與分析
2.1 單克隆抗體鑒定
經亞類鑒定試劑盒測定,單抗亞類為IgG1;純化前單抗蛋白質量濃度為46.85 mg/mL,辛酸-硫酸銨法純化后質量濃度為10.88 mg/mL,親和層析純化后質量濃度為2.21 mg/mL,兩種方法純化后效價均為2.56×106,將原腹水及辛酸-硫酸銨法、親和層析兩種純化后的抗體進行SDS-PAGE電泳,結果如圖1、2所示,可直接觀察出純化前腹水中雜蛋白較多,辛酸-硫酸銨法純化后,可去除一部分雜蛋白,目的蛋白條帶逐漸清晰,而親和層析純化法后,條帶清晰,只有重鏈及輕鏈兩部分,分別位于50、25 kD處,純度較高,進一步測定親和力常數為8.92×108L/mol。

圖1 親和層析純化腹水Fig.1 Affinity chromatography of purified ascite

圖2 腹水單抗純化 SD S-P AG E凝膠電泳圖Fig.2 SDS-PAGE gels electrophoresis of purified ascites
2.2 雙抗夾心ELISA法的建立
2.2.1 包被單抗及酶標抗體質量濃度的確定
反應體系中此條件最為關鍵,優化方法采用方陣法,結果如表1所示,根據經驗值OD值在1.0~1.5之間建立標準曲線比較合適,綜合判斷選擇單抗稀釋1 000 倍,酶標抗體稀釋2 000 倍。

表1 包被單抗及酶標抗體質量濃度Table1 Coat in g c on centrati on s of McAb and diluti on of H RP-Ab
2.2.2 樣品稀釋液的確定
為降低空白值,提高準確性,故對稀釋液進行優化,由圖3可以看出,a組與b組P值相近,c組略低,但是b組與c組N值較低,且b組P/N值最大,因此確定0.05% PBST為樣品稀釋液。

圖3 稀釋液的確定Fig.3 Determination of the appropriate diluent
2.2.3 封閉劑及封閉時間的確定
在包被后,一般采用化學試劑或無關蛋白作為封閉劑,將酶標板未結合的位點進行封閉,減少非特異性吸附,提高靈敏度,本實驗研究4 種封閉劑效果,結果如圖4所示。由圖4可以看出,0.1 mol/L氯化銨作為封閉劑時,P/N值最大,說明0.1 mol/L氯化銨封閉效果最佳。進一步研究氯化銨的封閉時間,結果如圖5所示,可以看出,37 ℃、60 min為最佳封閉時間。
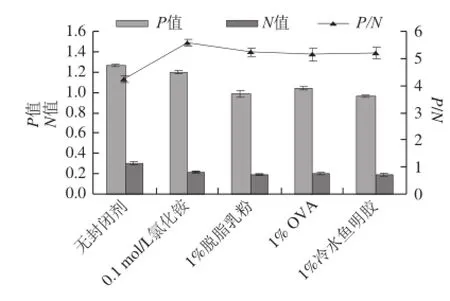
圖4 封閉劑的確定Fig.4 Determination of sealant

圖5 封閉時間的確定Fig.5 Determination of blocking time
2.2.4 抗原及酶標抗體作用時間的確定
不同反應時間其OD450 nm值相差較大,為提高靈敏度及重復性,需對抗原、酶標抗體反應時間進行優化,結果如圖6所示,可以看出,抗原作用60 min時,P/N值最大,故抗原最佳作用時間為60 min;酶標抗體作用時間如圖7所示,酶標抗體最佳作用時間為30 min。
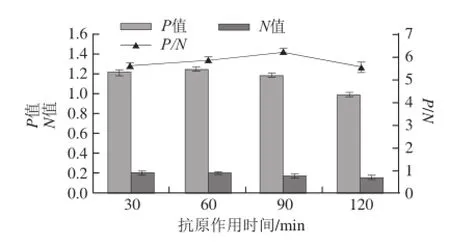
圖6 抗原作用時間的確定Fig.6 Determination of antigen action time

圖7 酶標抗體作用時間的確定Fig.7 Determination of reaction time of enzyme linked antibody
2.2.5 標準曲線及最低檢出限實驗結果
牛IgG在7.8~1 000 ng/mL范圍內,OD值與牛IgG質量濃度的對數值呈良好的線性關系。經計算,回歸方程為y = 0.470 3 lgx-0.158 2,相關系數R2= 0.992 6。隨機選擇20 個孔做空白孔檢測,求出平均值和變異系數s,最低檢出限為平均值加3 倍變異系數(+3s),經計算最低檢出限為7.06 ng/mL。
2.2.6 精密度實驗結果
對200 ng/mL標準牛IgG樣品分別進行批內和批間重復檢測,結果如表2所示,所建立的雙抗夾心ELISA法,其批內檢測平均值為197 ng/mL,變異系數為4.52%;批間檢測平均值為205 ng/mL,變異系數為4.94%,精密度符合要求。

表2 批內與批間的變異系數Table 2 Intra-assay and in ter-assayC Vs
2.2.7 加標回收率實驗結果
以100、200、500 ng/mL三個添加量測定樣品中IgG含量及回收率,結果見表3,可以看出,牛初乳樣品IgG含量為53.56 ng/mL,回收率為91.85%~102.45%,在80%~120%之間均在合理范圍內;變異系數為3.30%~5.32%,均在10%以下。

表3 加標回收率測定結果Table 3 Results of spiked recovery
2.2.8 實際樣品檢測結果
按優化的ELISA方法測定10 份樣品中牛IgG的含量,結果如表4所示。由于不同奶牛個體差異,所產牛初乳中IgG含量各不相同,IgG含量為50.29~79.68 mg/mL,平均值為65.40 mg/mL。

表4 牛初乳樣品中IgG含量Table 4 C on centrati on s of bov in e IgG in colostrum samples
3 討 論
牛初乳因含有大量的免疫球蛋白而備受關注,其檢測方法不斷發展,其中免疫學方法已成為主要的測定方法。其中免疫擴散法最為普遍,此方法是將樣品或標準牛IgG滴加于含兔抗牛IgG抗體的瓊脂板小孔中,經24 h擴散后,形成肉眼沉淀環,然后測量沉淀環的直徑,在一定質量濃度范圍內,牛IgG的含量與沉淀環的直徑呈正比,該方法操作簡便,設備要求低,結果直觀,但由于擴散直徑的測量誤差較大,導致結果準確度和靈敏度都較低,檢測效率低。我國保健食品中IgG的測定采用高效親和色譜法,主要是借助于偶聯Protein A或Protein G的親和色譜柱進行定量,線性范圍為0.2~1.0 mg/mL[19],準確度高,但操作相對繁瑣。ELISA法具有特異性強、檢測效率高等優點,適用于牛IgG的檢測。在出口牛乳制品中IgG測定的標準中,采用間接競爭ELISA法,檢測線性范圍為0~51.2 mg/L[20],可滿足目前國內牛初乳制品的質量要求,但是競爭法為兩種抗原競爭有限抗體,故與夾心法存在一定差別。研究表明,對于分子質量較大的蛋白物質的測定,夾心ELISA比競爭ELISA靈敏度高,而夾心ELISA測定牛IgG時,需要兩種抗體,即包被抗體和酶標抗體。若都采用同一動物來源的多克隆抗體,競爭表位,反應值低;若采用不同動物來源的抗體,易產生交叉反應,使背景值高,降低了方法的靈敏度。在夾心ELISA研究開發中,獲得親和力強、特異性好的配對抗體成為首要的技術步驟。單克隆抗體與多克隆抗體相比,具一定的優越性,具有特異性強、效價高、重復性好等優點。本研究制備特異性強的單克隆抗體,經純化后純度高,效價為2.56×106,親和力常數為3.9×108L/mol,在107~1012范圍內,屬高親和力抗體。另外,由于測定目標物質為牛初乳中IgG,封閉劑分為化學試劑或無關蛋白,在包被酶標板后,對酶標板未結合的位點進行封閉,減少非特異性結合,相對于化學試劑,蛋白試劑儲存效果不好,而一般市面蛋白封閉劑,例如牛血清白蛋白等蛋白試劑可能殘留IgG,如果采用進口試劑,成本較高,且實驗結果顯示氯化銨溶液封閉效果較好。
在此基礎上,對ELISA反應體系中的抗體質量濃度、稀釋液、封閉條件及反應時間等進行了優化,并對方法的準確性、精確性和適用性進行了評價。優化后的ELISA方法為:將單抗稀釋1 000 倍在4 ℃過夜包被后,加0.1 mol/L氯化銨37 ℃封閉60 min,加樣品后37 ℃反應60 min,加入2 000 倍稀釋的酶標兔抗牛抗體后37 ℃反應30 min,最后加底物顯色測值,此法回歸方程為y= 0.470 3 lgx-0.158 2,R2= 0.992 6,在7.8~1 000 ng/mL范圍內有良好的線性相關,最低檢出限能達到7.06 ng/mL,加標回收率平均值為95.87%,變異系數低于10%,穩定性好。在實際檢測中,奶牛在分娩后第一次分泌的乳汁牛初乳IgG最高,含量為50~100 mg/mL,然后將快速下降,1~2周后其含量基本與常乳一致[21-23],采用此研究方法分別檢測10份牛初乳樣品,IgG含量在為50.29~79.68 mg/mL。奶牛雖存在個體差異,但此牛場奶牛分娩3 d內所分泌的初乳能滿足初乳制品加工要求。綜合結果,本研究利用所獲抗體,建立了雙抗夾心ELISA方法,操作簡便,結果靈敏度高、準確性好、重復性強,可用于牛初乳中IgG的檢測。
[1] GAPPER L W, COPESTAKE D J, OTTER D E, et al.Analysis of bovine immunoglobulin G in milk, colostrums and dietary supplements: a review[J].Analytical and Bioanalytical Chemistry,2007, 389(1): 93-109.DOI:10.1007/s00216-007-1391-z.
[2] 徐麗, 生慶海, 王玉良, 等.牛初乳制品功能性成分的分析[J].中國乳品工業, 2004, 32(4): 18-20.DOI:10.3969/ j.issn.1001-2230.2004.04.005.
[3] GOMES V, MADUREIRA K M, SORINANO S, et al.Factors affecting immunoglobulin concentration in colostrum of healthy Holstein cows immediately after delivery[J].Pesquisa Veterinária Brasileira, 2011, 31(Suppl 1): 53-56.DOI:10.1590/S0100-736X2011001300009.
[4] MORETTI D B, NORDI W M, LIMA A L, et al.Lyophilized bovine colostrum as a source of immunoglobulins and insulin-like growth factor for newborn goat kids[J].Livestock Science, 2012, 145(1/2/3): 223-229.DOI:10.1016/j.livsci.2012.02.007.
[5] NEAVE H W, VICKERS L, VEIRA D M.Preparation of a highimmunoglobulin product from bovine colostrum[J].Animal Feed Science and Technology, 2013, 179(1/2/3/4): 133-137.DOI:10.1016/ j.anifeedsci.2012.11.007.
[6] QUIGLEY J D, LAGO A, CHAPMAN C E, et al.Evaluation of the Brix refractometer to estimate immunoglobulin G concentration in bovine colostrum[J].Journal of Dairy Science, 2013, 96(2): 1148-1155.DOI:10.3168/jds.2012-5823.
[7] GODDEN S, MCMARTIN S, FEIRTAG J, et al.Heat-treatment of bovine colostrum.Ⅱ Effects of heating duration on pathogen viability and immunoglobulin G[J].Journal of Dairy Science, 2006, 89(9): 3476-3483.DOI:10.3168/jds.S0022-0302(06)72386-4.
[8] DONAHUE M, GODDEN S M, BEY R, et al.Heat treatment of colostrum on commercial dairy farms decreases colostrum microbial counts while maintaining colostrum immunoglobulin G concentrations[J].Journal of Dairy Science, 2012, 95(5): 2697-2702.DOI:10.3168/jds.2011-5220.
[9] ABERNETHY G, OTTER D.Determination of immunoglobulin G in bovine colostrum and milk powders, and in dietary supplements of bovine origin by protein g affinity liquid chromatography: collaborative study[J].Journal of AOAC International, 2010, 93(2): 622-627.
[10] HOLLAND P T, CARGILL A, SELWOOD A L, et al.Determination of soluble immunoglobulin g in bovine colostrum products by protein g affinity chromatography-turbidity correction and method validation[J].Journal of Agricultural and Food Chemistry, 2001, 59(10): 5248-5256.DOI:10.1021/jf200839b.
[11] LEE S H, JAEKAL J, BAE C S, et al.Enzyme-linked immunosorbent assay, single radial immunodiffusion, and indirect methods for the detection of failure of transfer of passive immunity in dairy calves[J].Journal of Veterinary Internal Medicine, 2008, 22(1): 212-218.DOI:10.1111/j.1939-1676.2007.0013.x.
[12] TEIXEIRA A G V, BICALHO M L S, MACHADO V S, et al.Heat and ultraviolet light treatment of colostrum and hospital milk: effects on colostrum and hospital milk characteristics and calf health and growth parameters[J].The Veterinary Journal, 2013, 197(2): 175-181.DOI:10.1016/j.tvjl.2013.03.032.
[13] SOUSA S G, SANTOS M D, FIDALGO L G, et al.Effect of thermal pasteurisation and high-pressure processing on immunoglobulin content and lysozyme and lactoperoxidase activity in human colostrum[J].Food Chemistry, 2014, 151: 79-85.DOI:10.1016/ j.foodchem.2013.11.024.
[14] VERWEIJ J J, KOETS A P, EISENBERG S W F.Effect of continuous milking on immunoglobulin concentrations in bovine colostrum[J].Veterinary Immunology and Immunopathology, 2014, 160(3/4): 225-229.DOI:10.1016/j.vetimm.2014.05.008.
[15] GOSCH T, APPRICH S, KNEIFEL W, et al.A combination of microfiltration and high pressure treatment for the elimination of bacteria in bovine colostrum[J].International Dairy Journal, 2014,34(1): 41-46.DOI:10.1016/j.idairyj.2013.06.014.
[16] MILA H, FEUGIER A, GRELLETA, et al.Immunoglobulin G concentration in canine colostrum evaluation and variability[J].Journal of Reproductive Immunology, 2015, 112: 24-28.DOI:10.1016/ j.jri.2015.06.001.
[17] 任立松, 盧士英, 周玉, 等.檸檬黃色素免疫學檢測方法的研究[J].食品科學, 2009, 30(12): 258-261.DOI:10.3321/ j.issn:1002-6630.2009.12.059.
[18] 張瑩, 周玉, 李巖松, 等.抗κ-酪蛋白單克隆抗體的制備及其特性鑒定[J].中國畜牧獸醫, 2014, 41(3): 24-27.
[19] 衛生部.GB/T 5009.194—2003 保健品中免疫球蛋白IgG的測定[S].北京: 中國標準出版社, 2003: 537-542.
[20] 國家質量監督檢驗檢疫總局.SN/T 3132—2012 出口牛乳制品中牛免疫球蛋白G的測定: 酶聯免疫法[S].北京: 中國標準出版社,2012.
[21] CONESA C, LAVILLA M, SANCHEZ L, et al.Determination of IgG levels in bovine bulk milk samples from different regions of Spain[J].European Food Research and Technology, 2005, 220(2): 222-225.DOI:10.1007/s00217-004-1016-0.
[22] ABDEL-SALAMA Z, GHANY S H, HARITH M A.Evaluation of immunoglobulins in bovine colostrum using laser induced fluorescence[J].Talanta, 2014, 129: 15-19.DOI:10.1016/ j.talanta.2014.04.033.
[23] 馬燕芬, 陳志偉, 魏曉兵, 等.高效液相色譜法測定牛初乳中IgG含量的方法研究[J].飼料工業, 2007, 28(5): 33-38.DOI:10.3969/ j.issn.1001-991X.2007.05.010.
Development of Double Antibody Sandwich ELISA for Detection of Bovine Colostrum Immunoglobulin G
LIU Jin1, WANG Liwei1,2, YUE Xiqing1,*
(1.College of Food Science, Shenyang Agricultural University, Shenyang 110866, China;2.College of Science, Liaoning Technology University, Fuxin 123000, China)
The hybridoma cells secreting monoclonal antibody (McAb) against bovine colostrum immunoglobulin G (IgG)were developed by cell fusion technology after immunization of BALB/c mice with bovine IgG.McAbs were obtained by purification of mouse ascites.A double antibody sandwich enzyme-linked immunosorbent assay (ELISA) technique was established for the detection of bovine colostrum IgG.The linear range was 7.8-1 000 ng/mL and the limit of detection (LOD)was 7.06 ng/mL.The intra-assay and inter-assay coefficient of variations were 4.52% and 4.94%, respectively.The recovery rate was 91.85%-102.45%.The ELISA method can provide a simple, accurate and stabile approach for the rapid detection of bovine colostrum IgG.
bovine colostrum; immunoglobulin G (IgG); monoclonal antibody; sandwich ELISA
10.7506/spkx1002-6630-201614013
TS252.7
A
1002-6630(2016)14-0074-06
劉金, 王麗威, 岳喜慶.牛初乳中免疫球蛋白G雙抗夾心ELISA檢測方法的建立[J].食品科學, 2016, 37(14): 74-79.
DOI:10.7506/spkx1002-6630-201614013. http://www.spkx.net.cn
LIU Jin, WANG Liwei, YUE Xiqing.Development of double antibody sandwich elisa for detection of bovine colostrum immunoglobulin G[J].Food Science, 2016, 37(14): 74-79.(in Chinese with English abstract) DOI:10.7506/spkx1002-6630-201614013. http://www.spkx.net.cn
2015-10-03
2011年度國家星火計劃項目(2011GA650001)
劉金(1991—),女,碩士研究生,研究方向為動物性產品加工。E-mail:liujin911216@163.com
*通信作者:岳喜慶(1966—),男,教授,博士,研究方向為動物性產品加工。E-mail:yxqsyau@126.com

