急性胰腺炎與腸內營養
林燕青 林連捷 鄭長青
?
急性胰腺炎與腸內營養
林燕青林連捷鄭長青
急性胰腺炎(AP)是一種發病率和病死率均較高的暴發性疾病,營養支持在AP中的應用受到越來越廣泛的關注。大量研究表明,腸內營養(EN)優于全腸外營養(TPN),但對EN的時機選擇仍存在爭議。近年來的研究對超早期EN的療效提出了質疑,而鼻胃管與鼻空腸管用于EN具有相同療效的觀點正逐漸被接受。
急性胰腺炎;腸內營養;鼻胃管;鼻空腸管
急性胰腺炎(AP)是一種由多種病因引起的胰酶激活,繼而以胰腺局部炎性反應為主要特征,伴或不伴有其他器官功能改變的疾病。AP患者,尤其是重癥急性胰腺炎(SAP)患者,機體處于負氮平衡狀態,蛋白質分解、糖原異生和脂肪動員增加,導致機體內環境紊亂,免疫功能低下和營養不良。通過營養支持治療,機體的總蛋白、總水分、總脂肪可以得到較好的保留,在部分患者中甚至含量有所增加,因此營養支持已成為治療AP的重要措施之一。
不同地區關于AP營養支持的指南差異較大。2012年國際指南協會(ICGC)基于11個地區的診治指南總結發布了《急性胰腺炎營養治療的國際共識指南》[1],2013年國際胰腺病協會/美國胰腺協會(IAP/APA)發布了最新的AP診治指南[2],中國也于2013年修訂了新的診治指南[3]。三個指南在營養支持的適應證方面達成了共識,在其他方面則分歧較多(具體見表1)。主要的爭論點在于:(1)腸內營養(EN)與腸外營養(PN)的選擇;(2)EN時機的選擇;(3)鼻胃管(NG)與鼻空腸管(NJ)的選擇。
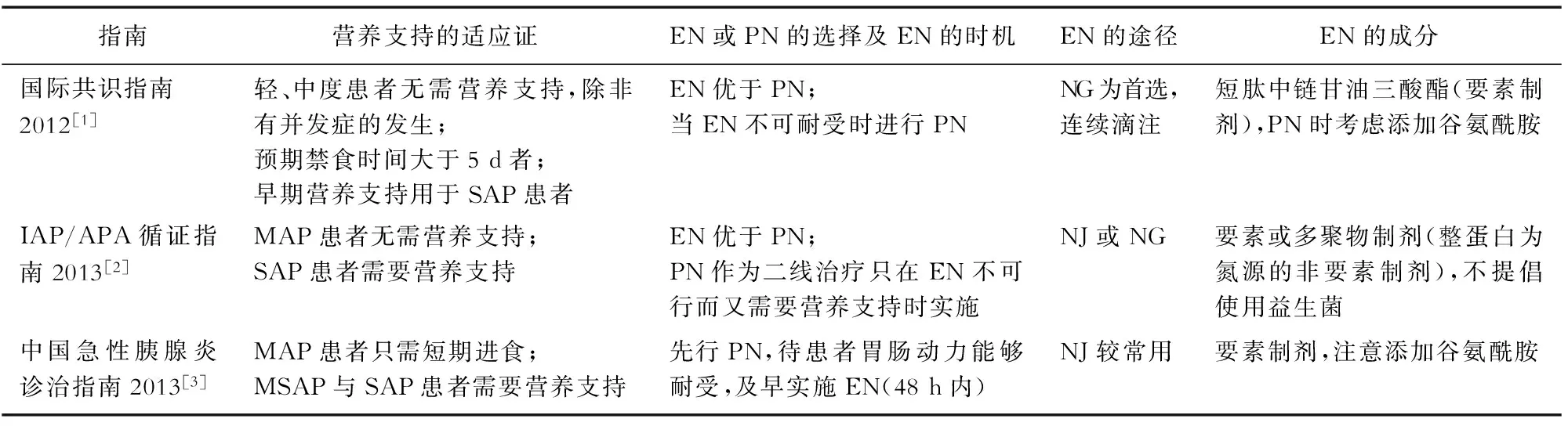
表1 三個診治指南的比較
注:MAP輕癥急性胰腺炎;MSAP中重癥急性胰腺炎
1 營養支持的適應證
近年來發布的指南在營養支持的適應證方面已基本達成共識,即對于MAP患者只需短期禁食后便可恢復經口進食,而對SAP患者則強烈推薦實施營養支持。美國胃腸病學會(AGA)推薦,若患者無惡心嘔吐癥狀,腹痛緩解后即可經口進食少渣、低脂軟食,無需從流食過渡[4]。
然而一項包括35例輕、中度(AP國際多學科分型:輕度無胰腺壞死與器官衰竭;中度有無菌性胰腺壞死和/或一過性器官衰竭)AP患者的隨機對照研究表明,給予NG營養可以減輕腹痛,縮短腹痛持續時間,進而減少阿片類止痛藥的使用,并且可以降低經口進食的不耐受風險[5]。但因其為小樣本試驗,確切療效有待大型臨床試驗進一步驗證。近期也有研究嘗試在SAP患者入院72 h內即予低流量(248~330 kcal/d)經口進食,發現其也可促進腸道功能的早期恢復[6],為AP的營養支持提供了新的方式。
2 EN與PN的選擇
過去認為,PN期間胰腺的外分泌功能是“減少和靜止”的,能達到“胰腺休息”的目的。但全腸外營養(TPN)本身可以導致膽汁淤積、代謝紊亂加劇、腸道細菌移位、導管膿毒癥等并發癥,且費用昂貴。相比而言,EN的營養物質經門靜脈系統吸收并輸送至肝臟,符合生理狀態,有助于維持腸道黏膜結構和功能的完整性,減少腸道菌群移位,促進SAP患者營養狀態的改善。另有研究認為EN可以降低高血糖的發生率[7]。EN與PN相比還能減少感染性并發癥的發生[8]。2012年的一項包括8個隨機對照試驗共381例pSAP(預測可能進展為SAP)患者的Meta分析表明,EN組患者在病死率、感染性并發癥發生率、器官功能衰竭發生率及外科干預率方面均低于PN組[9]。目前EN用于AP的治療已得到了普及。
3 EN時機的選擇
何時開始EN才能發揮較好的治療作用一直未有定論。近期發布的胰腺炎診治指南也只建議EN優于PN,對于開始EN的具體時間并沒有明確規定。近年來有研究建議早期實施EN,并得到了許多臨床研究的支持(見表2)。然而關于“早期”的概念,爭議頗多,有研究提議入院72 h內給予EN,也有提議入院48 h內給予EN,更有提出超早期EN,即入院24 h內給予EN。一項包括93例患者的隨機對照試驗提示,早期EN(EEN)組(入院72 h內行EN)的病死率較低,住院時間較短,需要機械通氣的患者數與胰腺感染發生率都小于延遲進行EN(DEN2)組(入院3~7 d行EN)。因此該研究建議在入院72 h內開始實施EN[10]。另有一項在動物SAP模型上完成的隨機對照實驗進一步證實了入院72 h內行EN的有效性與安全性[11]。
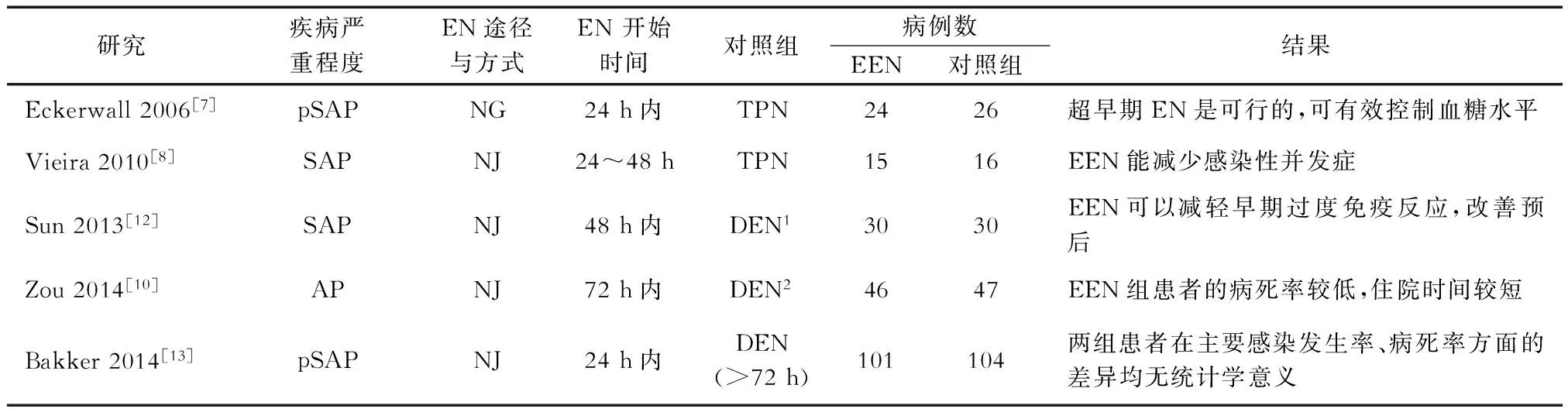
表2 有關EEN的研究
注:DEN1延遲進行EN(>8 d);DEN2延遲進行EN(入院3~7 d)
Sun等[12]完成的一項包括60例SAP患者的隨機對照試驗提示,入院48 h內給予EN可以減輕SAP患者早期的過度免疫反應,且不會引起免疫抑制,可改善預后。另有一項囊括11個隨機對照研究共775例患者的Meta分析也證實,入院48 h內實施EN可以減少各種并發癥的發生[14]。目前尚無相關報道表明入院48 h內行EN有負面作用。
一項囊括12個臨床隨機對照試驗的Meta分析表明,相較于TPN和DEN,入院24 h內給予EN可以降低胰腺感染、器官功能衰竭、高血糖癥、導管相關性感染等并發癥的風險,降低病死率;然而,相較于入院24~72 h內給予EN,則差異無統計學意義[15]。為了進一步尋找支持EEN的循證依據,荷蘭開展了一項為期3年的臨床隨機對照試驗(PYTHON試驗),選取了208例符合SAP診斷標準(亞特蘭大分型)的AP患者,隨機分為兩組,一組患者24 h內給予NJ營養(EEN組),另一組患者72 h后經口進食(按需組,不耐受者給予NJ營養)。事件終點為主要并發癥(感染性胰腺壞死、菌血癥、肺炎等)的發生或隨訪6個月內死亡。結果提示,EEN組的101例患者中有30例發生終點事件(30%),按需組則為28例(104例患者,27%),差異無統計學意義。兩組患者在主要感染發生率、病死率方面的差異也無統計學意義。因此認為,對于高危的AP患者,在降低感染率或病死率方面,EEN并不優于72 h后經口進食[13]。
4 EN的部位與途徑
早期有大量研究倡議使用NJ,認為其一方面能很好地抑制胰腺外分泌,實行“胰腺休息”;另一方面還具有胃腸減壓功能。然而越來越多的研究表明,NG與NJ在療效方面的差異并無統計學意義。Eatock等[16]將50例SAP患者隨機分為NG組與NJ組,結果提示兩組患者在急性生理功能和慢性健康狀況評分系統Ⅱ(APACHE Ⅱ評分)、C反應蛋白(CRP)水平、視覺模擬疼痛評分及鎮痛需求方面的差異無統計學意義,在住院時間及病死率方面的差異亦無統計學意義。另一項包括78例SAP患者的隨機對照試驗發現,使用NG與NJ在感染性并發癥方面的差異也無統計學意義[17]。2014年的一項關于NG的療效與不良反應的系統評價指出,在147例接受NG的患者中,有133例耐受(90%),87%達到了能量給予目標(75%),與NJ相比較,差異無統計學意義。在腹脹腹瀉、惡心嘔吐、腹痛惡化、導管脫落、誤吸等并發癥方面,兩者的差異也沒有統計學意義[18]。目前國外的指南已基本達成一致意見,認為NG與NJ同樣有效安全,考慮到操作難度的差異,NG一般作為首選,部分患者無法耐受NG時可改用NJ,但國內的診治指南依然將NJ作為首選。NG與胰腺外分泌之間的關聯,NG與“胰腺休息”的治療理論之間的矛盾都有待進一步的研究。
對于AP患者,無論使用NJ還是NG,均推薦采用連續滴注,目前關于滴注速度的研究較少,有研究表明,經NG或NJ低速(1~1.5 mL/min)滴注半要素營養制劑具有相同的可耐受性[19]。臨床上可參考危重患者的NG滴注速度,一般為100 mL/h,每24 h增加10~20 mL/h。IAP/APA推薦能量輸入應控制在25~35 kcal·kg-1·d-1或1.5~1.8倍基礎能量消耗。
在SAP早期行EN大多選擇要素制劑,之后逐漸過渡到整蛋白型,但關于AP患者行EN時谷氨酰胺、益生菌等輔助成分的添加尚未達成共識。ICGC循證指南認為,在PN時可靜脈補充谷氨酰胺,國內的指南也建議添加谷氨酰胺,但對添加方式未明確規定。國內外指南都沒有關于添加益生菌的推薦,其中IAP/APA循證指南特意指出不推薦使用益生菌。
5 小結與展望
營養支持在SAP的治療過程中是必不可少的,EN治療AP可明顯降低感染發生率、縮短住院時間并減少住院費用,明顯降低患者的病死率。但不是所有的AP患者均需EN,MAP患者只需短暫禁食后便可恢復飲食。SAP患者的機體處于高分解與代謝狀態,EN可以糾正機體的負氮平衡,增強免疫力,改善預后,且行EN應注意選擇適當的時機。NG與NJ的選擇不能僅僅依據臨床研究,還需考慮患者的耐受性。綜上所述,臨床上AP患者行EN時,要從適應證、時機、途徑、制劑、輸入方式和速度以及是否添加輔助成分等多方面進行考慮。
1 Mirtallo JM, Forbes A, McClave SA, et al. International consensus guidelines for nutrition therapy in pancreatitis[J]. JPEN J Parenter Enteral Nutr, 2012, 36: 284-291.
2 Working Group IAP/APA Acute Pancreatitis Guidelines. IAP/APA evidence-based guidelines for the management of acute pancreatitis[J]. Pancreatology, 2013, 13 (4 Suppl 2): e1-e15.
3 中華醫學會消化病學分會胰腺疾病學組, 中華胰腺病雜志編輯委員會, 中華消化雜志編輯委員會. 中國急性胰腺炎診治指南(2013年,上海)[J]. 中華消化雜志, 2013, 33: 217-222.
4 Tenner S, Baillie J, DeWitt J, et al. American College of Gastroenterology guideline: management of acute pancreatitis[J]. Am J Gastroenterol, 2013, 108: 1400-1415.
5 Petrov MS, McIlroy K, Grayson L, et al. Early nasogastric tube feeding versus nil per os in mild to moderate acute pancreatitis: a randomized controlled trial[J]. Clin Nutr, 2013, 32: 697-703.
6 Pupelis G, Plaudis H, Zeiza K, et al. Oral feeding in necrotizing pancreatitis[J]. Acta Chir Belg, 2014, 114: 34-39.
7 Eckerwall GE, Axelsson JB, Andersson RG. Early nasogastric feeding in predicted severe acute pancreatitis: A clinical, randomized study[J]. Ann Surg, 2006, 244: 959-965; discussion 965-957.
8 Vieira JP, Araújo GF, Azevedo JR, et al. Parenteral nutrition versus enteral nutrition in severe acute pancreatitis[J]. Acta Cir Bras, 2010, 25: 449-454.
9 Yi F, Ge L, Zhao J, et al. Meta-analysis: total parenteral nutrition versus total enteral nutrition in predicted severe acute pancreatitis[J]. Intern Med, 2012, 51: 523-530.
10 Zou L, Ke L, Li W, et al. Enteral nutrition within 72 h after onset of acute pancreatits vs delayed initiation[J]. Eur J Clin Nutr, 2014, 68: 1288-1293.
11 Yan Q, Ni J, Zhang GL, et al. Effects of combined enteral nutrition support on hemorrheologic parameters and the level of inflammatory factors in rabbits with severe acute pancreatitis[J]. Zhonghua Yi Xue Za Zhi, 2011, 91: 2006-2010.
12 Sun JK, Mu XW, Li WQ, et al. Effects of early enteral nutrition on immune function of severe acute pancreatitis patients[J]. World J Gastroenterol, 2013, 19: 917-922.
13 Bakker OJ, van Brunschot S, van Santvoort HC, et al. Early versus on-demand nasoenteric tube feeding in acute pancreatitis[J]. N Engl J Med, 2014, 371: 1983-1993.
14 Li JY, Yu T, Chen GC, et al. Enteral nutrition within 48 hours of admission improves clinical outcomes of acute pancreatitis by reducing complications: a meta-analysis[J]. PLoS One, 2013, 8: e64926.
15 Li X, Ma F, Jia K. Early enteral nutrition within 24 hours or between 24 and 72 hours for acute pancreatitis: evidence based on 12 RCTs[J]. Med Sci Monit, 2014, 20: 2327-2335.
16 Eatock FC, Chong P, Menezes N, et al. A randomized study of early nasogastric versus nasojejunal feeding in severe acute pancreatitis[J]. Am J Gastroenterol, 2005, 100: 432-439.
17 Singh N, Sharma B, Sharma M, et al. Evaluation of early enteral feeding through nasogastric and nasojejunal tube in severe acute pancreatitis: a noninferiority randomized controlled trial[J]. Pancreas, 2012, 41: 153-159.
18 Nally DM, Kelly EG, Clarke M, et al. Nasogastric nutrition is efficacious in severe acute pancreatitis: a systematic review and meta-analysis[J]. Br J Nutr, 2014, 112: 1769-1778.
19 Kumar A, Singh N, Prakash S, et al. Early enteral nutrition in severe acute pancreatitis: a prospective randomized controlled trial comparing nasojejunal and nasogastric routes[J]. J Clin Gastroenterol, 2006, 40: 431-434.
(本文編輯:周駿)
10.3969/j.issn.1673-534X.2016.02.002
110004沈陽,中國醫科大學附屬盛京醫院消化內科
林連捷,Email: linlj@sj-hospital.org
2015-05-12)

