席夫堿的一鍋法合成及還原
董志兵,劉 方,王 敏,劉 敏,曾夢甜,許 萬
武漢工程大學化學與環境工程學院,湖北 武漢 430074
席夫堿的一鍋法合成及還原
董志兵,劉方,王敏,劉敏,曾夢甜,許萬
武漢工程大學化學與環境工程學院,湖北 武漢 430074
席夫堿是一種應用廣泛的配體,它能與元素周期表中的大多數金屬形成配合物,部分席夫堿配體穩定性差,但席夫堿還原化合物的穩定性普遍較好,所以研究高效合成席夫堿還原化合物的方法對拓寬席夫堿在配位化學中的應用具有重要意義.研究報道了一種“一鍋法”合成及還原席夫堿的方法,使用的還原劑為醋酸硼氫化鈉,反應條件溫和,反應快捷(只需2~3 h即可完成反應),產率高,中間體席夫堿可以不用分離而直接進行還原,反應的底物適用性廣,且可以用于大劑量的目標化合物的制備中.用該方法合成了8種席夫堿還原物,其中三種為鄰碘芳基席夫堿還原化合物,它們是許多醫藥、農藥的重要組成部分.
一鍋法;席夫堿;醋酸硼氫化鈉;還原
1 引 言
席夫堿最早是由Schiff H在1964年發現的,他在研究伯胺與活潑羰基的反應時發現了席夫堿(圖1).

圖1 席夫堿的合成Fig.1 Synthesis of Schiff base
席夫堿可以和元素周期表中的大多數金屬形成不同的配合物,是應用非常廣泛的配體.但在席夫堿金屬配合物的研究過程中,化學工作者發現部分席夫堿配體的穩定性差.席夫堿的這一缺陷制約了它在配位化學中的應用范圍.席夫堿的還原產物是將席夫堿配體選擇性地還原,這樣可以在一定程度上解決部分席夫堿穩定性差的問題.席夫堿還原化合物柔韌性較席夫堿有較大提高,在參與配位時有更大的自由度,而且芳香族席夫堿還原化合物還是高分子化合物、醫藥以及農藥的重要組成部分[1].鄰碘芳香族席夫堿還原化合物還是合成內酰胺[2]、喹唑啉[3]、吲哚衍生物[4]、苯并噻唑[5]等的重要原料,也能作為分子內芳基化反應[6]、分子內Heck反應[7]的底物.
文獻中的合成席夫堿還原化合物的方法一般涉及到使用劇毒的氰化物[8]以及昂貴的鈷-銠合金催化劑[9],而且反應時間長,選擇性低.本研究報道了一種“一鍋法”合成席夫堿還原化合物的方法,該反應條件溫和、底物普適性廣,反應快捷(2 h~3 h),合成的席夫堿還原化合物產率高(83%~92%).
2 實驗部分
2.1化學試劑與材料
所有底物都是來自Merck或Aldrich或Alfa Aesar,所有試劑都嚴格按照標準方法處理;GC(氣相色譜,流動相為氫氣)用帶自動注射器GC-8130 (Fisons)色譜儀測定詳細信息為:1個FI檢測器和1個-1710毛細管柱(0.25 μm×25 m×0.25 mm,Macherey-Nagel);核磁采用Agilent 400MR型核磁共振波譜儀,以CDC13為溶劑,TMS為內標;高分辨質譜用Finnigan MAT 95Q質譜儀測定,轟擊源為EI.
2.2席夫堿還原化合物的合成
典型操作(TP):1 C的合成,見圖2.
向溶有化合物(苯胺,4.66 g,50 mmol;苯甲醛,5.31 g,50 mmol;乙酸,6.00 g,100 mmol)的100 mL二氯乙烷溶液中分3次加入醋酸硼氫化鈉(31.78 g,150 mmol),反應液在室溫條件下攪拌2 h.TLC顯示原料完全反應,反應液真空條件下濃縮,濃縮得到的油狀物用水洗滌,二氯甲烷萃取水相,無水硫酸鎂干燥,濃縮有機相得白色固體8.42 g(1 C).
本實驗中所有合成的席夫堿的還原化合物歸納在表1中.

圖2 席夫堿還原化合物的合成路線Fig.2 Synthesis route of the reduced Schiff base compounds
2.2.11 C的合成(Tab.1,Entry 1)根據(TP),濃縮有機相得白色固體8.42 g(1 C),收率92%.熔點39oC;1H NMR(400 MHz,CDCl3)δ:7.39~
7.21(m,5H),7.15(t,J=7.8Hz,2H),6.70(t,J= 7.3Hz,1H),6.61(d,J=7.8Hz,2H),4.29(s,2H),3.97(s,1 H);13C NMR(100 MHz,CDCl3)δ:148.24,139.54,129.36,128.72,127.59,127.31,117.64,112.93,48.39;HRMS(ESI):m/z calcd for C13H13N:183.104 8,found183.105 6.
2.2.22 C的合成(Tab.1,Entry 2)根據(TP),濃縮有機相得無色油狀物13.91 g(2 C),收率90%.1H NMR(400 MHz,CDCl3)d 7.68(dd,J=7.8,1.4 Hz,1H),7.38~7.26(m,5H),7.18~7.13(m,1H),6.54(dd,J=8.0,1.2Hz,1H),6.45(td,J=7.6,1.5 Hz,1H),4.63(brs,1H),4.41(d,J=5.6 Hz,2H);13C NMR(100 MHz,CDCl3)d 147.00,139.01,138.65,129.42,128.73,127.30,127.21,118.83,111.04,85.32,48.30.HRMS(ESI):m/z calcd for C13H12IN:309.001 4,found 309.000 7.
2.2.33 C的合成(Tab.1,Entry 3)根據(TP),濃縮有機相得淡黃色油狀物16.83 g(3 C),收率87%.1H NMR(400 MHz,CDCl3)d:7.50(d,J= 8.3 Hz,1H),7.29~7.40(m,5H),6.67(d,J=1.9Hz,1H),6.59(dd,J=8.1,2.2 Hz,1H),4.63(br s,1H),4.36(d,J=5.4 Hz,2H);13C NMR(100 MHz,CDCl3)d:148.21,139.83,137.82,128.85,127.61,127.33,123.62,121.61,113.63,83.00,48.32.HRMS (ESI):m/z calcd for C13H11BrIN:386.912 0,found 386.912 6.
2.2.44 C的合成(Tab.1,Entry 4)根據(TP),濃縮有機相得得淡黃色油狀物14.92 g(4 C),收率88%.1H NMR(400 MHz,CDCl3)d:7.27~7.40(m,5H),6.79(dd,J=8.8,2.9 Hz,1H),6.49(d,J= 8.8 Hz,1H),4.36(d,J=5.4 Hz,2H),4.28(br s,1H),3.71(s,3H);13C NMR(100 MHz,CDCl3)d:152.00,141.91,139.02,128.71,127.22,124.65,115.52,111.51,85.33,56.01,49.15.HRMS (ESI):m/z calcd for C14H14INO:339.012 0,found 339.012 5.
2.2.55 C的合成(Tab.1,Entry 5)根據(TP),濃縮有機相得黃色固體9.05 g(5 C),收率85%.熔點50℃;1HNMR(400Mz,CDCl3)δ:7.35(m,4H),7.27(d,J=6.9Hz,1H),6.77(d,J=8.8Hz,2 H),6.60(d,J=8.8 Hz,2 H),4.28(s,2 H),3.77(s,1 H),3.74(s,3 H);13C NMR(100 MHz,CDCl3)δ:152.30,142.58,139.81,128.73,127.68,127.30,115.03,114.22,55.94,49.38.HRMS(ESI):m/z calcdforC14H15NO:213.115 4,found213.115 9.
2.2.66 C的合成(Tab.1,Entry 6)根據(TP),濃縮有機相得白色固體10.33 g(6 C),收率85%.熔點97℃;1H NMR(400 MHz,CDCl3)δ:7.28(d,J=8.4 Hz,2 H),6.87(d,J=8.5 Hz,2 H),6.77(d,J=8.8Hz,2H),6.59(d,J=8.8Hz,2H),4.19(s,2 H),3.79(s,3 H),3.73(s,3 H);13C NMR(100 MHz,CDCl3)δ:158.78,152.12,142.52,131.66,128.81,114.87,114.09,113.96,55.79,55.28,48.70.HRMS(ESI):m/z calcd for C15H17NO2:243.125 9,found 243.125 1.
2.2.77 C的合成(Tab.1,Entry 7)根據(TP),濃縮有機相得白色固體9.76 g(7 C),收率86%.熔點107℃;1H NMR(400 MHz,CDCl3)δ:7.26(d,J=7.8 Hz,2 H),7.15(d,J=7.8 Hz,2 H),6.77 (d,J=8.8 Hz,2 H),6.60(d,J=8.8 Hz,2 H),4.23 (s,2 H),3.74(s,4 H),2.34(s,3 H);13C NMR (100 MHz,CDCl3)δ:152.24,142.65,136.91,136.72,129.38,127.66,115.01,114.19,55.93,49.11,21.23.HRMS(ESI): m/zcalcdfor C15H17NO:227.131 0,found 227.131 8.
2.2.88 C的合成(Tab.1,Entry 8)根據(TP),濃縮有機相得黃色油狀物11.66 g(8 C),收率83%.1H NMR(400 MHz,CDCl3)δ:7.56(d,J= 8.1 Hz,2 H),7.45(d,J=8.0 Hz,2 H),6.76(d,J= 8.9Hz,2H),6.55(d,J=8.9Hz,2H),4.33(s,2H),3.88(s,1 H),3.71(s,3 H);13C NMR(100 MHz,CDCl3)δ:152.49,144.17,142.00,129.44(q,J= 32.4 Hz),127.59,125.60(q,J=3.8 Hz),122.99,115.04,114.24,55.83,48.73.HRMS(ESI):m/z calcd for C15H14F3NO:281.102 7,found 281.103 6.
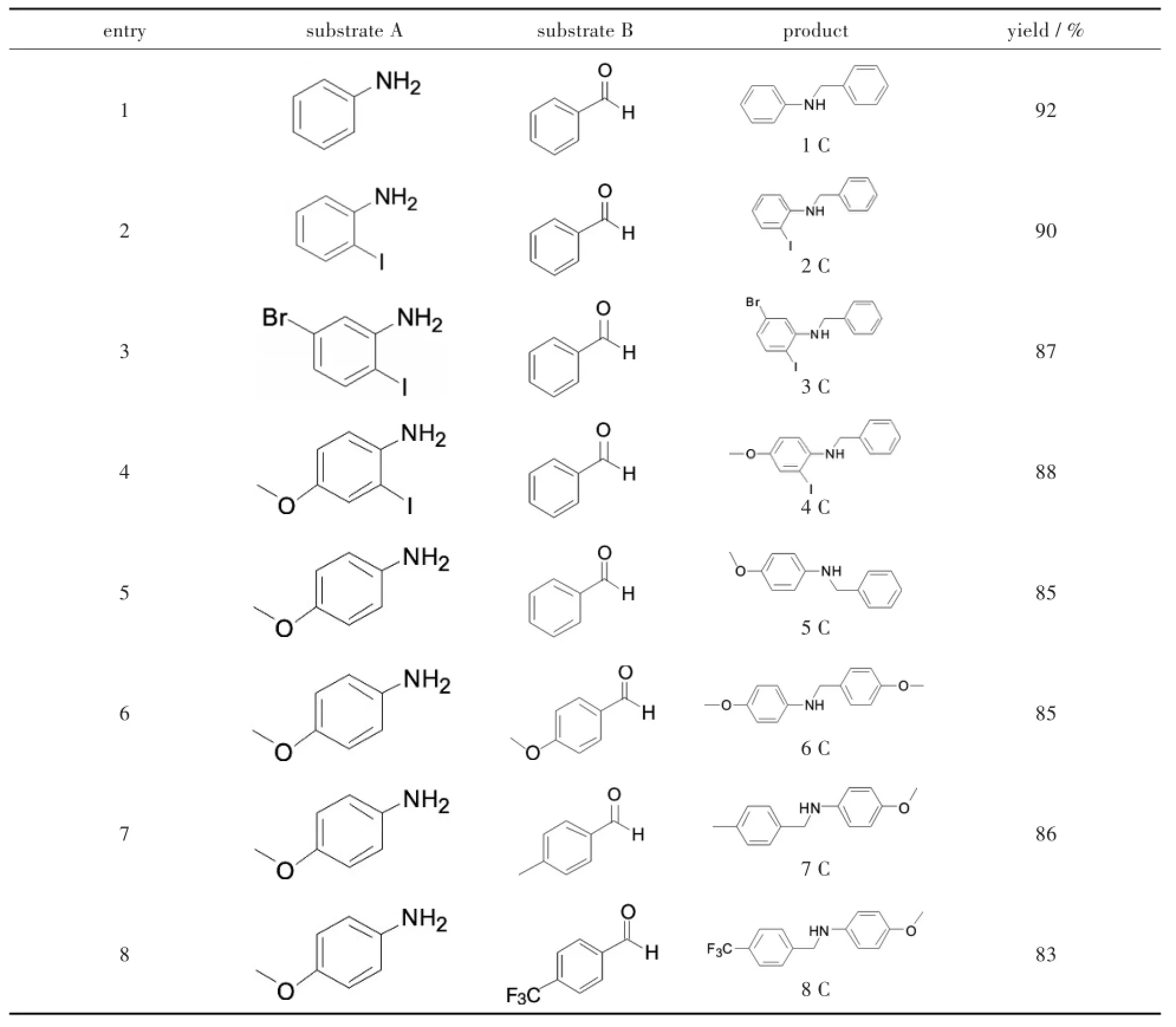
表1 合成席夫堿的還原化合物Tab.1 Synthesis of the Schiff base reduction compounds
3 結果與討論
本文以苯胺與苯甲醛為模板底物對反應條件進行探索,如圖3所示,反應條件的摸索采用GC或者GC-MS檢測.模板底物在對甲苯磺酸和甲醇或乙醇的反應體系中幾乎都沒有目標化合物生成,在乙酸和二氯乙烷反應體系中反應無法徹底完成,只有少量目標化合物生成.但在乙酸和二氯乙烷反應體系中加入3個當量的醋酸硼氫化鈉后,反應迅速徹底完成(Tab.1,Entry1),反應收率高(92%).醋酸硼氫化鈉是一種高效的高選擇性的還原試劑,用其對席夫堿進行選擇性還原,便可以定量快捷地合成席夫堿還原化合物,所得的產物易分離,產率高.對于空間位阻大的底物(Tab.1,Entry2~Entry4)的收率也可以達到87%以上,本方法的底物適用性較為廣泛,能適用于芳基席夫堿還原化合物的大劑量制備,還原產物可以不用分離而直接使用,因此具有較為重要的工業應用價值.

圖3 一鍋法合成席夫堿還原化合物的反應條件探索Fig.3 Exploration of reaction conditions of one-pot synthesis of the reduced Schiff base compounds
4 結 語
本研究報道了一種一鍋法制備芳基席夫堿還原化合物的方法:用醋酸硼氫化鈉原位對生成的席夫堿進行快速定量還原,所得的產物產率高,可以不用柱色譜分離而直接使用,該合成方法的底物普適性廣,也可以用于目標化合物的大量制備中.本方法合成簡單,方便快捷,可以為這類席夫堿還原化合物的合成提供一條重要的參考途徑.
[1] KUMAR V,SHARMA S,SHARMA U,et al.Synthesis of substituted amines and isoindolinones:catalytic reductive amination using abundantly available AlCl3/ PMHS[J].Green chemistry,2012,14:3410-3414.
[2]LANG S,CORR M,MUIR N,et al.First organophosphorus radical-mediated cyclisations to afford medium-sized rings:eight-membered lactones and sevenand eight-membered lactams[J].Tetrahedron letters,2005,46:4027-4030.
[3]ZHAO W,DONG X,JIANG M,et al.A facile copper-catalyzed one-pot domino synthesis of 5,12-dihydroindolo[2,1-b]quinazolines[J].Organic letters,2012,14(6):1420-1423.
[4] FIELDING M R,GRIGG R,URCH C J,Novel synthesis of oxindoles from carbamoyl chlorides via palladium catalysed cyclisation-anion capture[J].Chemical communications,2000,22(22):2239-2240.
[5]ZHANG X,ZENG W,LIANG Y,et al.Copper-catalyzed double C-S bonds formation via different paths:synthesis of benzothiazoles from NBenzyl-2-iodoaniline and potassium sulfide[J].Organic letters,2014,16:876-879.
[6] ROMAN D S,TAKAHASHI Y,CHARETTE A B.Potassium tert-butoxide promoted intramolecular arylation via a radical pathway[J].Organic letters,2011,13 (12):3242-3245.
[7]CROPPER E L,WHITE A J P.Ligand effects in the synthesis of N-heterocycles by intramolecular Heck reactions[J].Journal of organic chemistry,2006,71:1732-1735.
[8]LIZOS D E,MURPHY J A.Concise synthesis of (±)-horsfiline and(±)-coerulescine by tandem cyclisation of iodoaryl alkenyl azides[J].Organic biomolecular chemistry,2003(1):117-122.
[9] PARK J W,CHUNG Y K.Hydrogen-free Cobalt-Rhodium heterobimetallic nanoparticle catalyzed reductive amination of aldehydes and ketones with amines and nitroarenes in the presence of carbon monoxide and water[J].American Chemical Society catalysis,2015 (5):4846-4850.
本文編輯:張瑞
Synthesis and Reduction of Schiff Base by One-Pot Method
DONG Zhibing,LIU Fang,WANG Min,LIU Min,ZENG Mengtian,XU Wan
School of Chemistry and Environmental Engineering,Wuhan Institute of Technology,Wuhan 430074,China
Schiff base is a kind of widely-used ligand which can form complexes with most of metals in the periodic table.The stability of Schiff base ligand is bad,but the reduced Schiff base shows much better stability. Thus,it is very important to explore the synthetic method of the reducted Shiff base,which may broaden the applications of these compounds.A facile one-pot synthesis and reduction of Schiff base is reported by using sodium triacetoxyborohydride as the reductant.The reaction underwent in a smooth and rapid manner with high yield,and the intermediate Schiff base is reduced directly without further separation process.The obtained substrate has wide applicability and can be applied in scaled-up synthesis of the target molecular.By using this method,eight kinds of the reduced Schiff base derivatives were synthesized,three of them are ortho-iodinated phenyl amines,which are important starting materials for the drugs and pesticides synthesis.
one-pot;Schiff base;sodium triacetoxyborohydride;reduction
O621
A
10.3969/j.issn.1674-2869.2016.03.001
1674-2869(2016)03-0209-04
2016-04-05
董志兵,博士,教授.E-mail:zhibingdong80@aliyun.com

