基于濾紙的多電極原電池實驗設計
劉玲 丁偉
摘要:金屬片電極與浸漬相應金屬鹽溶液的濾紙可以組成原電池。如用銅片、鋅片、鉛片和錫片4種電極組成的兩個原電池整合在一個裝置內,便于對比分析各電極反應,同時又能節約實驗藥品。該原電池具有整合度高、裝置簡易等特點,既有利于教師進行課堂演示,又方便學生自主進行實驗。
關鍵詞:濾紙;多電極;原電池;電極電勢;實驗設計
文章編號:1005–6629(2016)9–0049–03 中圖分類號:G633.8 文獻標識碼:B
1 研究背景
原電池是電化學教學的重點和難點,其涉及氧化還原反應、電解質溶液和物理學中相關的電學知識,知識的認知難度較大[1],且內容抽象、理論性強,因此,純理論的教授方式往往達不到理想的教學效果。如果通過對原電池實驗的探究,將有效地提高這部分知識的教學成效,加深學生對原電池的感性認知,促進其對知識的有意義的建構,故原電池實驗對于相關知識的教學意義重大。
人教版選修《化學反應原理》教材[2]中關于原電池的實驗是將銅片和鋅片分別插入硫酸銅和硫酸鋅溶液中,使用鹽橋連接兩種溶液,外接電流計測量產生的電流。但實驗演示效果并不理想,且存在銅鋅原電池裝置所用到的鹽橋制作繁瑣、使用時間間隔不能過長[3]、實驗消耗藥品的量很大等不足,因此,有必要作進一步的深入研究。
2 實驗方案
2.1 實驗設計思路
以往研究有針對鹽橋制作較復雜的情況進行改進:用橡皮管將兩側均帶有支管的U形管與具支試管連接起來,橡皮管中充入瓊脂(或果凍),U形管中注入飽和的氯化鉀溶液,用作鹽橋[4];有針對原電池電壓較小且不穩定而對實驗裝置進行的改進:使用具有雙槽的容器,兩槽內均具有一對電極而使兩個原電池串聯起來以增大電壓[5];有為了克服演示實驗過程中觀賞性差、浪費大且有污染等不足的微型化改進:將玻璃管燒制成微型U形管用作電解槽,利用金屬絲做電極[6];還有為引起學生興趣而進行的趣味化改進:于永民[7]將市場上會吸水的玩具海洋寶寶球浸入稀硫酸中,將金屬絲插入其中觀察電流表數字變化等改進。綜合這些研究發現,這些改進都很有創意,但主要針對銅鋅原電池的電解質溶液、鹽橋和裝置結構等某一方面進行改進,大多數改進裝置中只有一對電極,而關于電極的改進則很少。基于此,本文設計了一個具有多對電極的原電池。考慮選用何種金屬作電極,首先,排除一些特別活潑的金屬,如鈉、鎂等;其次,鐵雖易得但Fe2+極不穩定易導致實驗失敗,故不選用;因銀比較昂貴所以也不選用;相比之下錫和鉛雖然在中學化學中不太常見,但在漁具店或市場上均易購買。最后選定用銅、鋅、錫、鉛四種金屬片做電極。為便于制作,體現微型化實驗設計,所以選用濾紙作為載體。
2.2 實驗儀器、藥品及材料
1 mol/L的鹽溶液[CuSO4、ZnSO4、Pb(NO3)2、KNO3以及SnCl2溶液]、金屬片(銅片、鋅片、鉛片和錫片)、定性濾紙(11cm)、蠟燭、酒精燈(或電熱板)、墊板、模板、刻刀、鉛筆、砂紙、萬用表(勝利儀器數字多用表,VC890D)和一次性手套
2.3 實驗內容
2.3.1 制作模板
選取一個硬紙板,利用刻刀制作有四個分區的模板。用鉛筆按照模板將濾紙劃分為四個分區,再用火柴梗蘸取蠟油,沿著鉛筆印跡涂抹。全部畫好后,將濾紙放在小蠟燭火焰上方(或電熱板)加熱一分鐘左右。使濾紙上的蠟融化并滲透到濾紙中,形成一個蠟的屏障以減小實驗過程中各分區溶液間的相互滲透。運用蠟油涂抹鉛筆印跡和濾紙烘烤時要仔細,要確保涂抹無遺漏。在烘烤濾紙時也要小心謹慎,既要確保蠟油滲透進濾紙,也要防止將濾紙引著,所以如果條件允許盡量使用電熱板。
2.3.2 制作電極
裁剪金屬片,將金屬片剪成1cm×2cm的薄片。為使實驗結果更精確,用砂紙仔細打磨金屬片,除去其表面的氧化層。
2.3.3 制電解液
配制1 mol/L與金屬片相應的鹽溶液和KNO3溶液,裝入滴瓶中待用。SnCl2溶液要現用現配,因為SnCl2易水解氧化,在配制時需要先用濃度至少為3 mol/L的鹽酸在通風櫥中溶解后再加水稀釋至所需濃度,在其溶解過程中盡量不要攪拌,并在溶液中放些許錫粒。在配制Pb(NO3)2溶液時,先在蒸餾水中加入兩滴稀HNO3,然后再放入稱量好的Pb(NO3)2固體進行溶解。目的是防止鉛離子水解生成不溶性的Pb(OH)2。
2.3.4 制原電池
將四個金屬片放入濾紙的四個分區內(也可以用膠帶固定),并在每個金屬片的相應分區滴上相應的金屬鹽溶液,每個金屬區域就是一個電極,中間區域滴兩滴1 mol/L的KNO3溶液。該區域起到鹽橋的作用,為加強實驗效果起著至關重要的作用。然后將“濾紙電池”放到墊板上。
2.3.5 測量電壓
打開萬用表,將量程調至為0~2V,用萬用表分別測量四個金屬片兩兩做電極的原電池電動勢并記錄(銅鋅原電池電動勢的測定情況如圖1所示)。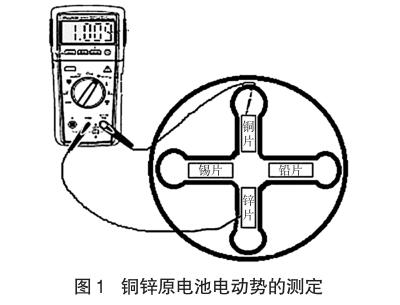
2.4 實驗結果及分析
為檢驗改進裝置的有效性,將計算的標準電動勢與實測電動勢進行比較,標準電動勢的計算方法如下:
當溫度為298K,參與電極反應的所有離子濃度均為1 mol/L,所有氣體的壓強為100kPa時,該電極的電極電勢是標準電極電勢。將正負兩極的標準電極電勢相減即得到原電池的標準電動勢:Eθ=φθ+-φθ-。以銅鋅原電池為例,計算電池Zn(s)|Zn2+||Cu2+|Cu(s)的標準電動勢Eθ。查表[8]可知正極φθ(Cu2+/Cu)=+0.3419V,負極φθ(Zn2+/Zn)=-0.7618V,電池的標準電動勢Eθ=φθ(Cu2+/Cu)-φθ(Zn2+/Zn)=(+0.3419V)-(-0.7618V)=1.104V(為方便與實測值比較保留三位小數)。依次求出ZnPb、Zn-Sn、Sn-Cu、Sn-Pb和Pb-Cu原電池的標準電動勢,分別為0.636V、0.626V、0.478V、0.010V和0.468V。因該實驗中所配制的鹽溶液濃度為1 mol/L,室內溫度也約為298K,反應中無氣體產生,因此可將實測電動勢與標準電動勢進行比較。各原電池的標準電動勢與實測電動勢如表1所示。
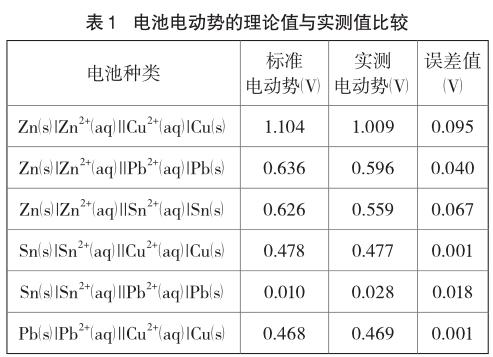
通過上表中數據可以看到,最小誤差只有0.001V,最大誤差也僅為0.095V。相對誤差較小,說明該改進實驗是有效的。總的來說該改進實驗的創新點在于:
(1)整合性。在教材知識的基礎上,另添加兩個電極并整合進一個裝置,可直觀地觀察到多對電化學反應現象。同時該實驗可作為拓展興趣實驗,利用該實驗既可以加深學生對電化學的理解,又可以拓寬學生的知識面,有利于發散性思維的發展。
(2)簡易性。改進裝置簡單、制作容易、操作便捷、取材方便;實驗現象明顯,且容易保存。
(3)靈活性。該裝置在使用時可靈活運用,使學生在學習中能運用歸納或演繹思維:學生可以通過觀察電極反應現象,判斷電池的正負極,加深對金屬活動性順序的認知;也可以基于初中階段有關金屬活動性順序的知識,先判斷電池的正負極,再通過觀察實驗現象進行驗證。
(4)輔助性。在原電池實驗中可以使用鹽橋加強實驗效果來輔助實驗。但鹽橋的制作和存儲非常不便。本實驗起鹽橋作用的硝酸鉀溶液在實驗室中比較常見,可就地取材。對于輔助實驗起到很重要的作用。
此外,可以通過增大電池的電壓(如增大電極的面積或電解液的濃度),或者串聯兩到三個電極使電壓能夠令二極管發光(小燈泡)或使小功率的音樂卡片或喇叭發聲,使實驗現象更加直觀,更加能夠吸引學生的注意力,從而提高學生學習化學的興趣。
3 結論
改進后的實驗裝置精簡、經濟。既利于教師進行演示,又可以提升學生的科學思維能力和科學探究能力。同時節約藥品也體現了綠色化學的理念,符合時代的要求。
參考文獻:
[1]洪燕芬.追溯歷史拓展實驗凸顯探究——“原電池”教學設計與反思[J].化學教學,2014,(6):41-43.
[2]人民教育出版社化學室.全日制普通高級中學教科書·化學[M].北京:人民教育出版社,2001.
[3]張艷.銅鋅原電池演示實驗裝置改進[J].化學教育,2013,(8):63.
[4]劉影,張勇,馬雙.原電池實驗改進[J].教學儀器與實驗,2012,4(28):14~15.
[5]莊如平.原電池實驗器的改進[J].教學儀器與實驗,2002,3(18):29.
[6]張新平.原電池原理微型實驗的研究[J].化學教育,2008,(8):63.
[7]于永民.若干電化學微型實驗的設計[J].化學教學,2013,(7):44~47.
[8]朱元保,沈子琛.電化學數據手冊[M].長沙:湖南科學技術出版社,1984.

